Beryllium
Beryllium ist ein chemisches Element mit dem Symbol Be und der Ordnungszahl 4. Sein Name lässt sich vom Mineral Beryll, einem berylliumhaltigen Edelstein, ableiten (altgriechisch βήρυλλος bēryllos, deutsch ‚meergrüner Edelstein, Beryll‘,[19] lateinisch beryllos ‚meergrüner indischer Edelstein, Beryll‘[20]).[21] In diesem Mineral sowie im Bertrandit ist auch der größte Teil des in der Erdkruste vorhandenen Berylliums gebunden. Beryllium gehört zu den seltener vorkommenden Metallen.[22]
| Eigenschaften | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | |||||||||||||||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Beryllium, Be, 4 | ||||||||||||||||||||||||||||||||||||
| Elementkategorie | Erdalkalimetalle | ||||||||||||||||||||||||||||||||||||
| Gruppe, Periode, Block | 2, 2, s | ||||||||||||||||||||||||||||||||||||
| Aussehen | weiß-grau metallisch | ||||||||||||||||||||||||||||||||||||
| CAS-Nummer | |||||||||||||||||||||||||||||||||||||
| EG-Nummer | 231-150-7 | ||||||||||||||||||||||||||||||||||||
| ECHA-InfoCard | 100.028.318 | ||||||||||||||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 5,3 ppm[1] | ||||||||||||||||||||||||||||||||||||
| Atomar [2] | |||||||||||||||||||||||||||||||||||||
| Atommasse | 9,0121831(5)[3] u | ||||||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | 105 (112) pm | ||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 96 pm | ||||||||||||||||||||||||||||||||||||
| Van-der-Waals-Radius | 153[4] pm | ||||||||||||||||||||||||||||||||||||
| Elektronenkonfiguration | [He] 2s2 | ||||||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 9.322699(7) eV[5] ≈ 899.5 kJ/mol[6] | ||||||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 18.21115(4) eV[5] ≈ 1757.11 kJ/mol[6] | ||||||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 153.896203(4) eV[5] ≈ 14848.72 kJ/mol[6] | ||||||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 217.7185843(17) eV[5] ≈ 21006.64 kJ/mol[6] | ||||||||||||||||||||||||||||||||||||
| Physikalisch [7] | |||||||||||||||||||||||||||||||||||||
| Aggregatzustand | fest | ||||||||||||||||||||||||||||||||||||
| Kristallstruktur | hexagonal (dichtest gepackt) | ||||||||||||||||||||||||||||||||||||
| Dichte | 1,848 g/cm3 (20 °C)[8] | ||||||||||||||||||||||||||||||||||||
| Mohshärte | 5,5 | ||||||||||||||||||||||||||||||||||||
| Magnetismus | diamagnetisch (χm = −2,3 · 10−5)[9] | ||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 1560 K (1287 °C) | ||||||||||||||||||||||||||||||||||||
| Siedepunkt | 3243 K[10] (2969 °C) | ||||||||||||||||||||||||||||||||||||
| Molares Volumen | 4,85 · 10−6 m3·mol−1 | ||||||||||||||||||||||||||||||||||||
| Verdampfungsenthalpie | 309 kJ/mol[10] | ||||||||||||||||||||||||||||||||||||
| Schmelzenthalpie | 7,95 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | 13000 m·s−1 | ||||||||||||||||||||||||||||||||||||
| Spezifische Wärmekapazität | 1825[1] J·kg−1·K−1 | ||||||||||||||||||||||||||||||||||||
| Austrittsarbeit | 4,98 eV[11] | ||||||||||||||||||||||||||||||||||||
| Elektrische Leitfähigkeit | 25 · 106 A·V−1·m−1 | ||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 190 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||
| Chemisch [12] | |||||||||||||||||||||||||||||||||||||
| Oxidationszustände | 2, 1, 0[13] | ||||||||||||||||||||||||||||||||||||
| Normalpotential | −1,97 V (Be2+ + 2 e− → Be) | ||||||||||||||||||||||||||||||||||||
| Elektronegativität | 1,57 (Pauling-Skala) | ||||||||||||||||||||||||||||||||||||
| Isotope | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | |||||||||||||||||||||||||||||||||||||
| NMR-Eigenschaften | |||||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||||||||||||||||||||
Entdeckt wurde es als Bestandteil des Minerals Beryll bereits 1798 von Louis-Nicolas Vauquelin und wegen des süßlichen Geschmacks der isolierten berylliumhaltigen Verbindungen (z. B. des Hydroxids) zunächst Glucine[23] genannt. Elementares Beryllium wurde erstmals 1828 von Friedrich Wöhler und unabhängig davon von Antoine Bussy hergestellt.[22]
Im Periodensystem steht Beryllium in der zweiten Hauptgruppe (2. IUPAC-Gruppe) und zählt daher zu den Erdalkalimetallen. Als Element der zweiten Periode zählt es zu den leichten Erdalkalimetallen. Es hat wegen des Verhältnisses zwischen Ladung und Durchmesser des zweiwertigen Ions aber einige für diese Gruppe ungewöhnliche Eigenschaften; zum Beispiel hat es eine höhere Dichte als seine beiden Homologe Magnesium und Calcium.[24][25]
Das stahlgraue Leichtmetall ist sehr hart und spröde, hat einen höheren Elastizitätsmodul als Stahl und wird meist als Legierungszusatz verwendet. In Verbindungen ist es zweiwertig. Im Vergleich mit den anderen leichten Alkali- und Erdalkalimetallen (Lithium, Natrium, Kalium, Magnesium und Calcium) ist es außergewöhnlich giftig und gesundheitsschädlich.[22][26]
Geschichte
Im Altertum und im Mittelalter dienten durchsichtige Beryllstücke vielfach als Lupe (Sehhilfe beim Lesen oder anderen Tätigkeiten im Nahbereich).[27]
Die erste überlieferte Erwähnung findet sich in der Naturalis historia aus dem 1. Jahrhundert, wo Plinius der Ältere die Ähnlichkeit zwischen den Mineralien Beryll und Smaragd (Beryll mit einer Spur Chrom) beschrieb. Er hielt sie für unterschiedliche Stoffe.[28]
Der Abbé R. J. Haüy stellte bei Beryll und Smaragd nach Härte und Dichte die gleichen physikalischen Eigenschaften sowie die gleiche Kristallform fest und veranlasste daraufhin den französischen Chemiker Louis-Nicolas Vauquelin zu einer Untersuchung.[29]

Vauquelin bewies 1798, dass Beryll und Smaragd chemisch nahezu identisch sind. Er isolierte auch ein Oxid aus beiden Mineralen, das er terre du béril (Beryllerde) nannte; es war den bekannten Aluminiumverbindungen zwar ähnlich, aber doch deutlich verschieden von diesen. Bis dahin wurde Beryll nach den vorangegangenen Analysen von T. Bergman,[30], F. C. Achard[31] M. H. Klaproth[32] und L. N. Vauquelin[33] für ein Calcium-Aluminiumsilicat gehalten. Dem neu entdeckten Stoff gaben die Herausgeber des Artikels von Vauquelin den Namen Glucine, wegen des süßen Geschmacks des Berylliumsalzes (griechisch γλυκύς glykys ‚süß‘).[34] Namen wie Glucinum, Glucinium oder Glycinium wurden in Frankreich und einigen anderen Ländern noch bis ins 20. Jahrhundert verwendet, obgleich bereits M. H. Klaproth und A. G. Ekeberg 1802 darauf hinwiesen, dass süßer Geschmack durchaus keine spezielle Eigenschaft der Salze des Berylliums ist, dass Salze des Yttriums ebenfalls süß schmecken und dass daher die Bezeichnung Beryllerde vorzuziehen sei.[35]
Die ersten Berichte über Versuche, das Element darzustellen, wurden 1809 von H. Davy und 1812 von F. Stromeyer veröffentlicht. Doch erst 1828 gelang es Friedrich Wöhler und kurz darauf Antoine Bussy, das Element durch Reduktion des Berylliumchlorids mit Kalium darzustellen. Wöhler nannte das neue Element Beryllium.[35] Das 1836 im Davidsonit (einer Beryll-Varietät[36]) entdeckte Element, das von T. Richardson Donium und von H. S. Boase Treenium genannt wurde, stellte sich als Beryllium heraus.[37] M. Awdejew nahm 1842 die ersten Bestimmungen des genauen Atomgewichtes vor. Julius Weeren (1854) und Henry Debray (1855) führten ebenfalls umfangreiche Untersuchungen des Metalls, seiner elementaren Eigenschaften und seiner Verbindungen durch. Auch Charles Arad Joy (1863) erforschte die Herstellung von Beryllverbindungen. Weiteren Kreisen wurde es wohl auf der Pariser Weltausstellung 1867 bekannt, wo erstmals eine größere Menge ausgestellt wurde.[35]
Das chemische Symbol Be wurde 1814 von J. J. Berzelius eingeführt.[38]
Große Fortschritte in der Chemie des Berylliums gelangen zwischen 1873 und 1885 durch Albert Atterberg, L. F. Nilson und O. Pettersson. In diesen Jahren wurde auch über die Valenz des Berylliums und seine Position im Periodensystem intensiv diskutiert. Zahlreiche weitere Forscher trugen später ebenfalls zur Entwicklung der Chemie des Berylliums bei.[39]
Reines Beryllium in kristalliner Form wurde erstmals 1899 von Paul Marie Alfred Lebeau durch Schmelzflusselektrolyse von Natriumtetrafluoridoberyllat (Na2[BeF4]) hergestellt. Nach dem Ersten Weltkrieg wurde Beryllium gleichzeitig von der Siemens & Halske AG (Alfred Stock und Hans Goldschmidt) in Deutschland und von der Union Carbide and Carbon Corporation (Hugh S. Cooper) in den Vereinigten Staaten produziert. Nach dem Zweiten Weltkrieg stellte in Amerika vor allem die Beryllium Corp. of America in Cleveland hochreines Beryllium her und in England erforschte das National Physical Laboratory das Element.[40][35]
1945 wurde Beryllium zusammen mit dem Alphastrahler Polonium als Neutronenquelle in der Atombombe Little Boy eingesetzt, die über Hiroshima abgeworfen wurde.[41]
Bis in die 1940er Jahre wurden Berylliumverbindungen als Bestandteil von Leuchtstoffröhren verwendet (zum Beispiel Zink-Mangan-Beryllium-Silikate), was aber beendet wurde, als immer mehr Fälle von Berylliose aufgedeckt wurden. Berylliose wurde 1946 auch anhand von Arbeitern dieser Industrie zuerst beschrieben.[26]
Vorkommen
Im Sonnensystem stellt Beryllium unter den Elementen, die leichter als Eisen sind, das seltenste dar (siehe gelistete Häufigkeiten im Sonnensystem). In der Erdhülle steht es mit einem Massenanteil von 5,3 ppm an 48. Stelle der Elementhäufigkeit. Es ist dabei in der oberen kontinentalen Lithosphäre stark angereichert, vergleicht man die Konzentrationen von 1,4 ppm in der unteren kontinentalen Kruste und 0,07 ppm im primitiven Mantel.
Beryllium ist ein typisch lithophiles Element. Es bildet eine charakteristische vierfache Koordination mit Sauerstoff im [BeO4]6−-Komplex. Geochemisch wird es in sauren und in alkalischen Magmen während des magmatischen Differenzierungsprozesses angereichert. Bei einem sauren Magma wird es in der pegmatitischen und hydrothermalen Restphase konzentriert, während es bei einem alkalischen Magma in das Gitter mehrerer gesteinsbildender und zusätzlicher Mineralien durch diadoche Einfangtechnik eintritt, was seine Konzentration in der Restphase verhindert.[42]
Mineralien, die Beryllium als wesentlichen Bestandteil enthalten, scheinen relativ spät entstanden zu sein. In terrestrischen Gesteinen älter als etwa 3 Milliarden Jahre wurden solche nicht nachgewiesen, sie treten wohl erst rund 1,5 Milliarden Jahre nach der Entstehung der Erde auf. In außerirdischen Gesteinen wurden bislang keine berylliumhaltigen Minerale gefunden. Meteorite, wie Chondrite, Achondrite, steinige Eisen- und Eisenmeteorite, enthalten Beryllium in Konzentrationen von 0 bis 400 ppb. Dabei werden in lokalen Calcium-Aluminium-reichen Einschlüssen (CAIs) bis zu 560 ppb erreicht, mit maximaler Konzentration in Melilith und Änderungsphasen von CAIs (649 ppb bzw. ≈ 1 ppm); die Affinität von Beryllium zu Melilith wird auf dessen strukturelle Ähnlichkeit mit Gugiait zurückgeführt.[43] Konzentrationen unter 10 ppm reichen selten aus, um ein Mineral mit Beryllium als wesentlichem Bestandteil zu stabilisieren. Normalerweise ist eine weitere Anreicherung erforderlich, damit die häufigeren Berylliummineralien entstehen können, beispielsweise auf rund 70 ppm für einen Beryll in granitischen Pegmatiten.[43]




Das seltene Element Beryllium kommt auf der Erde in einer Reihe verschiedener Mineralien vor. Die mengenmäßig wichtigsten sind Bertrandit (Be4Si2O7(OH)2) und Beryll (Be3Al2Si6O18).[44] Auch Phenakit kommt weltweit vor.[45] Beryllium tritt in der Struktur von knapp 40 Mineralien als formelwirksamer Bestandteil und in gut 50 weiteren Mineralien als diadocher Bestandteil auf (einige Quellen geben sogar 112,[43] die International Mineralogical Association 126[46] (Stand Juli 2019) Mineralien mit Beryllium als wesentlichem Element an). Von den rund 40 eigentlichen Berylliummineralien sind 26 Silikate (z. B. Beryll, Barylith, Phenakit), welche die enge geochemische Ähnlichkeit des Komplexes [BeO4]6− mit den Komplexen von [SiO4]4− und [AlO4]5− widerspiegeln.[42] Daneben sind Oxide (z. B. Bromellit, Chrysoberyll), Borate (z. B. Hambergit, Rhodizit), Antimonate (z. B. Swedenborgit), Phosphate (z. B. Beryllonit, Hurlbutit) sowie das bisher einzige bekannte Carbonat Niveolanit bekannt.[29] Beryll kommt in heterogenen zonierten Pegmatiten vor, Bertrandit stammt aus nicht-pegmatitischen Quellen.[42]
Die schönsten und wertvollsten berylliumhaltigen Mineralien sind unter anderem die Beryll-Varietäten Aquamarin, Smaragd und weitere „Berylle“, Chrysoberyll und dessen Varietät Alexandrit sowie Euklas, Phenakit und Tugtupit, die überwiegend als Schmucksteine verwendet werden. Beryllium-Lagerstätten finden sich bevorzugt im Äquatorialgürtel. In der Leckbachrinne im Habachtal (Hohe Tauern) südlich von Bramberg in Österreich wurde bis vor wenigen Jahren Smaragd gewonnen (siehe auch Smaragdbergwerk Habachtal). In den USA werden niedrighaltige Lagerstätten von Berylliumoxid-Erz in der Nevada-Wüste abgebaut. Die geschätzten Vorräte an förderbarem Beryllium liegen weltweit bei etwa 80.000 Tonnen.[44] Etwa 65 Prozent der Lagerstätten befinden sich in den USA (hauptsächlich in Form von Bertrandit im Gebiet der Spor Mountain in Utah[47]) und der Rest in Lagerstätten von Beryll in anderen Ländern. Abgebaut werden diese in Russland, Kanada, Brasilien, der Volksrepublik China, Madagaskar, Mosambik und Portugal.[48]
Beryllium kommt in Spuren in vielen Stoffen vor.[49]
| Stoff | Berylliumgehalt[50] |
|---|---|
| Kohle | 1,8–2,2 mg/kg |
| Kohlenasche | 46 mg/kg |
| Kaminemissionen aus Kohlekraftwerken | 0,8 µg/m3 |
| Zigaretten | bis 0,74 µg pro Zigarette |
| Düngemittel | < 200–13.500 µg/kg |
| US-Trinkwasser | 0,5 µg/l |
| Luft (US-Durchschnitt) | < 3 · 10−5 µg/m3 |
| Kidneybohnen | 2200 µg/kg |
| Knäckebrot | 112 µg/kg |
| Gartenerbsen | 109 µg/kg |
Herstellung
Das wichtigste Ausgangsmaterial für die Darstellung von Berylliumsalzen als Ausgangsstoff zur Herstellung von Beryllium ist der Beryll, der neben dem durch die Formel gegebenen Aluminiumgehalt meist noch Eisen enthält. Neben dem eigentlichen Aufschluss ist daher die Trennung des Berylliums vom Aluminium und Eisen von Bedeutung. Der Aufschluss erfolgt entweder mittels alkalischer Flussmittel[29]
oder mittels Fluoriden oder Silicofluoriden.[29]

Außer dem Beryll werden noch Gadolinit und Leukophan als Ausgangsmaterial für Berylliumsalze mit Aufschluss durch zum Beispiel Schwefelsäure oder Königswasser benutzt.[35]
Das entstehende Berylliumhydroxid wird mit Ammoniumbifluorid unter Bildung von Ammoniumfluoroberyllat umgesetzt, das wiederum bei erhöhten Temperaturen (> 125 °C) zu Berylliumfluorid und flüchtigem Ammoniumfluorid zersetzt wird.[29] Zur Erzeugung von Berylliumchlorid führt man Berylliumhydroxid durch Erhitzen in Berylliumoxid über, das bei 800 °C mit Kohlenstoff und Chlor unter Bildung des gewünschten wasserfreien Berylliumchlorid reagiert.[22]
Elementares Beryllium wird durch Reduktion von Berylliumfluorid mit Magnesium bei 1300 °C hergestellt.[22] Die Reaktion beginnt schon bei niedrigen Temperaturen, jedoch nimmt über 850 °C die Reaktionsgeschwindigkeit zu, nachdem sowohl Magnesium als auch Berylliumfluoride geschmolzen sind.[29]
Die Herstellung hochreinen, metallischen Berylliums erfolgt durch Schmelzflusselektrolyse von Berylliumchlorid mit Lithiumchlorid bei 500 °C oder Natriumchlorid bei 350 °C oder Berylliumfluorid mit Lithiumfluorid oder Kaliumfluorid bei 500 °C:[29]
Beryllium scheidet sich an der Kathode in Form eines feinen Berylliumpulvers ab, das von Zeit zu Zeit mit der Kathode aus der Schmelze gehoben sowie abgestreift und – nach Befreiung von anhaftendem Salz (Waschen mit Wasser) – durch Sintern bei 1150 °C in kompakte Stücke verwandelt wird.[22]
Die Weltjahresproduktion an Beryllium-Metall betrug 2018 etwa 230 t. Die bisher nachgewiesenen weltweiten Reserven belaufen sich auf über 100.000 t.[47] Der Preis für Beryllium als voll bearbeitete Luft- und Raumfahrtkomponente liegt zwischen 300 und 1500 €/kg.[51] Als Handelsprodukt in Form von Drähten oder Folien aus reinem Beryllium (> 99,5 % Berylliumgehalt) auch deutlich teurer (> 10.000 €/g.[52])
Eigenschaften
Physikalische Eigenschaften

Kristallines Beryllium ist von stahlgrauer Farbe, wobei gut ausgebildete Kristallflächen oft einen helleren Farbton zeigen. Die Mohs-Härte des Metalls liegt zwischen 6 und 7. Es ist diamagnetisch und bei normalen Temperaturen außerordentlich spröde und zerspringt leicht bei Schlagbeanspruchung. Bei höheren Temperaturen ist es verhältnismäßig duktil, jedoch ist eine Bearbeitung bei diesen Temperaturen wegen der sehr hohen Affinität des Metalls zum Sauerstoff sehr schwierig und kann ohne Materialverlust nur in einer Wasserstoff-Atmosphäre oder im Vakuum vorgenommen werden.[35] Das spröde Verhalten hängt von verschiedenen Faktoren ab, wie Temperatur, Korngröße, Reinheit (vor allem dem Berylliumoxidgehalt) und vom Verarbeitungsprozess. So ist sehr feinkörniges und hochreines (99,999 %) Beryllium bei normalen Temperaturen plastisch verformbar. Beryllium mit technischer Reinheit ist bei Temperaturen über 500 °C verformbar.[53]
Beryllium besitzt für ein Leichtmetall einen bemerkenswert hohen Schmelzpunkt. Neben der sehr hohen spezifischen Wärmekapazität von 1,825 kJ/(kg·K)[54][55] besitzt es einen um ein Drittel höheren Elastizitätsmodul als Stahl (Elastizitätsmodul 303 GPa, Schubmodul 135 GPa, Kompressionsmodul 110 GPa).[29] Die molare Wärmekapazität ist mit 16,45 J/(mol·K) jedoch deutlich kleiner als die der meisten anderen Metalle. Auch die Schwingungsdämpfung ist sehr hoch. Im sichtbaren Licht und nahen Ultraviolett reflektiert es etwa 50 %, im Infrarotbereich bei einer Wellenlänge von 10,6 µm etwa 98 %. Die Schallgeschwindigkeit in Beryllium ist 2,5 Mal höher als die von Stahl, der Wärmeausdehnungskoeffizient liegt bei Raumtemperatur etwa bei 11 · 10−6 pro K.[29] Da es nur vier Elektronen pro Atom hat, ist die Wechselwirkung mit Röntgenstrahlung sehr gering. Es ist somit sehr durchlässig für Röntgenstrahlung und wird in Röntgenröhren als Austrittsfenster benutzt. Alphastrahlung kann aus Beryllium Neutronen freisetzen:
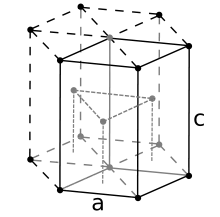
Beryllium kristallisiert normalerweise in einer hexagonal-dichtesten Packung, genannt α-Beryllium in der Raumgruppe P63/mmc (Nr. 194), im Gegensatz zu β-Beryllium mit einer kubisch raumzentrierten Form, die zwischen 1250 °C und ihrem Schmelzpunkt von 1287 °C stabil ist.[29]
Beryllium hat eine außerordentlich niedrige Poissonzahl von µ = 0,032, weist also im Zugversuch eine sehr geringe Querkontraktion auf, während andere Element-Metalle Werte von µ = 0,21 (Chrom) bis 0,44 oder 0,45 (Gold, Blei; Thallium) aufweisen.[56] Das bedeutet, dass eine Berylliumzugprobe im einachsigen Zugversuch kaum einschnürt, also ihren Querschnitt fast konstant beibehält.
Chemische Eigenschaften
Beryllium gehört zu den selteneren Metallen, das in Salzen sowohl kationisch (Berylliumsilicate) wie anionisch (in Beryllat-Oxoanionen BeO22-) vorkommt.[22]
Beryllium und seine Verbindungen ähneln durch ihre ausgeprägte Schrägbeziehung im Periodensystem in vieler Hinsicht dem Aluminium und dessen Verbindungen. Bei Raumtemperatur ist Beryllium an trockener Luft beständig und bleibt blank, da sich eine passivierende Oxidschicht bildet. Erst beim Erhitzen in Pulverform verbrennt es unter heller Feuererscheinung zu Berylliumoxid und Berylliumnitrid. Die Oxidschicht widersteht auch dem Angriff kalter oxidierende Säuren, z. B. konzentrierter Salpetersäure bis zu einer Konzentration von 6 M. Verunreinigungen mit Halogenid- und Sulfationen fördern die Lösung. In verdünnten nichtoxidierenden Säuren (z. B. Salzsäure, Schwefelsäure und Ammoniumhydrogendifluorid) löst es sich entsprechend seinem stark negativen Normalpotential (−1,847 V) lebhaft unter Wasserstoffentwicklung.[29][22]
Laugen greifen Beryllium unter Bildung von Beryllaten an.[29]
An feuchter Luft überzieht es sich mit einer Schicht aus Hydroxid, die sich beim Kontakt mit Wasser ausbildet. Bei höheren Temperaturen ist die Korrosionsbeständigkeit in Wasser abhängig von den Verunreinigungen des Metalls sowie des Korrosionsmediums, zusätzlich besteht die Gefahr der Lochfraßkorrosion. In reiner Form wird es durch Wasser selbst bei Rotglut nicht angegriffen.[22] In heißen Gasen wie Luft, Sauerstoff, Stickstoff und Kohlenstoffdioxid tritt merkliche Korrosion erst oberhalb von 600 °C ein.
Im Unterschied zu den übrigen Elementen der II. Hauptgruppe löst sich Beryllium, vor allem bei Erwärmung, auch in wässerigen Alkalilaugen unter Bildung von Beryllaten. Mit den Halogenen reagiert es bei Erhitzung unter Bildung von Halogeniden BeX2.[22]
Nur wenige Elemente bilden substantielle feste Lösungen im Beryllium, und zwar Kupfer, Nickel, Cobalt und in geringerem Maße Eisen. Silber hat eine begrenzte feste Löslichkeit in Beryllium. Die meisten Festlösungslegierungen sind wesentlich härter als das gereinigte Metall, d. h. Metall, aus dem mikrolegierungsartige Verunreinigungen entfernt wurden. Beryllium bildet viele intermetallische Verbindungen (zum Beispiel mit Titan), die oft eine wichtige Rolle sowohl bei Studien zur Legierungsentwicklung als auch bei der Herstellung von Beryllium-Verbundwerkstoffen spielen. Aluminium ist ein wichtiger Legierungszusatz, der keine intermetallische Verbindung mit Beryllium bildet. Auch weist Aluminium keine signifikante Feststofflöslichkeit in Beryllium und Beryllium in Aluminium auf, sodass Beryllium-Aluminium-Legierungen als Mischungen der beiden im Wesentlichen reinen Metalle erscheinen.[29]
Isotope
Es sind insgesamt 11 Isotope des Berylliums zwischen 5Be und 16Be bekannt. Von diesen ist nur eines stabil, das Isotop 9Be mit 5 Neutronen. Damit ist Beryllium eines von 22 Reinelementen. Die langlebigsten instabilen Isotope sind 7Be, das mit einer Halbwertszeit von 53,22 Tagen unter Elektroneneinfang in 7Li übergeht und 10Be, das mit einer Halbwertszeit von 1,51 Millionen Jahren unter Betazerfall zu 10B zerfällt.[57] Beide Isotope sind kosmogen.[58][59] Alle anderen Isotope haben nur kurze Halbwertszeiten von Sekunden oder Millisekunden.
Beim Einsatz in Kernreaktoren entstehen durch Neutroneneinfang und die folgenden Kernreaktionen gasförmige Produkte.[29]
Der Nachweis von 10Be wird zum Beispiel in der Geologie und Klimaforschung verwendet – in der Geologie zum Beispiel bei der Datierung der Offenlegung von Gestein. Damit lässt sich zum Beispiel der Rückzug von Gletschern datieren.[60] Die Konzentration von 10Be zeigt eine Korrelation mit der die Erde erreichenden kosmischen Strahlung. 10Be entsteht bei Reaktionen schneller Nukleonen aus der Höhenstrahlung mit Stickstoff und Sauerstoff der Luft. Die so entstandenen Spallationsprodukte adsorbieren an den Aerosolen der oberen Atmosphäre, die schließlich mit dem Regen auf die Erdoberfläche transportiert werden, wo sie sich mit dem stabilen 9Be vermischen.[61] Die Höhenstrahlung und damit die Entstehungsrate von 10Be hängen von der Stärke des Erdmagnetfeldes und der Sonnenaktivität ab (hohe Be-Konzentration bei geringer Sonnenaktivität). Da es sich bevorzugt auf Aerosoloberflächen niederschlägt, korrelieren hohe Berylliumkonzentrationen auch mit hohen Aerosolkonzentrationen in der Luft.[62][61] Hohe Konzentrationen treten in Warmzeiten, geringe in Kaltzeiten auf.[63] Da 10Be zusammen mit den übrigen Gasen der Atmosphäre in Eisbohrkernen eingeschlossen wird, kann durch Analyse dieser Einschlüsse über viele Jahrtausende der Zusammenhang zwischen Sonnenaktivität und globalem Temperaturverlauf analysiert werden.[64]
Das extrem kurzlebige Isotop 8Be (Halbwertszeit etwa 10−17 Sekunden) spielt eine wichtige Rolle in der Nukleosynthese, der Entstehung der chemischen Elemente in Gestirnen.[65]
An dem kurzlebigen Isotop 11Be wurde 2008 eine kernphysikalisch interessante Besonderheit nachgewiesen: Sein Atomkern besteht aus einem relativ kompakten Rumpfkern und einem einzelnen, locker gebundenen Neutron, das diesen als Halo umgibt.[66]
Verwendung
Der größte Teil (> 85 %) des weltweit hergestellten Berylliums wird für die Herstellung verschiedener Berylliumlegierungen (Berylliumgehalt weniger als 60 %) verwendet. Etwa 10 % werden für Produkte aus reinem Beryllium und Legierungen mit mehr als 60 % Berylliumgehalt eingesetzt. Das restliche Beryllium findet seinen Einsatz hauptsächlich in Berylliumoxidkeramiken.[51]
Gemessen am Wertschöpfungsumsatz wurden rund 22 % der Berylliumprodukte in Industriekomponenten, 21 % in der Unterhaltungselektronik, 16 % in der Automobilelektronik, 9 % in Verteidigungsanwendungen, 8 % in der Telekommunikationsinfrastruktur, 7 % in Energieanwendungen, 1 % in medizinischen Anwendungen und 16 % in anderen Anwendungen eingesetzt.[47]
Beryllium
Trotz der herausragenden Eigenschaften des Berylliums ist es wegen seines hohen Preises und seiner Gesundheitsgefährdung nur für wenige Anwendungen im Einsatz.[67]
Halbzeuge und Rohteile aus Berylliummetall werden vielfach als Sinterprodukte pulvermetallurgisch in HIP- und CIP-Verfahren hergestellt (heiß- und kaltisostatisches Pressen). Gussteile aus Beryllium finden wegen der anisotropen Eigenschaften und anderer Merkmale, wie Grobkörnigkeit, keine technische Verwendung.
Beryllium wird als Material für „Fenster“ von Röntgenröhren sowie Röntgen- und Gammastrahlungsdetektoren eingesetzt, wegen der Durchlässigkeit für diese Strahlen, insbesondere für die weichen (niederenergetischen) Anteile. Es wird eingesetzt für Moderatoren und Neutronenreflektoren in Kernreaktoren und Kernwaffen, als Neutronenquellen (zusammen mit einem Alphastrahler), in Kernfusionsanlagen wie JET (Joint European Torus) wegen des hohen Schmelzpunktes und der kleinen Ordnungszahl als Plasmabegrenzung (englisch limiter) sowie als Spiegelmaterial speziell für Weltraumteleskope wegen des geringen Gewichts und niedrigen Wärmeausdehnungskoeffizienten,[68][69] beispielsweise beim James-Webb-Weltraumteleskop.[70]
Beryllium ist auch zur Neutronenvermehrung im Brutmantel (Blanket) zukünftiger Fusionsreaktoren mittels der (n,2n)-Kernreaktion
vorgesehen.[71] Die Kombination aus hoher Neutronenmultiplikation, geringer Absorption und wirksamer Streuung bietet hierfür sehr günstige Eigenschaften.[29]
In der European Synchrotron Radiation Facility wird Beryllium als Material für refraktive Linsen für Röntgenstrahlung (Compound Refractive Lenses, CRL)[72] bis zu einer Energie von 40 keV verwendet.[73]
Beryllium findet bei Teilchenbeschleunigern wie dem Large Hadron Collider Verwendung als Baumaterial für vakuumdichte Röhren in den Detektoren, da Beryllium durchfliegende Teilchen schwächer streut als andere Materialien.[74]

Aufgrund des geringen Gewichts und der hohen Wärmekapazität wurde Beryllium in Bremsscheiben und anderen Teilen des Space Shuttles (Fensterbefestigungen und anderen thermisch und mechanisch hochbelasteten Teilen) eingesetzt.[75] Auch Rotoren in Kreiselkompassen, bewegliche Spiegel in optischen Systemen, Antriebssysteme in Magnetbandgeräten werden aus dem Metall hergestellt. Hochtöner von High-End-Lautsprechern werden aus Beryllium-Metall (von 1974 bis 1997 in der Yamaha Corporation[76]), als Kalottenmembran für ultrahohe Töne und inzwischen erfolgreich für High-End-Hochtonkalotten in Serienproduktion (FOCAL TBe-Linie,[77]) Koaxiallautsprecher mit Kalotten-Hochtönern und Konus-Mitteltönern aus Beryllium (TAD Labs)[78] eingesetzt.
Beryllium wird zudem für den Motorsport (z. B. Porsche 906) eingesetzt. Mercedes-Ilmor, Lieferant des McLaren-Formel-1-Teams, verwendete diesen Werkstoff beim Motorenbau. Der Werkstoff wurde nach einem Protest von Ferrari 2001 verboten. Als Begründung wurde genannt, dass der Werkstoff bei der Bearbeitung gesundheitsschädlich ist.[79]
Da Beryllium in Sternen durch die Energieerzeugungsprozesse zum großen Teil in andere Elemente umgewandelt wird, eignet es sich als Marker für die Bestimmung des Alters von Sternen.[80]
Berylliumlegierungen
Beryllium dient als Konstruktionswerkstoff in Legierungen mit Aluminium für beanspruchte und sehr leichte Produkte in der Flugzeug- und Weltraumtechnik. Beralcast (früher Lockalloy) und AlBeMet-AM162 (62 % Be, 38 % Al) sind Markennamen für Feinpulver, aus denen die Bauteile durch heißisostatisches Pressen hergestellt werden.[67] 70 bis 80 % des weltweit hergestellten Berylliums wird als Legierungsbestandteil in Berylliumkupfer (CuBe, CuCoBe) eingesetzt.[81] Daraus werden unter anderem funkenfreie, nichtmagnetische Werkzeuge hergestellt, die in explosionsgefährdeten Bereichen eingesetzt werden können. Kontakt- und Federwerkstoffe aus Berylliumkupfer zeichnen sich durch große Härte, Elastizität, Zugfestigkeit, Ermüdungsfestigkeit, Korrosionsbeständigkeit, Nichtmagnetisierbarkeit sowie gute elektrische und thermische Leitfähigkeit aus.[67] Berylliumkupfer kann daher für Kontaktfedern oder andere stromübertragende Federn,[22] z. B. in Drehspulmesswerken oder an Kohlebürsten, eingesetzt werden, ebenso für nichtmagnetisierbare Werkzeuge zum Einsatz in starken Magnetfeldern, beispielsweise zu Arbeiten an MRT-Geräten. Zu finden ist Berylliumkupfer in Präzisionssockeln für ICs sowie als Material für die Dosen von Dosenbarometern aufgrund der hohen Elastizität.[67] Daneben wird es in Relaiskontaktfedern[82] eingesetzt, dient in Hohlbananensteckern als Kontaktfedernmaterial,[83] wird als Material für Ventilführungen und Ventilsitze im Motorenbau (Verbrennungsmotoren)[84] und als CuBe- und CuCoBe-Elektroden für das Punktschweißen und für Kunststoffspritzdüsen eingesetzt.[67] CuBe kann auch als Material für Dynoden von Photoelektronenvervielfachern (unter anderem mit Berylliumoxid als Beschichtungsmaterial)[85] verwendet werden.[86]
Weiterhin dient Beryllium als Legierungsbestandteil mit Anteilen von etwa 0,0001–0,1 Gew.-% zur Verbesserung der Festigkeit und des Dehnungsverhaltens von Feinstdrähten („Bonddrähten“) aus Gold, die in der Halbleiterindustrie zum Kontaktieren von Bauelementen auf einem Verdrahtungsträger genutzt werden.[87]
Einige Uhrenfedern bestehen aus Eisen-Nickel-Beryllium, NiBe.[22]
Nickel-Beryllium-Legierungen werden für temperaturbelastete Verbindungselemente wie Thermostatschalter[88] und Nickel-Beryllium-Werkzeuge, sowie wegen der Anti-Klebeneigung für sekundäre Bor-Silikat-Gläser[88] und optische Gleitsichtgläser eingesetzt.[67]
Nachweis
Neben atomspektroskopischen Methoden kann Beryllium auch nasschemisch nachgewiesen werden. Dabei wird Beryllium als Berylliumhydroxid (durch Fällung mit Ammoniak) bestimmt, nachdem störende Ionen mit Chinolin-8-ol entfernt oder durch Ethylendiamintetraessigsäure maskiert worden sind. Zur photometrischen Bestimmung eignen sich Komplexe mit Pentan-2,4-dion, Morin, Thorin, Aluminon, Chromazurol und Chinalizarin.[81]
- Mit Chinalizarin bildet sich in alkalischer Lösung ein schwerlöslicher blauer Komplex. Zur Unterscheidung von einer ähnlich aussehenden Magnesiumverbindung wird der Berylliumkomplex in Gegenwart von NaOH durch Bromwasser zerstört, während der Mg-Komplex eine Zeit beständig ist. In Gegenwart von Ammoniak bleibt der Berylliumkomplex bei Zugabe von Bromwasser stabil, während der Mg-Komplex schnell zerstört wird.[89]
- In alkalischer Lösung bilden Be(II)-Salze mit Morin einen fluoreszierenden Farblack. Unter diesen Bedingungen fluoresziert die analoge Aluminiumverbindung nicht. Säuert man leicht an, verschwindet die Fluoreszenz der Be-Verbindung, während die Al-Verbindung fluoresziert.[90]
Zu den gebräuchlichen analytischen Techniken gehören die induktiv gekoppelte Plasma-Atomemissionsspektroskopie (ICP-AES), die induktiv gekoppelte Plasma-Massenspektroskopie (ICP-MS) und die Atomabsorptionsspektroskopie (AAS). Darüber hinaus wurde eine molekulare Fluoreszenzmethode für Beryllium entwickelt, die eine mit ICP-MS vergleichbare Empfindlichkeit aufweist. Daneben wurde eine Vielzahl alternativer Techniken erprobt. Dazu gehören die laserinduzierte Durchbruchsspektroskopie (LIBS), die mikrowelleninduzierte Plasmaspektroskopie (MIPS), die Aerosol-Laufzeit-Massenspektroskopie (TOFMS) und die oberflächenverstärkte Ramanspektroskopie. Im Allgemeinen erfordern diese Techniken eine deutlich geringere Probenvorbereitung. Aufgrund von Problemen mit mangelnder Präzision bei niedrigeren Analytenwerten und der unzureichenden Fähigkeit, Oberflächenwischtücher zu verarbeiten, haben sich diese Methoden jedoch nicht durchgesetzt.[49]
Toxikologie

Beryllium und Berylliumverbindungen können Ursache eines allergischen Kontaktekzems sein. Sie können an Haut bzw. Lunge zu einer granulomatösen Hautreaktion bzw. granulomatösen Erkrankung mit immunologischer Genese führen. Diese beruht, im Unterschied zu den meisten anderen bekannten allergischen Reaktionen an den Atemwegen, sehr wahrscheinlich auf einer zellvermittelten immunologischen Reaktion vom Spättyp.[26] Bei der Inhalation von Beryllium oder dessen Verbindungen entsteht durch die Wirkung der Makrophagen primär lösliches Berylliumoxid, das zirkuliert (Hapten), die Struktur körpereigener Proteine verändert und bei entsprechender genetischer Disposition als ein Allergen wirkt.[91] Aktuelle Studien weisen darauf hin, dass Beryllium nicht im eigentlichen Sinne akut toxisch ist, sondern die Auswirkungen eine Folge einer überschießenden allergischen Reaktion sind. Auch die krebserregende Wirkung ist nicht eindeutig nachgewiesen.[92]
Lösliche Berylliumverbindungen können aufgrund der Reizwirkung zu einer ausgeprägten, schlecht heilenden Dermatitis führen. Gelangen Berylliumsalzlösungen oder ungelöste Partikel infolge Verletzungen oder bei geschädigter Hautbarriere in die Haut, können Ulcera oder Nekrosen die Folge sein. Bis zur Mitte des 20. Jahrhunderts wurde aus Betrieben zur Berylliumgewinnung oder aus Beryllium verarbeitenden Betrieben häufiger über ein allergisches Kontaktekzem durch Berylliumsalze und seltener durch Berylliumoxid und Beryllium berichtet. In dieser Zeit waren vor allem berufliche Schnittverletzungen durch Leuchtstoffröhren, die z. B. Zink‐Mangan‐Beryllium‐Silikate enthielten, für keloid‐artige, schlecht heilende oder vernarbende Granulome durch in die Haut gelangte Berylliumsalze oder Berylliumoxid verantwortlich.[26]
Die Wirkung von Beryllium akkumuliert sich im menschlichen Körper und führt nach jahrelanger Latenzzeit zu schweren Erkrankungen. Gefährlich ist vor allem inhaliertes Beryllium oder inhalierte Berylliumsalze – insbesondere Berylliumfluorid oder Berylliumoxid in hoher Konzentration. Dies kann zu einer akuten Entzündung des Atemtraktes im Sinne einer Tracheobronchitis und Pneumonitis führen, in schweren Fällen zu einem Lungenödem. Außer in besonders schweren Fällen ist die Symptomatik mit Dyspnoe, Husten und Brustschmerz zumeist vollständig reversibel. Diese Erkrankungsform wurde zuerst bei Beschäftigten in der Gewinnung und Anreicherung von Beryllium bzw. Berylliumverbindungen aus berylliumhaltigen Erzen beobachtet. Nach einer Latenzzeit von bis zu 5 Jahren und mehr (in Einzelfällen bis zu 30 Jahren) kam es bei einem kleinen Teil der Betroffenen auch zu einer chronischen Lungenerkrankung (Berylliose). Diese tritt in der Regel als Folge einer chronischen Exposition gegen niedrige Beryllium-Konzentrationen auf. Die Krankheit kann durch einen Lymphozytentransformationstest nachgewiesen werden.[26]
Hierbei kommt es in der Lunge zur Bildung charakteristischer Epitheloidzellgranulome.[91] Verschlucktes Beryllium ist relativ ungefährlich, da es überwiegend wieder ausgeschieden wird.[29]
Sicherheitshinweise
Beryllium wurde 2013 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Beryllium waren die Besorgnisse bezüglich anderer Exposition / risikobasierter Bedenken. Die Neubewertung fand ab 2013 statt und wurde von Deutschland durchgeführt.[93] Anschließend wurde ein Abschlussbericht veröffentlicht, in dem festgestellt wurde, dass Beryllium aufgrund seiner Einstufung als krebserzeugend Kategorie 1B[15] und STOT RE1 (Berylliose) und SE3[15] die Anforderungen für SVHC-Substanzen (Substances of Very High Concern) erfüllt und entsprechend eingestuft werden sollte.[94]
Berylliumhaltige Legierungen – in fester Form und wie sie in den Endprodukten enthalten sind – weisen keine besonderen gesundheitlichen Risiken auf. Allerdings entstehen bei einigen Herstellungs-, Verarbeitungs- und Recyclingverfahren schwebende Partikel (Staub, Nebel oder Rauch) deren Einatmen zu ernsthaften Lungenerkrankungen führen kann. Bei der Berylliumverarbeitung ist deshalb Absaugung und Abkapselung bei der Spanabnahme unbedingt erforderlich.[95] Bei der Zerstörung berylliumoxidhaltiger elektronischer Bauteile kann Berylliumoxid freigesetzt werden, sie müssen daher entsprechend gekennzeichnet sein, was aber, insbesondere bei älteren Bauteilen, oft nicht der Fall ist.
Verbindungen
Beryllium hat in seinen Verbindungen mit elektronegativen Bindungspartnern praktisch ausschließlich die Oxidationsstufe +2. Die Oxidationsstufe +1 besitzt es als Ausnahme zum Beispiel in dem bei sehr hoher Temperatur durch Reaktion von Beryllium mit Berylliumchlorid zugänglichen und bei Raumtemperatur zersetzungsanfälligen Berylliummonochlorid.[22]
Das Berylliumkation Be2+ ist in der Erdalkaligruppe das am stärksten polarisierende Ion, sodass die Bindungen mit Beryllium ausgesprochen kovalent sind. Deswegen bildet Beryllium keine Verbindungen BeX2 (X = elektronegativer Rest) mit vorwiegend ionischem Bindungscharakter. Wie die kovalenten Borverbindungen gehören auch die kovalenten Berylliumverbindungen zu den elektronenungesättigten Verbindungen, die bei einwertigen Gruppen X zu Molekülen BeX2 führen, in denen dem Beryllium nur ein Elektronenquartett zukommt. Ähnlich wie das Bor, wenn auch weniger ausgeprägt, kann auch das Beryllium dieses Defizit an Elektronen durch Adduktbildung, durch pπpπ-Bindungen und durch Dreizentrenbindungen beseitigen.[22]
Die wichtigste Koordinationszahl des Berylliums ist vier, wobei es in der Regel als Tetraeder wie in Berylliumchlorid, aber auch quadratisch-planar wie in Berylliumphthalocyanin vorliegt. In Verbindungen BeX2 mit sperrigen Substituenten X oder im gasförmigen Zustand tritt Beryllium in seinen Verbindungen auch mit der Koordinationszahl drei (trigonal-planar), zwei (linear, wie in gasförmigem Berylliumchlorid) und eins (Berylliumoxid in der Gasphase) auf. In Ausnahmefällen beobachtet man darüber hinaus höhere Koordinationszahlen wie sechs oder sieben.[22]
Sauerstoffverbindungen
Beim gesamten kommerziellen Volumen ist Berylliumhydroxid die wichtigste Berylliumverbindung. Sie fällt bei der Versetzung von Berylliumsalzlösungen mit Basen aus.[22] Sie entsteht als Produkt der Extraktionsverfahren für Beryll- und Bertranditerze und wird als Zwischenprodukt für die Herstellung metallischen Berylliums, von Berylliumoxid und berylliumhaltiger Legierungen als Handelsprodukte eingesetzt. Berylliumhydroxid ist die wichtigste Verbindung zur Herstellung hochreinen Berylliumoxids, das aufgrund der keramischen Eigenschaften gesinterten Berylliumoxids für die Herstellung oder den Schutz von Materialien, die bei hohen Temperaturen in korrosiven Umgebungen eingesetzt werden, verwendet wird – so in Lasern und Elektronik, der Raumfahrt und Nukleartechnik.[96]
Prozesse für die Herstellung von Berylliummetall und für das Legieren mit Kupfer oder/und Nickel verwenden Berylliumhydroxid und Berylliumoxid als Ausgangsstoff.[67] Berylliumoxid selbst wird als gut wärmeleitender Isolator für Hochfrequenz-Leistungstransistoren, -Zirkulatoren und -Hochlastwiderstände eingesetzt. Wegen der Giftigkeit wird Berylliumoxid, wenn möglich, durch Aluminiumoxid, Bornitrid oder Aluminiumnitrid ersetzt.
Halogenverbindungen
Die farblosen Berylliumdihalogenide BeX2 (X = F, Cl, Br, I) können zum Beispiel direkt aus den Elementen oder durch Reaktion von HX mit Beryllium bzw. von X2 mit Berylliumoxid in Anwesenheit von Kohlenstoff dargestellt werden.[22] Berylliumfluorid wird in der Nukleartechnik und als Zwischenprodukt bei der Herstellung reinen Berylliums eingesetzt.[96]
Wasserstoffverbindungen
Das weiße, nichtflüchtige, hochpolymere Berylliumhydrid BeH2 (Beryllan) kann durch Umsetzung von Dimethylberyllium mit Diboran dargestellt werden. Mit Trimethylamin und Dimethylamin bildet Berylliumdihydrid Amide wie zum Beispiel das trimere Berylliumdiamid. Das farblose, an Luft entflammende, explosionsartig mit Wasser reagierende Berylliumboranat kann aus Berylliumchlorid und Lithiumborhydrid gewonnen werden.[22]
Weitere Verbindungen
Beryllium bildet eine große Zahl weiterer anorganischer, organischer und intermetallischer Verbindungen.[29] Sie werden zumeist zur Herstellung von Beryllium oder anderen Berylliumverbindungen verwendet.[96]
Mit Stickstoff bildet es bei hohen Temperaturen das kristalline farblose und sehr harte Berylliumnitrid Be3N2. Daneben kennt man noch ein stickstoffreicheres Nitrid, das farblose Berylliumdiazid BeN6. Bei Reaktion zwischen Berylliumoxid und Kohlenstoff bildet sich das ziegelrote Berylliumcarbid Be2C. Mit Bor bildet es eine Reihe von Berylliumboriden BenBm (Be5B, Be4B, Be2B, BeB32). Strukturell interessant ist ein beim Erhitzen wasserfreien Berylliumnitrats Be(NO3)2 entstehendes, sublimierbares, basisches Berylliumnitrat Be4O(NO3)6. Seine Struktur entspricht einem Be4-Tetraeder, dessen Mitte mit einem Sauerstoffatom besetzt ist und dessen sechs Be2-Kanten durch sechs (gewinkelte) Nitrat-Ionen überbrückt sind. Mit Essigsäure bilden sich die Berylliumverbindungen Berylliumacetat Be(C2H3O2)2 oder basisches Berylliumacetat Be4O(CH3COO)6.[22]
Berylliumverbindungen bilden ähnlich wie Aluminium oder Magnesium Alkyl- und Aryl-Derivate. Diese sind zur Bildung von at-Komplexen befähigt, die wiederum katalytische Eigenschaften besitzen können. Einige Verbindungen (wie zum Beispiel Beryllium-bis-pentan-2,4-dionat oder basisches Berylliumacetat) können unzersetzt destilliert werden und dienen als Zwischenprodukt zur Reinigung von Beryllium.[97] Berylliumdiorganyle BeR2 (R z. B. Me, Et, Pr iPr, Bu, tBu …) liegen als giftige, farblose, viskose Flüssigkeiten oder Feststoffe vor. Sie lassen sich wie erstere durch Metathese aus Berylliumchlorid und RMgX oder LiR sowie durch Transmetallierung aus Beryllium und HgR2 gewinnen.[22]
→ Kategorie:Berylliumverbindung
Literatur
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1215–1224.
Weblinks
- Was ist die Beryllium-Barriere? aus der Fernseh-Sendereihe alpha-Centauri (ca. 15 Minuten). Erstmals ausgestrahlt am 13. Apr. 2005.
Einzelnachweise
- Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Beryllium) entnommen.
- IUPAC, Standard Atomic Weights Revised 2013.
- Manjeera Mantina, Adam C. Chamberlin, Rosendo Valero, Christopher J. Cramer, Donald G. Truhlar: Consistent van der Waals Radii for the Whole Main Group. In: J. Phys. Chem. A. 113, 2009, S. 5806–5812, doi:10.1021/jp8111556.
- Eintrag zu beryllium in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: NIST, Gaithersburg, MD. doi:10.18434/T4W30F (https://physics.nist.gov/asd). Abgerufen am 11. Juni 2020.
- Eintrag zu beryllium bei WebElements, https://www.webelements.com, abgerufen am 11. Juni 2020.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Beryllium) entnommen.
- N. N. Greenwood, A. Earnshaw: Chemie der Elemente. 1. Auflage. VCH, Weinheim 1988, ISBN 3-527-26169-9, S. 136.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9, S. E-129 bis E-145. Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337, doi:10.1021/je1011086.
- Ludwig Bergmann, Clemens Schaefer, Rainer Kassing: Lehrbuch der Experimentalphysik. Band 6: Festkörper. 2. Auflage. Walter de Gruyter, 2005, ISBN 3-11-017485-5, S. 361.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Beryllium) entnommen.
- Corinna Czernetski, Merle Arrowsmith, Holger Braunschweig: A Neutral Beryllium(I) Radical In: Angewandte Chemie (Zeitschrift). doi:10.1002/anie.202108405.
- Eintrag zu Beryllium im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Beryllium in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. April 2017. (JavaScript erforderlich)
- V. S. Kushneva: Spravochnik po Toksikologii i Gigienicheskim Normativam. IzdAT, Moskau 1999, ISBN 5-86656-092-5, S. 23.
- Eintrag zu Beryllium, elemental in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Laboratory Investigation. Vol. 15, 1966, S. 176.
- Wilhelm Pape, Max Sengebusch (Bearb.): Handwörterbuch der griechischen Sprache. 3. Auflage, 6. Abdruck, Vieweg & Sohn, Braunschweig 1914. 1914, abgerufen am 23. Juli 2020.
- Karl Ernst Georges: Ausführliches lateinisch-deutsches Handwörterbuch. 8., verbesserte und vermehrte Auflage. Hahnsche Buchhandlung, Hannover 1918 (zeno.org [abgerufen am 23. Juli 2020]).
- Uwe Ocken: Die Entdeckung der Chemischen Elemente und die Etymologie ihrer Namen. Von der Antike über die Alchemie bis zum Atomzeitalter. BoD – Books on Demand, 2018, ISBN 978-3-7460-5759-0, S. 129 (eingeschränkte Vorschau in der Google-Buchsuche).
- A. F. Holleman, N. Wiberg: Lehrbuch der Anorganischen Chemie. De Gruyter, 2008, ISBN 978-3-11-020684-5, S. 1216 (abgerufen über De Gruyter Online).
- Vgl. Annales de Chimie (1798), S. 264 und 265 (eingeschränkte Vorschau in der Google-Buchsuche).
- Paddy Gannon: Revise AS Chemistry for AQA. Heinemann, 2005, ISBN 978-0-435-58318-7, S. 41 (eingeschränkte Vorschau in der Google-Buchsuche).
- Michael Clugston, Rosalind Flemming: Advanced Chemistry. OUP Oxford, 2000, ISBN 978-0-19-914633-8, S. 294 (eingeschränkte Vorschau in der Google-Buchsuche).
- Beryllium und seine Verbindungen [MAK Value Documentation in German language, 2002.] In: The MAK‐Collection for Occupational Health and Safety. doi:10.1002/3527600418.mb744041verd0034.
- Friedrich Kluge: Etymologisches Wörterbuch der deutschen Sprache. Walter de Gruyter GmbH & Co KG, 2012, ISBN 978-3-11-022365-1, S. 152 (eingeschränkte Vorschau in der Google-Buchsuche).
- Jeffrey A. Hurlbut: The history, uses, occurrences, analytical chemistry, and biochemistry of beryllium – a review. 16. Dezember 1974, DOW CHEMICAL U.S.A., RFP-2152.
- Kenneth A. Walsh: Beryllium Chemistry and Processing. ASM International, 2009, ISBN 978-0-87170-721-5, S. 27 (eingeschränkte Vorschau in der Google-Buchsuche).
- Disquisitio chemica de terra gemmarum, in Commentationes chemicae. Upsaliae 1777, S. 137.
- Bestimmung der Bestandtheile einiger Edelgesteine, Berlin 1779, S. 45.
- Beiträge zur chemischen Kenntnis der Mineralkörper. Posen-Berlin, 1802, Bd. 3, S. 215, 221.
- J. Mines 8, 1798, 533, Ann. Chim. 26, 1798, S. 155.
- Siehe redaktionelle Fußnote in den Annales de Chimie (1798) auf S. 169, online.
- Martin Hosenfeld u. a.: 26. Gmelins Handbuch der anorganischen Chemie. Beryllium. 8. Auflage. Verlag Chemie, Berlin 1930.
- Otto Linné Erdmann: Journal für praktische Chemie. J. A. Barth, 1837, S. 249 (eingeschränkte Vorschau in der Google-Buchsuche).
- Marco Fontani, Mariagrazia Costa, Mary Virginia Orna: The Lost Elements The Periodic Table’s Shadow Side. Oxford University Press, 2015, ISBN 978-0-19-938334-4, S. 78 (eingeschränkte Vorschau in der Google-Buchsuche).
- Lothar Dunsch: Jöns Jacob Berzelius. Springer-Verlag, 2013, ISBN 978-3-322-94554-9, S. 73 (eingeschränkte Vorschau in der Google-Buchsuche).
- Charles Lathrop Parsons: The Chemistry and Literature of Beryllium. BiblioBazaar, 2008, ISBN 978-0-559-26416-0.
- Johann Boillat: From Raw Material to Strategic Alloys. The Case of the International Beryllium Industry (1919–1939). 27. August 2016, doi:10.13140/rg.2.2.35545.11363 (researchgate.net [abgerufen am 3. Januar 2018]).
- Bruce Cameron Reed: Atomic Bomb: The Story of the Manhattan Project How nuclear physics became a global geopolitical game-changer. Morgan & Claypool Publishers, 2015, ISBN 978-1-62705-991-6, S. 23 (eingeschränkte Vorschau in der Google-Buchsuche).
- N. Krishna Rao, T. Sreenivas: Beryllium—Geochemistry, Mineralogy and Beneficiation. In: Mineral Processing and Extractive Metallurgy Review. 13, 1994, S. 19, doi:10.1080/08827509408914098.
- E. S. Grew, R. M. Hazen: Beryllium mineral evolution. In: American Mineralogist. 99, 2014, S. 999, doi:10.2138/am.2014.4675.
- Rheinisch-Westfälisches Institut für Wirtschaftsforschung (RWI Essen), Fraunhofer-Institut für System- und Innovationsforschung (ISI), Bundesanstalt für Geowissenschaften und Rohstoffe (BGR): Trends der Angebots- und Nachfragesituation bei mineralischen Rohstoffen. 2006.
- The Mineralogy of Beryllium. In: mindat.org. Hudson Institute of Mineralogy, abgerufen am 23. Juli 2019 (englisch).
- IMA: Mineral List with Database of Mineral Properties. Abgerufen am 23. Juli 2019.
- usgs.gov: Beryllium Statistics and Information. Abgerufen am 22. Juli 2019.
- K. J. Schulz, John H. DeYoung, Robert R. Seal, Dwight C. Bradley: Critical Mineral Resources of the United States Economic and Environmental Geology and Prospects for Future Supply. Government Printing Office, 2018, ISBN 978-1-4113-3991-0, S. E-16 (eingeschränkte Vorschau in der Google-Buchsuche).
- Michael J. Brisson, Amy A. Ekechukwu: Beryllium Environmental Analysis and Monitoring. Royal Society of Chemistry, 2009, ISBN 978-1-84755-903-6, S. 10 (eingeschränkte Vorschau in der Google-Buchsuche).
- Smith C., Ingerman L., Amata R.: TOXICOLOGICAL PROFILE FOR BERYLLIUM. Hrsg.: U.S. DEPARTMENT OF HEALTH AND HUMAN SERVICES Public Health Service Agency for Toxic Substances and Disease Registry. Atlanta, GA, USA 2002 (cdc.gov).
- BeST: Facts and Figures. Abgerufen am 3. August 2019.
- Datenblatt Beryllium wire, 0.25mm (0.01in) dia, annealed, 99.7% (metals basis) bei AlfaAesar, abgerufen am 3. August 2019 (PDF) (JavaScript erforderlich).
- Dennis R. Floyd, John N. Lowe: Beryllium Science and Technology. Springer, 2014, ISBN 978-1-4757-0668-0, S. 108 (eingeschränkte Vorschau in der Google-Buchsuche).
- Periodensystem.de: Daten zu Beryllium. Abgerufen am 22. September 2010.
- Die anomale molare Wärmekapazität von Beryllium ist mit etwa 11 J/(K·mol) deutlich geringer als die des Eisens mit 24,7 J/(K·mol). David Halliday, Robert Resnick: Physik. Teil 2, Walter de Gruyter, Berlin/ New York 1994, ISBN 3-11-013897-2, S. 1455.
- Mark Winter: Poisson’s ratio. In: Webelements.com.
- G. Audi, F. G. Kondev, Meng Wang, W. J. Huang, S. Naimi: The NUBASE2016 evaluation of nuclear properties. In: Chinese Physics C. 41, 2017, S. 030001, doi:10.1088/1674-1137/41/3/030001 (Volltext).
- J. M. Kaste, S. A. Norton, C. T. Hess: Environmental Chemistry of Beryllium-7. In: Reviews in Mineralogy and Geochemistry. 50, 2002, S. 271, doi:10.2138/rmg.2002.50.6.
- K. Horiuchi, E.L. Goldberg, K. Kobayashi, T. Oda, T. Nakamura, T. Kawai: Climate-induced variations of cosmogenic beryllium-10 in the sediments of Lake Baikal of the last 150ky from AMS, SRXRF and NAA data. In: Nuclear Instruments and Methods in Physics Research, Section A: Accelerators, Spectrometers, Detectors and Associated Equipment. 470, 2001, S. 396, doi:10.1016/S0168-9002(01)01085-3.
- R. C. Finkel, M. Suter: AMS in the earth sciences: technique and applications. In: Advances in Analytical Geochemistry. Volume 1, 1993, ISBN 1-55938-332-1, S. 1–114.
- Wilhelm T. Hering: Angewandte Kernphysik. Einführung und Übersicht. Springer-Verlag, 1999, ISBN 978-3-519-03244-1, S. 62 (eingeschränkte Vorschau in der Google-Buchsuche).
- Fritz Gassmann: Was ist los mit dem Treibhaus Erde. vdf, 1994, ISBN 3-7281-1935-0, S. 63 (eingeschränkte Vorschau in der Google-Buchsuche).
- Richard Pott: Allgemeine Geobotanik: Biogeosysteme und Biodiversität. Springer, 2005, ISBN 3-540-23058-0, S. 126 (eingeschränkte Vorschau in der Google-Buchsuche).
- J. B. Pedro, A. M. Smith, K. J. Simon, T. D. van Ommen, M. A. J. Curran: High-resolution records of the beryllium-10 solar activity proxy in ice from Law Dome, East Antarctica: measurement, reproducibility and principal trends. In: Climate of the Past. Band 7, Juli 2011, S. 707–721, doi:10.5194/cp-7-707-2011 (englisch, clim-past.net [PDF; 1,7 MB; abgerufen am 16. Juli 2013]).
- Elisabeth Vangioni, Michel Cassé: Cosmic origin of the chemical elements rarety in nuclear astrophysics. In: Frontiers in Life Science. 10, 2017, S. 84, doi:10.1080/21553769.2017.1411838.
- Atomkern mit Heiligenschein: Wissenschaftler vermessen erstmals Ein-Neutron-Halo mit Lasern. Auf: IDW online. 16. Februar 2009.
- Ralph Puchta: A brighter beryllium. In: Nature Chemistry. 3, 2011, S. 416, doi:10.1038/nchem.1033.
- Beryllium related details from NASA. NASA, archiviert vom Original am 29. Mai 2008; abgerufen am 4. März 2016.
- M. W. Werner, T. L. Roellig, F. J. Low, G. H. Rieke, M. Rieke, W. F. Hoffmann, E. Young, J. R. Houck, B. Brandl: The Spitzer Space Telescope Mission. In: Astrophysical Journal Supplement. Band 154, 2004, S. 1, doi:10.1086/422992, arxiv:astro-ph/0406223, bibcode:2004ApJS..154....1W.
- The James Webb Space Telescope: The Primary Mirror.
- Pavel Vladimirov, Dmitry Bachurin u. a.: Current Status of Beryllium Materials for Fusion Blanket Applications. In: Fusion Science and Technology. 66, 2017, S. 28, doi:10.13182/FST13-776.
- ESRF: Focusing compound refractive Beryllium lenses. Abgerufen am 28. Juli 2019.
- RXOPTICS: Lenses. Abgerufen am 28. Juli 2019.
- R. Veness, G. Simmons, C. Dorn: Development of Beryllium Vacuum Chamber Technology for the LHC. (PDF; 444 kB). Proceedings of IPAC2011, San Sebastián, Spain 2011.
- Lawrence Korb: Memories of the Apollo and Space Shuttle Programs. Page Publishing Inc, 2017, ISBN 1-68139-825-7 (eingeschränkte Vorschau in der Google-Buchsuche).
- Yamaha-Deutschland: NS-5000. Abgerufen am 18. August 2019.
- Focal.com: Beryllium tweeter. Abgerufen am 18. August 2019.
- TAD® PIONEER Professional Studio Loudspeaker Components: TAD® PIONEER Professional Studio Loudspeaker Components. Abgerufen am 18. August 2019.
- MotorSportMagazine.com: The secrets to Ferrari’s consistency. Abgerufen am 27. Juli 2019.
- Ifa.hawaii.edu: The Case of the Missing Beryllium. Abgerufen am 26. Juli 2019.
- Eintrag zu Beryllium. In: Römpp Online. Georg Thieme Verlag, abgerufen am 3. August 2019.
- Nnamdi Anyadike: Copper A Material for the New Millennium. Elsevier, 2002, ISBN 978-1-85573-870-6, S. 121 (eingeschränkte Vorschau in der Google-Buchsuche).
- A. Davidson: Handbook of Precision Engineering Mechanical Design Applications. Macmillan International Higher Education, 2016, ISBN 978-1-349-01023-3, S. 121 (eingeschränkte Vorschau in der Google-Buchsuche).
- Tim Gilles: Automotive Engines: Diagnosis, Repair, and Rebuilding. Cengage Learning, 2018, ISBN 978-1-337-67022-7, S. 241 (eingeschränkte Vorschau in der Google-Buchsuche).
- Shu Tao, Hong Chan, Harry van der Graaf: Secondary Electron Emission Materials for Transmission Dynodes in Novel Photomultipliers: A Review. In: Materials. 9, 2016, S. 1017, doi:10.3390/ma9121017.
- J. H. Richardson: Systematic Materials Analysis. Elsevier, 2012, ISBN 0-323-14756-9, S. 115 (eingeschränkte Vorschau in der Google-Buchsuche).
- Patentanmeldung DE19733954A1: Feinstdraht aus einer Goldlegierung, Verfahren zu seiner Herstellung und seine Verwendung. Angemeldet am 6. August 1997, veröffentlicht am 14. Januar 1999, Anmelder: Heraeus, Erfinder: Günther Herklotz, Jürgen Reuel, Lutz Schräpler, Christoph Simons.
- Joseph R. Davis: Nickel, Cobalt, and Their Alloys. ASM International, 2000, ISBN 978-0-87170-685-0, S. 102 (eingeschränkte Vorschau in der Google-Buchsuche).
- Gerhart Jander, Ewald Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie. 14. Auflage, Hirzel, Stuttgart 1995, S. 428–429.
- Gerhart Jander, Ewald Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie. 14. Auflage, Hirzel, Stuttgart 1995, S. 632–633.
- Werner Böcker, Helmut Denk, Philipp U. Heitz, Holger Moch, Gerald Höfler, Hans Kreipe: Lehrbuch Pathologie. Elsevier Health Sciences, 2019, ISBN 3-437-17143-7, S. 69 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dominik Naglav, Magnus R. Buchner, Georg Bendt, Florian Kraus, Stephan Schulz: Off the Beaten Track–A Hitchhiker's Guide to Beryllium Chemistry. In: Angewandte Chemie International Edition. 55, 2016, S. 10562, doi:10.1002/anie.201601809.
- Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): Beryllium, abgerufen am 20. Mai 2019.
- Europäische Chemikalienagentur (ECHA): Substance Evaluation Report und Conclusion Document.
- Beryllium Science & Technology Association: Berylliumhaltige Materialien. Sschmieden, Expositionskontrolle, Richtlinie.
- NCBI Bookshelf: Arsenic, Metals, Fibres and Dusts. Beryllium and Beryllium Compounds. Abgerufen am 25. Juli 2019.
- Eintrag zu Beryllium-Verbindungen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 3. August 2019.

