Indium
Indium ist ein chemisches Element mit dem Symbol In und der Ordnungszahl 49. Im Periodensystem der Elemente steht es in der 5. Periode und ist das vierte Element der 3. Hauptgruppe, der 13. IUPAC-Gruppe, oder Borgruppe. Indium ist ein seltenes, silberweißes und weiches Schwermetall. Seine Häufigkeit in der Erdkruste ist vergleichbar mit der von Silber. Indium ist für den menschlichen Körper nicht essentiell, genauso wenig sind toxische Effekte bekannt.[13] Das Metall wird heute zum größten Teil zu Indiumzinnoxid verarbeitet, das als transparenter Leiter für Flachbildschirme und Touchscreens eingesetzt wird. Seit der Jahrtausendwende hat die damit verbundene gestiegene Nachfrage zu einem deutlichen Anstieg der Indiumpreise und zu Diskussionen über die Reichweite der Vorkommen geführt.[14]
| Eigenschaften | ||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | ||||||||||||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Indium, In, 49 | |||||||||||||||||||||||||||||||||
| Elementkategorie | Metalle | |||||||||||||||||||||||||||||||||
| Gruppe, Periode, Block | 13, 5, p | |||||||||||||||||||||||||||||||||
| Aussehen | silbrig glänzend grau | |||||||||||||||||||||||||||||||||
| CAS-Nummer | ||||||||||||||||||||||||||||||||||
| EG-Nummer | 231-180-0 | |||||||||||||||||||||||||||||||||
| ECHA-InfoCard | 100.028.345 | |||||||||||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 0,1 ppm[1] | |||||||||||||||||||||||||||||||||
| Atomar [2] | ||||||||||||||||||||||||||||||||||
| Atommasse | 114,818(1)[3] u | |||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | 155 (156) pm | |||||||||||||||||||||||||||||||||
| Kovalenter Radius | 144 pm | |||||||||||||||||||||||||||||||||
| Van-der-Waals-Radius | 193 pm | |||||||||||||||||||||||||||||||||
| Elektronenkonfiguration | [Kr] 4d105s25p1 | |||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 5.7863556(7) eV[4] ≈ 558.3 kJ/mol[5] | |||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 18.87041(3) eV[4] ≈ 1820.72 kJ/mol[5] | |||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 28.04415(12) eV[4] ≈ 2705.85 kJ/mol[5] | |||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 55.45(4) eV[4] ≈ 5350 kJ/mol[5] | |||||||||||||||||||||||||||||||||
| 5. Ionisierungsenergie | 69.3(1,2) eV[4] ≈ 6686 kJ/mol[5] | |||||||||||||||||||||||||||||||||
| Physikalisch [6] | ||||||||||||||||||||||||||||||||||
| Aggregatzustand | fest | |||||||||||||||||||||||||||||||||
| Kristallstruktur | tetragonal | |||||||||||||||||||||||||||||||||
| Dichte | 7,31 g/cm3 | |||||||||||||||||||||||||||||||||
| Mohshärte | 1,2 | |||||||||||||||||||||||||||||||||
| Magnetismus | diamagnetisch (χm = −5,1 · 10−5)[7] | |||||||||||||||||||||||||||||||||
| Schmelzpunkt | 429,7485[8] K (156,5985 °C) | |||||||||||||||||||||||||||||||||
| Siedepunkt | 2273 K[9] (2000 °C) | |||||||||||||||||||||||||||||||||
| Molares Volumen | 15,76 · 10−6 m3·mol−1 | |||||||||||||||||||||||||||||||||
| Verdampfungsenthalpie | 225 kJ·mol−1[9] | |||||||||||||||||||||||||||||||||
| Schmelzenthalpie | 3,26 kJ·mol−1 | |||||||||||||||||||||||||||||||||
| Dampfdruck | 1 Pa bei 1196[10] K | |||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | 1215 m·s−1 bei 293,15 K | |||||||||||||||||||||||||||||||||
| Spezifische Wärmekapazität | 233 J·kg−1·K−1 | |||||||||||||||||||||||||||||||||
| Elektrische Leitfähigkeit | 12,5 · 106 A·V−1·m−1 | |||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 81,6 W·m−1·K−1 | |||||||||||||||||||||||||||||||||
| Chemisch [11] | ||||||||||||||||||||||||||||||||||
| Oxidationszustände | 3, 1 | |||||||||||||||||||||||||||||||||
| Normalpotential | −0,343 V (In3+ + 3e− → In) | |||||||||||||||||||||||||||||||||
| Elektronegativität | 1,78 (Pauling-Skala) | |||||||||||||||||||||||||||||||||
| Isotope | ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | ||||||||||||||||||||||||||||||||||
| NMR-Eigenschaften | ||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||||||||||||||
Geschichte
Indium wurde 1863 von den deutschen Chemikern Ferdinand Reich und Theodor Richter an der Bergakademie Freiberg entdeckt. Sie untersuchten eine in der Umgebung gefundene Sphalerit-Probe nach Thallium. Dabei fanden sie im Absorptionsspektrum anstatt der erwarteten Thallium-Linien eine bisher unbekannte indigoblaue Spektrallinie und damit ein bisher unbekanntes Element. Nach dieser erhielt das neue Element später seinen Namen. Kurze Zeit später konnten sie zunächst Indiumchlorid und -oxid, durch Reduktion von Indiumoxid mit Wasserstoff auch das Metall darstellen. Eine größere Menge Indium wurde erstmals auf der Weltausstellung 1867 in Paris gezeigt.[15]
Nach einer ersten Anwendung ab 1933 als Legierungsbestandteil in Zahngold begann der umfangreiche Einsatz von Indium mit dem Zweiten Weltkrieg. Die Vereinigten Staaten setzten es als Beschichtung in hoch beanspruchten Lagern von Flugzeugen ein. Nach dem Zweiten Weltkrieg wurde Indium vor allem in der Elektronikindustrie, als Lötmaterial und in niedrig schmelzenden Legierungen eingesetzt. Auch die Verwendung in Kontrollstäben von Kernreaktoren wurde mit der zunehmenden Verwendung der Kernenergie wichtig. Dies führte bis 1980 zu einem ersten starken Ansteigen des Indiumpreises. Nach dem Reaktorunfall von Three Mile Island gingen jedoch sowohl Nachfrage als auch Preis deutlich zurück.[16]
Ab 1987 wurden zwei neue Indiumverbindungen, der Halbleiter Indiumphosphid (InP) und das elektrisch leitende und in dünnen Schichten durchsichtige Indiumzinnoxid (ITO) entwickelt. Besonders Indiumzinnoxid wurde mit der Entwicklung von Flüssigkristallbildschirmen technisch interessant. Durch den hohen Bedarf wird seit 1992 der größte Teil des Indiums zu Indiumzinnoxid weiterverarbeitet.[16]
Vorkommen
Indium ist ein seltenes Element, sein Anteil an der kontinentalen Erdkruste beträgt nur 0,05 ppm.[17] Es ist damit von ähnlicher Häufigkeit wie Silber und Quecksilber. In gediegener, das heißt elementarer Form konnte Indium bisher (Stand 2014) nur sehr selten entdeckt werden. Als Typlokalität gilt dabei eine Tantalerz-Lagerstätte bei Olowjannaja in der russischen Region Transbaikalien. Daneben fand man gediegenes Indium unter anderem noch im Perzhanskoe-Erzfeld in der ukrainischen Oblast Schytomyr und im Tschatkalgebirge in der usbekischen Provinz Taschkent sowie in Gesteinsproben vom Mond.[18]
Auch an Mineralen, die Indium enthalten, sind nur wenige bekannt (aktuell 13 anerkannte Minerale, Stand 2014). Dies sind vor allem sulfidische Minerale wie Indit FeIn2S4, Laforêtit AgInS2 und Roquesit CuInS2 sowie die zu den Elementmineralen zählenden, natürlichen Legierungen Damiaoit PtIn2 und Yixunit Pt3In.[19] Diese sind jedoch selten und spielen für die Gewinnung von Indium keine Rolle.
Die größten Vorkommen von Indium liegen in Zinkerzen, insbesondere Sphalerit. Die theoretischen Reserven werden auf 16.000 Tonnen geschätzt, wirtschaftlich abbaubar sind davon etwa 11.000 Tonnen.[20] Die größten Vorkommen liegen in Kanada, China und Peru. Indiumhaltige Erze werden aber auch in Australien, Bolivien, Brasilien, Japan, Russland, Südafrika, den USA, Afghanistan und einigen europäischen Ländern gefunden. In Deutschland liegen Vorkommen im Erzgebirge (Freiberg, Marienberg, Geyer) und am Rammelsberg im Harz.[15]
Gewinnung und Darstellung

Indium wird fast ausschließlich als Nebenprodukt bei der Produktion von Zink oder Blei gewonnen. Eine wirtschaftliche Gewinnung ist möglich, wenn sich an bestimmten Stellen des Produktionsprozesses Indium anreichert. Dies sind etwa Flugstäube, die während des Röstens von Zinksulfid entstehen, und Rückstände, die bei der Elektrolyse während des nassen Verfahrens der Zinkherstellung zurückbleiben.[21] Diese werden mit Schwefelsäure oder Salzsäure umgesetzt und so in Lösung gebracht. Da die Konzentration an Indium in der Säure zu gering ist, muss sie angereichert werden. Dies geschieht etwa durch Extraktion mit Tributylphosphat oder Fällung als Indiumphosphat.
Die eigentliche Indiumgewinnung erfolgt elektrolytisch. Dazu wird eine Lösung von Indium(III)-chlorid in Salzsäure verwendet. Dieses wird mit Hilfe von Quecksilberelektroden zu elementarem Indium umgesetzt. Bei der Elektrolyse ist darauf zu achten, dass die Lösung kein Thallium mehr enthält, da die Standardpotentiale der beiden Elemente sehr ähnlich sind.[21]
Durch geeignete Verfahren wie Zonenschmelzverfahren[22] oder mehrmalige Elektrolyse von Indium(I)-chlorid-Salzschmelzen[21] kann das Rohprodukt weiter gereinigt und so über 99,99 % reines Indium gewonnen werden.
Produktion
Die Primärproduktion (Raffinerieproduktion) von Indium lag im Jahr 2006 zwischen 500[23] und 580 Tonnen.[20] Auf Grund der geringen natürlichen Vorräte von 11.000 Tonnen[20] bei gleichzeitig hoher Nachfrage zählt Indium zu den knappsten Rohstoffen auf der Erde. Im Jahr 2008 wuchsen insbesondere für China die Angaben zu den natürlichen Indium-Vorräten von 280 auf 8.000 Tonnen, was die Reichweite von vormals 6 auf 19 Jahre verlängerte. Die Sekundärproduktion, also das Recycling, übertrifft die Primärproduktion und lag im Jahr 2008 bei 800 Tonnen.[23]
| Land | Tonnen | Anteil an Weltproduktion |
|---|---|---|
| Volksrepublik China | 300 | 39,0 % |
| Südkorea | 240 | 32,0 % |
| Japan | 75 | 9,9 % |
| Kanada | 60 | 7,9 % |
| Frankreich | 50 | 6,6 % |
| Belgien | 20 | 2,6 % |
| Peru | 10 | 1,3 % |
| Russland | 5 | 0,7 % |
| Gesamt: | 760 | 100,0 % |
Die Indiumproduktion in China findet erst seit kurzer Zeit verstärkt statt. Im Jahr 1994 lag die produzierte Menge noch bei 10 Tonnen.[26] Seitdem vergrößerte sich der Anteil Chinas an der Weltproduktion auf 60 % im Jahr 2005. Die Produktion in anderen Ländern wie Japan, Kanada oder Frankreich konnte nur in geringem Umfang gesteigert werden oder verringerte sich durch Erschöpfung der Lagerstätten. So wurde 2006 die japanische Toyoha-Mine geschlossen und damit die dortige Produktion deutlich verringert.[14]
Da die Nachfrage nach Indium stärker als die Produktion gestiegen ist, ergab sich ein starker Anstieg des Indiumpreises von 97 Dollar 2002 auf 827 Dollar pro Kilogramm im Jahr 2005.[20] Recycling von Indium erfolgt vor allen durch Wiederverwertung von Rückständen aus dem Sputtern.[20] Das einzige Land, in dem derzeit in größeren Mengen Indium wiedergewonnen wird, ist Japan.[14]
In der industriellen Dünnschichttechnologie ist die Wiederverwertung indiumhaltiger Sputtertargets auf Grund ihrer stückigen Natur und dem geringen Demontageaufwand bei hoher Materialwertigkeit gängige betriebliche Praxis.[27] Im Gegensatz zu Wänden und Einbauten der Sputterkammer sowie etwaiger Strukturierungsabfälle.[28] Die Substitution von Indium in der transparent-leitenden Schicht (TCO) mittels Zinkoxid insbesondere bei Kupfer-Indium-Gallium-Diselenid- (CIGS),[29] aber auch bei a-Si- bzw. c-Si-Solarzellen[30] ist ebenso wie die Nutzung von Sekundärmaterial für den Einsatz in Indiumtargets geringer Reinheit[31] aktuelles Thema der öffentlich geförderten Forschung der funktionalen und ressourcen-ökonomischen Materialwissenschaft.
Indium kann zwar in den meisten Anwendungen durch andere Stoffe ersetzt werden, dabei verschlechtern sich jedoch häufig die Eigenschaften des Produktes oder die Wirtschaftlichkeit der Produktion. So kann etwa Indiumphosphid durch Galliumarsenid ersetzt werden und auch für Indiumzinnoxid sind einige – wenn auch physikalisch nicht optimale – Ersatzstoffe möglich.[20]
Eigenschaften
Physikalische Eigenschaften
Indium ist ein silbrig-weißes Metall mit einem niedrigen Schmelzpunkt von 156,60 °C.[8] Einen niedrigeren Schmelzpunkt besitzen unter den reinen (unlegierten) Metallen nur Quecksilber, Gallium und die meisten Alkalimetalle. Über einen sehr großen Bereich von fast 2000 K ist das Metall flüssig. Flüssiges Indium hinterlässt auf Glas dauerhaft einen dünnen Film (Benetzung).
Das Metall besitzt eine hohe Duktilität und sehr geringe Härte (Mohs-Härte: 1,2).[1] Es ist daher möglich, Indium wie Natrium mit dem Messer zu schneiden. Gleichzeitig hinterlässt es auf Papier einen sichtbaren Strich. Unterhalb einer Sprungtemperatur von 3,41 Kelvin ist Indium supraleitend.[32] Eine Besonderheit des Indiums, die es mit dem Zinn gemeinsam hat, sind die charakteristischen Geräusche, die beim Verbiegen von Indium zu hören sind („Zinngeschrei“).
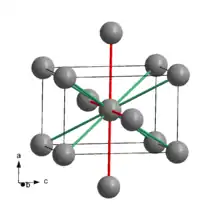
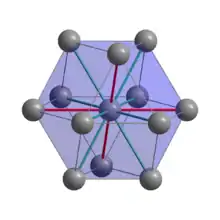
Von Indium ist bei Normalbedingungen nur eine kristalline Modifikation bekannt, die im tetragonalen Kristallsystem in der Raumgruppe I4/mmm (Raumgruppen-Nr. 139) und damit in einem tetragonal-innenzentrierten Gitter mit den Gitterparametern a = 325 pm und c = 495 pm sowie zwei Formeleinheiten in der Elementarzelle kristallisiert.
Ein Indiumatom wird in der Kristallstruktur von zwölf weiteren Atomen umgeben, wobei vier aus den benachbarten Elementarzellen stammen und einen geringeren Abstand (325 pm; rote Bindungen) als die acht auf den Ecken der Elementarzelle befindlichen Atome aufweisen (337 pm; grüne Bindungen). Als Koordinationspolyeder ergibt sich durch die Koordinationszahl 4 + 8 = 12 ein verzerrtes Kuboktaeder. Die Kristallstruktur kann daher als eine tetragonal verzerrte, kubisch-dichteste Kugelpackung beschrieben werden.
In Hochdruckexperimenten wurde eine weitere Modifikation entdeckt, die oberhalb von 45 GPa stabil ist und im orthorhombischen Kristallsystem in der Raumgruppe Fmmm (Nr. 69) kristallisiert.[33]
| Kristallsystem | tetragonal |
| Raumgruppe | I4/mmm (Nr. 139) |
| Gitterparameter (Elementarzelle) |
a = (b) = 325 pm c = 495 pm |
| Zahl (Z) der Formeleinheiten |
Z = 2 |
Chemische Eigenschaften
Die chemischen Eigenschaften des Indiums ähneln denen der Gruppennachbarn Gallium und Thallium. So ist Indium wie die beiden anderen Elemente ein unedles Element, das bei hohen Temperaturen mit vielen Nichtmetallen reagieren kann. An der Luft ist es bei Raumtemperatur stabil, da sich wie bei Aluminium eine dichte Oxidschicht bildet, die das Material durch Passivierung vor weiterer Oxidation schützt. Erst bei hohen Temperaturen findet die Reaktion zu Indium(III)-oxid statt.
Während Indium von Mineralsäuren wie Salpetersäure oder Schwefelsäure angegriffen wird, ist es nicht löslich in heißem Wasser, Basen und den meisten organischen Säuren. Auch Salzwasser greift Indium nicht an. Indium ist bei Raumtemperatur das in Quecksilber am besten lösliche Metall.[21]
Isotope
Von Indium sind 38 verschiedene Isotope und weitere 45 Kernisomere von 97In bis 135In bekannt.[35] In der Natur kommen davon nur zwei Isotope vor, 113In (64 Neutronen) mit 4,29 Prozent und 115In (66 Neutronen) mit 95,71 Prozent[35] Anteil an der natürlichen Isotopenverteilung. Das häufige Isotop 115In ist schwach radioaktiv, es ist ein Betastrahler mit einer Halbwertszeit von 4,41 · 1014 Jahren. Somit hat ein Kilogramm Indium eine Aktivität von 250 Becquerel. Beide natürlichen Isotope können mit Hilfe der NMR-Spektroskopie nachgewiesen werden. Die stabilsten künstlichen Isotope 111In und 114mIn haben Halbwertszeiten von 2,8 bzw. 50 Tagen, 113mIn nur 99 Minuten. 111In und 113mIn werden in der medizinischen Diagnostik für bildgebende Verfahren (Szintigrafie und SPECT) verwendet.[36][37]
Verwendung
Metall

Indium ist vielseitig verwendbar, sein Einsatz ist jedoch durch die Seltenheit und den hohen Preis beschränkt. Der größte Teil des produzierten Indiums wird nicht als Metall eingesetzt, sondern zu einer Reihe von Verbindungen weiterverarbeitet. Allein für die Produktion von Indiumzinnoxid wurden im Jahr 2000 65 %[15] der Gesamtproduktion an Indium verwendet. Auch andere Verbindungen, wie Indiumphosphid und Indiumarsenid werden aus dem produzierten Indium gewonnen. Genaueres über die Verwendung von Indiumverbindungen findet sich im Abschnitt Verbindungen.
Metallische Werkstücke können durch galvanisch abgeschiedene Indiumüberzüge geschützt werden. So beschichtete Werkstoffe etwa aus Stahl, Blei oder Cadmium sind danach beständiger gegen Korrosion durch organische Säuren oder Salzlösungen und vor allem Abrieb. Indiumschutzschichten wurden früher oft für Gleitlager in Automobilen oder Flugzeugen verwendet. Seit dem deutlichen Anstieg des Indiumpreises ist dies jedoch nicht mehr wirtschaftlich. Mit Indium beschichtete Flächen besitzen einen hohen und gleichmäßigen Reflexionsgrad über alle Farben hinweg und können daher als Spiegel verwendet werden.
Der Schmelzpunkt von Indium liegt relativ niedrig und ist sehr genau bestimmbar. Aus diesem Grund ist er einer der Fixpunkte bei der Aufstellung der Temperaturskala.[8] Diese Eigenschaft wird auch für die Kalibrierung in der dynamischen Differenzkalorimetrie (DSC) genutzt.[38]
Wegen des hohen Einfangquerschnittes sowohl für langsame als auch für schnelle Neutronen ist Indium ein geeignetes Material für Steuerstäbe in Kernreaktoren. Auch als Neutronendetektoren können Indiumfolien verwendet werden. Indium ist gasdicht und auch bei tiefen Temperaturen leicht zu verformen und wird daher in sogenannten Indiumdichtungen in Kryostaten eingesetzt.
Auch als Lot für viele Materialien spielt Indium auf Grund einiger spezieller Eigenschaften eine Rolle. So verformt es sich beim Abkühlen nur in geringem Maß. Dies ist vor allem beim Löten von Halbleitern für Transistoren wichtig. Ebenso spielt eine Rolle, dass Indium in der Lage ist, auch nichtmetallische Stoffe wie Glas und Keramik zu verlöten.[16][39]
Mit „Indiumpillen“ wurden Germaniumplättchen beiderseits anlegiert, um erste Transistoren herzustellen.[40]
Legierungen
Indium kann mit vielen Metallen legiert werden. Viele dieser Legierungen, vor allem mit den Metallen Bismut, Zinn, Cadmium und Blei, besitzen einen niedrigen Schmelzpunkt von 50 bis 100 °C.[41] Dadurch ergeben sich Anwendungsmöglichkeiten beispielsweise in Sprinkleranlagen, Thermostaten und Sicherungen. Da das ebenfalls verwendbare Blei giftig ist, dient Indium als ungefährlicher Ersatzstoff. Der Zweck dieser Legierungen liegt darin, dass sie bei zu hohen Umgebungstemperaturen, die durch Feuer oder hohe Stromstärken verursacht werden, schmelzen. Durch das Schmelzen wird dann der Stromkreis unterbrochen oder die Sprinkleranlage ausgelöst. Indium-Gallium-Legierungen besitzen häufig noch niedrigere Schmelzpunkte und sind in Hochtemperaturthermometern enthalten. Eine spezielle Gallium-Indium-Zinn-Legierung ist Galinstan. Diese ist bei Raumtemperatur flüssig und dient als ungefährlicher Ersatzstoff für Quecksilber oder Natrium-Kalium-Legierungen.
Es gibt noch einige weitere indiumhaltige Legierungen, die in unterschiedlichen Gebieten eingesetzt werden. In klinischen Studien wurden Quecksilberlegierungen mit Kupfer und 5 bzw. 10 % Indium als Amalgamfüllung erprobt.[42] In der Speicherschicht einer CD-RW ist unter anderem Indium enthalten.[43]
Investment
Seit einigen Jahren gibt es Indiumbarren, die von Kapitalanlegern als risikoreiche Beimischung in ihr Metall-Portfolio aufgenommen werden können. Dabei gibt es nicht nur einige wenige Anbieter in Deutschland, sondern der Markt an sich ist relativ illiquide und eine Handelbarkeit wie bei Gold oder Silber ist in diesem Umfang bei Indium nicht gegeben.[44]
Nachweis
Ein möglicher chemischer Nachweis ist das Ausfällen von Indiumionen mit Hilfe von 8-Hydroxychinolin aus essigsaurer Lösung.[45] Normalerweise wird Indium nicht auf chemische Weise nachgewiesen, sondern über geeignete spektroskopische Verfahren. Leicht ist Indium über die charakteristischen Spektrallinien bei 451,14 nm und 410,18 nm nachzuweisen.[15] Da diese im blauen Spektralbereich liegen, ergibt sich die typische blaue Flammenfärbung. Für eine genauere quantitative Bestimmung bieten sich die Röntgenfluoreszenzanalyse und die Massenspektrometrie als Untersuchungsmethode an.
Toxizität und Sicherheit
Während von Indiummetall keine toxischen Effekte bekannt sind, zeigte es sich jedoch, dass Indiumionen im Tierversuch mit Ratten und Kaninchen embryonentoxische und teratogene Effekte besitzen.[46] Bei einer Einmalgabe von 0,4 mg · kg−1 InCl3 an trächtigen Ratten konnten Missbildungen wie beispielsweise Gaumenspalten und Oligodaktylie beobachtet werden. Diese Erscheinungen waren gehäuft festzustellen, wenn Indiumtrichlorid am 10. Schwangerschaftstag appliziert wurde. Bei Mäusen waren dagegen keine Missbildungen zu beobachten.[47][48][49][50] Bei Indiumnitrat wurde eine Toxizität für Wasserorganismen (aquatische Toxizität) festgestellt.[51]
Kompaktes Indiummetall ist nicht brennbar. Im feinverteilten Zustand als Pulver oder Staub ist es dagegen wie viele Metalle leichtentzündlich und brennbar. Brennendes Indium darf wegen der Explosionsgefahr durch entstehenden Wasserstoff nicht mit Wasser gelöscht werden, sondern muss mit Metallbrandlöschern (Klasse D) gelöscht werden.[12]
Verbindungen
Indium bildet eine Reihe von Verbindungen. In ihnen hat das Metall meist die Oxidationsstufe +III. Die Stufe +I ist seltener und instabiler. Die Oxidationsstufe +II existiert nicht, Verbindungen, in denen formal zweiwertiges Indium vorkommt, sind in Wirklichkeit gemischte Verbindungen aus ein- und dreiwertigem Indium.
Indiumoxide

Indium(III)-oxid ist ein gelber, stabiler Halbleiter. Reines Indium(III)-oxid wird wenig verwendet, in der Technik wird der größte Teil zu Indiumzinnoxid weiterverarbeitet. Es handelt sich hierbei um Indium(III)-oxid, das mit einer geringen Menge Zinn(IV)-oxid dotiert ist. Dadurch wird die Verbindung zu einem transparenten und leitfähigem Oxid (TCO-Material). Diese Kombination von Eigenschaften, die nur wenige weitere Materialien besitzen, bedingt eine breite Anwendung. Insbesondere als Stromleiter in Flüssigkristallbildschirmen (LCD), organischen Leuchtdioden (OLED), Touchscreens und Solarzellen wird Indiumzinnoxid verwendet. In weiteren Anwendungen wie beheizbaren Autoscheiben und Solarzellen konnte das teure Indiumzinnoxid durch preiswerteres aluminiumdotiertes Zinkoxid (AZO) ersetzt werden.[52]
YInMn-Blau ist ein Mischoxid aus Yttrium-, Indium- und Manganoxiden, das ein sehr reines und brillantes Blau zeigt.
Verbindungshalbleiter
Viele Indiumverbindungen sind von großer Bedeutung für die Halbleitertechnik. Dies betrifft insbesondere Verbindungen mit Elementen der 5. und 6. Hauptgruppe (15. und 16. IUPAC-Gruppe), wie Phosphor, Arsen oder Schwefel. Diejenigen mit Elementen der 5. Hauptgruppe werden zu den III-V-Verbindungshalbleitern gezählt, diejenigen mit Chalkogenen zu den III-VI-Verbindungshalbleitern. Die Zahl richtet sich jeweils nach der Anzahl an Valenzelektronen in den beiden Verbindungsbestandteilen. Indiumnitrid, Indiumphosphid, Indiumarsenid und Indiumantimonid haben unterschiedliche Anwendungen in verschiedenen Dioden, wie Leuchtdioden (LED), Fotodioden oder Laserdioden. Die jeweilige Anwendung hängt von der benötigten Bandlücke ab. Indium(III)-sulfid (In2S3) ist ein III-VI-Halbleiter mit einer Bandlücke von 2 eV, der anstelle von Cadmiumsulfid in Solarzellen verwendet wird.[53] Einige dieser Verbindungen – vor allem Indiumphosphid und Indiumarsenid – spielen eine Rolle in der Nanotechnologie. Indiumphosphid-Nanodrähte besitzen eine stark anisotrope Photolumineszenz und können eventuell in hochempfindlichen Photodetektoren oder optischen Schaltern eingesetzt werden.[54]
Neben den einfachen Verbindungshalbleitern gibt es auch halbleitende Verbindungen, die mehr als ein Metall enthalten. Ein Beispiel ist Indiumgalliumarsenid (InxGa1−xAs) ein ternärer Halbleiter mit einer im Vergleich zu Galliumarsenid verringerten Bandlücke. Kupferindiumdiselenid (CuInSe2) besitzt einen hohen Absorptionsgrad für Licht und wird daher in Dünnschichtsolarzellen eingesetzt (CIGS-Solarzelle).
Weitere Indiumverbindungen
Mit den Halogenen Fluor, Chlor, Brom und Iod bildet Indium eine Reihe von Verbindungen. Sie sind Lewis-Säuren und bilden mit geeigneten Donoren Komplexe. Ein wichtiges Indiumhalogenid ist Indium(III)-chlorid. Dieses wird unter anderem als Katalysator für die Reduktion organischer Verbindungen eingesetzt.[55]
Es existieren auch organische Indiumverbindungen mit den allgemeinen Formeln InR3 und InR. Sie sind wie viele metallorganische Verbindungen empfindlich gegen Sauerstoff und Wasser. Indiumorganische Verbindungen werden als Dotierungsreagenz bei der Produktion von Halbleitern genutzt.[56]
Literatur
- Ulrich Schwarz-Schampera, Peter M. Herzig: Indium: Geology, mineralogy, and economics. Springer, Berlin/ New York 2002, ISBN 3-540-43135-7.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- Norman N. Greenwood, A. Earnshaw: Chemie der Elemente. 1. Auflage. Verlag Chemie, Weinheim 1988, ISBN 3-527-26169-9.
- Hans Breuer: dtv-Atlas Chemie 1. Allgemeine und anorganische Chemie. Dtv, 1981, ISBN 3-423-03217-0.
- Harry H. Binder: Lexikon der chemischen Elemente – das Periodensystem in Fakten, Zahlen und Daten. Hirzel, Stuttgart 1999, ISBN 3-7776-0736-3.
Weblinks
Einzelnachweise
- Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag 1999, ISBN 3-7776-0736-3.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Indium) entnommen.
- CIAAW, Standard Atomic Weights Revised 2013.
- Eintrag zu indium in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: NIST, Gaithersburg, MD. doi:10.18434/T4W30F (https://physics.nist.gov/asd). Abgerufen am 11. Juni 2020.
- Eintrag zu indium bei WebElements, https://www.webelements.com, abgerufen am 11. Juni 2020.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Indium) entnommen.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9, S. E-129 bis E-145. Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- H. Preston-Thomas: The International Temperature Scale of 1990. (ITS-90). In: Metrologia. 27, 1990, S. 3–10.
- Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337, doi:10.1021/je1011086.
- Kapitel von D. Stull in: Dwight E. Gray (Hrsg.): American Institute of Physics handbook. 3. Auflage. McGraw-Hill, New York 1972, ISBN 0-07-001485-X.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Indium) entnommen.
- Eintrag zu Indium, Pulver in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. April 2017. (JavaScript erforderlich)
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- Die stofflichen Grenzen des Wachstums. (Memento vom 29. April 2015 im Internet Archive) In: Pressespiegel Physik der Uni Augsburg. (PDF-Datei; 267 kB)
- Ulrich Schwarz-Schampera, Peter M. Herzig: Indium: Geology, mineralogy, and economics. Springer, Berlin/ New York 2002, ISBN 3-540-43135-7.
- Mineral Commodity Profile: Indium der usgs mineral resources (engl.; PDF-Datei; 1,1 MB).
- K. H. Wedepohl: The composition of the continental crust. In: Geochimica et Cosmochimica Acta. 1995, 59, 7, 1217–1232.
- www.mindat.org/Indium.
- Webmineral – Indium, Elementinformationen und Mineralliste.
- Indium bei usgs mineral resources (2009) (PDF-Datei; 85 kB).
- Wilhelm Morawiez: Herstellung von hochreinem Indium durch Amalgam-Elektrolyse. In: Chemie Ingenieur Technik – CIT. 36, 6, 1964, S. 638–647.
- Lucien F. Trueb: Die chemischen Elemente, Ein Streifzug durch das Periodensystem. S. Hirzel Verlag Stuttgart/ Leipzig 1996, ISBN 3-7776-0674-X.
- Indium and Gallium Supply Sustainability September 2007 Update, 22nd EU PV Conference, Milan, Italy, 16. Februar 2009.
- Indium. (pdf) In: Mineral Commodity Summaries. U.S. Geological Survey, Januar 2020, abgerufen am 11. September 2020 (amerikanisches Englisch).
- Charles "Sky" Anderson: Indium Statistics and Information. In: National Minerals Information Center. U.S. Geological Survey, abgerufen am 11. September 2020 (amerikanisches Englisch).
- Indium bei usgs mineral resources (1996) (PDF-Datei; 12 kB).
- G. Bräuer: Transparent leitfähige Oxide -Eigenschaften, Herstellung und Anwendungsgebiete. (Memento vom 14. Juli 2014 im Internet Archive) Vortrag im Rahmen der Veranstaltung „Nano Surface: Industrielle Oberflächentechnik“ in Gießen am 19. Juli 2005.
- Roadmap Ressourceneffiziente Photovoltaik 2020+. (Memento vom 17. April 2012 im Internet Archive) Im Rahmen des vom BMBF geförderten Forschungsprojekts „Materialeffizienz und Ressourcenschonung (MaRess)“. Wuppertal, November 2010. ISSN 1867-0237.
- H. Steiger u. a.: (Zn,Mg)O als Teil der Fensterschicht für Chalkopyrit Solarzellen. Zusammenfassung im Rahmen des FVS-Workshops „TCO-Materialforschung“ 2002 des ForschungsVerbund Erneuerbare Energien.
- F. Fenske u. a.: Al-dotierte ZnO-Schichten für a-Si/c-Si Solarzellen. Zusammenfassung im Rahmen des FVS-Workshops „TCO-Materialforschung“ 2002 des ForschungsVerbund Erneuerbare Energien.
- Kurzbeschreibung des Forschungsvorhabens „Einsatz von Sekundärmaterial in der Herstellung von Chalkopyrit Photovoltaik (SECUMAT-CIS)“ im Rahmen der BMBF Förderinitiative „Validierung des Innovationspotenzials wissenschaftlicher Forschung“. (Memento vom 22. Dezember 2015 im Internet Archive)
- physikalische Eigenschaften des Indiums bei www.webelements.com.
- K. Takemura, H. Fujihaza: High-pressure structural phase transition in indium. In: Physical Review, Serie 3. B – Condensed Matter. 47, 1993, S. 8465–8470.
- J. Graham, A. Moore, G. V. Raynor: The effect of temperature on the lattice spacings of indium. In: Journal of the Institute of Metals. 84, 1954, S. 86–87.
- G. Audi, O. Bersillon, J. Blachot, A. H. Wapstra: The NUBASE evaluation of nuclear and decay properties. In: Nuclear Physics. Band A 729, 2003, S. 3–128. doi:10.1016/j.nuclphysa.2003.11.001. (PDF; 1,0 MB).
- J. A. Burdine: Indium-113m radiopharmaceuticals for multipurpose imaging. In: Radiology. Band 93, Nummer 3, September 1969, S. 605–610, doi:10.1148/93.3.605. PMID 5822736.
- M. L. Thakur: Gallium-67 and indium-111 radiopharmaceuticals. In: The International journal of applied radiation and isotopes. Band 28, Nummer 1–2, 1977 Jan-Feb, S. 183–201. PMID 67094 (Review).
- Physikalisch-Technische Bundesanstalt: Wärme- und Wärmestromkalibrierung Dynamischer Differenz-Kalorimeter.
- Dieter Weber: Bonding ceramic sputter targets to metal holders. Abgerufen am 19. Oktober 2014.
- Nigel Calder: The Transistor, 1948–58. In: New Scientist. 4, 86, 1958, S. 342–345 (eingeschränkte Vorschau in der Google-Buchsuche).
- N. N. Greenwood, A. Earnshaw: Chemie der Elemente. 1. Auflage. VCH Verlagsgesellschaft, 1988, ISBN 3-527-26169-9.
- G. H. Johnson, D. J. Bales, L. V. Powell: Clinical evaluation of high-copper dental amalgams with and without admixed indium. In: American journal of dentistry. Band 5, Nummer 1, Februar 1992, S. 39–41. PMID 1524741.
- Wolfram Schiffmann, Helmut Bähring, Udo Hönig: Technische Informatik 3: Grundlagen der PC-Technologie. Springer, 2011, ISBN 978-3-642-16811-6, S. 222 (eingeschränkte Vorschau in der Google-Buchsuche).
- https://www.handelsblatt.com/finanzen/maerkte/devisen-rohstoffe/gefragte-industriemetalle-wie-private-anleger-vom-geschaeft-mit-seltenen-erden-profitieren-koennen/25114070.html
- Hans Breuer: dtv-Atlas Chemie 1. Allgemeine und anorganische Chemie. Dtv, ISBN 3-423-03217-0.
- G. Ungváry, E. Szakmáry, E. Tátrai, A. Hudák, M. Náray, V. Morvai: Embryotoxic and teratogenic effects of indium chloride in rats and rabbits. In: J. Toxicol. Environ. Health A. 1, 59, 2000, S. 27–42. PMID 11261900.
- M. Nakajima u. a.: Comparative developmental toxicity study of indium in rats and mice. In: Teratog Carcinog Mutagen. 20/2000, S. 219–227. PMID 10910472.
- R. E. Chapin u. a.: The reproductive and developmental toxicity of indium in the Swiss mouse. In: Fundam Appl Toxicol. 27/1995, S. 140–148. PMID 7589924.
- M. Nakajima u. a.: Developmental toxicity of indium chloride by intravenous or oral administration in rats. In: Teratog Carcinog Mutagen. 18/1998, S. 231–238. PMID 9876012.
- M. Nakajima u. a.: Developmental toxicity of indium in cultured rat embryos. In: Teratog Carcinog Mutagen. 19/1999, S. 205–209. PMID 10379844.
- J. L. Zurita u. a.: Toxicological assessment of indium nitrate on aquatic organisms and investigation of the effects on the PLHC-1 fish cell line. In: Sci Total Environ. 387/2007, S. 155–165. PMID 17804041.
- Günter Bräuer: Transparent leitfähige Oxide – Eigenschaften, Herstellung und Anwendungsgebiete. (Memento vom 30. Januar 2012 im Internet Archive) (PDF-Datei; 1,5 MB) Dresden/Braunschweig/Gießen 2005.
- N. Barreau, S. Marsillac, D. Albertini, J.C. Bernede: Structural, optical and electrical properties of β-In2S3>-3xO3x thin films obtained by PVD. In: Thin Solid Films. 403–404, 2002, S. 331–334.
- Jianfang Wang, Mark S. Gudiksen, Xiangfeng Duan, Yi Cui, Charles M. Lieber: Highly Polarized Photoluminescence and Photodetection from Single Indium Phosphide Nanowires. In: Science. 293, 5534, 2001, S. 1455–1457.
- Organic Chemistry Portal: Indium als Reduktionsmittel. (englisch).
- Christoph Elschenbroich: Organometallchemie. 5. Auflage. Teubner, Wiesbaden, 2005, ISBN 3-519-53501-7.
