Lochfraßkorrosion
Lochfraßkorrosion, auch Lochkorrosion oder Lochfraß genannt, bezeichnet klein erscheinende Korrosionsstellen bzw. punktförmige Löcher in Materialoberflächen, insbesondere bei passivierten Metallen, die sich in der Tiefe trogförmig teils erheblich ausweiten. Lochfraßkorrosion bleibt wegen ihrer an der Oberfläche geringen Ausdehnung häufig lange unbemerkt.
Entstehung
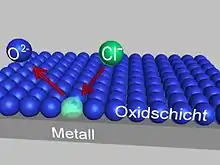
Während bei aktiven metallischen Werkstoffen, wie beispielsweise Baustählen, der metallische Abtrag durch Korrosion gleichmäßig erfolgt, tritt bei passivierten Metallen, die sich in einem chlorid- oder bromidhaltigen Elektrolyten befinden, an Fehlstellen der aus Oxiden bestehenden Passivschicht häufig eine punktförmige Korrosion auf. An diesen Fehlstellen, zum Beispiel durch eingelagerte Fremdmetallpartikel, wird aus der Oxidschicht des passivierten Metalls der Sauerstoff durch Chlorid- bzw. Bromidionen verdrängt. Durch Anlagerung von weiteren Chlorid- und Bromidionen entsteht ein Bereich, der nicht mehr durch eine Oxidschicht geschützt ist. Diese Stelle bietet nun einen Angriffspunkt für Korrosion.[1] Unter günstigen Umständen kann es zu einer sogenannten Repassivierung kommen: Das Chloridion wird wieder durch Sauerstoff verdrängt, die schützende Oxidschicht ist somit repariert.
Andernfalls schreitet die Lochkorrosion fort. Folgende Mechanismen fördern die Lochfraßkorrosion:
- Durch den geringen Lochdurchmesser gelangt wenig Sauerstoff in das Loch, wodurch die Repassivierung behindert wird. Da der Sauerstoffgehalt außerhalb des Lochs wesentlich größer ist als im Loch, bildet sich außerdem ein Konzentrationselement.
- Das kleine Loch bildet die Anode, die restliche Oberfläche die Kathode. Da die Korrosionsgeschwindigkeit durch das Flächenverhältnis von Kathode zu Anode bestimmt wird, schreitet die Reaktion mit großer Geschwindigkeit voran.
- Das gelöste Metall im Loch bildet z. B. mit Chloridionen Salze. Durch Hydrolyse entstehen Oxonium-Ionen, die den Elektrolyt im Loch ansäuern. Durch den abgesenkten pH-Wert erhöht sich das freie Korrosionspotential und damit die Korrosionsgeschwindigkeit.
Bedingungen
Kritische Bedingungen für das Auftreten von Lochkorrosion sind:
- hoher Chloridgehalt im korrosiven Medium
- hoher Sulfatgehalt (bei Kupferwerkstoffen)
- hohe Temperaturen
- niedriges Elektrodenpotential des Werkstoffs
- niedriger pH-Wert des Elektrolyten
- geringe Sauerstoffkonzentration im Elektrolyt (dadurch keine Repassivierung)
- niedrige Strömungsgeschwindigkeit des Mediums (z. B. in Wasserkreisläufen)
Vermeidung
Werkstoff
Werkstoffe, an denen Lochkorrosion auftreten kann, sind u. a. rostfreie Stähle (z. B. 1.4301, V2A), Kupferlegierungen in Wasserkreisläufen oder auch Aluminium- oder Magnesiumlegierungen.
Chrom-Nickel-Stähle werden beispielsweise durch Legieren mit Molybdän gegen Lochfraßkorrosion beständig gemacht. Durch den Molybdänzusatz wird die Passivschicht auf der Stahloberfläche stabilisiert und der Stahl kann schneller repassivieren. Lokale Chromverarmung, etwa durch zum Glühen gebrachte Chromcarbid-Bildung, kann diesen Schutz jedoch zerstören und führt zu interkristalliner Korrosion. Zur Vermeidung dieser „Sensibilisierung“ wurden sogenannte ELC-Stähle mit nur sehr geringem Kohlenstoffgehalt entwickelt, die somit keine Chromcarbide bilden können.
Besonders widerstandsfähige Werkstoffe sind 1.4362, 1.4404, 1.4462 und 1.4571.[2]
Sonderfall Glaskorrosion
Lochfraßkorrosion kann als Sonderphänomen auch bei der Verwitterung bestimmter historischer Gläser entstehen, wenn beim Schmelzprozess die Mischungsverhältnisse der Kalium-, Natrium- und Calciumanteile ungünstig gewählt wurden. Solche umweltsensitiven, auf Luftfeuchte in Kombination mit säurebildenden Luftschadstoffen reagierende Glasvarietäten gibt es beispielsweise bei mittelalterlichen Bleiglasfenstern.[3]
Einzelnachweise
- google.books Gustav Peter, René Muntwyler, Marc Ladner: Baustofflehre. Bau und Energie, vdf Hochschulverlag AG, 2. Auflage 2005, ISBN 978-3-7281-3005-1
- Werkstoffkorrosion durch Wasser
- Dieter R. Fuchs, Helmut Patzelt und Helmut K. Schmidt: Umweltbedingte Schädigungen an historischen Glasfenstern: Phänomene, Mechanismen, Konservierungskonzepte. In: Engin Bagda et al. (Hrsg.): Umwelteinflüsse auf Oberflächen: Belastungs- und Abbaumechanismen in Abhängigkeit von Umwelt- und Klimaeinflüssen. expert-Verlag, 1989. S. 174–192.
Literatur
- Horst Briehl: Chemie der Werkstoffe. 3. Auflage. Springer Fachmedien, Wiesbaden 2014, ISBN 978-3-658-06225-5.
- Georg Henkel, Benedikt Henkel, Jan Rau: Topographie und Morphologie funktionaler Edelstahloberflächen. Expert Verlag, Renningen 2008, ISBN 978-3-8169-2845-4.
Weblinks
- Korrosionsarten von Aluminium und seinen Legierungen (abgerufen am 7. September 2018)
- Lochfraßkorrosion und Lochmorphologie (abgerufen am 7. September 2018)
- Korrosion bei Edelstählen (abgerufen am 7. September 2018)
- Rostfreier Stahl und Korrosion (abgerufen am 7. September 2018)
- Korrosion an Edelstahl-Rohrleitungen (abgerufen am 7. September 2018)