Molybdän
Molybdän [molʏpˈdɛːn] (von griech. Μόλυβδος mólybdos für Blei) ist ein chemisches Element mit dem Elementsymbol Mo und der Ordnungszahl 42. Es zählt zu den Übergangsmetallen, im Periodensystem steht es in der 5. Periode sowie der 6. Nebengruppe (Gruppe 6) oder Chromgruppe.
| Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Molybdän, Mo, 42 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementkategorie | Übergangsmetalle | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe, Periode, Block | 6, 5, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aussehen | grau metallisch | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Nummer | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EG-Nummer | 231-107-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ECHA-InfoCard | 100.028.279 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 14 ppm[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomar [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 95,95(1)[3] u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | 145 (190) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 154 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronenkonfiguration | [Kr] 4d5 5s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 7.09243(4) eV[4] ≈ 684.32 kJ/mol[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 16.16(12) eV[4] ≈ 1559 kJ/mol[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 27.13(12) eV[4] ≈ 2618 kJ/mol[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 40.33(6) eV[4] ≈ 3891 kJ/mol[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Ionisierungsenergie | 54.417(19) eV[4] ≈ 5250 kJ/mol[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalisch [6] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aggregatzustand | fest | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | kubisch raumzentriert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte | 10,28 g/cm3 (20 °C)[7] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohshärte | 5,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetismus | paramagnetisch (χm = 1,2 · 10−4)[8] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 2896 K (2623 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 4885 K[9] (4612 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molares Volumen | 9,38 · 10−6 m3·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungsenthalpie | 617 kJ/mol[9] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzenthalpie | 36 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | 6190 m·s−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrische Leitfähigkeit | 18,2 · 106 A·V−1·m−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 139 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemisch [10] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationszustände | 2, 3, 4, 5, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Normalpotential | −0,152 V (MoO2 + 4e− + 4 H+ → Mo + 2 H2O) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativität | 2,16 (Pauling-Skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NMR-Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Geschichte
Molybdän, das in Lagerstätten in der Regel als Molybdänglanz (Molybdändisulfid) vorkommt, wurde lange Zeit mit Bleiglanz oder auch Graphit[12] verwechselt. 1778 gelang es Carl Wilhelm Scheele, aus Molybdänglanz durch Behandlung mit Salpetersäure das weiße Molybdän(VI)-oxid MoO3 (auch Molybdäntrioxid oder Wasserbleierde genannt) herzustellen. 1781 reduzierte Peter Jacob Hjelm das Oxid mit Kohle zum elementaren Molybdän. Wegen seiner schwierigen Bearbeitbarkeit (reines Molybdän lässt sich plastisch verformen, jedoch schon die Verunreinigung mit 1 ppm Sauerstoff oder Stickstoff lässt Molybdän stark verspröden) fand Molybdän lange Zeit keine Beachtung. Ende des 19. Jahrhunderts bemerkten Mitarbeiter des französischen Unternehmens Schneider & Co. bei der Herstellung von Panzerplatten die nützlichen Eigenschaften von Molybdän in Stahllegierungen. In den beiden Weltkriegen war die Nachfrage nach dem Metall groß, nach dem Zweiten Weltkrieg fielen die Preise dramatisch. Unterhalb der Alpeiner Scharte im Valsertal in Tirol, wo sich die bedeutendste Molybdänkonzentration der Ostalpen befindet, wurde im Zweiten Weltkrieg mit großem Aufwand ein Bergwerk angelegt, ohne dass jemals Molybdän gewonnen werden konnte.[13] Das einzige westeuropäische Bergwerk wurde bis 1973 in Knaben, Norwegen betrieben.
Vorkommen
Molybdän kommt meistens als Molybdänit (Molybdänglanz, MoS2) vor. Daneben gibt es noch Wulfenit (Gelbbleierz, PbMoO4) und Powellit Ca(Mo,W)O4. Zur Verhüttung gelangt überwiegend das durch den Kupferbergbau anfallende Koppelprodukt Molybdänit. Das MoS2-Konzentrat, wie es die Minen in Richtung „Röster“ verlässt, enthält rund 50–60 % Molybdän. Große Vorkommen finden sich in den Vereinigten Staaten, Chile, China, Kanada und Peru.
Molybdän in gediegener, das heißt elementarer Form konnte bisher (Stand: 2011) nur in vier Proben nachgewiesen werden: Auf der Erde in einer Gesteinsprobe vom Vulkan Korjakskaja Sopka auf der russischen Halbinsel Kamtschatka sowie in drei Gesteinsproben des Mondes vom Apollonius-Hochland (Luna 20), dem Mare Crisium (Luna 24) und dem Mare Fecunditatis (Luna 16).[14] Da die Entdeckungen allerdings ohne Prüfung durch die IMA/CNMNC veröffentlicht wurden, gilt der Status von Molybdän als Mineral bisher nicht als gesichert, auch wenn es die Mineral-System-Nr. 1.AC.05 (nach der 9. Auflage der Strunzʼschen Mineralsystematik) trägt.[15]
Gewinnung, Darstellung und Preis
Die Hauptmenge des Molybdäns wird als Nebenprodukt bei der Kupferherstellung gewonnen und nur ca. 30 % direkt aus Molybdänerzen. Alle Erze werden in der Hauptsache zu Ammoniumheptamolybdat umgearbeitet. Dieses wird durch Calcinieren bei ca. 400 °C in Molybdäntrioxid MoO3 überführt. Letzteres wird in zwei Stufen durch Wasserstoff zum reinen Molybdänpulver reduziert. Erste Stufe führt bei 500–600 °C zum metastabilen braunviolettem Molybdändioxid MoO2, die zweite Stufe führt bei ca. 1100 °C zum reinen Metallpulver.[16] Zum kompakten Metall wird Molybdän im HIP-Verfahren, durch Umschmelzen im Lichtbogenofen unter Argon als Schutzgas oder im Elektronenstrahlofen verdichtet. Einkristalle werden nach dem Zonenschmelzverfahren hergestellt. Die Molybdänrückgewinnung aus Schrott beträgt annähernd 100 %, da keine Oxidationsverluste auftreten.
Die Weltproduktion lag 2007 bei 211.000 Tonnen (2006 179.000 t).[17] 2007 erzeugten die USA – als größter Produzent – 62.000 Tonnen, China 60.000 t und Chile 45.000 t.[17] 2013 betrug die Gesamtmenge des produzierten Molybdäns 258.000 Tonnen; Hauptproduzenten waren China (101.000 t), die USA (60.700 t), Chile (38.700 t) und Peru (18.100 t). Der USGS gibt als Preise für Molybdän 34,83 USD je kg im Jahre 2010 und 22,85 USD je kg für 2013 an.[18] Die London Metal Exchange listete Molybdän im Laufe des Jahres 2018 für ca. 25 USD/kg.[19]
Eigenschaften

Molybdän ist ein Übergangsmetall der 5. Periode. Das hochfeste, zähe und harte Metall besitzt einen silbrigweißen Glanz. Von allen Elementen der 5. Periode besitzt es den höchsten Schmelzpunkt. Von nichtoxidierenden Säuren (auch Flusssäure) wird es ebenso wie das schwere Homologe Wolfram nicht angegriffen. Deshalb wird Molybdän in großen Mengen zur Herstellung von säurebeständigen Edelstählen und Nickelwerkstoffen eingesetzt. Oxidierende Säuren wie heiße konzentrierte Schwefelsäure, Salpetersäure oder Königswasser führen zu hohen Abtragsraten. Ebenso unbeständig ist Molybdän in oxidierenden Alkalischmelzen.
Verwendung
In kleinen Zusätzen dient es zur Härtung und zur Verhinderung der Anlassversprödung von Stahl. Mehr als zwei Drittel des hergestellten Molybdäns werden zur Erzeugung von Metalllegierungen wie Ferro-Molybdän verbraucht. Wolframverknappung im Ersten Weltkrieg führte zu vermehrtem Einsatz von Molybdän zur Herstellung von hochfesten Werkstoffen. Bis heute ist Molybdän ein Legierungselement zur Steigerung von Festigkeit, Korrosions- und Hitzebeständigkeit. Molybdänhaltige Hochleistungswerkstoffe wie Hastelloy®, Incoloy® oder Nicrofer® haben viele technische Verfahren erst möglich oder ökonomisch sinnvoll gemacht.
Molybdän wird wegen seiner hohen Temperaturbeständigkeit zur Herstellung von Teilen für extreme Anwendungsfälle wie in der Luft- und Raumfahrt oder Metallurgietechnik verwendet. In der Ölverarbeitung wird es als Katalysator zur Schwefelentfernung eingesetzt.
Molybdändisulfid ist aufgrund seiner Schichtstruktur ein ideales Schmiermittel, auch bei erhöhten Temperaturen. Es kann als Feststoff wie Graphit, aber auch suspendiert in herkömmlichen Schmierölen verwendet werden.
Auch in elektronischen Bauteilen ist Molybdän zu finden. In TFTs (Dünnschichttransistoren) dient es als leitende Metallschicht und auch bei Dünnschichtsolarzellen wird es als metallischer Rückleiter verwendet.
Molybdänfolien dienen als gasdichte Stromdurchleitung in Quarzglas, u. a. an Halogenglühlampen und Hochdruck-Gasentladungslampen.
In den gleichen Lampentypen können auch Molybdändrähte zum Einsatz kommen, wenn statt Quarzglas ein Glas (meist Aluminosilikatgläser) verwendet wird, das eine an Molybdän angepasste thermische Ausdehnung besitzt und somit für eine Glas-Metall-Verbindung in Frage kommt.
Molybdate werden zur Imprägnierung von Stoffen verwendet, um diese schwer entflammbar zu machen.
Molybdän findet auch in der Röntgendiagnostik als Targetmaterial in der Anode Verwendung. Röntgenröhren mit Molybdänanode werden wegen der niedrigeren Energie der Charakteristischen Röntgenstrahlung ( bei 17,4 keV und bei 19,6 keV im Vergleich zu 58/59,3 keV bzw. 67,0/67,2/69,1 keV von Wolfram) des Molybdäns v. a. bei der Untersuchung der weiblichen Brust (Mammographie) eingesetzt.
In der Nuklearmedizin wird Spalt-Molybdän in Technetium-99m-Generatoren eingesetzt. Das relativ langlebige 99Mo (HWZ 66 h) zerfällt hierbei innerhalb des RNG in 99mTc (Technetium, HWZ 6 h). Auf diese Weise kann dieses wichtige Technetium-Isotop direkt vor Ort für Untersuchungszwecke gewonnen werden.
Physiologie
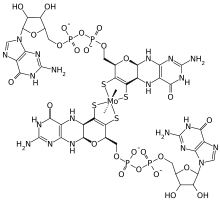
Als Spurenelement ist Molybdän für nahezu alle lebenden Organismen essenziell, da es wesentlicher Bestandteil des aktiven Zentrums einer ganzen Anzahl von Enzymen wie der Nitrogenase, Nitratreduktase oder Sulfitoxidase ist. Lebewesen nutzen molybdänhaltige Enzyme u. a. zur Purinzersetzung und Harnsäurebildung. Die bioverfügbare, d. h. die von Organismen aufgenommene Form von Molybdän ist das Molybdat-Ion MoO42−. Dieses wird in mehreren Schritten als Molybdän-Cofaktoren in die entsprechenden Enzyme eingebaut. Dort kann das Mo-Atom zwischen den Oxidationszahlen +IV, +V und +VI wechseln, und so Ein-Elektronen-Redoxreaktionen katalysieren.[20]
Molybdän ist für Pflanzen essenziell. Durch Molybdänmangel kann ein Boden unfruchtbar sein, was erklärt, warum eine Düngung mit Ammoniumheptamolybdat den Ertrag auf solchen Böden steigert. In Pflanzen und Tieren beträgt die Molybdänkonzentration einige ppm. Molybdän ist ein sehr wichtiges Spurenelement, vor allem für Leguminosen. Die mit den Leguminosen in Symbiose lebenden Bakterien (Knöllchenbakterien) sind in der Lage, mit einem molybdänhaltigen Enzym (Nitrogenase) Luftstickstoff zu binden. Sie benötigen Molybdän für zwei Prozesse: Fixierung von molekularem Stickstoff und Nitratreduktion.
Auch für die menschliche Ernährung ist Molybdän essenziell. Der Schätzwert der DGE für Jugendliche und Erwachsene geht von 50 bis 100 µg Molybdän als angemessene Tageszufuhr aus. Ein Molybdänmangel kommt bei normaler Ernährung nicht vor und ist deshalb extrem selten. Werden hohe Aufnahmen (10–15 mg/Tag) erreicht – zum Beispiel durch molybdänreiche Böden, so treten gichtähnliche Symptome, Gelenkschmerzen und Lebervergrößerungen auf.[21]
Der Molybdän-Cofaktor-Mangel tritt jedoch nur als Erbkrankheit auf; dabei ist eines der Enzyme mutiert, die die Biosynthese der Molybdän-Cofaktoren katalysieren.[22]
Verbindungen
Molybdän bildet in den Oxidationsstufen 2 bis 6 zahlreiche Verbindungen.[23] Am bekanntesten sind die vom Molybdän(VI)-oxid abgeleiteten Molybdate, wie beispielsweise unterschiedliche Ammoniummolybdate. Molybdän(IV)-oxid entsteht durch Reduktion von Molybdän(VI)-oxid. Peroxomolybdate lassen sich aus Molybdatlösungen und Wasserstoffperoxid herstellen und sind sehr reaktionsfähig. Molybdänblau ist eine Bezeichnung für unterschiedliche Molybdänoxidhydroxide.
| +6 | zwischen +6 und +5 | +4 |
|---|---|---|
| MoO3 | Mo4O11, Mo5O14, Mo8O23, Mo9O26, Mo17O47 | MoO2 |
Molybdän bildet mit Chlor mehrere Chloride in den Oxidationsstufen 2 bis 5. So erhält man MoCl5 durch Erhitzen von Molybdänpulver im Chlorstrom, MoCl4 durch Reduktion von MoCl5. Mit Fluor wird bevorzugt das Molybdän(VI)-fluorid gebildet. Daneben sind eine Reihe von Oxidfluoriden, wie das MoOF4, und Oxofluoromolybdate, wie K2[MoOF5], bekannt.
Mit Schwefel werden mehrere Molybdänsulfide gebildet: Darunter das Molybdän(IV)-sulfid und das Molybdän(VI)-sulfid, von dem sich Thiomolybdate ableiten lassen, wie das Ammoniumtetrathiomolybdat(VI) (NH4)2[MoS4].
Komplexverbindungen mit Cyaniden sind beispielsweise Oktacyanomolybdat(IV), wie K4[Mo(CN)8]. Thiocyanate bilden Hexathiocyanomolybdat(III)-Komplexe wie (NH4)3[Mo(SCN)6]. Molybdän bildet außerdem unterschiedliche Carbonylkomplexe, wie z. B. [Mo(CO)5]2− mit der Oxidationsstufe −2, und Carbonyle mit nullwertigem Molybdän, wie das Molybdänhexacarbonyl.
Sicherheitshinweise
Molybdänstaub und -verbindungen wie Molybdän(VI)-oxid und wasserlösliche Molybdate weisen eine leichte Toxizität auf, wenn sie inhaliert oder oral eingenommen werden.
Tests lassen vermuten, dass Molybdän im Gegensatz zu vielen anderen Schwermetallen relativ wenig toxisch wirkt. Akute Vergiftungen sind wegen der dazu notwendigen Mengen unwahrscheinlich. Im Bereich von Molybdänbergbau und -herstellung könnten höhere Molybdänexpositionen vorkommen. Bisher sind aber keine Krankheitsfälle bekannt geworden.
Obwohl natürliches Molybdän zu 9,63 % das radioaktive Isotop 100Mo enthält, sind normalerweise keine besonderen Sicherheitsvorkehrungen zum Strahlenschutz erforderlich. Auch in der praktischen Anwendung kann in der Regel auf eine Abschirmung verzichtet werden. Die Strahlung ist wegen der langen Halbwertszeit sehr schwach und kann nur mit hohem Aufwand gemessen werden.
Nachweis
Ein qualitativer Nachweis sechswertigen Molybdäns ist über die Bildung von Heteropolysäuren mit Phosphat möglich. Gibt man zu einer schwefelsauren molybdathaltigen Lösung Phosphorsäure, fällt kristallines Molybdängelb aus. Bei Zusatz des milden Reduktionsmittels Ascorbinsäure färbt sich die Lösung stark blau (Bildung von Molybdänblau). Bei geringeren Konzentrationen von Molybdat kommt es zu keiner Fällung, sondern nur einer Farbänderung der Lösung.
Diese Reaktionen werden auch zur photometrischen Bestimmung von Molybdat oder Phosphat im Spurenbereich eingesetzt. Molybdän kann alternativ mittels Atomspektrometrie bestimmt werden. In der Polarografie ergibt sechswertiges Molybdän in Schwefelsäure einer Konzentration von 0,5 mol/l zwei Stufen bei −0,29 und −0,84 V (gegen SCE). Diese sind auf Reduktion zum Mo(V) bzw. Mo(III) zurückzuführen.
Weblinks
- International Molybdenum Association – englischsprachige Seite mit zahlreichen Informationen und Links
Einzelnachweise
- Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Molybdän) entnommen.
- CIAAW, Standard Atomic Weights Revised 2013.
- Eintrag zu molybdenum in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: NIST, Gaithersburg, MD. doi:10.18434/T4W30F (https://physics.nist.gov/asd). Abgerufen am 11. Juni 2020.
- Eintrag zu molybdenum bei WebElements, https://www.webelements.com, abgerufen am 11. Juni 2020.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Molybdän) entnommen.
- N. N. Greenwood, A. Earnshaw: Chemie der Elemente. 1. Auflage. 1988, ISBN 3-527-26169-9, S. 1291.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9, S. E-129 bis E-145. Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337, doi:10.1021/je1011086.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Molybdän) entnommen.
- Eintrag zu Molybdän in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. April 2017. (JavaScript erforderlich)
- Vgl. auch Wilhelm Hassenstein, Hermann Virl: Das Feuerwerkbuch von 1420. 600 Jahre deutsche Pulverwaffen und Büchsenmeisterei. Neudruck des Erstdruckes aus dem Jahr 1529 mit Übertragung ins Hochdeutsche und Erläuterungen von Wilhelm Hassenstein. Verlag der Deutschen Technik, München 1941, S. 108 (Zwitter-Bleischweif, molybdaena<,> plumbago).
- SAGEN.at - Das Bergwerk unter der Alpeiner Scharte - Molybdänbergbau. Abgerufen am 7. März 2017.
- Mindat - Molybdenum (englisch).
- IMA/CNMNC List of Mineral Names - Molybdenum (englisch, PDF 1,8 MB, S. 191: Status (N) = published without approval by the CNMNC).
- Lucien F. Trueb: Die chemischen Elemente. Ein Streifzug durch das Periodensystem. S. Hirzel Verlag, Stuttgart/ Leipzig 1996, ISBN 3-7776-0674-X.
- Statistik bei der United States Geological Society (Molybdenum) (PDF; 60 kB).
- MINERAL COMMODITY SUMMARIES 2015. (PDF 2,3 MB, S. 106–107) USGS, abgerufen am 14. Oktober 2015 (englisch).
- lme.com - Historical price graph for Molybdenum. Abgerufen am 7. Juli 2018.
- G. Schwarz, R. R. Mendel, M. W. Ribbe: Molybdenum cofactors, enzymes and pathways. In: Nature. Band 460, Nr. 7257, 2009, S. 839–847, PMID 19675644.
- D-A-CH: Referenzwerte für die Nährstoffzufuhr, 2000.
- Jochen Reiss, Rita Hahnewald: Molybdenum cofactor deficiency: Mutations in GPHN, MOCS1, and MOCS2. In: Human Mutation. 32, 2011, S. 10–18, doi:10.1002/humu.21390.
- Heinrich Remy: Lehrbuch der Anorganischen Chemie. Band II, Akademische Verlagsgesellschaft Geest & Portig, Leipzig 1961, S. 200–208.
- Erwin Riedel, Christoph Janiak: Anorganische Chemie. 8. Auflage. Walter de Gruyter GmbH & Co. KG, Berlin 2011, ISBN 978-3-11-022566-2, S. 819.