Zinn
Zinn ist ein chemisches Element mit dem Elementsymbol Sn (lateinisch stannum) und der Ordnungszahl 50. Im Periodensystem steht es in der 5. Periode und in der 4. Hauptgruppe, bzw. 14. IUPAC-Gruppe oder Kohlenstoffgruppe. Das silberweiß glänzende und sehr weiche Schwermetall lässt sich mit dem Fingernagel ritzen. Zinn hat einen für Metalle sehr niedrigen Schmelzpunkt. Seine Hauptverwendung lag früher im Bereich der Herstellung von Geschirr, das von Zinngießern innerhalb der städtischen Handwerkszünfte bis ins 19. Jahrhundert als weit verbreitete Gebrauchs- und Ziergegenstände als Bestandteile der bürgerlichen Haushalte hergestellt wurden. Moderne Nutzung erfolgt im Bereich von Elektrolöten sowie im Verzinnen von lebensmittelechten Konserven oder auch in der Medizin. Historisch hat der Mensch Zinn zuerst als Beimengung zum Kupfer als Legierungsmittel zur Herstellung der Bronze genutzt.[14]
| Eigenschaften | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Zinn, Sn, 50 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementkategorie | Metalle | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe, Periode, Block | 14, 5, p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aussehen | silbrig glänzend (β-Zinn), grau (α-Zinn) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Nummer | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EG-Nummer | 231-141-8 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ECHA-InfoCard | 100.028.310 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 35 ppm[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomar [2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 118,710(7)[3] u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | 145 (145) pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 139 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van-der-Waals-Radius | 217 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronenkonfiguration | [Kr] 4d10 5s2 5p2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 7.343918(12) eV[4] ≈ 708.58 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 14.63307(9) eV[4] ≈ 1411.88 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 30.506(3) eV[4] ≈ 2943.4 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 40.74(4) eV[4] ≈ 3931 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Ionisierungsenergie | 77.03(4) eV[4] ≈ 7432 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalisch [6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aggregatzustand | fest | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | α-Zinn kubisch (Diamantstruktur) β-Zinn tetragonal (Strukturtyp A5) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte | 5,769 g/cm3 (20 °C) (α-Zinn)[7] 7,265 g/cm3 (20 °C) (β-Zinn)[7] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohshärte | 1,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetismus | α-Zinn diamagnetisch (χm = −2,3 · 10−5)[8] β-Zinn paramagnetisch (χm = 2,4 · 10−6)[8] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 505,08 K (231,93 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 2893 K[9] (2620 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molares Volumen | 16,29 · 10−6 m3·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungsenthalpie | 290 kJ·mol−1[9] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzenthalpie | 7,03[10] kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampfdruck | 5,78 · 10−21 Pa bei 505 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | 2500 m·s−1 bei 293,15 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Austrittsarbeit | 4,42 eV[11] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrische Leitfähigkeit | 8,69 · 106 A·V−1·m−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 67 W·m−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemisch [12] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationszustände | (−4), 4, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Normalpotential | −0,137 V (Sn2+ + 2 e− → Sn) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativität | 1,96 (Pauling-Skala) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotope | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NMR-Eigenschaften | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Etymologie
Das Wort Zinn (ahd., mhd. zin) ist vielleicht verwandt mit ahd. zein „Stab“, „Stäbchen“, „Zweig“ (siehe Zain). Der Duden weist in diesem Zusammenhang darauf hin, dass das Metall früher in Stabform gegossen wurde.[15] Eine andere Erklärung geht davon aus, dass das Hauptzinnerz Kassiterit (Zinnstein) auch in Form von Nadeln oder „Stäbchen“ auftritt.
Geschichte
Vorgeschichte
Die metallurgische Verarbeitung von Zinn begann etwas später als die von Kupfer. Während die Erschmelzung von Kupfer für die Vinča-Kultur auf 5400–4800 v. Chr. auf dem Balkan datiert wurde, ist diese für den Vorderen Orient auf dem Gebiet des heutigen Iran und der Türkei zwischen 5200 und 5000 v. Chr. erfolgt.[16] Die älteste datierte Legierung von Zinnbronze aus dem Zinnmineral Stannit wurde in der Ausgrabungsstätte Pločnik auf dem Gebiet des heutigen Serbien auf ca. 4650 v. Chr. datiert.[17][18] Im südtürkischen Taurusgebirge, wo auch Zinnerz abgebaut worden sein könnte, wurden das Bergwerk Kestel und die Verarbeitungsstätte Göltepe entdeckt und auf etwa 3000 v. Chr. datiert. Ob es sich hier um die Quelle des großen vorderasiatischen Zinnverbrauches handelte, bleibt vorläufig offen. Zinnbronzen, Gold und Kupfer wurden zuerst nur wegen ihrer Farbigkeit als Schmuck verwendet. Die ersten Metallschmiede der Vinča-Kultur wählten die zinnhaltigen Mineralien mutmaßlich wegen deren schwarz-grüner Färbung aus, die Ähnlichkeit zu manganreichen Kupfererzen besaßen. Den Metallschmieden der Zinnbronzen waren die spezifischen Eigenschaften des neuen Metalls bewusst, was aus den angewendeten Techniken bei der Verarbeitung der zinnreichen Erze abgeleitet werden kann.[19]
Am Ende des 3. Jahrtausends v. Chr. (botanische Datierungen auf 2021 und 2016 v. Chr.) ließen im Elbtal ansässige Eliten Jahr für Jahr in den Sommermonaten Zinngraupen an der Roten Weißeritz bei Schellerhau durchgraben. Die Arbeiter lebten in der Saison in einfachen Laubhütten, das Zinn wurde in die festen Siedlungen im Elbtal geschafft, welche dadurch prosperierten und zu Reichtum und Ansehen kamen. Das Erzgebirge entwickelte sich damals zu einem zentralen Lieferanten für ganz Europa. Zinn war für die Bronzeherstellung wesentlich. Die in Schellerhau vom Forschungsprojekt Archeo Montan entdeckten Spuren des Bergbaus sind die derzeit ältesten in Europa.[20]
Ägypten, vorderasiatische und asiatische Hochkulturen
Durch die Legierung Bronze, deren Bestandteile Kupfer und Zinn sind, gelangte Zinn zu größerer Bedeutung (Bronzezeit). Für Ägypten bestätigt sich die Verwendung von Zinn durch Funde kleiner Bronzestatuetten aus der Zeit der Pyramiden (4. Dynastie, um 2500 v. Chr.).[14] Auch in einem ägyptischen Grabmal aus der 18. Dynastie (um 1500 v. Chr.) wurden Gegenstände aus Zinn gefunden. In Indien war die Bronzeherstellung bereits um 3000 v. Chr. bekannt. Seit dem 2. Jahrtausend v. Chr. wurde Zinn in Mittelasien an der Route der späteren Seidenstraße nachweislich in größerem Maße in Bergwerken abgebaut. Ab etwa 1800 v. Chr. (Shang-Dynastie) ist Zinn in China bekannt. Ein Schriftwerk über die Künste jener Zeit, das Kaogong ji (Zhou-Dynastie, ab 1122 v. Chr.), beschreibt eingehend die Mischungsverhältnisse von Kupfer und Zinn, die je nach Art der für sakrale Gefäße, Gongs, Schwerter und Pfeilspitzen, Äxte oder Ackerbaugerät zu verwendenden Bronze verschieden waren. Bereits früher dürfte es in den eigentlichen asiatischen Lagerstätten in Yunnan und auf der Halbinsel Malakka bekannt gewesen sein. Im Tal des Euphrat wurden seit 2000 v. Chr. Bronzegeräte und deren Herstellung zu einem bedeutenden Kulturfaktor; die Technik wurde dann von Griechen und Römern weiterentwickelt.
Früher Handel: Vorder- und Mittelasien, Phönizier
Die Ausbreitung des Handels mit Zinn bestätigt ebenfalls seine frühe und weitreichende Nutzbarmachung. Es wurde zunächst aus Zentralasien mit Karawanen in die Gebiete des heutigen Nahen und Mittleren Ostens gebracht. Dort holte man sich das Zinnerz ab dem 3. Jahrtausend v. Chr. aus den Lagerstätten des alten Reiches Elam östlich des Tigris und aus den Bergen von Chorasan an der persischen Grenze zu Turkmenistan und Afghanistan. Von dort scheint man es in das Land der Pharaonen weitergeliefert zu haben. In der Bibel wird Zinn im 4. Buch Mose erstmals erwähnt (Numeri 31,22 ).
Die Phönizier hatten wahrscheinlich auf dem Seeweg Verbindungen mit den zinnreichen indischen Inseln Malakka und Bangka, ohne dass dazu genaue Angaben zu machen sind. Später transportierten die Phöniker das Zinnerz mit ihren Schiffen entlang der spanischen und französischen Küstengebiete bis zu den Inseln in der Nordsee. Auf diesen Fahrten entdeckten sie auf den sogenannten Zinninseln, zu denen möglicherweise die Insel Wight gehörte, und in den Bergen von Cornwall zinnreiche Gebiete, bauten dort das Erz ab und führten es in andere Länder aus. In kleinerem Maße begann der Zinnerzabbau in handelsmöglichen Ausmaßen auch in Frankreich (u. a. am Cap de l'Etain), in Spanien (Galicien) und in Etrurien (Cento Camerelle bei Campiglia Marittima).
Griechen und Römer
In den Epen Homers sowie bei Hesiod tauchen Zinneinlagen als Schmuckornament an Streitwagen und Wehrschilden des Agamemnon sowie des Herakles auf; für Achilles werden zinnerne (wohl »verzinnte«) Beinschienen beschrieben.[21] Durch Plautus wird Zinn erstmals als Geschirr für Speisen erwähnt.[22] Als Gebrauchsmetall für Geschirr war es bei den Griechen wohl nicht bekannt.[22] Das Zinn, das die Griechen für den Bronzeguss benutzten, stammte nach Herodot von den Kassiteriden, deren geographische Lage diesem aber unbekannt war. Diese Inseln werden auch von Strabon erwähnt und beschrieben, der sie weit nördlich von Spanien lokalisiert, in der Nähe Britanniens.[23]
Der römische Schriftsteller Plinius der Ältere nannte Zinn in seiner Naturgeschichte plumbum album („weißes Blei“); Blei hingegen war plumbum nigrum („schwarzes Blei“). Er beschreibt daneben auch das Verzinnen von Kupfermünzen und berichtet von zinnernen Spiegeln und Ampullen und beschreibt, dass Bleiwasserrohre mit Zinnlegierung verlötet wurden.[22] Die hohe Nachfrage nach dem in der Alchemie dem Jupiter zugeordneten Zinn[24] wird sogar als ein Grund für die römische Besetzung Britanniens angeführt. In der südwestlichen Region Cornwall wurde von 2100 v. Chr. bis 1998 Zinnerz gefördert, in der Antike ein wichtiger Zinnlieferant des Mittelmeerraums und bis ins späte 19. Jahrhundert der größte der Welt. Im Lateinischen heißt Zinn stannum, daher rührt auch das chemische Symbol (Sn).
Mittelalter
Während der Völkerwanderung erlahmte der bergmännische Abbau von Zinnerzen völlig. Nur wenige Kultgegenstände wurden noch gefertigt. Im Konzil von Reims (813) wird neben Gold und Silber ausdrücklich nur Zinn für die Herstellung solcher Gegenstände gestattet. Die Gräberfunde von Capetiennes bestätigen dies insofern, als es zur Zeit der ersten Kreuzzüge üblich war, Priester mit Zinnkelchen und Bischöfe wie auch Äbte mit Zinnkrummstäben beizusetzen.
Der Brauch, kleine Bildnisse aus Zinnlegierung, sogenannte Pilgerzeichen, auf der Brust zu tragen, stammt vermutlich ebenfalls aus der Zeit der Kreuzzüge. Je nach Region waren dies in Mittel- und Südfrankreich St. Denis bzw. St Nicolas, in England der Heilige Thomas von Canterbury. Die von den palästinischen Pilgerorten heimgebrachten religiösen Münzen und Ampullen, kleinen Glöckchen und Pfeifen waren aus Zinn. Sie mussten nach anerkanntem Vollzug der Pilgerfahrt zur Abwendung eventuellen Missbrauchs in Flüsse und Seen geworfen werden.[25]
Ab 1100 begann die Bevölkerung in Europa nach und nach das bisher aus Ton und Holz bestehende Essgeschirr durch solches aus dem stabileren Zinn zu ersetzen. Um 1200 begann in den größeren Städten die handwerkliche Verarbeitung des Zinns in Zinngießereien. Die Venezianer pflegten damals Handelsbeziehungen zu den zinnreichen indischen Inseln Malakka und Bangka.
Lange nachdem Bronze durch Eisen verdrängt worden war (Eisenzeit), erlangte Zinn Mitte des 19. Jahrhunderts durch die industrielle Herstellung von Weißblech von Neuem große Bedeutung.
Vorkommen


Primäre Zinnvorkommen umfassen Greisen-, hydrothermale Gang- und seltener auch Skarn- und Vulkanisch-exhalative-Lagerstätten (VHMS). Da das wirtschaftlich bedeutendste Zinnmineral Kassiterit SnO2, auch Zinnstein genannt, ein sehr stabiles Schwermineral ist, kommt ein großer Teil der Zinnproduktion auch aus sekundären Seifenlagerstätten. In einigen primären Lagerstätten besitzt auch das Sulfidmineral Stannit Cu2FeSnS4 Bedeutung für die Zinnproduktion. Auf primären Zinnlagerstätten kommt das Element oft mit Arsen, Wolfram, Bismut, Silber, Zink, Kupfer und Lithium vergesellschaftet vor.
Zur Gewinnung von Zinn wird das Erz zuerst zerkleinert und dann durch verschiedene Verfahren (Aufschlämmen, elektrische/magnetische Scheidung) angereichert. Nach der Reduktion mit Kohlenstoff wird das Zinn knapp über seine Schmelztemperatur erhitzt, so dass es ohne höher schmelzende Verunreinigungen abfließen kann. Heute gewinnt man einen Großteil durch Recycling und hier durch Elektrolyse.
In der kontinentalen Erdkruste ist es mit einem Anteil von etwa 2,3 ppm vorhanden.[26]
Die aktuellen Reserven für Zinn werden mit 4,7 Millionen Tonnen angegeben, bei einer Jahresproduktion von 289.000 Tonnen im Jahr 2015.[27] Zu über 80 % kommt die Produktion derzeit aus Seifenlagerstätten (Sekundärlagerstätten) an Flüssen sowie im Küstenbereich, vornehmlich aus einer Region beginnend in Zentralchina über Thailand bis nach Indonesien. Die größten Zinnvorkommen der Erde wurden 1876 im Kinta Valley (Malaysia) entdeckt. Dort wurden bis heute etwa 2 Millionen Tonnen geschürft.[28] Das Material in den Schwemmlandlagerstätten hat einen Metallanteil von etwa 5 %. Erst nach verschiedenen Schritten zur Konzentrierung auf etwa 75 % wird ein Schmelzprozess eingesetzt.
In Deutschland sind größere Ressourcen im Erzgebirge vorhanden, wo das Metall vom 13. Jahrhundert an bis 1990 gewonnen wurde. Beispiele sind die Greisenlagerstätte Altenberg und die Skarnlagerstätte Pöhla. Durch verschiedene Firmen findet derzeit auch Exploration auf Zinn im Erzgebirge statt. Im August 2012 veröffentlichte erste Untersuchungsergebnisse für die Orte Geyer und Gottesberg, einen Ortsteil von Muldenhammer, lassen Vorkommen in Höhe von rund 160.000 Tonnen Zinn für beide Orte insgesamt vermuten. Diese Zahlen bestätigen prinzipiell auch Angaben, wie sie nach zu DDR-Zeiten vorgenommenen Prospektionen geschätzt wurden. Nach Aussage der Deutschen Rohstoff AG handelt es sich um das weltweit größte noch unerschlossene Zinnvorkommen. Da einerseits der Erzgehalt mit 0,27 Prozent für Gottesberg und 0,37 Prozent für Geyer verhältnismäßig gering ist, andererseits das Erz verhältnismäßig schwer aus dem Gestein zu lösen ist, ist offen, ob sich der Abbau wirtschaftlich lohnen würde. Sollte es dazu kommen, würden als Nebenprodukt auch Zink, Kupfer und Indium anfallen.[29]
Die bedeutendste Fördernation für Zinn ist China, gefolgt von Indonesien und Myanmar. In Europa war 2009 Portugal der größte Produzent, wo es als Beiprodukt der VHMS Lagerstätte Neves Corvo gefördert wird.
Wirtschaftliche Bedeutung
Der Jahresweltverbrauch an Zinn liegt bei etwa 300.000 t. Davon werden etwa 35 % für Lote, etwa 30 % für Weißblech und etwa 30 % für Chemikalien und Pigmente eingesetzt. Durch die Umstellung der Zinn-Blei-Lote auf bleifreie Lote mit Zinnanteilen > 95 % wird der jährliche Bedarf um etwa 10 % wachsen. Die Weltmarktpreise steigen in den letzten Jahren kontinuierlich. So wurden an der LME (London Metal Exchange) 2003 noch etwa 5000 US-Dollar pro Tonne bezahlt, im Oktober 2021 jedoch mehr als 35.000 US-Dollar pro Tonne.[30][31] Die zehn größten Zinnverbraucher (2003) weltweit sind nach China auf Platz 1 die Länder USA, Japan, Deutschland, übriges Europa, Korea, übriges Asien, Taiwan, Großbritannien und Frankreich.
Die weltweite Finanzkrise ab 2007 sowie ein schwaches Wirtschaftswachstum in den Schwellen- und Entwicklungsländern setzte den Preis unter Druck. Im August 2015 sank der Preis je Tonne kurzfristig auf unter 14.000 US-Dollar. Im Oktober 2015 hatte der Preis sich wieder leicht auf rund 16.000 US-Dollar erholt. Durch den starken US-Dollar kommt der günstige Preis nur teilweise in vielen Verbraucherländern an.[32] Die weltweite Produktion lag 2011 bei rund 253.000 Tonnen, von denen alleine 110.000 Tonnen in China gefördert worden sind; weitere 51.000 Tonnen stammten aus Indonesien.
Kassiterit wurde von der US-amerikanischen Börsenaufsicht SEC als sogenanntes „conflict mineral“ eingestuft,[33] dessen Verwendung für Unternehmen gegenüber der SEC berichtspflichtig ist. Als Grund hierfür werden die Produktionsorte im Osten des Kongo angeführt, die von Rebellen kontrolliert werden und so im Verdacht stehen, bewaffnete Konflikte mitzufinanzieren.[34]
| Rang | Land | Fördermenge | Reserven | |||
|---|---|---|---|---|---|---|
| 2015 | 2009 (t) | 2009 | 2015 (t) | 2015 | 2017 (t) | |
| 1 | 115.000 | 40 % | 110.000 | 38 % | 1.100.000 | |
| 2 | 55.000 | 19 % | 52.000 | 18 % | 800.000 | |
| 3 | – | – | 34.300 | 12 % | 110.000 | |
| 4 | 13.000 | 4,5 % | 25.000 | 8,7 % | 700.000 | |
| 5 | 19.000 | 6,6 % | 20.000 | 6,9 % | 400.000 | |
| 6 | 37.500 | 13,0 % | 19.500 | 6,7 % | 100.000 | |
| 7 | 1.400 | 0,5 % | 7.000 | 2,4 % | 370.000 | |
| 8 | 9.400 | 3,3 % | 6.400 | 2,2 % | 110.000 | |
| 9 | 3.500 | 1,2 % | 5.400 | 1,9 % | 11.000 | |
| 10 | 2.380 | 0,8 % | 3.800 | 1,3 % | 250.000 | |
| 11 | – | – | 2.500 | 0,9 % | – | |
| 12 | – | – | 2.000 | 0,7 % | – | |
| 13 | – | – | 900 | 0,3 % | – | |
| 14 | 120 | 0,04 % | 100 | 0,03 % | 170.000 | |
| – | 1.200 | 0,4 % | – | – | 350.000 | |
| – | 30 | 0,01 % | – | – | – | |
| andere | 2.000 | 0,7 % | 100 | 0,03 % | 180.000 | |
| Summe | 260.000 | 100 % | 289.000 | 100 % | 4.700.000 | |
Eigenschaften

Zinn kann drei Modifikationen mit verschiedener Kristallstruktur und Dichte annehmen:
- α-Zinn (kubisches Diamantgitter, 5,75 g/cm3) ist unterhalb von 13,2 °C stabil und besitzt einen Bandabstand von EG = 0,1 eV. Damit wird es je nach Interpretation als Halbmetall oder Halbleiter eingeordnet. Seine Farbe ist grau.
- β-Zinn (verzerrt oktaedrisch, 7,31 g/cm3) bis 162 °C, Oberfläche silberweiß.
- γ-Zinn (rhombisches Gitter, 6,54 g/cm3) oberhalb von 162 °C oder unter hohem Druck.
Daneben kann noch eine zweidimensionale Modifikation namens Stanen (ähnlich der Kohlenstoffmodifikation Graphen) synthetisiert werden.
Natürliches Zinn besteht aus zehn verschiedenen stabilen Isotopen; das ist die größte Anzahl unter allen Elementen. Außerdem sind noch 28 radioaktive Isotope bekannt.
Die Rekristallisation von β-Zinn zu α-Zinn bei niedrigen Temperaturen äußert sich als die sogenannte Zinnpest.
Beim Verbiegen des relativ weichen Zinns, beispielsweise von Zinnstangen, tritt ein charakteristisches Geräusch, das Zinngeschrei (auch Zinnschrei), auf. Es entsteht durch die Reibung der β-Kristallite aneinander. Das Geräusch tritt jedoch nur bei reinem Zinn auf. Bereits niedrig legiertes Zinn zeigt diese Eigenschaft nicht; z. B. verhindern geringe Beimengungen von Blei oder auch Antimon das Zinngeschrei. Das β-Zinn hat einen abgeflachten Tetraeder als Raumzellenstruktur, aus dem sich zusätzlich zwei Verbindungen ausbilden.
Durch die Oxidschicht, mit der Zinn sich überzieht, ist es sehr beständig. Von konzentrierten Säuren und Basen wird es allerdings unter Entwicklung von Wasserstoffgas zersetzt. Jedoch ist Zinn(IV)-oxid ähnlich inert wie Titan(IV)-oxid. Zinn wird von unedleren Metallen (z. B. Zink) reduziert; dabei scheidet sich elementares Zinn schwammig oder am Zink haftend ab.
Isotope
Zinn besitzt insgesamt zehn natürlich vorkommende Isotope. Diese sind 112Sn, 114Sn, 115Sn, 116Sn, 117Sn, 118Sn, 119Sn, 120Sn, 122Sn und 124Sn. 120Sn ist dabei mit 32,4 % Anteil an natürlichem Zinn das häufigste Isotop. Von den instabilen Isotopen ist 126Sn mit einer Halbwertszeit von 230.000 Jahren das langlebigste.[36] Alle anderen Isotope haben eine Halbwertzeit von nur maximal 129 Tagen, jedoch existiert bei 121Sn ein Kernisomer mit 44 Jahren Halbwertzeit.[36] Als Tracer werden am häufigsten die Isotope 113Sn, 121Sn, 123Sn und 125Sn verwendet. Zinn hat als einziges Element drei stabile Isotope mit ungerader Massenzahl und mit zehn stabilen Isotopen die meisten stabilen Isotope von allen Elementen überhaupt.
Nachweis
Als qualitative Nachweisreaktion für Zinnsalze wird die Leuchtprobe durchgeführt: Die Lösung wird mit ca. 20%iger Salzsäure und Zinkpulver versetzt, wobei naszierender Wasserstoff frei wird. Der naszierende, atomare Wasserstoff reduziert einen Teil des Zinns bis zum Stannan SnH4. In diese Lösung wird ein Reagenzglas eingetaucht, das mit kaltem Wasser und Kaliumpermanganatlösung gefüllt ist; das Kaliumpermanganat dient hier nur als Kontrastmittel. Dieses Reagenzglas wird im Dunkeln in die nichtleuchtende Bunsenbrennerflamme gehalten. Bei Anwesenheit von Zinn entsteht sofort eine typisch blaue Fluoreszenz, hervorgerufen durch SnH4.[1][37]
Zur quantitativen Bestimmung von Zinn eignet sich die Polarographie. In 1 ᴍ Schwefelsäure ergibt Zinn(II) eine Stufe bei −0,46 V (gegen Kalomelelektrode, Reduktion zum Element). Stannat(II) lässt sich in 1 ᴍ Natronlauge zum Stannat(IV) oxidieren (−0,73 V) oder zum Element reduzieren (−1,22 V).[38] Im Ultraspurenbereich bieten sich die Graphitrohr- und Hydridtechnik der Atomspektroskopie an. Bei der Graphitrohr-AAS werden Nachweisgrenzen von 0,2 µg/l erreicht. In der Hydridtechnik werden die Zinnverbindungen der Probelösung mittels Natriumborhydrid als gasförmiges Stannan in die Quarzküvette überführt. Dort zerfällt das Stannan bei ca. 1000 °C in die Elemente, wobei der atomare Zinndampf spezifisch die Sn-Linien einer Zinn-Hohlkathodenlampe absorbiert. Hier sind 0,5 µg/l als Nachweisgrenze angegeben worden.[39]
Weitere qualitative Nachweisreagenzien sind Diacetyldioxim, Kakothelin, Morin und 4-Methylbenzol-1,2-dithiol. Zinn kann auch mikroanalytisch über die Bildung von Goldpurpur nachgewiesen werden.[40]
Biologische Wirkung
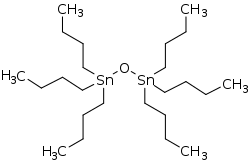
Metallisches Zinn ist auch in größeren Mengen an sich ungiftig. Die Giftwirkung einfacher Zinnverbindungen und Salze ist gering. Einige organische Zinnverbindungen dagegen sind hochtoxisch. Die Trialkyl-Zinnverbindungen (insbesondere TBT, engl. „Tributyltin“, Tributylzinn) und Triphenylzinn wurden mehrere Jahrzehnte in Anstrichfarben für Schiffe verwendet, um die sich an den Schiffsrümpfen festsetzenden Mikroorganismen und Muscheln abzutöten. Dadurch kam es in der Umgebung von großen Hafenstädten zu hohen Konzentrationen an TBT im Meerwasser, die die Population diverser Meereslebewesen bis heute beeinträchtigen. Die toxische Wirkung beruht auf der Denaturierung einiger Proteine durch die Wechselwirkung mit dem Schwefel aus Aminosäuren wie beispielsweise Cystein.
Verwendung
Traditionelle Verwendung und traditionelle Berufe



Seit Jahrhunderten wird reines Zinnblech großflächig zur Herstellung als Orgelmetall im Sichtbereich verwendet. Diese behalten ihre silbrige Farbe über viele Jahrzehnte. Das weiche Metall wird aber in der Regel in einer Legierung mit Blei, dem sogenannten Orgelmetall, verwendet und hat für die Klangentfaltung sehr gute vibrationsdämpfende Eigenschaften. Zu tiefe Temperaturen sind wegen der Umwandlung in α-Zinn für Orgelpfeifen schädlich; siehe Zinnpest. Viele Haushaltsgegenstände, Zinngerät (Geschirr), Tuben, Dosen und auch Zinnfiguren wurden früher ganz aus Zinn gefertigt, rundweg der einfacheren Verarbeitungstechnologie der Zeit entsprechend. Mittlerweile jedoch wurde das relativ kostbare Material meist durch preiswertere Alternativen ersetzt. Ziergegenstände und Modeschmuck werden weiterhin aus Zinnlegierungen, Hartzinn bzw. Britanniametall hergestellt.
Seit dem Mittelalter war der Zinngießer ein spezieller Handwerksberuf, der sich bis heute, allerdings in ganz geringem Umfang, erhalten hat. Er ist heute rechtlich in der Berufsbezeichnung Metall- und Glockengießer/-in aufgegangen. Aufgabe des Zinnputzers war die Reinigung von vor allem oxidierten, aus Zinn gefertigten Gegenständen mit einem Kaltwasserauszug des Ackerschachtelhalms, der volkstümlich deshalb auch Zinnkraut genannt wurde. Es war ein eher wenig angesehenes Wandergewerbe und wurde in den Häusern bürgerlicher oder großbäuerlicher Haushalte ausgeübt.
Heutige Verwendung
Als Legierungsbestandteil wird Zinn vielfältig verwendet, mit Kupfer zu Bronze oder anderen Werkstoffen legiert. Nordisches Gold, die Legierung der goldfarbigen Euromünzen, beinhaltet unter anderem 1 % Zinn. Algerisches Metall enthält 94,5 % Zinn.
Als Bestandteil von Metall-Legierungen mit niedrigem Schmelzpunkt ist Zinn unersetzlich. Weichlot (sogenanntes Lötzinn) zur Verbindung elektronischer Bauteile (beispielsweise auf Leiterplatten) wird mit Blei (eine typische Mischung ist etwa 63 % Sn und 37 % Pb) und anderen Metallen in geringerem Anteil legiert. Die Mischung schmilzt bei etwa 183 °C. Seit Juli 2006 darf jedoch kein bleihaltiges Lötzinn in elektronischen Geräten mehr verwendet werden (siehe RoHS); man setzt nun bleifreie Zinnlegierungen mit Kupfer und Silber ein, z. B. Sn95.5Ag3.8Cu0.7 (Schmelztemperatur ca. 220 °C).
Da man aber diesen Legierungen nicht traut (Zinnpest und „Tin whiskers“), ist bei der Fertigung elektronischer Baugruppen für Medizintechnik, Sicherheitstechnik, Messgeräte, Luft- u. Raumfahrt sowie für militärische/polizeiliche Verwendung weiterhin die Verwendung bleihaltiger Lote zulässig. Im Gegenteil ist der Einsatz bleifreien Lotes in diesen sensiblen Bereichen trotz RoHS verboten.
Hochreine Zinn-Einkristalle eignen sich auch zur Herstellung von elektronischen Bauteilen.
In der Floatglasherstellung schwimmt die zähflüssige Glasmasse bis zur Erstarrung auf einer spiegelglatten flüssigen Zinnschmelze.
Zinnverbindungen werden dem Kunststoff PVC als Stabilisatoren beigemischt. Tributylzinn dient als sog. Antifouling-Zusatz in Anstrichstoffen für Schiffe und verhindert den Bewuchs der Schiffskörper, es ist mittlerweile jedoch umstritten und weitgehend verboten.
In Form einer transparenten Zinnoxid-Indiumoxid-Verbindung ist es elektrischer Leiter in Anzeigegeräten wie LC-Displays. Das reine, weiße, nicht sehr harte Zinndioxid besitzt eine hohe Lichtbrechung und wird im optischen Bereich und als mildes Poliermittel eingesetzt. In der Zahnheilkunde wird Zinn auch als Bestandteil von Amalgamen zur Zahnfüllung eingesetzt. Die sehr toxischen organischen Zinnverbindungen finden als Fungizide oder Desinfektionsmittel Verwendung.
Zinn wird anstelle von Blei auch zum Bleigießen verwendet. Stannum metallicum („metallisches Zinn“) findet auch bei der Herstellung von homöopathischen Arzneimitteln sowie als Bandwurmgegenmittel Verwendung.
Unter der Bezeichnung Argentin wurde Zinnpulver früher zur Herstellung von unechtem Silberpapier und unechter Silberfolie verwendet.
Weißblech ist verzinntes Eisenblech, es wird beispielsweise für Konservendosen oder Backformen verwendet. Tin, das englische Wort für Zinn, ist gleichzeitig ein englisches Wort für Dose bzw. Konservenbüchse.
Zu dünner Folie gewalzt nennt man es auch Stanniol, das beispielsweise für Lametta Verwendung findet. Jedoch ist Zinn im 20. Jahrhundert durch das viel preiswertere Aluminium verdrängt worden. Bei manchen Farbtuben und Weinflaschenverschlüssen findet Zinn ebenfalls Verwendung.
Zinn wird in der EUV-Lithografie zur Herstellung von integrierten Schaltkreisen („Chips“) – als notwendiger Bestandteil bei der Erzeugung von EUV-Strahlung durch Zinn-Plasma – eingesetzt.[41]
Verbindungen
Zinnverbindungen kommen in den Oxidationsstufen +II und +IV vor. Zinn(IV)-Verbindungen sind stabiler, da Zinn ein Element der 4. Hauptgruppe ist und zudem der Effekt des inerten Elektronenpaares noch nicht so stark ausgeprägt ist wie bei den schwereren Elementen dieser Gruppe, z. B. dem Blei. Zinn(II)-Verbindungen lassen sich deshalb leicht in Zinn(IV)-Verbindungen umsetzen. Viele Zinnverbindungen sind anorganischer Natur, es ist aber auch eine Reihe von zinnorganischen Verbindungen (Zinnorganylen) bekannt.
Oxide und Hydroxide
- Zinn(II)-oxid SnO

- Zinn(II,IV)-oxid Sn2O3
- Zinn(IV)-oxid SnO2
- Zinn(II)-hydroxid Sn(OH)2
- Zinn(IV)-hydroxid Sn(OH)4, CAS-Nummer: 12054-72-7
Halogenide
- Zinn(II)-fluorid SnF2
- Zinn(II)-chlorid SnCl2
- Zinn(IV)-chlorid SnCl4
- Zinn(IV)-bromid SnBr4
- Zinn(II)-iodid SnI2
- Zinn(IV)-iodid SnI4
Salze
- Zinn(II)-sulfat SnSO4
- Zinn(IV)-sulfat Sn(SO4)2
- Zinn(II)-nitrat Sn(NO3)2
- Zinn(IV)-nitrat Sn(NO3)4
- Zinn(II)-oxalat Sn(COO)2
- Zinn(II)-pyrophosphat Sn2P2O7
- Zinkhydroxystannat ZnSnO3 · 3 H2O, CAS-Nummer: 12027-96-2
Chalkogenide
- Zinn(II)-sulfid SnS
- Zinn(IV)-sulfid SnS2
- Zinn(II)-selenid SnSe
Organische Zinnverbindungen
- Dibutylzinndilaurat (DBTDL) C32H64O4Sn
- Dibutylzinnoxid (DBTO) (H9C4)2SnO
- Dibutylzinndiacetat C12H24O4Sn, CAS-Nummer: 1067-33-0
- Diphenylzinndichlorid C12H10Cl2Sn
- Tributylzinnhydrid C12H28Sn
- Tributylzinnchlorid (TBTCL) (C4H9)3SnCl
- Tributylzinnfluorid (TBTF) C12H27FSn, CAS-Nummer: 1983-10-4
- Tributylzinnsulfid (TBTS) C24H54SSn2, CAS-Nummer: 4808-30-4
- Tributylzinnoxid (TBTO) C24H54OSn2
- Triphenylzinnhydrid C18H16Sn
- Triphenylzinnhydroxid C18H16OSn
- Triphenylzinnchlorid C18H15ClSn
- Tetramethylzinn C4H12Sn
- Tetraethylzinn C8H20Sn
- Tetrabutylzinn C16H36Sn
- Tetraphenylzinn (H5C6)4Sn
Weitere Verbindungen
- Stannan SnH4
- Natriumstannat Na2SnO3
- Kaliumstannat K2SnO3, CAS-Nummer: 12142-33-5
- Zinndifluorborat Sn(BF4)2, CAS-Nummer: 13814-97-6
- Zinn(II)-2-ethylhexanoat Sn(OOCCH(C2H5)C4H9)2
- Zinn(II)-oleat Sn(C17H34COO), CAS-Nummer: 1912-84-1
- Zinntellurid SnTe
- Indiumzinnoxid, ein Mischoxid üblicherweise aus 90 % Indium(III)-oxid (In2O3) und 10 % Zinn(IV)-oxid (SnO2)
Eine Übersicht über weitere Zinnverbindungen bietet die Kategorie:Zinnverbindung.
Literatur
- Ludwig Mory, E. Pichelkastner, B. Höfler: Bruckmann’s Zinn-Lexikon. München 1977, ISBN 3-7654-1361-5.
- Vanessa Brett: Zinn. Herder, Freiburg 1983, ISBN 3-451-19715-4.
- K. A. Yener, A. Adriaens, B. Earl, H. Özbal: Analyses of Metalliferous Residues, Crucible Fragments, Experimental Smelts, and Ores from Kestel Tin Mine and the Tin Processing Site of Göltepe, Turkey. In: P. T. Craddock, J. Lang (Hrsg.): Mining and Metal Production Through The Ages. The British Museum Press, London 2003, ISBN 0-7141-2770-1, S. 181–197.
Weblinks
Einzelnachweise
- Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Zinn) entnommen.
- CIAAW, Standard Atomic Weights Revised 2013.
- Eintrag zu tin in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: NIST, Gaithersburg, MD. doi:10.18434/T4W30F (https://physics.nist.gov/asd). Abgerufen am 11. Juni 2020.
- Eintrag zu tin bei WebElements, https://www.webelements.com, abgerufen am 11. Juni 2020.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Zinn) entnommen.
- N. N. Greenwood, A. Earnshaw: Chemie der Elemente. 1. Auflage. VCH, Weinheim 1988, ISBN 3-527-26169-9, S. 482.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Properties of the Elements and Inorganic Compounds, S. 4-142 – 4-147. Die Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337, doi:10.1021/je1011086.
- G. G. Graf: Tin, Tin Alloys, and Tin Compounds. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag, Weinheim 2005, doi:10.1002/14356007.a27_049.
- Ludwig Bergmann, Clemens Schaefer, Rainer Kassing: Lehrbuch der Experimentalphysik. Band 6: Festkörper. 2. Auflage. Walter de Gruyter, Berlin 2005, ISBN 3-11-017485-5, S. 361.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Zinn) entnommen.
- Eintrag zu Zinn, Pulver in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. April 2017. (JavaScript erforderlich)
- Ludwig Mory: Schönes Zinn – Geschichte Formen und Probleme. Bruckmann, München 1977, ISBN 3-7654-1416-6, S. 11.
- Zinn bei Duden online.
- Miljana Radivojević, Thilo Rehren, Ernst Pernicka, Dušan Šljivar, Michael Brauns, Dušan Borić: On the origins of extractive metallurgy: new evidence from Europe. In: Journal of Archaeological Science. Volume 37, Issue 11, November 2010, S. 2775–2787 (PDF)
- Miljana Radivojević, Thilo Rehren, Julka Kuzmanović-Cvetković, Marija Jovanović, Peter Northover: Tainted ores and the rise of tin bronzes in Eurasia, c. 6500 years ago. In: Antiquity. Volume 87, Issue 338, Dezember 2013, S. 1030–1045. (PDF)
- Miljana Radivojević, Thilo Rehren, Julka Kuzmanović-Cvetković, Marija Jovanović: Why are there tin bronzes in the 5th millenium Balkans? In: Selena Vitezović, Dragana Antonović (Hrsg.): Archaeotechnology: studying Technology from prehistory to the Middle Ages. Srpsko Arheološko Društvo, Belgrad 2014, S. 235–256 (Academia.edu)
- Miljana Radivojević, Thilo Rehren, Julka Kuzmanović-Cvetković, Marija Jovanović, J. Peter Northover: Tainted ores and the rise of tin bronzes in Eurasia, c. 6500 years ago. 2015, S. 1041.
- Sachsens Geschichte begann viel früher als gedacht. Forscher finden im Erzgebirge einen jahrtausendealten Bergbau. Die Geschichte Sachsens muss umgeschrieben werden. In: Sächsische Zeitung vom 2. November 2018 (abgerufen am 2. November 2018).
- Homer: Ilias 18, 613.
- Ludwig Mory: Schönes Zinn – Geschichte Formen und Probleme. Bruckmann, München 1977, ISBN 3-7654-1416-6, S. 12.
- Strabon: Geografie. 3,5,14.
- Jörg Barke: Die Sprache der Chymie: am Beispiel von vier Drucken aus der Zeit zwischen 1574-1761. (= Germanistische Linguistik. 111). Tübingen 1991, S. 385.
- Ludwig Mory: Schönes Zinn – Geschichte Formen und Probleme. Bruckmann, München 1977, ISBN 3-7654-1416-6, S. 13.
- K. H. Wedepohl: The composition of the continental crust. In: Geochimica et Cosmoschimica Acta. 59/7, 1995, S. 1217–1232; doi:10.1016/0016-7037(95)00038-2.
- USGS – Tin Statistics and Information – Mineral Commodity Summaries 2017 (PDF-Datei; 29 kB).
- Tin chapter (Memento vom 24. November 2015 im Internet Archive) (PDF-Datei; 2,56 MB), S. 112.
- Christoph Seidler: Probebohrung bestätigt riesiges Zinnvorkommen. In: Spiegel online. 30. August 2012, abgerufen am gleichen Tage.
- London Metal Exchange: Tin Prices (Memento vom 14. Mai 2008 im Internet Archive) Abgerufen am 24. November 2015.
- The London Metal Exchange: LME Tin | London Metal Exchange. Abgerufen am 27. Oktober 2021 (britisches Englisch).
- Zinnpreis je Tonne.
- SEC, Conflict Minerals – Final Rule (2012), S. 34–35. (PDF, 1,96 MB, engl.)
- SEC Adopts Rule for Disclosing Use of Conflict Minerals (engl.), abgerufen am 3. September 2012.
- USGS – Tin Statistics and Information – Mineral Commodity Summaries 2011 (PDF-Datei; 27 kB).
- G. Audi, O. Bersillon, J. Blachot, A. H. Wapstra: The NUBASE evaluation of nuclear and decay properties. In: Nuclear Physics. Band A 729, 2003, S. 3–128. doi:10.1016/j.nuclphysa.2003.11.001. (PDF; 1,0 MB).
- Im Lehrbuch der analytischen und präparativen anorganischen Chemie wird als Ursache der Leuchterscheinung eine – wahrscheinlich unzutreffende – Reduktion zu Zinn(II)-chlorid SnCl2 genannt.
Jander, Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie. 2006, ISBN 3-7776-1388-6, S. 499. - J. Heyrovský, J. Kůta: Grundlagen der Polarographie. Akademie-Verlag, Berlin 1965, S. 516.
- K. Cammann (Hrsg.): Instrumentelle Analytische Chemie. Spektrum Akademischer Verlag, Heidelberg/ Berlin 2001, S. 4–47.
- Eintrag zu Zinn. In: Römpp Online. Georg Thieme Verlag, abgerufen am 19. März 2014.
- Christian Wagner, Noreen Harned: EUV lithography: Lithography gets extreme. In: Nat Photon. Band 4, Nr. 1, 2010, S. 24–26, doi:10.1038/nphoton.2009.251.
-chloride-xtal-1996-3D-balls-front.png.webp)
-iodide-sample.jpg.webp)