Fluoride
Fluoride sind die Salze der Fluorwasserstoffsäure (HF), die auch als Flusssäure bekannt ist. Sie enthalten in ihrem Ionengitter als negative Gitterbausteine (Anionen) Fluorid-Ionen (F−). Daneben werden auch kovalente, nicht-ionische Verbindungen von Nichtmetallen sowie organische Fluorverbindungen wie etwa die Fluorkohlenwasserstoffe oder Carbonsäurederivate veraltet und falsch als Fluoride bezeichnet. Auch die sog. Sauerstofffluoride haben mit salzartigen Fluoriden nichts zu tun und auch nichts mit Oxiden, denn in ihnen hat der Sauerstoff keine negative, sondern eine positive Oxidationszahl.
Natürliches Vorkommen
Fluoride kommen in Form vieler Mineralien in der Natur und im menschlichen Körper vor. Wichtigster Vertreter ist der Fluorit (CaF2), ferner Yttrofluorit, ein Additions-Mischkristall mit YF3, und Cerfluorit (auch Yttrocerit), der neben Yttrium noch Cer, Erbium und Hydratwasser enthält. Weitere Fluoride sind Frankdicksonit (BaF2), Gagarinit (NaCaYF6), Tysonit (auch Fluocerit, (Ce,La,Se)F3) und Neighborit (NaMgF3). Komplexe Fluoride enthalten ein weiteres Element innerhalb eines Anion-Komplexes, wie etwa Bor, Aluminium oder Silicium, und bilden dann z. B. Hexafluorosilikate oder Tetrafluorborate. Vertreter sind hier das Ferruccit (NaBF4), Avogadrit ((K,Cs)BF4), Malladrit (Na2SiF6), Hieratit (K2SiF6), Kryolithionit (Na3Al2Li3F12), Kryolith (Na3AlF6), Elpasolith (K2Na[AlF6]), Jarlit (NaSr2[AlF6]2), Usovit (Ba2Mg[AlF6]2) und Weberit (Na2MgAlF7).[1]
Anorganische Fluoride
Wichtige salzartige Fluoride
Einige wichtige Fluoride sind:
- Aluminiumfluorid (AlF3)
- Ammoniumfluorid (NH4F)
- Calciumfluorid (CaF2, Fluorit oder Flussspat)
- Natriumfluorid (NaF)
- Zinn(II)-fluorid (SnF2)
Hydrogendifluoride

Neben den einfachen Fluoriden existieren auch Hydrogendifluoride der Zusammensetzung Me+[HF2]−, wie etwa Natriumhydrogendifluorid (NaHF2) und Kaliumhydrogendifluorid (KHF2). Diese enthalten das lineare [FHF]−-Anion. Darstellung ist aus wässrigen Lösungen der Fluoride unter Anwesenheit eines Überschusses Fluorwasserstoff (HF) möglich. Beim Erhitzen spalten die Hydrogendifluoride den Fluorwasserstoff wieder ab.[1]
Darstellung:
Zersetzung durch Erhitzen:
Auch molekular aufgebaute anorganische Fluorverbindungen wie die Hexafluoride Platin(VI)-fluorid, Uran(VI)-fluorid oder Plutonium(VI)-fluorid werden häufig als Fluoride bezeichnet.
Organische Fluoride
In den meisten organischen Fluoriden ist das Fluoratom kovalent gebunden, Beispiele:
- Sarin (C4H10FO2P),
- Tetrafluormethan (CF4)
- Trifluormethan (CHF3)
- Chlordifluormethan (CHClF2)
Es gibt jedoch auch organische Fluorverbindungen in denen das Fluoratom salzartig als Fluorid-Anion enthalten ist. Beispiele:
Nachweis
Physikalische Analyseverfahren
Professionell werden heute Fluoride in Mineralien und Feststoffen mit Röntgenfluoreszenzanalyse, Röntgenbeugung oder Massenspektrometrie bestimmt, in Flüssigkeiten mit Fluorid-Elektroden, IR- oder NMR-Verfahren.
Nasschemisch
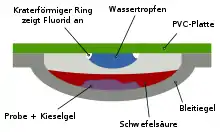
Mit einfachen Labormethoden lässt sich Fluorid durch den Bleitiegeltest oder die Ätzprobe nachweisen. Versetzt man eine fluoridhaltige Probe mit Schwefelsäure, so entsteht Fluorwasserstoff, der das Glasbehältnis anätzt.
Gibt man die Probe in einen Bleitiegel mit gepulverter Kieselsäure oder Natriumsilicat und überschichtet anschließend mit Schwefelsäure, so bildet sich Siliciumtetrafluorid-Gas:
Der Tiegel wird wieder verschlossen und die Abdeckung mit Wasser befeuchtet. Das Siliciumtetrafluorid reagiert mit dem Wasser wieder zu Silicat, das sich kraterförmig im Wassertropfen absetzt.[2]
Anwendungen
Fluoride werden vor allem als Flussmittel in der Metallurgie, zur Synthese von organischen Fluorchemikalien sowie zur gasdichten Versiegelung von Kraftstoffbehältern verwendet; dabei werden die Kunststofftanks aus z. B. PA (Polyamid) mit dem gelösten Fluorid bedampft, dadurch diffundiert dieses ca. 3–4 Mikrometer in die Oberfläche ein.
Als Fluoridierung bezeichnet man die Zugabe von Fluoriden insbesondere zu Speisesalz, Trinkwasser, Milch, Tabletten und Zahnpasten zur Prophylaxe von Zahnkaries.
Fluorid kann sowohl topisch als auch systemisch verabreicht die Kariesprophylaxe unterstützen.[3] Diese Maßnahmen unterstützen seit Jahrzehnten die Kariesprophylaxe. Es wird angenommen, dass es bei Anwesenheit von Fluoriden in der Mundhöhle zu einer „beschleunigten“ Remineralisation mit Calcium- und Phosphationen aus dem Speichel kommt.[3] Das Bundesinstitut für Risikobewertung kam 2018 zu dem Schluss, dass es keine eindeutigen Belege dafür gebe, „dass eine Zahnpasta mit 500 ppm (= 500 mg/l) Fluorid (entspricht 0,05 % Fluoridanteil) weniger wirksam ist als eine mit 1000 ppm (0,1 % Fluorid)“.[4] Ein Cochrane-Report von 2019 weist darauf hin, dass Fluorid-enthaltene Zahnpasten erst ab einer Konzentration von 1000 ppm wirksam bei der Kariesprophylaxe sind.[5]
| F--Anteil [%] | Menge pro Anwendung [mg] | |
|---|---|---|
| Zahncreme | bis 0,15 | 2,25 (bei 1,5 g Zahncreme) |
| Kinderzahncreme | 0,05 | 0,25 (erbsengroße Menge, ca. 0,5 g) |
| Fluoridsalz | 0,031 | 0,62 (bei 2 g Salz) |
| Fluorid-Gelee | 1,25 | 12,5 (bei 1,0 g Gelee) |
| Touchierlösung | 1,0 | 5,0 (bei 0,5 ml Lösung) |
| Spüllösung | 0,025 | 2,5 (bei 10 ml Lösung) |
| Fluoridlack | 0,10–2,26 | 0,5–7,5 (bei 0,19–0,50 ml Lack) |
| Polierpaste | 0,1–3,0 | 1,0–30,0 (bei 1,0 g Paste) |
Die empfohlene tägliche Gesamtaufnahme von Fluoriden liegt bei Erwachsenen bei etwa 3,5 mg[6], die geschätzte tatsächliche zwischen 0,4 und 1,5 mg.[7] Laut einem im Jahr 2013 veröffentlichten Gutachten der Europäischen Behörde für Lebensmittelsicherheit (EFSA) ist Fluorid kein essentieller Nährstoff, da es weder Wachstumsprozessen noch der Zahnentwicklung dient und Zeichen eines Fluoridmangels nicht identifiziert werden konnten.[8]
Der Fluoridgehalt bei Prophylaxeprodukten wie Zahnpasta wird als Salz angegeben, nicht für die Bewertung der Toxikologie (siehe unten) als Fluoridion.[6] Bei einem Produkt mit 5 % Natriumfluorid liegt die Fluoridmenge demnach bei 2,5 %.
Toxikologie
Die Toxikologie von Fluoriden ist von zahlreichen Faktoren abhängig, wie der Art des Fluorids, dessen Löslichkeitsverhalten (leicht löslich sind Natriumfluorid oder Zinnfluorid, schwerlöslich Calciumfluorid)[6], Art der Einwirkung, die Resorptionsgeschwindigkeit im Magen, dem Säure-Basen-Haushalt und dem pH-Wert des aufgenommenen Fluorids.
Grundsätzlich kommen Fluoride überall vor, auch im Grundwasser. In Deutschland beträgt die Konzentration des Trinkwassers überwiegend etwa weniger als 0,25 mg F− pro Liter.[6] In Gegenden mit hoher Fluorid-Mineraldichte (z. B. in Indien, China, Zentralafrika oder Südamerika) kann das Trinkwasser ca. 10 mg Fluoride pro Liter enthalten.[9] Durch das ubiquitäre Vorkommen im Grundwasser enthält praktisch die gesamte Vegetation Fluoride, getrockneter Tee durchschnittlich 100 mg/kg.[9] Damit werden sie über die Nahrung und mit dem Trinkwasser täglich aufgenommen (etwa 0,5–0,8 mg Fluorid).[10] Bei oraler Aufnahme erfolgt eine schnelle und nahezu vollständige Resorption löslicher Fluoride über die Magenschleimhaut, da die Salze durch die Salzsäure des Magens Fluorwasserstoff bilden, der als ungeladenes Molekül rasch resorbiert wird. Für diese Aufnahme spielt es keine Rolle, ob die Fluoride natürlicherweise in der Nahrung/Trinkwasser enthalten sind oder industriell ergänzt wurden (Fluoridierung).[9] Allgemein werden über die Nahrung 80 % aufgenommen, über die Lunge erfolgt eine Aufnahme nur in geringen Mengen.[6] Fluoride gelangen zu 60–80 % in den Blutkreislauf.[10] Dort befinden sich Fluoride überwiegend im Plasma (typische Konzentration 0,13–0,46 ppm bzw. mg/l, abhängig von der Fluoridaufnahme und den Knochenstoffwechsel), der Rest in den Erythrozyten.[6] Im Plasma beträgt die Halbwertszeit etwa 4 bis 10 Stunden. Vom Blut aus gelangen Fluoride in die Knochen und werden dort eingebaut.[10] Daher befindet sich der allergrößte Teil des Fluorides im menschlichen Körper in den Knochen und in den Zähnen (gerade an der Oberfläche sich entwickelnder Zähne), durchschnittlich hat jeder Mensch etwa 2,6 g Fluoride im Körper.[6] Bei Heranwachsenden wird die Hälfte des täglich aufgenommenen Fluorids im Skelett eingelagert, die andere Hälfte ausgeschieden (generell über die Nieren).[6] Das im Knochen befindliche Fluorid ist aber nicht irreversibel gebunden und wird bei geringerer Fluoridaufnahme auch wieder herausgelöst. Da die Plazenta nicht vollständig permeabel für Fluoride ist, liegt die Fluoridkonzentration im Blut des Fötus niedriger als die im Blut der Mutter. Muttermilch selbst enthält wenig Fluorid.[6] Der Speichel enthält vergleichsweise wenig Fluoride (0,05 ppm F−).[6]
Die sicher toxische Dosis (certainly toxic dose, CTD) bzw. akut toxische Dosis liegt bei 32 bis 64 mg Fluorid pro Kilogramm Körpergewicht, bei einem 75 kg schweren Erwachsenen also bei etwa 3,5 g.[6] In der Literatur werden auch 5–10 g bei einem Erwachsenen angegeben.[6] Die sogenannte wahrscheinliche toxische Dosis (probably toxic dose, PTD) ist die Minimaldosis, bei der sich Toxizitäten und Symptome zeigen können, und die neben einer Einweisung in eine Klinik auch ein unmittelbares therapeutisches Eingreifen erfordert.[6] Sie liegt bei 5 mg Fluorid pro Kilogramm Körpergewicht[6]
Zum Vergleich: In einer Tube Zahnpasta (100 g bzw. 75 ml) mit einem Fluoridgehalt von 1000 ppm befinden sich 100 mg Fluorid. Ein 15 kg schweres Kind hätte beim Verzehr der gesamten Tube Zahnpasta die wahrscheinlich toxische Dosis damit überschritten.
Die Giftwirkung beruht teils auf der Ausfällung des vom Stoffwechsel benötigten Calcium als Calciumfluorid, teils aus der Wirkung als Protoplasma- und Zellgift, das bestimmte Enzymsysteme und die Proteinsynthese hemmt. Sie äußert sich in Schädigungen des Skeletts, der Zähne, der Lungenfunktion, der Haut und in Stoffwechselstörungen. Wasserunlösliche oder schwerlösliche Fluoride wie Calciumfluorid und Aluminiumfluorid besitzen eine wesentlich geringere Toxizität. Es besteht jedoch immer die Gefahr der Bildung des ebenfalls hochtoxischen Fluorwasserstoffs beim Kontakt mit starken Säuren.
Symptome einer akuten Fluoridvergiftung sind starke Schmerzen in Magen und Darm und hinter dem Brustbein, Krämpfe, Bewusstlosigkeit und schwere Stoffwechselstörungen. Fluorwasserstoff verursacht in höheren Konzentrationen starke Verätzungen bis zur Zerstörung von Zellen.
Als Antidot bei Fluoridvergiftungen dient Calciumgluconat.[11][12] Als Erste-Hilfe-Maßnahme sind auch andere calciumhaltige Mittel wirksam; beispielsweise kann es helfen, Milch zu trinken, um damit die Resorption der Fluoridionen zu hemmen.[13]
Falls Fluoride chronisch aufgenommen werden, also über einen längeren Zeitraum, kann bereits eine geringere Dosis zu negativen Folgeerscheinungen führen (Fluorose).[14]
Siehe auch
Einzelnachweise
- Wissenschaft-Online-Lexika: Eintrag zu Fluoride, in: Lexikon der Geologie, abgerufen am 10. Juli 2008.
- Biltz-Klemm-Fischer, 1966.
- Matthias Epple, Joachim Enax: Moderne Zahnpflege aus chemischer Sicht. In: Chemie in unserer Zeit. Band 52, Nr. 4, 2018, S. 218–228, doi:10.1002/ciuz.201800796.
- Für gesunde Zähne: Fluorid-Vorbeugung bei Säuglingen und Kleinkindern. (PDF) Stellungnahme Nr. 015/2018 des BfR. In: BfR. 31. Mai 2018, abgerufen am 7. September 2020.
- Tanya Walsh et al.: Fluoride toothpastes of different concentrations for preventing dental caries. In: The Cochrane Database of Systematic Reviews. Band 3, 4. März 2019, S. CD007868, doi:10.1002/14651858.CD007868.pub3, PMID 30829399, PMC 6398117 (freier Volltext).
- Jean-Francois Roulet, Susanne Fath, Stefan Zimmer: Zahnmedizinische Prophylaxe: Lehrbuch und Praxisleitfaden. 5. Auflage. Elsevier Health Sciences, 2017, ISBN 978-3-437-18744-5, S. 137 ff.
- Zahnpasta - Fluorid und Zink – gefährlich? - Stiftung Warentest. In: Stiftung Warentest. 10. Oktober 2020, abgerufen am 10. Oktober 2020.
- Scientific Opinion on Dietary Reference Values for fluoride. In: EFSA Journal. Band 11, Nr. 8, 2013, ISSN 1831-4732, S. 3332, doi:10.2903/j.efsa.2013.3332.
- Guidelines for drinking-water quality, 4th edition, incorporating the 1st addendum. In: WHO. 24. April 2017, S. 370–373, abgerufen am 27. Oktober 2020 (englisch).
- Johannes Einwag: Das sind die Fakten. Die neuen Fluoridempfehlungen. In: Zahnärztliche Mitteilungen. 16. November 2019, abgerufen am 12. September 2020.
- Eintrag zu Antidot. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. November 2013.
- Eintrag zu Gluconate. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. November 2013.
- Jürgen Stein (Hrsg.): Praxishandbuch klinische Ernährung und Infusionstherapie. Springer 2003, ISBN 978-3-642-55896-2, S. 120, eingeschränkte Vorschau in der Google-Buchsuche
- G.M. Whitford: The Metabolism and Toxicity of Fluoride. Monographs in Oral Science (Editor Howard M. Myers) Vol. 13, Karger, Basel 1989
Weblinks
- Groundwater Assessment Platform - Übersichtskarten mit Hinweis darauf, welche Quellen mehr als 1,5 mg Fluorid pro Liter aufweisen. Abgerufen am 10. September 2020.

