Isotop
Als Isotope (von altgriechisch ἴσος ísos „gleich“ und τόπος tópos „Ort, Stelle“) bezeichnet man Atomarten, deren Atomkerne gleich viele Protonen, aber unterschiedlich viele Neutronen enthalten. Sie haben die gleiche Ordnungszahl, stellen daher das gleiche Element dar, weisen aber verschiedene Massenzahlen auf; es gibt also Sauerstoffisotope, Eisenisotope usw. Die verschiedenen Isotope eines Elements verhalten sich chemisch fast identisch.
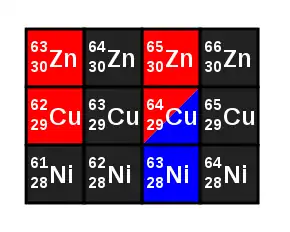
Der Name kommt daher, dass die Isotope eines Elements im Periodensystem am gleichen Ort stehen. Getrennt voneinander dargestellt werden sie in einer Nuklidkarte. Die Bezeichnung Isotop ist älter als der Begriff Nuklid, der ganz allgemein „Atomart“ bedeutet. „Isotop“ wird daher nach wie vor oft auch im Sinne von Nuklid benutzt, d. h. auch dann, wenn nicht nur von Atomen eines und desselben Elements die Rede ist. Der Begriff Isotop wurde von Frederick Soddy geprägt, der für seine Arbeiten und Erkenntnisse im Bereich der Isotope und Radionuklide 1921 den Nobelpreis für Chemie erhielt.
Von jedem bekannten Element, mit Ausnahme des erst 2006 erstmals synthetisierten Oganesson, sind mehrere Isotope nachgewiesen (s. Liste der Isotope und Nuklidkarte). Insgesamt gibt es rund 3300 bekannte Nuklide. Etwa 240 davon sind stabil. Alle anderen sind instabil, das heißt, ihre Atome wandeln sich durch radioaktiven Zerfall nach mehr oder weniger langer Zeit in andere Atome um. Bei manchen traditionell als stabil angesehenen Nukliden ist diese Zeit so lang, dass ihr Zerfall erst in heutiger Zeit entdeckt wurde oder noch in Experimenten gesucht wird.
Von den 91 natürlich vorkommenden Elementen werden in der Natur 69 als Gemische mehrerer Isotope (Mischelemente) vorgefunden. Die übrigen 22 heißen Reinelemente. Das chemische Atomgewicht von Mischelementen ist der Durchschnittswert der verschiedenen Atommassen der beteiligten Isotope.
Bezeichnung und Formelschreibweise
Die Bezeichnungsweise ist in Nuklid ausführlich beschrieben. Im Text wird ein Isotop mit dem Elementnamen oder -symbol mit der angehängten Massenzahl bezeichnet, beispielsweise Sauerstoff-16 oder O-16, Eisen-56 oder Fe-56. Ausnahmen bilden manchmal die Wasserstoffisotope (siehe folgenden Abschnitt).
Als Formelzeichen wird die Massenzahl dem Elementsymbol links oben hinzugefügt. Die Kernladungszahl ist schon durch den Namen (das Elementsymbol) gegeben, kann aber zusätzlich links unten an das Elementsymbol geschrieben werden, sofern sie – z. B. bei Kernreaktionen – von Interesse ist, wie in
Tritt in der Bezeichnung noch ein m auf (z. B. 16m1N), so ist damit ein Kernisomer gemeint. Wenn hinter dem m eine Zahl steht, ist dies eine Nummerierung, falls mehrere Isomere existieren.
Chemische Reaktionen von Isotopen
Isotope eines Elements haben die gleiche Elektronenhülle. Dadurch unterscheiden sie sich nicht in der Art der möglichen Reaktionen, sondern nur in ihrer Reaktionsgeschwindigkeit, weil diese etwas masseabhängig ist.
Der relative Massenunterschied ist bei schweren Elementen allerdings sehr gering. Das Verhältnis der Atommassen von Uran-238 und Uran-235 beträgt 1 : 1,013; in ihrem chemischen Verhalten ist kein merklicher Unterschied, zum Trennen müssen physikalische Methoden eingesetzt werden (siehe Urananreicherung). Bei den Lithiumisotopen Lithium-7 und Lithium-6 beträgt das Verhältnis 1 : 1,17; hier sind physikalisch-chemische Trennmethoden möglich (siehe Lithium). Die Massenunterschiede der drei Wasserstoffisotope sind sehr groß (1H : 2H : 3H wie 1 : 2 : 3), weshalb sie chemisch leicht unterschiedlich reagieren und sogar eigene Namen und chemische Symbole erhielten:
- Das weitaus häufigste Wasserstoffisotop 1H wird auch als Protium oder leichter Wasserstoff bezeichnet.
- Das Isotop 2H wird auch als Deuterium oder schwerer Wasserstoff bezeichnet. Symbol: D.
- Das Isotop 3H wird auch als Tritium oder überschwerer Wasserstoff bezeichnet. Symbol: T.
Das unterschiedliche chemisch-physikalische Verhalten von H und D zeigt sich bei der Elektrolyse von Wasser. Wasser mit dem normalen 1H reagiert bevorzugt und wird in Wasserstoff und Sauerstoff zerlegt, während sich Wassermoleküle, die D (2H Deuterium, Schwerer Wasserstoff) enthalten, im Restwasser anreichern (gegenüber dem natürlichen Mengenverhältnis von etwa 1 : 7.000).
Mischelemente und Reinelemente
So gut wie alle auf der Erde natürlich vorkommenden Nuklide sind entweder stabil (d. h. ein Zerfall wurde nicht beobachtet) oder sind radioaktiv mit einer Halbwertszeit, die nicht wesentlich kleiner als das Erdalter ist. Diese bezeichnet man als primordiale Nuklide.
Insgesamt sind etwa 245 stabile Nuklide bekannt (siehe Nuklidkarte: stabile Nuklide sind mit schwarzem Hintergrund dargestellt). Allerdings ist bei „stabil“ zu unterscheiden, ob der Zerfall des Nuklids naturgesetzlich ausgeschlossen erscheint oder ob er möglich erscheint, aber noch nicht beobachtet wurde. Die Anzahl der im letzteren Sinn stabilen Nuklide hat sich mit der Zeit immer wieder verringert: Durch verbesserte Nachweismethoden sind einige ehemals als stabil angesehene Nuklide später als radioaktiv erkannt worden. Mit dem Nachweis der Radioaktivität von Bismut-209 im Jahr 2003 ergab sich, dass Blei-208 das schwerste stabile Nuklid und somit Blei das schwerste Element mit stabilen Isotopen ist.[1]
In der Natur vorkommende Elemente sind meistens Mischelemente, d. h. Isotopengemische. Die meisten natürlichen Isotope hat Zinn mit 10 Isotopen, gefolgt von Xenon mit 9 natürlichen Isotopen, von denen 8 stabil sind. Elemente, die dagegen nur aus einem natürlichen Isotop bestehen, nennt man Reinelement. Ein Reinelement hat also genau ein primordiales Isotop. Diese Eigenschaft haben 19 stabile und 3 langlebige instabile Elemente.
Bekannte Isotope
Wasserstoff
Wasserstoff ist das Element mit dem stärksten chemischen Isotopeneffekt. Schwerer Wasserstoff (2H oder Deuterium) dient im Schwerwasserreaktor als Moderator. Überschwerer Wasserstoff (3H oder Tritium) ist radioaktiv. Er entsteht in der Atmosphäre durch die kosmische Strahlung sowie in Kernreaktoren. Tritium wurde zwischen etwa 1960 und 1998 in Leuchtfarben für Uhr-Zifferblätter usw. verwendet. In größeren Mengen sollen Deuterium und Tritium in Zukunft als Brennstoff für Kernfusionsreaktoren gebraucht werden.
Helium
Helium ist das Element mit dem stärksten physikalischen Isotopeneffekt. Insbesondere im Tieftemperaturbereich verhalten sich die beiden Heliumisotope sehr verschieden, da 3He ein Fermion und 4He ein Boson ist.
Kohlenstoff
Ein bekanntes Isotop ist das radioaktive 14C, das zur Altersbestimmung von organischen Materialien (Archäologie) benutzt wird (Radiokohlenstoffmethode). Natürlicher Kohlenstoff liegt hauptsächlich in den stabilen Isotopen 12C und 13C vor. 14C entsteht in hohen atmosphärischen Schichten aus Stickstoff.
Sauerstoff
Das Verhältnis der beiden stabilen Sauerstoffisotope 18O und 16O wird zur Untersuchung von Paläo-Temperaturen herangezogen. Die stabilen Sauerstoffisotope eignen sich auch als natürliche Tracer in aquatischen Systemen.[2]
Uran
Das Isotop 235U dient als Brennstoff in Kernkraftwerken. Für die meisten Reaktortypen muss das Natururan dazu an 235U angereichert werden. Fast reines 235U wird in manchen Kernwaffen verwendet.
Isotope in der Analytik
In Messungen des optischen Spektrums mit genügender Auflösung können Isotope eines Elements an ihren Spektrallinien unterschieden werden (Isotopieverschiebung).
Die Isotopenzusammensetzung in einer Probe wird in der Regel mit einem Massenspektrometer bestimmt, im Fall von Spurenisotopen mittels Beschleuniger-Massenspektrometrie.
Radioaktive Isotope können oft anhand ihrer Zerfallsprodukte oder der abgegebenen ionisierenden Strahlung identifiziert werden.
Isotope spielen ferner eine Rolle in der NMR-Spektroskopie. So hat beispielsweise das gewöhnliche Kohlenstoff-Isotop 12C kein magnetisches Moment und ist daher nicht beobachtbar. Untersuchungen am Kohlenstoff können daher nur mithilfe des wesentlich selteneren 13C-Isotops erfolgen.
Isotope werden auch in der Aufklärung von Reaktionsmechanismen oder Metabolismen mit Hilfe der sogenannten Isotopenmarkierung verwendet.
Die Isotopenzusammensetzung des Wassers ist an verschiedenen Orten der Welt verschieden und charakteristisch. Diese Unterschiede erlauben es etwa bei Lebensmitteln wie Wein oder Käse, die Deklaration des Ursprungsortes zu überprüfen.
Die Untersuchung von bestimmten Isotopen-Mustern (insbesondere 13C-Isotopen-Mustern) in organischen Molekülen wird als Isotopomeren-Analyse bezeichnet. Sie erlaubt unter anderem die Bestimmung intrazellulärer Stoffflüsse in lebenden Zellen. Darüber hinaus ist die Analyse von 13C/12C-, 15N/14N- sowie 34S/32S-Verhältnissen in der Ökologie heute weit verbreitet. Anhand der Fraktionierung lassen sich Stoffflüsse in Nahrungsnetzen nachverfolgen oder die Trophieniveaus einzelner Arten bestimmen. Auch in der Medizin dienen stabile Isotope als natürliche Tracer.
In der Hydrologie werden aus den Konzentrationsverhältnissen von Isotopen Rückschlüsse auf hydrologische Prozesse gezogen. Der Wasserkreislauf begleitet die meisten Stoffflüsse ober- und unterhalb der Erdoberfläche. Das Vienna Standard Mean Ocean Water (VSMOV) dient oft als Referenz.
Die Geochemie befasst sich mit Isotopen in Mineralen, Gesteinen, Boden, Wasser und Erdatmosphäre.
Literatur
- Werner Stolz: Radioaktivität. Grundlagen, Messung, Anwendungen. 5. Auflage. Teubner, Wiesbaden 2005, ISBN 3-519-53022-8.
- Bogdan Povh, K. Rith, C. Scholz, F. Zetsche: Teilchen und Kerne. Eine Einführung in die physikalischen Konzepte. 7. Auflage. Springer, Berlin/Heidelberg 2006, ISBN 978-3-540-36685-0.
- Klaus Bethge, Gertrud Walter, Bernhard Wiedemann: Kernphysik. 2. Auflage. Springer, Berlin/Heidelberg 2001, ISBN 3-540-41444-4.
- Hanno Krieger: Grundlagen der Strahlungsphysik und des Strahlenschutzes. 2. Auflage. Teubner, Wiesbaden 2007, ISBN 978-3-8351-0199-9.
Weblinks
- Große Isotopentabelle bei der International Atomic Energy Agency (IAEA)
Einzelnachweise
- Pierre de Marcillac, Noël Coron, Gérard Dambier, Jacques Leblanc, Jean-Pierre Moalic: Experimental detection of α-particles from the radioactive decay of natural bismuth. In: Nature. Band 422, Nr. 6934, April 2003, S. 876–878, Ergebnistabelle 1, doi:10.1038/nature01541.
- Paul Königer: Tracerhydrologische Ansätze zur Bestimmung der Grundwasserneubildung. Inst. für Hydrologie, Freiburg i. Br. 2003, DNB 969622139 (PDF – zugl. Dissertation, Universität Freiburg).