Brom
Brom [bʁoːm] (altgriechisch βρῶμος brōmos „Gestank“) ist ein chemisches Element mit dem Elementsymbol Br und der Ordnungszahl 35. Im Periodensystem steht es in der 7. Hauptgruppe, bzw. der 17. IUPAC-Gruppe und gehört damit zusammen mit Fluor, Chlor, Iod, Astat und Tenness zu den Halogenen. Elementares Brom liegt unter Normbedingungen (Temperatur = 0 °C und Druck = 1 atm) in Form des zweiatomigen Moleküls Br2 in flüssiger Form vor. Brom und Quecksilber sind die einzigen natürlichen Elemente, die unter Normbedingungen flüssig sind.
| Eigenschaften | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Brom, Br, 35 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementkategorie | Halogene | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe, Periode, Block | 17, 4, p | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Aussehen | gasförmig: rotbraun flüssig: rotbraun fest: metallisch glänzend | |||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Nummer | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| EG-Nummer | 231-778-1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ECHA-InfoCard | 100.028.890 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 6,0 ppm[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomar [2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 79,904 (79,901 – 79,907)[3] u | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | 115 (94) pm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 120 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Van-der-Waals-Radius | 185 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronenkonfiguration | [Ar] 3d10 4s2 4p5 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 11.81381(6) eV[4] ≈ 1139.86 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 21.591 eV[4] ≈ 2083.2 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 34.871(19) eV[4] ≈ 3364.5 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 47.782(12) eV[4] ≈ 4610.3 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Ionisierungsenergie | 59.595(25) eV[4] ≈ 5750 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 6. Ionisierungsenergie | 87.390(25) eV[4] ≈ 8431.9 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 7. Ionisierungsenergie | 103.03(19) eV[4] ≈ 9941 kJ/mol[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalisch [6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aggregatzustand | flüssig | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | orthorhombisch | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte | 3,12 g·cm−3[7] bei 300 K | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetismus | diamagnetisch (χm = −2,8 · 10−5)[8] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 265,8 K (−7,3 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 331,7 K[9] (58,5 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Molares Volumen | (fest) 19,78 · 10−6 m3·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungsenthalpie | 30 kJ/mol[9] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzenthalpie | 5,8 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampfdruck | 2,2 · 104[7] Pa bei 293 K | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 0,12 W·m−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemisch [10] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationszustände | ±1, 3, 5, 7 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Normalpotential | 1,066 V (Br + e− → Br−) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativität | 2,96 (Pauling-Skala) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotope | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| NMR-Eigenschaften | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| MAK |
Schweiz: 0,1 ml·m−3 bzw. 0,7 mg·m−3[12] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||||||||||||||||||||||||||||||||
In der Natur kommt Brom nicht elementar, sondern nur in verschiedenen Verbindungen vor. Die wichtigsten Verbindungen sind die Bromide, in denen Brom in Form des Anions Br− auftritt. Die bekanntesten Bromide sind Natriumbromid und Kaliumbromid. Bromide sind ein Bestandteil des Meerwassers und besitzen einige biologische Funktionen.
Entdeckung

Brom wurde 1826 durch den französischen Chemiker Antoine-Jérôme Balard aus Meeresalgen der Salzwiesen bei Montpellier gewonnen und von diesem als bisher unbekannter Stoff erkannt.
Bereits zwei Jahre vor Balard stellte der deutsche Chemiker Justus von Liebig 1824 unwissentlich elementares Brom her. Er hatte den Auftrag, die Salzsolen von Salzhausen[16] zu analysieren, da die Stadt ein Kurbad plante.[17] Bei der Untersuchung dieser Sole fand Liebig eine neue Substanz, die er als Iodchlorid deutete. 13 Jahre später gab er zu, dass ihn seine nachlässige Analyse um die Entdeckung eines neuen Elements gebracht habe. Liebig schrieb dazu: „Ich kenne einen Chemiker, der, als er in Kreuznach war, die Mutterlaugen der Saline untersuchte.“ Im weiteren beschrieb er dann sein Missgeschick und schloss mit den Worten: „Seit dieser Zeit hat er keine Theorien mehr aufgestellt, wenn sie nicht durch unzweifelhafte Experimente unterstützt und bestätigt wurden; und ich kann vermelden, dass er daran nicht schlecht getan hat.“[18][19]
Auch Karl Löwig hat sich mit Brom befasst, das er bereits vor 1825 durch Einleiten von Chlor in Kreuznacher Solewasser gewann, jedoch kam Balard ihm mit der Publikation seiner Entdeckung zuvor.
Eine industrielle Produktion erfolgte ab 1860. Aufgrund seines stechenden Geruchs schlug Joseph Louis Gay-Lussac den Namen „Brom“ (griech. für „Bocksgestank der Tiere“[20]) vor.
Vorkommen
Brom kommt in Form von Bromiden, den Salzen der Bromwasserstoffsäure, vor. Mengenmäßig finden sich die größten Vorkommen als gelöste Bromide im Meerwasser. Auch Vorkommen natürlicher Salzlagerstätten (Stein- und Kalisalze) enthalten geringe Anteile an Kaliumbromid und Kaliumbromat. Brom kann auch in der Atmosphäre in der Form von molekularem Brom und Bromoxid vorkommen und kann die atmosphärische Ozonchemie maßgeblich beeinflussen und dabei über weite Distanzen transportiert werden. Während des polaren Frühlings zerstören regelmäßig größere Konzentrationen (>10ppt) BrO fast das gesamte troposphärische Ozon. Diese Ereignisse sind mittels der DOAS-Methode auch von Satelliten zu beobachten. In tropischen Regionen mit hoher Bioaktivität wurden starke Emissionen halogenierter Kohlenwasserstoffe beobachtet, die letztendlich durch Photolyse zur Bildung von BrO und zur Ozonzerstörung beitragen können.
Brom ist für Tiere in Spuren essenziell. Bromid fungiert als Cofaktor bei einer Stoffwechsel-Reaktion, die notwendig zum Aufbau der Kollagen-IV-Matrix im Bindegewebe ist.[21]
Gewinnung und Darstellung
Die industrielle Herstellung elementaren Broms erfolgt durch Oxidation von Bromidlösungen mit Chlor.
- Durch Oxidation von Kaliumbromid durch Chlor entstehen Brom und Kaliumchlorid
Als Bromidquelle nutzt man überwiegend Sole und stark salzhaltiges Wasser aus großer Tiefe sowie Salzseen, vereinzelt auch Meerwasser.[22] Eine Gewinnung aus den Restlaugen der Kaligewinnung ist nicht mehr wirtschaftlich. Seit 1961 hat sich die jährlich gewonnene Menge an Brom von rund 100.000 Tonnen auf über eine halbe Million Tonnen mehr als verfünffacht. Die größten Brom-Produzenten sind die Vereinigten Staaten, China, Israel, sowie Jordanien.[23]
Im Labor kann Brom durch Umsetzung von Natriumbromid mit Schwefelsäure und Braunstein in der Hitze dargestellt werden. Das Brom wird dabei durch Destillation abgetrennt.
- Aus Natriumbromid, Mangan(IV)-oxid und Schwefelsäure entstehen Brom, Mangan(II)-sulfat, Natriumsulfat und Wasser.
Eigenschaften

Physikalische Eigenschaften
Die Dichte von Brom beträgt 3,12 g/cm3. Die schwere rotbraune Flüssigkeit bildet chlorähnlich riechende Dämpfe, die giftiger sind als Chlor. Festes Brom ist dunkel, bei weiterer Abkühlung hellt es auf. In Wasser ist es mäßig, in organischen Lösungsmitteln wie Alkoholen, Kohlenstoffdisulfid oder Tetrachlorkohlenstoff sehr gut löslich. In Wasser gelöstes Brom reagiert langsam unter Zwischenbildung von Hypobromiger Säure (HBrO) und Sauerstoffabgabe zu Bromwasserstoff (HBr). Die kinetisch gehemmte Reaktion wird durch (Sonnen-)Licht beschleunigt, Bromwasser wird daher in braunen, wenig lichtdurchlässigen Flaschen aufbewahrt.
Chemische Eigenschaften
Brom verhält sich chemisch wie das leichtere Chlor, reagiert aber im gasförmigen Zustand weniger energisch. Feuchtigkeit erhöht die Reaktivität des Broms stark. Mit Wasserstoff reagiert es im Gegensatz zum Chlor erst bei höheren Temperaturen unter Bildung von Bromwasserstoff (farbloses Gas).
Mit vielen Metallen (z. B. Aluminium) reagiert es exotherm unter Bildung des jeweiligen Bromids. Feuchtem Brom widerstehen nur Tantal und Platin.[24]
Verwendung

- Chemisches Polieren von Galliumarsenid (als Lösung in Methanol)
- mehrfach bromierte Biphenyle bzw. Diphenylether als Flammschutzmittel in Verbundwerkstoffen wie FR-4, wie sie bei Leiterplatten eingesetzt werden. Im Jahr 2000 wurden 38 % des Broms für die Herstellung von bromierten Flammschutzmitteln verwendet.[25]
- Methylbromid als Schädlingsbekämpfungsmittel
- Desinfektionsmittel (milder als Chlor)
- in Form von Bromiden, beispielsweise Kaliumbromid, als nebenwirkungsreiches Arzneimittel (Narkose-, Beruhigungs- und Schlafmittel; Behandlung therapieresistenter Epilepsien mit generalisiert tonisch-klonischen Anfällen, früher – etwa auch zur Behandlung der „Hysterie“[26] – sehr beliebt; heute obsolet). 1928 wurde eins von fünf Rezepten in den USA für bromhaltige Medikamente ausgestellt.[27]
- Fotoindustrie (Silberbromid als Bestandteil der lichtempfindlichen Suspension)
- Alkali-Hypobromite als Bleichmittel
- im Labor als Indikator (ungesättigte Kohlenstoffverbindungen entfärben Bromwasser, d. h. Addition von Brom)
- im Chemieunterricht zur experimentellen Veranschaulichung von Additionsreaktionen und Substitutionsreaktionen[28]
- Bromate als Oxidationsmittel
- bromhaltiger Kautschuk zur Herstellung „luftdichter“ Reifen
- Tränengas, z. B. in Form von Monobromaceton
- in Mitteln zum Schutz gegen das Nervengas Soman bei US-Soldaten im Irak-Krieg
- Früher in Form von Alkylbromiden als Scavenger zum Entfernen des Bleis aus Zylindern bei der Nutzung von verbleitem Benzin
Nachweis
Bromidionen können qualitativ mit Hilfe von Chlorwasser und Hexan nachgewiesen werden.
Zum nasschemischen Nachweis der Bromidionen kann man sich auch wie bei den anderen Nachweisreaktionen für Halogenide die Schwerlöslichkeit des Silbersalzes von Bromid zu Nutze machen. Das Gleiche gilt für die volumetrische Bestimmung der Halogenide durch Titration.
Zur Spurenbestimmung und Speziierung von Bromid und Bromat wird die Ionenchromatografie eingesetzt. In der Polarografie ergibt Bromat eine kathodische Stufe bei −1,78 V (gegen SCE, in 0,1 mol/l KCl), wobei es zum Bromid reduziert wird. Mittels Differenzpulspolarografie können auch Bromatspuren erfasst werden.
Sicherheitshinweise
Elementares Brom ist sehr giftig und stark ätzend, Hautkontakt führt zu schwer heilenden Verätzungen. Inhalierte Bromdämpfe führen zu Atemnot, Lungenentzündung und Lungenödem. Auch auf Wasserorganismen wirkt Brom giftig.
Im Labor wird beim Arbeiten mit Brom meist eine dreiprozentige Natriumthiosulfatlösung bereitgestellt, da sie verschüttetes Brom oder Bromwasserstoff sehr gut binden kann. Hierbei bilden sich Natriumbromid, elementarer Schwefel und Schwefelsäure. Durch die entstehende Säure kann weiteres Thiosulfat zu Schwefel und Schwefeldioxid zerfallen:
Die Aufbewahrung von Brom erfolgt in Behältern aus Glas, Blei, Monel, Nickel oder Teflon.[7]
Verbindungen
→ Kategorie: Bromverbindung
Brom bildet Verbindungen in verschiedenen Oxidationsstufen von −1 bis +7. Die stabilste und häufigste Oxidationsstufe ist dabei −1, die höheren werden nur in Verbindungen mit den elektronegativeren Elementen Sauerstoff, Fluor und Chlor gebildet. Dabei sind die ungeraden Oxidationsstufen +1, +3, +5 und +7 stabiler als die geraden.
Bromwasserstoff und Bromide
Anorganische Verbindungen, in denen das Brom in der Oxidationsstufe −1 und damit als Anion vorliegt, werden Bromide genannt. Diese leiten sich von der gasförmigen Wasserstoffverbindung Bromwasserstoff (HBr) ab. Diese ist eine starke Säure und gibt in wässrigen Lösungen leicht das Proton ab. Bromide sind in der Regel gut wasserlöslich, Ausnahmen sind Silberbromid, Quecksilber(I)-bromid und Blei(II)-bromid.
Besonders bekannt sind die Bromide der Alkalimetalle, vor allem das Natriumbromid. Auch Kaliumbromid wird in großen Mengen, vor allem als Dünger und zur Gewinnung anderer Kaliumverbindungen, verwendet.
Bleibromid wurde früher in großen Mengen bei der Verbrennung von verbleitem Kraftstoff freigesetzt (wenn dem Benzin Dibrom-Ethan zugesetzt war um das Blei flüchtig zu machen, siehe Tetraethylblei#Antiklopfmittel für Motorenbenzin).
Bromoxide
Es ist eine größere Anzahl Verbindungen von Brom und Sauerstoff bekannt. Diese sind nach den allgemeinen Formeln BrOx (x = 1–4) und Br2Ox (x = 1–7) aufgebaut. Zwei der Bromoxide, Dibromtrioxid (Br2O3) und Dibrompentaoxid (Br2O5) lassen sich als Feststoff isolieren.[29]
Bromsauerstoffsäuren
Neben den Bromoxiden bilden Brom und Sauerstoff auch mehrere Säuren, bei denen ein Bromatom von einem bis vier Sauerstoffatomen umgeben ist. Dies sind die Hypobromige Säure, die Bromige Säure, die Bromsäure und die Perbromsäure. Sie sind als Reinstoff instabil und nur in wässriger Lösung oder in Form ihrer Salze bekannt.
Interhalogenverbindungen
Brom bildet vorwiegend mit Fluor, zum Teil auch mit den anderen Halogenen eine Reihe von Interhalogenverbindungen. Bromfluoride wie Bromfluorid und Bromtrifluorid wirken stark oxidierend und fluoriend. Während Brom in den Fluor-Brom- und Chlor-Brom-Verbindungen als elektropositiveres Element in Oxidationsstufen +1 im Bromchlorid bis +5 im Brompentafluorid vorliegt, ist es in Verbindungen mit Iod der elektronegativere Bestandteil. Mit diesem Element sind die Verbindungen Iodbromid und Iodtribromid bekannt.
Organische Bromverbindungen
Eine Vielzahl von organischen Bromverbindungen (auch Organobromverbindungen) wird synthetisch hergestellt. Wichtig sind die Bromalkane, die Bromalkene sowie die Bromaromaten. Eingesetzt werden sie unter anderem als Lösungsmittel, Kältemittel, Hydrauliköle, Pflanzenschutzmittel, Flammschutzmittel oder Arzneistoffe.
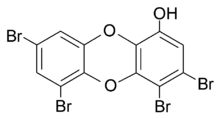
Zu den Organobromverbindungen gehören auch die polybromierten Dibenzodioxine und Dibenzofurane.
Literatur
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 438–440.
Weblinks
Einzelnachweise
- Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus webelements.com (Brom) entnommen.
- Angegeben ist der von der IUPAC empfohlene Standardwert, da die Isotopenzusammensetzung dieses Elements örtlich schwanken kann, ergibt sich für das mittlere Atomgewicht der in Klammern angegebene Massenbereich. IUPAC, Standard Atomic Weights Revised 2013 (ciaaw.org).
- Eintrag zu bromine in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: NIST, Gaithersburg, MD. doi:10.18434/T4W30F (https://physics.nist.gov/asd). Abgerufen am 11. Juni 2020.
- Eintrag zu bromine bei WebElements, https://www.webelements.com, abgerufen am 11. Juni 2020.
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus webelements.com (Brom) entnommen.
- Eintrag zu Brom in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. August 2016. (JavaScript erforderlich)
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9, S. E-129 bis E-145. Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337 (doi:10.1021/je1011086).
- Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus webelements.com (Brom) entnommen.
- Eintrag zu Bromine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 7726-95-6 bzw. Brom), abgerufen am 2. November 2015.
- Gigiena i Sanitariya. (English translation HYSAAV.), Vol. 35 (11), 1970, S. 11.
- Eintrag zu Bromine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- W. B. Deichmann: Toxicology of Drugs and Chemicals. Academic Press, New York 1969, S. 645.
- Sehenswürdigkeiten in Bad Salzhausen (Memento vom 18. Februar 2008 im Internet Archive).
- W. H. Brock: Justus von Liebig: eine Biografie des großen Wissenschaftlers und Europäers. Vieweg Verlag, Braunschweig 1999.
- J. Liebig: Über Laurent's Theorie der organischen Verbindungen. 1838, S. 554.
- T. K. Langebner: Justus von Liebig und das »Handbuch der Chemie«, II. (Memento vom 2. Dezember 2008 im Internet Archive) In: ÖAZ aktuell. Hauptartikel 17/2001.
- Wilhelm Gemoll, Karl Vretska: Griechisch-Deutsches Schul- und Handwörterbuch. 9. Auflage. Verlag Hölder-Pichler-Tempsky, ISBN 3-209-00108-1
- A. Scott McCall u. a.: Bromine Is an Essential Trace Element for Assembly of Collagen IV Scaffolds in Tissue Development and Architecture. In: Cell. 157(6), 2014, S. 1380–1392; doi:10.1016/j.cell.2014.05.009.
- Stephen M. Jasinski: 2006 Minerals Yearbook. (PDF; 56 kB) United States Geological Survey, November 2007, abgerufen am 17. September 2011 (englisch).
- Mineral Commodity Summaries 2011. (PDF; 27 kB) United States Geological Survey, 24. Januar 2011, abgerufen am 17. September 2011 (englisch).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 440.
- Linda S. Birnbaum, Daniele F. Staskal: Brominated Flame Retardants: Cause for Concern? In: Environ Health Perspect. 112, 2004, S. 9–17. doi:10.1289/ehp.6559. PMC 1241790 (freier Volltext)
- Ann Dally: Women under the knife. A history of surgery. New York 1991, S. 187.
- Hans Bangen: Geschichte der medikamentösen Therapie der Schizophrenie. Berlin 1992, ISBN 3-927408-82-4, S. 22.
- Klaus Ruppersberg: Brom in der Schule. In: Nachrichten aus der Chemie. Band 63, Nr. 5. Wiley, Weinheim 29. April 2015, S. 540–542, doi:10.1002/nadc.201590166, urn:nbn:de:0111-pedocs-122991.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 487–488.


