Plutonium
Plutonium ist ein chemisches Element mit dem Elementsymbol Pu und der Ordnungszahl 94, der höchsten Ordnungszahl aller natürlich vorkommenden Elemente. Im Periodensystem steht es in der Gruppe der Actinoide (7. Periode, f-Block) und zählt zu den Transuranen. Benannt wurde es nach dem Zwergplaneten Pluto.
| Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Plutonium, Pu, 94 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementkategorie | Actinoide | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe, Periode, Block | Ac, 7, f | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aussehen | silbriges Metall | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-Nummer | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EG-Nummer | 231-117-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ECHA-InfoCard | 100.028.288 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 2 · 10−15 ppm[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomar [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 244,0642 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius | 151 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenter Radius | 187 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronenkonfiguration | [Rn] 5f6 7s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 6.02576(25) eV[3] ≈ 581.4 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 11.5(4) eV[3] ≈ 1110 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 21.1(4) eV[3] ≈ 2040 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 35.0(4) eV[3] ≈ 3380 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Ionisierungsenergie | 49.0(1,9) eV[3] ≈ 4730 kJ/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physikalisch [5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aggregatzustand | fest | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modifikationen | 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | monoklin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte | 19,816 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetismus | paramagnetisch (χm = 6,2 · 10−4)[6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 912,5 K (639,4 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 3509 K (3230 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molares Volumen | 12,29 · 10−6 m3·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungsenthalpie | 325 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzenthalpie | 11,48[7] kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | 2260 m·s−1 bei 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spezifische Wärmekapazität | 130 J·kg−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrische Leitfähigkeit | 6,8 · 105 A·V−1·m−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 6,74[7] W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemisch [8] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationszustände | +3, +4, +5, +6, (+7) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Normalpotential | −2,031 V (Pu3+ + 3 e− → Pu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativität | 1,28 (Pauling-Skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gefahren- und Sicherheitshinweise | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

Radioaktiv | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Plutonium ist ein giftiges und radioaktives Schwermetall. Es wird in kleinsten Spuren in sehr alten Gesteinen gefunden. Größer ist die Menge, die künstlich in Kernkraftwerken erzeugt wird.
Als eines der wenigen spaltbaren Elemente spielt es eine wichtige Rolle für den Bau von Kernwaffen. So war es das Spaltmaterial der Atombombe, die am 9. August 1945 auf Nagasaki abgeworfen wurde (Fat Man). Beim Betrieb von Kernreaktoren entsteht Plutonium aus dem Uran im Kernbrennstoff.
Geschichte


Plutonium wurde von den US-Amerikanern Glenn T. Seaborg, J. W. Kennedy, E. M. McMillan, Michael Cefola und Arthur Wahl entdeckt. Am 14. Dezember 1940 stellten sie das Isotop 238Pu durch Beschuss von Uran 238U mit Deuteronen in einem Zyklotron her. Dazu wurden zunächst Proben des Isotops 238U in Form des Oxids U3O8 in dünner Schicht auf einer Kupferplatte aufgetragen. Bei der Kernreaktion mit Deuteronen werden je zwei Neutronen emittiert; das zunächst entstehende Neptunium zerfällt zu 238Pu. Den eindeutigen Nachweis für das Element 94 erbrachte Arthur Wahl am 23./24. Februar 1941.[10][11]
Das zweite Isotop wurde durch Beschuss mit schnellen Neutronen erzeugt:
- Die angegebenen Zeiten sind Halbwertszeiten.
Sie benannten es im März 1942 nach dem damals als äußersten Planeten geltenden Pluto, der wiederum nach dem gleichnamigen Gott der Unterwelt benannt ist: „[…] benannt nach dem jenseits des Neptuns folgenden Planeten Pluto, angesichts der infernalischen Wirkung der Pu-Bombe erscheint die Ableitung des Namens von Pluto, dem Gott der Unterwelt gerechtfertigter!“[12] So wurden die drei schwersten damals bekannten Elemente Uran, Neptunium und Plutonium nach den Planeten Uranus, Neptun und Pluto benannt[13].
Die erste wägbare Menge von etwa 4 µg wurde im August/September 1942 von Burris B. Cunningham, M. Cefola und Louis B. Werner isoliert.[14]
Die Entdeckung wurde während des Zweiten Weltkrieges geheim gehalten. Im Rahmen des US-amerikanischen Manhattan-Projekts wurde Plutonium erstmals in größerem Maßstab hergestellt. Die Atombombe, mit der durch den Trinity-Test die erste Kernwaffenexplosion der Menschheit herbeigeführt wurde, sowie Fat Man, die Bombe, mit der die japanische Stadt Nagasaki zerstört wurde, enthielten Plutonium 239Pu als Spaltstoff. Joseph Hamilton führte an Versuchspersonen Plutonium-Verteilungsstudien durch, die aufgrund der extremen Giftwirkung des Plutoniums heute umstritten sind.
In Deutschland hatte bereits vor der Entdeckung des Plutoniums Carl Friedrich von Weizsäcker darauf hingewiesen, dass in Kernreaktoren ein neues spaltbares Element 239Eka Re (Eka-Rhenium) entstehen müsse.[15] Auch Friedrich Georg Houtermans sagte 1942 die Existenz von Transuranen in einem Geheimbericht theoretisch voraus. Im Rahmen des deutschen Uranprojekts wurden jedoch bis Kriegsende nach heutigem Kenntnisstand keine signifikanten Mengen an Plutonium hergestellt.[16]
Vorkommen
Natürliches Vorkommen
Plutonium ist das letzte, allerdings extrem seltene, bisher bekannte natürlich vorkommende Element des Periodensystems. Mit einem Gehalt von 2 · 10−19 Gew.-%[7][17] ist es eines der seltensten Elemente der Erdkruste. In Uranvorkommen kann es in winzigen Mengen durch Absorption natürlich freigesetzter Neutronen aus Uran entstehen. Auf 140 Milliarden Uranatome soll ein Plutoniumatom kommen. Der US-amerikanische Chemiker D. F. Peppard extrahierte im Jahr 1951 Mikrogrammmengen 239Pu aus einem kongolesischen Pechblendekonzentrat. Für jedes Mikrogramm waren 100 Tonnen Pechblende notwendig.[18]
Von den Naturreaktoren von Oklo in Gabun sowie von einer benachbarten Uranlagerstätte ist bekannt, dass dort vor etwa 1,5 bis 2 Milliarden Jahren über mehrere Jahrtausende Kernspaltung als Kettenreaktion in natürlichem Umfeld auftrat. Durch die Anlagerung von Spaltungsneutronen an 238U entstanden dort etwa 2 bis 4 Tonnen 239Pu. In einigen Teilen der Oklo-Lagerstätte trug die auch direkte Spaltung von 239Pu nennenswert zur Gesamtkernspaltung bei. Etwa ein Drittel des insgesamt gespaltenen 235U soll aus dem Alphazerfall von 239Pu gestammt haben. Etwaige Reste des erzeugten Plutoniums sind mittlerweile komplett zerfallen.
Mit verfeinerter Spurenanalytik gelang es, im Mineral Bastnäsit, das nach dem Fundort Bastnäs in Schweden benannt wurde, geringste Spuren des langlebigsten Plutoniumisotops 244Pu nachzuweisen. Dieses Plutonium stammt aus der Entstehungszeit des Sonnensystems, ist also ein primordiales Nuklid. Die gefundenen Mengen sind so gering, dass sie erst im Jahr 1971, also lange nach der künstlichen Erzeugung von Plutonium in Kernreaktoren, entdeckt wurden.[19][20]
Es wird berichtet, dass 244Pu in geringster Menge aus Sedimenten am Meeresboden isoliert wurde, die aus Sternenstaub kommen sollen. Hierfür werden als Urheber Verschmelzungen von Neutronensternen vermutet.[21]
Künstliches Vorkommen
Plutonium entsteht in Kernwaffen und in Kernreaktoren durch Transmutation von Uran. Mittlerweile (2016) haben die Nuklearmächte und andere Staaten, die Kernkraftwerke betreiben, ein Gesamtinventar von hunderten Tonnen auf diese Weise künstlich erzeugten Plutoniums, darunter Russland 180 Tonnen und USA 90 Tonnen separierten Plutoniums.[22]
Freisetzung durch anthropogene Ursachen
Anthropogen wurde Plutonium zwischen 1945 und 1980 durch oberirdische Kernwaffentests in einer Menge von drei bis fünf Tonnen[20] freigesetzt, die in Spuren weltweit nachweisbar sind. Weitere Mengen wurden durch verschiedene unbeabsichtigte Ereignisse und Unfälle freigesetzt.
- Freisetzungen bei Kernwaffenunfällen und bei Unfällen in Kernwaffen-Laboratorien
- Fehlgeschlagene Weltraummissionen und Wiedereintritt von Satelliten mit Radionuklidbatterien, wie durch Transit 5BN-3, Kosmos 954 und Apollo 13
- Brand des Reaktors der Plutoniumfabrik von Sellafield (damals Windscale) im Jahre 1957
- Unfälle mit Atom-U-Booten[23]
- im Abwasser von Kernforschungsanlagen[24] und von Aufarbeitungsanlagen[25][26]
- Mitunter erfolgte in der Vergangenheit legale und illegale Verklappung radioaktiver Abfälle in die Ozeane[27]
- Der Großteil des bei der Reaktorkatastrophe von Tschernobyl entwichenen Plutoniums blieb in einem Umkreis von 100 Kilometer um den Reaktor.[28] Auch 1957 beim Kyschtym-Unfall in der russischen Majakanlage entwichen erhebliche Mengen an Plutonium, die hauptsächlich lokal und regional abgelagert wurden.
Gewinnung und Darstellung
Plutonium entsteht unvermeidlich in den mit 238U-reichen Isotopengemischen betriebenen Kernkraftwerken. Dabei wird ein Teil des eingesetzten 238U durch Einfang eines Neutrons und nachfolgenden Betazerfall in 239Pu umgewandelt.
- (HWZ: 24110 a)
- Die angegebenen Zeiten sind Halbwertszeiten.
Ein weiteres Neutron führt in den meisten Fällen zur Kernspaltung, zum Teil entsteht jedoch das Isotop 240Pu (HWZ: 6560 a). Da dieses Isotop nur schlecht spaltbar ist, führt weiterer Neutroneneinfang zur Entstehung von 241Pu (HWZ: 14 a), das wiederum gut spaltbar ist. Allerdings werden nicht alle Atome gespalten, so dass bei einigen davon der Brutprozess zu 242Pu (HWZ: 373000 a) und noch schwereren Isotopen fortgesetzt werden kann. Weil jedoch das spaltbare 243Pu eine sehr kurze Halbwertszeit hat (5 h), ist ein weiterer Neutroneneinfang, der meistens zur Spaltung oder – in selteneren Fällen – zur Erzeugung von Plutonium 244Pu führt, unwahrscheinlich. Der Plutonium-Brutprozess ist daher praktisch beim 243Pu zu Ende und führt über den Betazerfall von 243Pu zum Americium-Isotop 243Am (HWZ: 7370 a).
Da jede Stufe dieser aufeinander aufbauenden Kernreaktionen eine gewisse Zeit braucht, ändern sich im Laufe der Zeit die relativen Mengen der Isotope im Reaktorkern. Die Raten, mit der die Kernreaktionen ablaufen, hängen von der Geschwindigkeitsverteilung der Neutronen ab. Weil ein großer Teil der leicht spaltbaren Isotope jedoch gespalten wird und sich nicht in andere Isotope umwandelt, nimmt die mögliche Ausbeute (Effizienz) des Brutprozesses mit der Erzeugung jedes weiteren leicht spaltbaren Isotops ab.
Das leichtere Isotop 238Pu wird bei Bedarf gezielt hergestellt. Es entsteht durch Einfang mehrerer Neutronen aus dem Uran-Isotop 235U. Dabei entsteht zuerst ein 236U-Kern in einem angeregten Zustand, der eine Halbwertszeit von 120 Nanosekunden hat und sich mit hoher Wahrscheinlichkeit spaltet. Angeregte 236U-Kerne können jedoch auch durch Emission von Gamma-Strahlung in den langlebigen Grundzustand übergehen. Durch weiteren Neutroneneinfang und β-Zerfall entsteht Neptunium 237Np. Nach einer gewissen Bestrahlungszeit wird das Neptunium, das fast ausschließlich aus 237Np besteht, aus den Brennstäben extrahiert. Das Neptunium wird nun in Form von reinen Neptunium-Brennstäben wieder in einen Reaktor eingefügt und mit Neutronen bestrahlt. Es wandelt sich dabei durch Neutroneneinfang in 238Np um, das unter Aussendung von Betastrahlung zu 238Pu zerfällt.
- Die angegebenen Zeiten sind Halbwertszeiten.
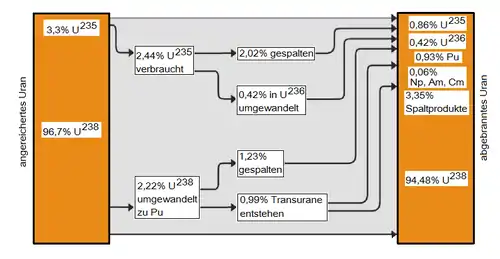
Die so behandelten Brennstäbe enthalten auch schwerere Plutoniumisotope. Außerdem werden einige der Neptunium-Atome auch von Neutronen über 6,27 MeV Energie getroffen, wodurch in geringer Menge auch 236Pu entsteht. Dieses zerfällt über die Thorium-Reihe, in der der starke Gammastrahler Thallium 208Tl vorkommt.
Wird 239Pu durch schnelle, also nicht abgebremste Neutronen gespalten, ist die durchschnittliche Zahl neu freigesetzter Neutronen pro gespaltenem Atomkern besonders hoch. In einem solchen Reaktor kann daher theoretisch mehr 238U in neues 239Pu umgewandelt werden, als gleichzeitig durch Spaltung verbraucht wird. Er wird deshalb als Brutreaktor oder „schneller Brüter“ bezeichnet. In der Praxis wurde aber bisher eine maximale Konversionsrate von 0,7 verwirklicht, das Funktionieren einer Brutreaktoren-Wirtschaft somit bisher nicht im Großen demonstriert.
Das Plutonium befindet sich nach der Herstellung zusammen mit den Spaltprodukten und unverbrauchtem Rest-Kernbrennstoff in den abgebrannten Brennelementen. Durch den PUREX-Prozess können in Wiederaufarbeitungsanlagen das entstandene Plutonium und das ebenfalls erwünschte Uran aus ihnen herausgelöst werden. Dazu wird das Material zunächst in Salpetersäure gelöst und das Plutonium und Uran mit Tri-n-butyl-phosphat extrahiert. Die Spaltprodukte und anderen Bestandteile bleiben dabei zurück. Im Jahr werden etwa 20 Tonnen Plutonium, überwiegend in Form des Isotops 239Pu, produziert.[29]
Die Weitergabe von spaltbarem Material (wie 239Pu und 241Pu) sowie von Materialien, die zu ihrer Herstellung geeignet sind, an Staaten, die keine Kernwaffen besitzen, unterliegt laut Absatz III des Atomwaffensperrvertrages der Kontrolle der Internationale Atomenergie-Organisation (IAEO).[30] In Deutschland regelt das Atomgesetz den Umgang mit spaltbarem Material. Es bestimmt, wer unter welchen Bedingungen Plutonium in Deutschland befördern und besitzen darf.[31]
Eigenschaften
Physikalische Eigenschaften
Plutonium ist bei Normalbedingungen ein silberglänzendes Schwermetall mit hoher Dichte (19,86 g/cm3[32]). Wie von allen Actinoiden existieren auch von Plutonium ausschließlich radioaktive Isotope. Es ist selbsterwärmend, pro 1 kg Plutonium entstehen etwa 2 Watt Wärmeleistung (bezogen auf 239Pu).[33] Plutonium ist im Vergleich mit anderen Metallen ein schlechter Leiter für Wärme und elektrischen Strom. Das Metall kristallisiert abhängig von der Temperatur in insgesamt sechs allotropen Modifikationen. Diese unterscheiden sich zum Teil deutlich in ihren Dichten. Die bei Raumtemperatur stabile Modifikation α-Pu ist monoklin. In Plutonium besteht bei höheren Temperaturen der seltene Fall einer Dichteanomalie, die Dichte nimmt bei der Phasenumwandlung zur δ’- und ε-Modifikation wieder zu. Auch beim Schmelzen wird, wie bei Wasser, die Dichte größer.[34] Flüssiges Plutonium besitzt die höchste Viskosität aller Elemente im flüssigen Zustand.[35] Trotz einer für Metalle anormal hohen magnetischen Suszeptibilität und der Tendenz zur Ordnung bei tiefen Temperaturen zeigt Plutonium keine Ordnung über größere Bereiche und muss deshalb als paramagnetisch bezeichnet werden.[34] Für die Messung stört allerdings das ständige Erwärmen durch den Zerfall des Plutoniums 239Pu. Dadurch sind keine Temperaturen nahe dem absoluten Nullpunkt erreichbar.
Modifikationen bei Atmosphärendruck Bezeichnung
der PhaseStabil im
TemperaturbereichDichte (Temperatur) Kristallsystem Bravais-Gitter Raumgruppe α-Pu[36] 0 K – 395 K 19,77 g/cm3 (293 K) monoklin primitiv P21/m (Nr. 11) β-Pu[37] 395 K – 479 K 17,7 g/cm3 (395 K) monoklin raumzentriert I2/m (Nr. 12, Stellung 3) γ-Pu[38] 479 K – 592 K 17,14 g/cm3 (479 K) orthorhombisch flächenzentriert Fddd (Nr. 70) δ-Pu[39] 592 K – 730 K 15,9 g/cm3 (592 K) monoklin basiszentriert Cm (Nr. 8) δ’-Pu[40] 730 K – 749 K 16,0 g/cm3 (730 K) tetragonal raumzentriert I4/mmm (Nr. 139) ε-Pu[41] 749 K – 914 K 16,5 g/cm3 (749 K) kubisch raumzentriert Im3m (Nr. 229) flüssig[42] 914 K – 3503 K 16,63 g/cm3 (914 K) — — —
Weiterhin ist eine Hochdruckmodifikation bekannt, die aus α-Pu bei einem Druck oberhalb von 40 GPa gewonnen wurde und in der Raumgruppe P63 (Raumgruppen-Nr. 173) kristallisiert.[43]
Chemische Eigenschaften

Plutonium ist ein unedles und sehr reaktives Metall. An der Luft reagiert es schnell mit Sauerstoff und Luftfeuchtigkeit. Dabei wird das Metall zunächst matt und überzieht sich mit einer dunkel blauschwarzen Oxidhaut, beim längeren Stehen an der Luft bildet sich eine dickere, graugrüne, pulverig abreibende Oxidschicht.[44] Das Metall reagiert beim Erhitzen mit den meisten Nichtmetallen und Wasser. Bei Raumtemperatur wird es dagegen von Wasser und alkalischen Lösungen nicht angegriffen. In konzentrierter Salpetersäure ist es wegen Passivierung nicht löslich.[33] Löslich ist Plutonium in Salzsäure und fluoridhaltiger Salpetersäure. Die Fluoridionen unterdrücken hierbei die ansonsten einsetzende Passivierung des Metalls. Die chemischen Eigenschaften des Plutoniums ähneln denen anderer Actinoiden. Ähnlich wie bei vielen anderen dieser Elemente bestimmt bei Plutonium die starke Radioaktivität die chemischen Eigenschaften mit, da durch die entstehende Wärme Bindungen aufgebrochen werden können. Auch die freiwerdende Strahlung kann zum Bruch von Bindungen führen.
Plutonium besitzt eine Reihe von Verbindungen, in denen es in den Oxidationsstufen +3 bis +7 vorliegen kann. Damit bildet Plutonium zusammen mit Neptunium die höchste Oxidationsstufe aller Actinoiden. Die stabilste Stufe ist +4. In wässriger Lösung haben die Plutoniumionen charakteristische Farben, so ist das Pu3+-Ion violett, Pu4+ braun, PuVO2+ purpurfarben, PuVIO22+ orange und PuVIIO23+ grün.[45]
Biologische Aspekte
Eine biologische Funktion des Plutoniums ist nicht bekannt. Weitere Forschungen und Untersuchungen konzentrierten sich auf mikrobielle Wechselwirkungen mit Plutonium, um auf diesem Wege kontaminierte Deponien und Umgebungen zu sanieren.[46] Enterobakterien der Gattung Citrobacter können durch die Phosphataseaktivität in ihrer Zellwand Pu(IV) aus wässriger Lösung ausfällen und als Lanthan-Phosphat-Komplex binden.[47]
Isotope
Von Plutonium wurden 20 Isotope und 15 Kernisomere mit Massenzahlen von 228 bis 247 vermessen.[48] Die Halbwertszeiten liegen zwischen 37 · 10−12 s für das Isomer 236″m1Pu und 80 Mio. Jahren für 244Pu. Die langlebigsten Isotope mit Halbwertszeiten größer als 11 Tagen haben Massenzahlen zwischen 236 und 244. Das Isotop 243Pu ist mit einer Halbwertszeit von weniger als 5 Stunden[48] eine Ausnahme. Einige der Plutonium-Isotope werden als Ausgangspunkte für radioaktive Zerfallsreihen angesehen.
- 236Pu zerfällt über die Thorium-Reihe. Es kommt mit einer Halbwertszeit von 2,858 Jahren[48] durch α-Zerfall auf die Zwischenstufe 232U, die mit einer Halbwertszeit von 68,9 Jahren zu 228Th zerfällt, das auf dem Hauptstrang der Reihe liegt. Dieses Isotop wird in Kernreaktoren, die mit Uran betrieben werden, nur in winzigen Mengen erbrütet.
- 237Pu wandelt sich mit einer Halbwertszeit von 45,2 Tagen[48] zu 99,9958 % durch Elektroneneinfang in das Neptunium-Isotop 237Np um, das der offizielle Startpunkt der Neptunium-Reihe ist. Die restlichen 0,0042 % zerfallen durch α-Zerfall zu Uran 233U, das ebenfalls über die Neptunium-Reihe zerfällt.
- 238Pu ist ein α-Strahler mit einer Halbwertszeit von 87,7 Jahren.[48] Es zerfällt zunächst in 234U und weiter über die Zerfallskette der Uran-Radium-Reihe.
- 239Pu ist das am häufigsten produzierte Plutoniumisotop. Es hat eine Halbwertszeit von 24.110 Jahren[48] und zerfällt überwiegend unter Abgabe von α-Strahlung in 235U. Der weitere Zerfall folgt der Uran-Actinium-Reihe für natürliche Radioaktivität, die bei 235U beginnt. Zu einem Anteil von 3 · 10−10 % tritt Spontanspaltung auf.
- 240Pu zerfällt mit einer Halbwertszeit von 6564 Jahren[48] durch α-Strahlung in 236U. Dieses Uran-Isotop zerfällt mit einer Halbwertszeit von 23,4 Mio. Jahren zum natürlichen 232Th. Der weitere Zerfall folgt der Thorium-Reihe.
- 241Pu wird oft als Beginn der Neptunium-Reihe bezeichnet, da es (bei Verlängerung der Reihe) vor dem Neptunium steht. Es zerfällt mit einer Halbwertszeit von 14,35 Jahren[48] und einer Wahrscheinlichkeit von 99,9975 % mit einem β-Zerfall zu 241Am, sowie mit 0,0025 % Wahrscheinlichkeit unter α-Zerfall zu 237U. 241Am zerfällt unter α-Zerfall (t1/2 = 432,2 a) und 237U durch β-Zerfall zum gleichen langlebigen Neptuniumisotop 237Np, welches ein Alphastrahler ist und eine Halbwertszeit von 2,14 Mio. Jahre aufweist. Diese sehr lange Halbwertszeit ist das Problem für die Sicherheitsnachweise von Endlagern, wenn 241Pu nicht in Mischoxidbrennelementen in einer Kernspaltung zu Isotopen transmutiert wird, in dessen Zerfallsreihe kein 237Np vorkommt.
- 242Pu zerfällt über die gleiche Zerfallskette wie 238Pu. Während jedoch 238Pu als Seitenarm beim 234U auf die Zerfallskette kommt, steht 242Pu noch vor dem 238U. Plutonium 242Pu zerfällt durch α-Zerfall in 238U, den Beginn der natürlichen Uran-Radium-Reihe. Mit einer Halbwertszeit von 375.000 Jahren[48] ist es nach 244Pu das langlebigste Isotop.
- 243Pu ist mit einer Halbwertszeit von 4,956 h[48] kurzlebig. Es geht zunächst durch β-Strahlung in Americium 243Am über, das in Neptunium 239Np übergeht und weiter zu 239Pu zerfällt. Damit steht es in Verlängerung der Uran-Actinium-Reihe.
- 244Pu ist wegen seiner vergleichsweise langen Halbwertszeit von 80 Mio. Jahren[48] (Das Alter der Erde entspricht 56 Halbwertszeiten) das einzige in winzigsten Spuren (2 · 10-20 %) natürlich vorkommende Plutonium-Isotop.[19] Es ist der Ausgangspunkt der Thorium-Reihe, die darum manchmal auch Plutonium-Thorium-Reihe genannt wird. 244Pu zerfällt durch α-Zerfall zu 240U, dieses durch zwei β-Zerfälle über 240Np zu 240Pu, dieses dann wieder durch zwei weitere α-Zerfälle über 236U zum 232Th. Danach folgt der Zerfall der Thorium-Reihe.
Spaltbarkeit
Alle Plutoniumisotope mit ungerader Neutronenzahl zählen zu den wenigen Nukliden, die leicht, d. h. schon durch thermische Neutronen gut spaltbar sind. Der entsprechende Wirkungsquerschnitt beträgt beim 239Pu 752 Barn (b) und beim 241Pu 1010 b, bei den geradzahligen 238Pu, 240Pu und 242Pu dagegen nur 17 b, 0,4 b bzw. < 0,2 b.[49] Das recht kurzlebige geradzahlige 236Pu (Halbwertszeit 2,9 Jahre) hat mit 169 b einen mittelgroßen Spaltquerschnitt.[50]
Alle langlebigen Plutoniumisotope spalten sich auch spontan. Die Spontanspaltungsrate ist bei 239Pu am geringsten und nimmt sowohl zu den leichteren als auch den schwereren Isotopen hin stark zu. Von Spontanspaltung betroffen sind sowohl die Isotope mit ungerader als auch gerader Neutronenzahl. Insbesondere weist 240Pu eine ca. 70.000-fach höhere Spontanspaltungsrate als 239Pu auf. Da die bei der Spontanspaltung freigesetzten Neutronen bei einer Atombombe zu einer Frühzündung und stark reduzierten Explosionswirkung führen können, ist 240Pu für Kernwaffen unerwünscht. Waffenplutonium enthält möglichst wenig 240Pu, ist aber nie ganz frei davon.
Alle Plutoniumisotope, auch solche mit gerader Neutronenzahl, lassen sich durch schnelle Neutronen spalten, und sind daher prinzipiell für den Bau von Kernwaffen geeignet. Die Spaltbarkeit von Plutonium durch schnelle Neutronen nimmt mit zunehmender Neutronenzahl ab.[51]
Die für den Atombombenbau relevante kritische Masse wird sowohl von der Spaltbarkeit mit langsamen als auch mit schnellen Neutronen bestimmt, da aufgrund der vergleichsweise geringen Spaltquerschnitte mit schnellen Neutronen (1 bis 3 Barn) in einer Atombombe ein Teil der Neutronen nach zahlreichen Stößen mit Plutonium-Kernen doch auf thermische Energien abgebremst wird, bevor er eine erneute Kernspaltung auslösen kann. Bei 236Pu beträgt die kritische Masse 8,04–8,42 kg,[52] bei 237Pu, welches sich sowohl durch schnelle wie langsame Neutronen sehr gut spalten lässt, nur 3,1 kg. Beide vorgenannten Isotope werden jedoch wegen ihrer hohen Spontanspaltungsrate, kurzen Halbwertszeit, hohen Wärmeproduktion und komplizierten Gewinnung nicht für Kernwaffen verwendet. Das für Nuklearbatterien verwendete 238Pu hat nach Berechnungen eine kritische Masse von ca. 9,04–10,31 kg.[53] Beim wichtigsten Isotop für Kernwaffen, 239Pu, beträgt die kritische Masse (wie auch bei allen anderen Angaben ohne Moderator und/oder Reflektor) 10 kg.[54] Bei 241Pu sind es schon 12,27–13,04 kg.[52]
§ 2 Abs. 1 des Atomgesetzes (Deutschland) ordnet die Plutonium-Isotope 239Pu und 241Pu als "besondere spaltbare Stoffe" den Kernbrennstoffen zu.
Zwei der vielen Möglichkeiten für die neutroneninduzierte Kernspaltung von 239Pu:
Verwendung
Nur 238Pu und 239Pu werden in größeren Mengen verwendet. 238Pu ist, wenn es aus Neptunium erbrütet wird, mit anderen Plutoniumisotopen verunreinigt.[55] Nur 238Pu, das über den Umweg von Curium 242Cm erbrütet wird, ist frei von 236Pu.
239Pu ist immer mit 240Pu und noch geringeren Mengen von 241Pu und 242Pu verunreinigt.[56]
Verwendung in Kernkraftwerken
Beim Betrieb von Kernreaktoren entsteht aus dem Uran in den Brennelementen Plutonium. Dieses wird, nach Abtrennung in einer Wiederaufarbeitungsanlage, zusammen mit angereichertem Uran zu MOX-Brennelementen für Leichtwasserreaktoren verarbeitet. Dort erhöht die Verwendung von MOX anstelle von reinem Uranbrennstoff bestimmte Betriebsrisiken geringfügig: der Anteil der verzögerten Neutronen (siehe Kritikalität) nimmt um einige Prozent ab und der schnelle Neutronenfluss – der Strahlenschaden am Reaktordruckbehälter bewirkt – nimmt um wenige Prozent zu.
Ein MOX-Brennstoff mit etwa zehnfach höherer Anreicherung der spaltbaren Isotope wird in Brutreaktoren verwendet.[57]
Militärische Verwendung
Für Kernwaffen geeignetes Waffenplutonium (englisch weapons grade Plutonium) muss möglichst viel 239Pu und möglichst wenig 240Pu enthalten. Ab einem Gehalt von etwa 92 % 239Pu gilt Plutonium als waffenfähig. Nach Ansicht der IAEO ist jedoch jedes Plutonium grundsätzlich geeignet für militärische Zwecke. Als Reaktorplutonium wird Plutonium bezeichnet, das im Normalbetrieb von Kernkraftwerken anfällt; es kann bis zu 31 % 240Pu enthalten.[58]
240Pu ist nicht durch thermische Neutronen spaltbar, zerfällt aber durch Spontanspaltung. Dabei werden Neutronen frei, die eine unerwünschte Frühzündung der Plutoniumbombe bewirken können und die Berechnung der Sprengkraft ungenau machen. Militärisch ist eine exakte Zündung und präzise Voraussage der Sprengkraft erwünscht. Auch die Zerfallswärme des Alphastrahlers 238Pu wirkt störend.
Für die Produktion von Waffenplutonium in Kernreaktoren ist eine möglichst kurze Bestrahlungszeit erforderlich: je länger diese ist, desto mehr 240Pu entsteht aus 239Pu (siehe auch Kernreaktor#Brutreaktionen). Deshalb lässt sich aus einem Kernreaktor mit laufender Stromerzeugung Waffenplutonium sinnvoll nur gewinnen, wenn es sich um einen Druckröhrenreaktor handelt, denn nur bei ihm können einzelne Brennelemente bei laufendem Betrieb ausgetauscht werden (Reaktortypen z. B. CANDU, RBMK). Dagegen befinden sich bei den deutschen Kernkraftwerken alle Brennelemente zusammen im Reaktordruckbehälter, und eine Brennelemententnahme erfordert ein aufwändiges Herunterfahren („Abfahren“) der Anlage, was nicht geheim zu halten wäre (z. B. keine Wasserdampfwolken über den Kühltürmen mehr).[59]
Russland erzeugte sein Waffenplutonium in speziell dafür gebauten Reaktoren des Typs ADE; der letzte von ihnen wurde nach 46 Jahren Betrieb 2010 stillgelegt.
Die USA und Russland haben sich 2010 im Plutonium Management and Disposition Agreement darauf geeinigt, ihre Bestände an Waffen-Plutonium um je 34 Tonnen zu verringern. Ein ergänzendes Protokoll unterzeichneten die Außenminister Hillary Clinton und Sergei Lawrow in Washington. Russland kostet dies 2,5 Mrd. Dollar; davon übernehmen die USA 400 Mio. Dollar. Beseitigt werden kann das Plutonium durch Endlagerung nach einer Vermischung mit anderen Nuklearabfällen oder durch eine Umarbeitung in MOX-Elemente.[60]

Radionuklidbatterien für die Raumfahrt
Eine ausreichend große, kompakt angeordnete Menge von 238Pu erhitzt sich durch seinen eigenen radioaktiven Zerfall bis zur Weißglut und gibt dabei nur sehr geringe Mengen von Gammastrahlung ab, sodass man mit der dünnsten Abschirmung im Vergleich zu fünf anderen potenziell geeigneten Nukliden auskommt.[61] Es wird deshalb in oxidierter Form als chemisch träges Plutoniumdioxid zur Erzeugung elektrischer Energie in Radionuklidbatterien verwendet.
Radionuklidbatterien werden wegen ihrer Langlebigkeit in der interplanetaren Raumfahrt eingesetzt, vor allem für Raumsonden, die das äußere Sonnensystem erreichen sollen. Denn Solarzellen liefern in großer Sonnenentfernung nicht mehr genug Energie. Eingebaut wurden solche Nuklearbatterien beispielsweise in die Voyager-Sonden, Cassini-Huygens (1997–2005 zu Saturn) oder New Horizons (2006–2015 zu Pluto); ebenso in Perseverance (2020 Marsrover). Früher wurden Radionuklidbatterien mit Plutonium 238Pu auch in erdumkreisenden Satelliten verwendet.[62]
1964 verglühte der Satellit Transit 5BN-3 der USA mit einer Radionuklidbatterie an Bord bei einem Fehlstart etwa 50 Kilometer über dem Pazifik. Der Satellit enthielt knapp ein Kilogramm Plutonium, welches sich anschließend messbar auf der gesamten Nordhalbkugel verteilte.[63]
1996 stürzte die russische Sonde Mars 96, an der Deutschland beteiligt war, mit 270 Gramm Plutonium an Bord ab – in den Pazifik oder auf das südamerikanische Festland.[64]
236Pu-freies 238Pu wurde in den 1970er Jahren in Herzschrittmachern verwendet,[65][66] und wurde über den Umweg der wenig ergiebigen und deshalb teuren Erbrütung von Curium 242Cm produziert. Dieses entsteht durch einen Neutroneneinfang von Americium 241Am, das wiederum aus 241Pu gewonnen wird.[67]
- Die angegebenen Zeiten sind Halbwertszeiten.
Neutronenquelle
Ferner wird 238Pu zusammen mit Beryllium als Neutronenquelle verwendet, wobei ein α-Teilchen aus dem Zerfall des Plutoniums den Berylliumkern trifft und unter Aussendung eines Neutrons in diesen eingebaut wird.
Toxizität
Plutonium ist wie viele andere Schwermetalle giftig und schädigt besonders die Nieren. Es bindet ebenfalls an Proteine im Blutplasma und lagert sich unter anderem in den Knochen und der Leber ab. Die für einen Menschen tödliche Dosis liegt wahrscheinlich im zweistelligen Milligrammbereich, für Hunde beträgt die LD50-Dosis 0,32 mg/kg Körpergewicht.[34] Die chemische Giftigkeit von Plutonium wird jedoch von vielen anderen Stoffen übertroffen.
Viel gefährlicher als die chemische Wirkung ist – wegen der verschiedenen physikalischen Eigenschaften isotopenabhängig – seine hohe Radioaktivität, die Erbgutschäden und damit u. a. Krebs verursachen kann, aber auch Symptome wie bei einer normalen Schwermetallvergiftung. Bereits die Inhalation von 40 Nanogramm 239Pu reicht aus, um den Grenzwert der Jahres-Aktivitätszufuhr für Inhalation und Ingestion zu erreichen.[68] Die von Plutonium 239Pu ausgesendete α-Strahlung wird zwar außerhalb des Körpers bereits durch die oberste Hautschicht aus abgestorbenen Zellen abgeschirmt, diesen Schutz gibt es aber nicht bei Inkorporation, beispielsweise durch Inhalation von Plutonium enthaltenden Staub, oder durch kontaminierte Nahrung.
Nach Untersuchungen von Arnulf Seidel vom Institut für Strahlenbiologie des Kernforschungszentrum Karlsruhe führen kleine Dosen 239Pu im Langzeitversuch erst nach frühestens zehn Jahren bei Hunden zu Knochenkrebs, wobei es eine fünfmal größere Gefährlichkeit als Radium zeigt. Der Grund dafür kann eine ungleichmäßige Verteilung des Plutoniums im Skelett sein, die zu punktuell stark bestrahlten Stellen führt.[69]
Das wie auch 240Pu in Kernreaktoren immer miterbrütete 241Pu zerfällt mit etwa 14 Jahren Halbwertszeit in Americium 241Am, das große Mengen relativ weicher Gammastrahlung abgibt. In gelagertem Plutonium erreicht die Konzentration von 241Am nach etwa 70 Jahren ihren Höchststand. Weil die Plutoniumisotope selbst kaum Gammastrahlung abgeben, nimmt diese Strahlung (und damit die Dicke der benötigten Abschirmung) wegen des gebildeten Americiums zunächst deutlich zu, um dann nach etwa 70 Jahren Lagerung wieder abzunehmen. Wegen der längeren Halbwertzeit von 241Am (432 Jahre) erfolgt diese Abnahme deutlich langsamer als der Anstieg.[70]
Sicherheitshinweise
Einstufungen nach der CLP-Verordnung liegen nicht vor, obwohl die chemische Giftigkeit bekannt ist. Beim Umgang mit Plutonium ist vor allem wegen seiner starken Radioaktivität äußerste Vorsicht geboten. Da die α-Strahlung des Plutoniums nur auf kurze Reichweiten wirkt, ist besonders darauf zu achten, dass das Metall nicht in den Körper gelangt. Da während des Zerfalls Wärme entsteht, muss diese abgeführt werden. Dazu bewahrt man Plutonium am besten unter trockener zirkulierender Luft auf.[33] Feinverteiltes Plutonium ist pyrophor.
Weiterhin muss unbedingt verhindert werden, dass eine kritische Masse entsteht, die zur nuklearen Kettenreaktion und damit zu unkontrollierter Energie- und Strahlungsfreisetzung führt. Die Unterkritikalität kann entweder durch ausreichend kleine Massen oder eine sichere Geometrie erreicht werden. Bei dieser ist die Oberfläche groß genug, so dass mehr Neutronen verloren gehen als bei neutroneninduzierten Spaltungen entstehen. Eine weitere Möglichkeit ist der Einsatz neutronenabsorbierender Materialien wie Bor, die diese vor möglichen neuen Spaltungsreaktionen abfangen. Grundsätzlich ist zu beachten, dass die kritische Masse durch die Anwesenheit bestimmter Stoffe, insbesondere Wasser, aufgrund derer neutronenmoderierenden oder -reflektierenden Wirkungen auch stark gesenkt werden kann.
Verbindungen

→ Kategorie Plutoniumverbindung
Oxide
Die stabilste und wichtigste Sauerstoffverbindung ist Plutoniumdioxid (PuO2). Diese Verbindung ist ein Feststoff mit hoher Schmelztemperatur. Es ist gegenüber Wasser stabil und nicht in diesem löslich. Plutonium wird daher in Radionuklidbatterien und Kernkraftwerken in Form dieses Oxids verwendet. Neben Plutoniumdioxid sind auch Plutonium(III)-oxid Pu2O3 und Plutonium(II)-oxid PuO bekannt.[71]
Halogenide
Mit den Halogenen Fluor, Chlor, Brom und Iod bildet Plutonium zahlreiche Verbindungen. Von allen Halogenen ist eine entsprechende Plutoniumverbindung in der Oxidationsstufe +3 bekannt. Daneben existieren noch Plutonium(IV)-fluorid, Plutonium(IV)-chlorid und Plutonium(VI)-fluorid.[72]
| Oxidationszahl | F | Cl | Br | I |
| +6 | Plutonium(VI)-fluorid PuF6 rotbraun |
|||
| +4 | Plutonium(IV)-fluorid PuF4 rotbraun |
Plutonium(IV)-chlorid PuCl4 |
||
| +3 | Plutonium(III)-fluorid PuF3 violett |
Plutonium(III)-chlorid PuCl3 grün |
Plutonium(III)-bromid PuBr3 grün |
Plutonium(III)-iodid PuI3 grün |
Boride
Es gibt vier bekannte Plutoniumboride. Sie werden genutzt, um die Neutronenemission von Plutoniummaterial und damit die Gefahr einer Kritikalität zu vermindern.
Metallorganische Verbindungen
Analog zu Uranocen, einer Organometallverbindung in der Uran von zwei Cyclooctatetraen-Liganden komplexiert ist, wurden die entsprechenden Komplexe von Thorium, Protactinium, Neptunium, Americium und auch des Plutoniums, (η8-C8H8)2Pu, dargestellt.[73]
Analytik
Für Plutonium gibt es aufgrund seiner Seltenheit keine klassischen, nasschemischen Nachweismethoden. Deshalb werden nur instrumentelle Verfahren eingesetzt.
α-Spektrometrie
Plutonium wird häufig über die α-Strahlung der Isotope 239(40)Pu und 238Pu nachgewiesen. Eine direkte Analyse ist oft nicht möglich, sodass vorangehende Separationstechniken durchgeführt werden müssen. Häufig kommt dabei die Ionenaustauschchromatographie zum Einsatz. Mit Hilfe der α-Spektrometrie konnte 239(40)Pu in maritimen Sedimenten mit einer Nachweisgrenze von 1 mBq/g bestimmt werden.[74]
Elementmassenspektrometrie (MS)
Für die Plutoniumbestimmung kommen in der Massenspektrometrie die ICP-Ionisierung (ICP, induktiv-gekoppeltes Plasma, Massenspektrometrie mit induktiv gekoppeltem Plasma) und die AMS (Beschleuniger-Massenspektrometrie) zum Einsatz. Im Vergleich zur ICP-MS ist die AMS sensitiver aber apparativ aufwändig und kostenintensiv, da ein Teilchenbeschleuniger zur Ionisierung verwendet werden muss. Mit der AMS konnte am VERA-System in Wien eine Nachweisgrenze von etwa 106 Atomen des Isotops 239Pu erreicht werden. Mit Hilfe der ICP-Technik konnte eine Nachweisgrenze von 108 Atomen 239Pu erzielt werden, was einer Aktivität von 0,1 mBq entspricht.[75][76]
Optische Emissionsspektrometrie (OES)
Plutonium kann auch mit einer laserbasierten Variante der optischen Emissionsspektrometrie (OES) nachgewiesen werden. Bei der Laser Induced Breakdown Spectroscopy (LIBS) nutzt man kurze Laserimpulse zur Verdampfung und Emissionsstimulation der Probe. Zur Emissionsmessung steht ein breites Spektrum an Linien zur Verfügung, wobei aufgrund der besten Intensitätswerte meist auf die Linien bei 295,16 nm, 300,06 nm und 363,22 nm zurückgegriffen wird. Mit dieser Technik konnte eine Nachweisgrenze von 10−8 g/mL erzielt werden.[77][78] Die gleiche Nachweisgrenze konnte mit der optischen Emissionsspektrometrie mittels induktiv gekoppeltem Plasma (ICP-OES) erzielt werden.[77]
Laserinduzierte photoakustische Spektrometrie (LIPAS)
Bei der LIPAS-Technik wird ein hochenergetischer Laserimpuls in die Probelösung geschickt, welcher eine photoakustische Welle induziert. Mit Hilfe eines piezoelektrischen Detektors wird die Amplitude dieser Welle bestimmt. Mit dieser Technik konnte sechswertiges Plutonium mit einer Nachweisgrenze von 0,5 µg/mL nachgewiesen werden.[79][80]
Produktionsnachweis außerhalb des Reaktors
Forscher des Sandia National Laboratories wollen die beim Betazerfall von Spaltprodukten emittierten Antineutrinos dazu verwenden, die Produktion von Plutonium in Kernreaktoren zu messen, damit die IAEO nicht mehr auf Schätzungen angewiesen ist und kein Plutonium unbemerkt für den Bau von Atomwaffen abgezweigt werden kann. Wegen der extrem hohen Produktionsrate von Antineutrinos in Kernreaktoren würde schon ein Detektor mit 1 m3 Detektorflüssigkeit vor dem Kernkraftwerk reichen.[81]
Plutoniuminventar
Deutschland meldete zum Ende des Jahres 2009 einen Plutoniumbestand von 5,4 t separiertem unbestrahltem Plutonium in frischen MOX-Brennelementen oder anderen gefertigten Produkten an die IAEO. Hinzu kamen 86,9 t Plutonium in bestrahlten Brennelementen, welche an den deutschen Reaktoren gelagert wurden sowie weitere 5,9 t in bestrahltem Brennstoff, der an anderen Standorten gelagert wurde.[82]
Die Schweiz berichtete an die IAEO zum Ende des Jahres 2010 einen Plutoniumbestand von weniger als 50 kg separiertem Plutonium. Hinzu kamen 13 t Plutonium in bestrahlten Brennelementen, welche an den Reaktorstandorten gelagert wurden sowie weitere 4 t in bestrahltem Brennstoff, der an anderen Standorten gelagert wurde.[83]
Das weltweite Inventar an Plutonium ist zum Stand des Jahres 1999 angegeben.[84] Die Angaben beruhen auf Schätzungen des Department of Energy. Die Zahlen in Klammern geben den aus dem abgebrannten Brennstoff extrahierten Plutoniumanteil an. Für Kasachstan wurde laut des Bulletin of the Atomic Scientist[84] die Plutoniumqualität durch das Department of Energy falsch klassifiziert und sollte kommerziell sein. Waffenfähiges Plutonium (weapons grade) enthält weniger als 7 % des Isotops 240Pu. Plutonium kommerzieller Qualität (commercial grade) setzt sich aus Brennstoffplutonium (fuel grade) mit 7 bis 18 % 240Pu und Reaktorplutonium (reactor grade) mit mehr als 19 % 240Pu zusammen.
Staat
(Stand 1999)waffenfähig (in t) kommerzielle
Qualität (in t)Argentinien 0 6 Belgien 0 23–31 Brasilien 0 0,6 Großbritannien 7,6 98,4 (51) Volksrepublik China 1,7–2,8 1,2 Frankreich 6–7 151–205 (70) Deutschland 0 75–105 (17) Indien 0,15–0,25 6 Israel 0,3–0,5 0 Japan 0 119–262 (21) Kasachstan 2–3* 0 Nordkorea 0,025–0,035 0 Russland 140–162 65 (30) USA 85 257,2 (14,5) Gesamt 242,3–267,4 802,4–1037,4 (≈203,5)
2000 haben USA und Russland ein Abkommen geschlossen, jeweils 34 t Plutonium zu entsorgen oder zu entschärfen. Vor dem Hintergrund politischer Spannungen erklärt der Kreml im Oktober 2016 „Russland ist es nicht mehr möglich, dieses Abkommen alleine umzusetzen“.[85]
Literatur
- Kate Brown: Plutopia: Nuclear Families, Atomic Cities, and the Great Soviet and and American Plutonium Disasters. Oxford University Press, New York 2013, ISBN 978-0-19-985576-6.
- David L. Clark, Siegfried S. Hecker, Gordon D. Jarvinen, Mary P. Neu: Plutonium. In: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements. Springer, Dordrecht 2006, ISBN 1-4020-3555-1, S. 813–1264 (doi:10.1007/1-4020-3598-5_7).
Weblinks
- Eintrag zu Plutonium. In: Römpp Online. Georg Thieme Verlag, abgerufen am 3. Januar 2015.
- Shenda M. Baker: Plutonium, Chemical & Engineering News, 2003
- Plutonium: Human Health Fact Sheet (englisch, PDF, 57 kB)
- Plutonium Manufacture and Fabrication (englisch)
- Institute for Energy and Environmental Research (englisch)
- Altlast Plutonium, Deutschlandfunk
Einzelnachweise
- https://www.seilnacht.com/Lexikon/94Pluton.html Thomas Seilnacht zu Plutonium, abgerufen am 9. Nov. 2019
- Die Werte der atomaren und physikalischen Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Plutonium) entnommen.
- Eintrag zu plutonium in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: NIST, Gaithersburg, MD. doi:10.18434/T4W30F (https://physics.nist.gov/asd). Abgerufen am 13. Juni 2020.
- Eintrag zu plutonium bei WebElements, https://www.webelements.com, abgerufen am 13. Juni 2020.
- Die Werte der atomaren und physikalischen Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Plutonium) entnommen.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Magnetic Susceptibility of the Elements and Inorganic Compounds, S. 4-145. Die Werte dort sind auf g·mol−1 bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3, S. 469–476.
- Die Werte der atomaren und physikalischen Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Plutonium) entnommen.
- Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieses Element entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- G. T. Seaborg, E. McMillan, J. W. Kennedy, A. C. Wahl: Radioactive Element 94 from Deuterons on Uranium. In: Physical Review. 69 (7–8), 1946, S. 366–367 (doi:10.1103/PhysRev.69.367).
- J. W. Kennedy, G. T. Seaborg, E. Segrè, A. C. Wahl: Properties of Element 94. In: Physical Review. 70 (7–8), 1946, S. 555–556 (doi:10.1103/PhysRev.70.555).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1948.
- Marco Fontani: The Lost Elements. Oxford University Press, 2014, ISBN 978-0-19-938336-8 (eingeschränkte Vorschau in der Google-Buchsuche).
- B. B. Cunningham, L. B. Werner: The First Isolation Of Plutonium. In: Journal of the American Chemical Society. 71 (5), 1949, S. 1521–1528 (doi:10.1021/ja01173a001).
- Carl Friedrich von Weizsäcker: Eine Möglichkeit der Energiegewinnung aus Uran 238, 17. Juli 1940. In: Geheimdokumente zum deutschen Atomprogramm 1938–1945. Deutsches Museum, abgerufen am 8. März 2010.
- Markus Becker: Nuklear-Forensik: "Heisenberg-Würfel" verrät Details über Hitlers Atomprogramm. In: Spiegel Online. 19. März 2009, abgerufen am 7. Mai 2009.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1949.
- D. F. Peppard, M. H. Studier, M. V. Gergel, G. W. Mason, J. C. Sullivan, J. F. Mech: Isolation of Microgram Quantities of Naturally-occurring Plutonium and Examination of its Isotopic Composition. In: J. Am. Chem. Soc. 73 (6), 1951, S. 2529–2531 (doi:10.1021/ja01150a034).
- D. C. Hoffman, F. O. Lawrence, J. L. Mewherter, F. M. Rourke: Detection of Plutonium-244 in Nature. In: Nature. 234, 1971, S. 132–134 (doi:10.1038/234132a0).
- kernenergie-wissen.de: Was ist Plutonium? (Memento vom 25. Dezember 2013 im Internet Archive)
- Jan Dönges, Spuren im Ozeanboden: Als Plutonium auf die Erde rieselte, Spektrum.de, 2021-05-17, abgerufen über: https://www.spektrum.de/news/spuren-im-ozeanboden-als-plutonium-auf-die-erde-rieselte/1874062
- Pavel Podvig: Can the US-Russia plutonium disposition agreement be saved? Bulletin of the Atomic Scientists, 28. April 2016.
- Plutonium in den Tiefen der Weltmeere; Plutonium in the environment en.wo, abgerufen am 2. Mai 2012.
- Karlsruhe (Germany) Kernforschungszentrum: KFK.. 1993 (eingeschränkte Vorschau in der Google-Buchsuche).
- Johannes Friedrich Diehl: Radioaktivität in Lebensmitteln. John Wiley & Sons, 2008, ISBN 978-3-527-62374-7, S. 82 (eingeschränkte Vorschau in der Google-Buchsuche).
- Rudolf Stagl: Auswirkungen der Offenlegungspflicht der plutoniumverarbeitenden Anlage Rocky Flats auf Wahrnehmung und Bodenmarkt im Raum Denver/Boulder (Colorado, U.S.A.). Reimer, 1986, ISBN 978-3-496-00881-1 (eingeschränkte Vorschau in der Google-Buchsuche).
- Lasse Ringius: Radioactive waste disposal at sea – public ideas, transnational policy entrepreneurs, and environmental regimes. MIT Press, Cambridge 2001, ISBN 0-262-18202-5, S. 23 (eingeschränkte Vorschau in der Google-Buchsuche), abgerufen am 2. Mai 2012.
- Presseerklärung der IAEO zu Tschernobyl (1995) S. 9 (Memento vom 13. April 2006 im Internet Archive) (PDF; 180 kB).
- dtv-Atlas zur Chemie. Band 1, dtv, 2000.
- Deutsche Übersetzung des Atomwaffensperrvertrags des deutschen Bundesaußenministeriums.
- Gesetz über die friedliche Verwendung der Kernenergie und den Schutz gegen ihre Gefahren (Atomgesetz).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 2149.
- Norman N. Greenwood, Alan Earnshaw: Chemie der Elemente. 1. Auflage. VCH Verlagsgesellschaft, Weinheim 1988, ISBN 3-527-26169-9.
- Plutonium: An Element at odds with itself. In: Los Alamos Science. 26, 2000. (PDF; 881 kB)
- www.kernchemie.de (Plutonium – Element mit vielen Facetten).
- W. H. Zachariasen, F. H. Ellinger: The Crystal Structure of alpha Plutonium Metal. In: Acta Cryst. 16, 1963, S. 777–783 (doi:10.1107/S0365110X63002012).
- W. H. Zachariasen, F. H. Ellinger: The Crystal Structure of beta Plutonium Metal. In: Acta Cryst. 16, 1963, S. 369–375 (doi:10.1107/S0365110X63000992).
- W. H. Zachariasen: Crystal Chemical Studies of the 5f-Series of Elements. XXIV. The Crystal Structure and Thermal Expansion of γ-Plutonium. In: Acta Cryst. 8, 1955, S. 431–433 (doi:10.1107/S0365110X55001357).
- K. T. Moore, P. Söderlind, A. J. Schwartz, D. E. Laughlin: Symmetry and Stability of δ Plutonium: The Influence of Electronic Structure. In: Physical Review Letters. 96 (20), 2006, S. 206402/1–206402/4 (doi:10.1103/PhysRevLett.96.206402).
- F. H. Ellinger: Crystal structure of delta’ plutonium and the thermal expansion characteristics of delta, delta’ and epsilon plutonium. In: Journal of Metals. 8, 1956, S. 1256–1259.
- J. B. Ball, J. A. Lee, P. G. Mardon, J. A. L. Robertson: Determination de quelques proprietes physiques du plutonium metal. In: Memoires Scientifiques de la Revue de Metallurgie. 57, 1960, S. 49–56.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Density of Molten Elements and Representative Salts, S. 4-141.
- S. Dabos-Seignon, J. P. Dancausse, R. Gering, S. Heathman, U. Benedict: Pressure induced phase transition in α-Pu. In: Journal of Alloys and Compounds. 190, 1993, S. 237–242 (doi:10.1016/0925-8388(93)90404-B).
- Georg Brauer (Hrsg.): Handbuch der Präparativen Anorganischen Chemie. 3., umgearb. Auflage. Band II. Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 1293.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1956.
- The Biochemical Periodic Tables – Plutonium.
- P. Yong, L. E. Macaskie: Bioaccumulation of Lanthanum, Uranium and Thorium, and Use of a Model System to develop a Method for the Biologically-mediated Removal of Plutonium from Solution. In: Journal of Chemical Technology & Biotechnology. Band 71, Nr. 1, 1998, S. 15–26, doi:10.1002/(SICI)1097-4660(199801)71:1<15::AID-JCTB773>3.0.CO;2-8.
- G. Audi, O. Bersillon, J. Blachot, A. H. Wapstra: The NUBASE evaluation of nuclear and decay properties. In: Nuclear Physics. Band A 729, 2003, S. 3–128. doi:10.1016/j.nuclphysa.2003.11.001. (PDF; 1,0 MB).
- G. Pfennig, H. Klewe-Nebenius, W. Seelmann-Eggebert (Hrsg.): Karlsruher Nuklidkarte. 6. Auflage. korrig. Nachdr. 1998.
- Isotopendaten zu Plutonium-236 auf atom.kaeri.re.kr, abgerufen am 12. August 2012.
- Isotopendaten zu Plutonium auf atom.kaeri.re.kr, abgerufen am 12. August 2012; für Details zunächst das Isotop wählen, dann auf „n-XS Summary“ klicken.
- Institut de Radioprotection et de Sûreté Nucléaire: Evaluation of nuclear criticality safety data and limits for actinides in transport (Memento vom 18. November 2014 im Internet Archive) (PDF, S. 15–16).
- Updated Critical Mass Estimates for Plutonium-238.
- Informationskreis Kernenergie (Hrsg.): Basiswissen Kernenergie (Memento vom 17. Juni 2012 im Internet Archive) (PDF; 8,9 MB).
- Cassini-Huygens: Spacecraft (siehe Table 2–3) (Memento vom 19. Januar 2012 im Internet Archive) (PDF; 625 kB).
- Institute for Energy and Environmental Research.
- Erich Übelacker: Atom-Energie. (= Was ist was. Band 3). Tessloff Verlag, Nürnberg 1995, ISBN 3-7886-0243-0, S. 29.
- World Nuclear Association: Plutonium (englisch) (Memento vom 29. Dezember 2013 im Internet Archive).
- Reaktor-Plutonium und Waffen-Plutonium (Stand 2005).
- Waffenplutonium-Reaktor nach 46 Jahren stillgelegt. In: Russland-Aktuell. 15. April 2010.
- Nuklide für RTGs (PDF; 297 kB) letzte Seite.
- Cassini-Huygens: Spacecraft (siehe Table 2–2) (Memento vom 19. Januar 2012 im Internet Archive) (PDF; 625 kB).
- Zitat: »Seine Radioaktivität sei „auf allen Kontinenten und in jeder Höhe“ messbar, stellte ein Report der OECD 1989 fest.« In: Die Zeit. 39/1997.
- Streit um den Plutoniumantrieb der Saturnsonde Cassini. In: Die Zeit. 39/1997.
- Herzschrittmacher mit Plutonium (engl.)
- Plutonium-Herzschrittmacher: Atombatterie in der Brust. In: Spiegel Online. 22. November 2009, abgerufen am 5. April 2015.
- Basiswissen-Kernenergie: Plutonium-Batterien (Memento vom 26. Dezember 2013 im Internet Archive).
- Uni Oldenburg: Gefährlichkeit von Uran-238 und Plutonium-239 im Vergleich.
- Franz Frisch: Klipp und klar, 100 × Energie. Bibliographisches Institut AG, Mannheim 1977, ISBN 3-411-01704-X, S. 184.
- BREDL Southern Anti-Plutonium Campaign (Memento vom 29. April 2015 im Internet Archive).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1972.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1968–1971.
- Christoph Elschenbroich: Organometallchemie. 6. Auflage. Wiesbaden 2008, ISBN 978-3-8351-0167-8, S. 589.
- T. Miura, S. Oikawa, T. Kishimoto, S. Banba, T. Morimoto: Rapid separation of plutonium in environmental samples using an anion exchange resin disk. In: Journal of Radioanalytical and Nuclear Chemistry. 250, 2001, S. 449–452 (doi:10.1023/A:1017936703216).
- E. Hrnecek, P. Steier, A. Wallner: Determination of plutonium in environmental samples by AMS and alpha-spectrometry. In: Applied Radiation and Isotopes. 63 (5–6), 2005, S. 633–638 (doi:10.1016/j.apradiso.2005.05.012. PMID 15982894).
- L. Fifield, R. Cresswell, M. di Tada, T. Ophel, J. Day, A. Clacher, S. King, N. Priest: Accelerator mass spectrometry of plutonium isotopes. In: Nuclear Instruments and Methods in Physics Research B. 117 (3), 1996, S. 295–303 (doi:10.1016/0168-583X(96)00287-X).
- X. Claudon, J. Birolleau, M. Lavergne, B. Miche, C. Bergey: Simultaneous determination of americium and plutonium by inductively coupled plasma-atomic emission spectrometry. In: Spectrochimica Acta. 42B (1–2), 1987, S. 407–411 (doi:10.1016/0584-8547(87)80080-0).
- C. Pasquini, J. Cortez, L. Silva, F. Gonzaga: Laser Induced Breakdown Spectroscopy. In: Journal of the Brazilian Chemical Society. 18 (3), 2007 (doi:10.1590/S0103-50532007000300002).
- N. Surugaya, S.Sato, S. Jitsukata, M. Watahiki: Application of Laser-induced Photoacoustic Spectroscopy for Determination of Plutonium Concentration in Nuclear Waste Solutions. In: Analytical Sciences. 24, 2008, S. 527–530. PMID 18403847.
- K. Adelhelm, W. Faubel, H. Ache: Laser induced photoacoustic spectroscopy in liquid samples: temperature and solvent effects. In: Fresenius Journal of Analytical Chemistry. 338, 1990, S. 259–264 (doi:10.1007/BF00323020).
- Antineutrinos überwachen Plutoniumproduktion.
- Communication Received from Germany. Concerning its Policies regarding the Management of Plutonium . (Memento vom 22. Oktober 2013 im Internet Archive) PDF bei www.iaea.org
- Communication Received from Switzerland. Concerning its Policies Regarding the Management of Plutonium. (Memento vom 22. Oktober 2013 im Internet Archive) PDF bei www.iaea.org
- World Plutonium Inventories. In: The Bulletin of the Atomic Scientist. September/October 1999, S. 71.
- Russland stoppt Vernichtung von waffenfähigem Plutonium orf.at, 3. Oktober 2016.