Actinoide
Actinoide [-noˈiːdə] („Actiniumähnliche“; griech.: Endung -οειδής (-oeides) „ähnlich“) ist eine Gruppenbezeichnung bestimmter ähnlicher Elemente. Zugerechnet werden ihr das Actinium und die 14 im Periodensystem folgenden Elemente: Thorium, Protactinium, Uran und die Transurane Neptunium, Plutonium, Americium, Curium, Berkelium, Californium, Einsteinium, Fermium, Mendelevium, Nobelium und Lawrencium. Im Sinne des Begriffs gehört Actinium nicht zu den Actiniumähnlichen, jedoch folgt die Nomenklatur der IUPAC hier dem praktischen Gebrauch. Die frühere Bezeichnung Actinide entspricht nicht dem Vorschlag der Nomenklaturkommission, da nach diesem die Endung „-id“ für binäre Verbindungen wie z. B. Chloride reserviert ist; die Bezeichnung ist aber weiterhin erlaubt.[1][2] Alle Actinoide sind Metalle und werden auch als Elemente der Actiniumreihe bezeichnet.
| 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr |
|
Lage im Periodensystem
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Begriffliche Abgrenzung
- Die Transurane sind die Elemente mit einer höheren Ordnungszahl als Uran, d. h. die Actinoide beginnend mit Neptunium (93) sind auch Transurane.
- Als Transactinoide bezeichnet man die Elemente mit Ordnungszahlen ab 104 (Rutherfordium). Sie folgen im Periodensystem auf die Actinoide. Alle Transactinoide sind auch Transurane, da sie Ordnungszahlen größer als die des Urans haben.
- Im Zusammenhang mit Kernbrennstoffen und radioaktivem Abfall werden Neptunium, Americium, Curium, Berkelium und Californium auch als minore Actinoide bezeichnet.
- Die Actinoid-Nuklide sind Schwermetalle. In der Reaktorphysik wird bei Abbrandberechnungen der Schwermetall-Begriff etwas eingeschränkt. Als Schwermetalle bezeichnet man in diesem Zusammenhang nur die durch Neutronen spaltbaren Schwermetall-Nuklide. Spaltbar sind alle Schwermetall-Nuklide ab Actinium 225,[3] also auch alle Nuklide der Actinoide. Massen von Spaltprodukten und Massen der überwiegend durch Neutroneneinfang in einem Kernreaktor entstandenen schweren Nuklide werden meist relativ zur Masse der anfangs eingesetzten so definierten Schwermetalle angegeben.
Entdeckung und Gewinnung
| Z | Element | Jahr | Methode |
|---|---|---|---|
| 93 | Neptunium | 1940 | Beschuss von 238U mit Neutronen |
| 94 | Plutonium | 1941 | Beschuss von 238U mit Deuteronen |
| 95 | Americium | 1944 | Beschuss von 239Pu mit Neutronen |
| 96 | Curium | 1944 | Beschuss von 239Pu mit α-Teilchen |
| 97 | Berkelium | 1949 | Beschuss von 241Am mit α-Teilchen |
| 98 | Californium | 1950 | Beschuss von 242Cm mit α-Teilchen |
| 99 | Einsteinium | 1952 | Als Produkt von Kernwaffenexplosionen |
| 100 | Fermium | 1952 | Als Produkt von Kernwaffenexplosionen |
| 101 | Mendelevium | 1955 | Beschuss von 253Es mit α-Teilchen |
| 102 | Nobelium | 1964–1968 | Beschuss von 243Am mit 15N oder 238U mit 22Ne oder 249Cf mit 12C |
| 103 | Lawrencium | 1961–1971 | Beschuss von 252Cf mit 10B oder 252Cf mit 11B oder 243Am mit 18O |
Im Jahr 1934 publizierte die deutsche Chemikerin Ida Noddack eine Arbeit[5] über drei Lücken im Periodischen System der Elemente, die später mit den Elementen Francium, Astat und Promethium gefüllt wurden. Gleichsam nebenbei merkte sie an, dass es denkbar sei, dass bei der Beschießung schwerer Kerne mit Neutronen diese Kerne in mehrere größere Bruchstücke zerfallen. Aber nicht nur das. Denkbar sei auch, dass Elemente mit Ordnungszahlen Z > 92, also Transurane, gebildet werden könnten.
Tatsächlich synthetisierten Edwin M. McMillan und Philip H. Abelson erstmals im Jahr 1940 die ersten nicht in der Natur vorkommenden Actinoid-Nuklide 239U, 239Np und 239Pu durch Beschuss von Uran mit Neutronen.[6]
Da im Jahr 1940 noch kein Kernreaktor in Betrieb war, konnten die Neutronen nur aus einer Neutronenquelle stammen.
Obwohl bei dieser Kernreaktion letztlich auch ein Plutonium-Isotop entsteht, konnte Plutonium wahrscheinlich wegen der geringen Ausbeute noch nicht nachgewiesen werden. Als Entdeckungsjahr von Plutonium gilt das Jahr 1941, wie die Tabelle Entdeckung der Transurane zeigt.
Plutonium wurde von den US-Amerikanern Glenn T. Seaborg, J. W. Kennedy, E. M. McMillan, Michael Cefola und Arthur Wahl entdeckt. Ende 1940 stellten sie das Plutonium-Isotop 238Pu durch Beschuss des Uran-Isotops 238U mit Deuteronen her, die in einem Zyklotron beschleunigt worden waren. Nachdem der eindeutige Nachweis für das Element 94 erbracht worden war, erhielt es 1941 den Namen Plutonium. Der Name lag nahe, da die beiden Vorgängerelemente nach den Planeten Uranus und Neptun benannt worden waren. Details über die Kernreaktionen sind im Artikel Plutonium nachzulesen.
Damit eine Transmutation mit elektrisch geladenen Teilchen wie Deuteronen stattfinden kann, müssen diese Teilchen auf eine Energie beschleunigt werden, die ausreicht, um die Coulombbarriere von Urankernen zu überwinden oder diese zumindest zu durchtunneln. Das war erstmals mit einem Zyklotron möglich. Die erste wägbare Menge Plutonium von etwa 4 µg wurde 1942 isoliert.[7]

Ende 1942 wurde der erste Kernreaktor Chicago Pile in Betrieb genommen. Mit Kernreaktoren konnten vergleichsweise größere Mengen der Elemente Plutonium und Americium gewonnen werden, die als Targetmaterial dienten. In Verbindung mit geladenen Teilchen, mit beschleunigten α-Teilchen, wurden dann die Nuklide der Elemente Curium, Berkelium und Californium entdeckt. Der Vorteil des Verfahrens, der Beschuss beschleunigter geladener Teilchen auf leichtere Actinoide, ist, dass auch massereiche, neutronenarme Nuklide erhalten werden können, die durch eine Neutronenbestrahlung nicht gebildet werden.
Das effektivste Verfahren, um synthetische Actinoide zu erzeugen, ist die Transmutation von Uran- oder Thorium-Nukliden im Kernbrennstoff eines Kernreaktors durch Neutroneneinfang oder (n,2n)-Reaktionen. Dieses Verfahren ist auf nicht allzu massereiche Actinoid-Nuklide beschränkt, etwa bis zu Massenzahlen von A = 252. Rechnerisch (s. u) werden meist nur Nuklide bis A < 248 einbezogen.[8]
Americium zum Beispiel wurde in einem Zweistufenprozess entdeckt. In der ersten Stufe werden synthetische Actinoide in einem Kernreaktor gebildet, zum Beispiel 239Pu. Plutonium wird nach Entnahme des Kernbrennstoffs durch Wiederaufarbeitung chemisch extrahiert. Dann wird das Plutonium erneut im Reaktor oder mittels einer Quelle mit Neutronen bestrahlt. Der seit Mitte der 1960er Jahre betriebene 85 MW High-Flux-Isotope Reactor am Oak Ridge National Laboratory in Tennessee, USA ist auf die Herstellung von Transcuriumelementen (Z > 96) speziell ausgelegt.[9]
Die massereichen Elemente Einsteinium und Fermium wurden durch den Test der ersten amerikanischen Wasserstoffbombe, Ivy Mike, am 1. November 1952 auf dem Eniwetok-Atoll auf unsere Erde gebracht. Nur wenige Wochen später wurden sie im Lawrence Berkeley National Laboratory, das an der geheimen Waffentwicklung nicht beteiligt war, auf Filterpapieren und in Ablagerungen an Korallen völlig unerwartet entdeckt.[10] Bei der Wasserstoffbombenexplosion waren bis zu 16 Neutronen von einem Kern von 238U eingefangen worden. Dieser Zwischenkern zerfiel sehr schnell über eine Kette von Betazerfällen in Nuklide der bis dahin unbekannten Elemente. Das Uran stammte aus der Ummantelung der Wasserstoffbombe, die aus fünf Tonnen Natururan bestand.
Aus Gründen der militärischen Geheimhaltung durften die Ergebnisse zunächst nicht publiziert werden. Um sich dennoch die Priorität der Entdeckungen der beiden neuen Elemente zu sichern, wurden parallel erfolgreich Schwerionenreaktionen durchgeführt. 238U wurde mit 14N-Ionen, die an einem Zyklotron erzeugt wurden, bombardiert. Auf diesem Wege wurde zunächst Einsteinium synthetisiert und in der Publikation auf die Entdeckung von 1952 verwiesen. Ähnlich verfuhr man mit Fermium, das durch Beschuss mit 239Pu mit 14N-Ionen erzeugt wurde.
Wie die Tabelle zeigt, führten Schwerionenreaktionen auch zu den Elementen Mendelevium, Nobelium und Lawrencium mit den Ordnungszahlen 101 bis 103. Mit Schwerionenreaktionen wurden auch die Elemente mit höheren Ordnungszahlen synthetisiert.
Bildung und Gewinnung im Kernreaktor
Der Kernreaktor nimmt, was die Actinoide betrifft, nicht nur deshalb eine herausragende Stellung ein, weil er ohne Actinoide nicht betrieben werden könnte, sondern weil es nur innerhalb eines Kernreaktors möglich ist, größere wägbare Mengen von „höheren“ Actinoid-Nukliden zu bilden. Dieser Abschnitt beschreibt, welche Actinoid-Nuklide das sind und in welchem Massenanteil (relativ zur ursprünglichen Schwermetallmasse) sie gebildet werden.
In einem Kernreaktor werden zu Beginn des Betriebs große Mengen von Actinoiden in Form von Kernbrennstoff eingebracht, zum Beispiel mit 235U angereichertes Uran. In einem Leistungsreaktor sind Actinoidmassen in der Größenordnung von 100 t enthalten.[11] Aus diesem Kernbrennstoff werden neben der gewünschten Energiefreisetzung durch Kernspaltung synthetische „höhere“ Actinoide durch Transmutation erzeugt. Gelingt es bei der Wiederaufarbeitung nicht, diese zu entfernen, so haben Actinoide auf den meisten Zeitskalen den höchsten Anteil an der Radioaktivität des Atommülls. Dies liegt an der Tatsache, dass bei den Spaltprodukten eine „Lücke“ der Halbwertszeiten zwischen Caesium-135 und Strontium-90 im Bereich um dreißig Jahre und Technetium-99 im Bereich um hunderttausende Jahre besteht. Diese „Lücke“ wird aber (sofern sie vorhanden sind) von den Actinoiden „aufgefüllt“.
Actinoid-Nuklide in einem Kernreaktor
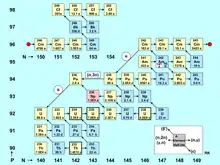
Die Abbildung Nuklidkarte: Bildung und Zerfall von Actinoiden in einem Kernreaktor ist eine Nuklidkarte in der Anordnung nach Segrè. Das heißt, die Anzahl der Neutronen wird nach rechts zunehmend, die Anzahl der Protonen nach oben zunehmend aufgetragen. Um die Zeichnungsfläche sinnvoll zu nutzen, ist der Nuklidpfad am roten Punkt unterteilt.
Jedes Quadrat der Abbildung stellt ein Actinoid-Nuklid dar, das in einem Kernreaktor auftreten kann. Die Abbildung zeigt auch das Netzwerk von Bildung und Zerfall von Actinoid-Nukliden, ausgelöst durch den Neutroneneinfang freier Neutronen und durch andere Kernreaktionen. Ein ähnliches Schema findet man in einer Arbeit[8] aus dem Jahr 2014. Dort sind die Isotope von Thorium und Protactinium, die zum Beispiel in Salzschmelzenreaktoren eine große Rolle spielen, und die Isotope der Elemente Berkelium und Californium nicht enthalten.
Die Bildung von Actinoid-Nukliden wird in erster Linie geprägt durch:
- Neutroneneinfang-Reaktionen (n,γ), die in der Abbildung durch einen kurzen Rechtspfeil dargestellt sind.
- Berücksichtigt werden aber auch die (n,2n)-Reaktionen und die seltener auftretenden (γ,n)-Reaktionen, die beide durch einen kurzen Linkspfeil markiert sind.
- Noch seltener und nur ausgelöst von schnellen Neutronen tritt die (n,3n)-Reaktion auf, die in der Abbildung mit einem Beispiel vertreten ist, markiert durch einen langen Linkspfeil.
Außer diesen neutronen- oder gammainduzierten Kernreaktionen wirkt sich auch die radioaktive Umwandlung der Actinoid-Nuklide auf den Nuklid-Bestand in einem Reaktor zu einem gegebenen Zeitpunkt (Abbrandzustand) aus. Diese Zerfallsarten sind in der Abbildung durch Diagonalpfeile markiert.
Eine große Rolle für die Bilanz der Teilchendichten der Nuklide spielt der Beta-Minus-Zerfall, markiert mit aufwärts zeigenden Diagonalpfeilen. Die Quadrate der Nuklide dieses Zerfallstyps haben in der Nuklidkarte eine hellblaue Füllfarbe. Zwei Nuklide sind nur zum Teil betaaktiv. Das rosafarben hinterlegte Nuklid 236Np wandelt sich zu 86 % durch Elektroneneinfang und zu 14 % durch Beta-Minus-Zerfall (hellblaue Ecke) um. Ebenfalls zwei Zerfallsarten, aber in nahezu umgekehrtem Verhältnis (83 % Beta-Minus-Zerfall, 17 % Elektroneneinfang) zeigt auch der Grundzustand von 242Am (rosa Ecke). Dieses Nuklid besitzt außerdem einen langlebigen metastabilen Zustand (weiß hinterlegt), der in der Regel durch 242m1Am symbolisiert wird. Nuklide mit Positronen-Emissionen (Beta-Plus-Zerfälle) kommen in einem Kernreaktor nicht vor, da quasi ausschließlich Kerne mit Neutronenüberschuss bzw. „gerade genug“ Neutronen gebildet werden.
Die Actinoid-Nuklide, die sich unter Aussendung von α-Teilchen spontan umwandeln, sind in der Nuklidkarte der Abbildung mit einer gelben Füllfarbe versehen worden. Der α-Zerfall spielt wegen der langen Halbwertszeiten (T1/2) bei Bildung und Zerfall der Actinoide während der Aufenthaltsdauer des Brennstoffs in einem Leistungsreaktor (max. ca. 3 Jahre) so gut wie keine Rolle. Ausnahmen sind die beiden relativ kurzlebigen Nuklide 242Cm (T1/2 = 163 d) und 236Pu (T1/2 = 2.9 a). Nur für diese beiden Fälle ist der α-Zerfall durch lange, abwärts zeigende Pfeile auf der Nuklidkarte markiert.
Alle in der Abbildung angegebenen Halbwertszeiten sind die aktuellen evaluierten Nukleardaten NUBASE2012,[12] abgerufen über den Nukleardaten-Viewer JANIS 4.[3] Manche Halbwertszeiten sind gerundet.
Zur Bedeutung von Abbrandprogrammen
Nur bei der ersten Inbetriebnahme des Reaktors kennt man die Zusammensetzung an Nukliden des Kernbrennstoffs genau. Es ist aber für jeden Zeitpunkt (Abbrandzustand) erforderlich, grundlegende physikalische Größen wie den Neutronenfluss zu kennen. Zu den grundlegenden physikalischen Größen gehören auch die Teilchendichten und Massendichten aller im Reaktor gebildeten Actinoid-Nuklide. Das betrifft sowohl die der anfangs eingebrachten (oder was davon noch vorhanden ist) als auch die der im Reaktorbetrieb gebildeten Nuklide. Die tatsächlichen Teilchendichten (und Massendichten) der Actinoid-Nuklide in Abhängigkeit vom Abbrand im laufenden Betrieb zu messen, ist nicht möglich. Erst nach der Entladung von Kernbrennstoff können diese Größen im Prinzip chemisch oder massenspektrometrisch untersucht werden. Die allermeisten Leistungs-Kernreaktoren erfordern zum Entfernen oder Hinzufügen von Brennstoff die komplette Abschaltung und anschließendes „wieder hoch fahren“. Bei Druckwasserreaktoren kommt hinzu, dass der Innendruck erst ab- und dann wieder aufgebaut werden muss. Das ist sehr aufwendig. Deshalb kommt einer Berechnung, die den Betriebsablauf eines Kernreaktors begleitet, ein hoher Stellenwert zu.
Die Entwicklung der Teilchendichten (und Massendichten) von Nukliden in einem Kernreaktor wird in Abhängigkeit vom mittleren Abbrand (engl. Burnup, Depletion) vereinfacht in sog. Abbrandprogrammen berechnet, zum Beispiel:
- ORIGEN,[13] das erste weltweit verbreitete Programm zur Berechnung der Nuklidbildungen in Abhängigkeit vom Abbrand aus dem Jahr 1973,
- OrigenArp,[14] ein Programm zur Berechnung der Teilchendichten von Nukliden in Abhängigkeit vom Abbrand aus dem Jahr 2010, das auch in das Programmsystem SCALE (s. u.) integriert ist.
Für eine detaillierte Analyse werden hochkomplexe Reaktorprogrammsysteme (Neutronen-Transportprogramme) eingesetzt, deren Leistungsumfang weit über den der zuvor genannten Programme hinausgeht und deren Anwendung eine lange Einarbeitungszeit erfordert, zum Beispiel:
- SCALE, ein großes Programmsystem für unterschiedliche neutronenphysikalische Berechnungen, so u. a. auch für Abbrand- und Abschirmrechnungen,[15]
- HELIOS, ein Zell- und Abbrandprogrammsystem für Berechnungen in Neutronen-Transportnäherung.[16]
In letzteren Programmsystemen sind neben der anfänglichen Materialzusammensetzung auch geometrische Details von Reaktorbauteilen (Zellen) vorzugeben. Von Zeit zu Zeit werden solche Rechnungen mit den Ergebnissen von chemischer und massenspektrometrischer Analyse von entladenem Kernbrennstoff verglichen[8] und gegebenenfalls genauere Messungen noch unsicherer Nukleardaten oder genauere Berechnungsmethoden angestoßen.
Entwicklung der Massen der Actinoide im Kernreaktor
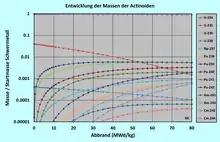
Die Abbildung Entwicklung der Massen der Actinoide ... zeigt die Zu- oder Abnahme der Massen der 14 häufigsten Actinoid-Nuklide in einem Druckwasserreaktor, der mit angereichertem Uran betrieben wird. Die Zahlenwerte wurden für eine größere Brennstoff-Zelle in Abhängigkeit vom Abbrand (der spezifischen Energiefreisetzung) berechnet. Die Berechnungen wurden im Jahr 2005 mit dem Programmsystem HELIOS 1.8 ausgeführt.[17] Als Anfangsanreicherung des Nuklids 235U wurde für dieses Beispiel 4 % gewählt. Die Punkte auf den Kurven der Abbildung markieren die Schrittweiten in der Abbrandrechnung. Die Schrittweite ist anfangs kleiner, um auch diejenigen Spaltprodukte genauer zu erfassen, die ihre Sättigung sehr schnell erreichen. Das trifft vor allem auf die starken Neutronenabsorber 135Xe (Näheres hierzu unter Xenonvergiftung) und 149Sm zu. Eine ähnliche Abbildung, eingeschränkt auf Uran- und Plutonium-Isotope, findet man im Lehrbuch Neutron Physics von Paul Reuss.[18]
Die Masse jedes Nuklids wird durch die anfangs eingesetzte Masse an Schwermetall, der Masse des Urans, geteilt. Dargestellt sind die Massenanteile aller Nuklide, die anfangs vorhanden waren (drei Uran-Nuklide) oder die mit einer Masse von mindestens 10 g pro eingesetzter Tonne Schwermetall nach einem Abbrand von maximal 80 MWd/kg gebildet werden.
Wie die Abbildung zeigt, nehmen die Massen der drei anfangs vorhandenen Uranisotope 238U, 235U und 234U mit steigendem Abbrand monoton ab. Gleichzeitig nehmen die Massen der höheren Actinoide fast linear zu (man beachte die logarithmische Skalierung der Ordinate). Von allen synthetischen Actinoiden nimmt die Masse des Nuklids 239Pu am stärksten zu. Damit wächst auch die Anzahl der Spaltungen der Kerne des Nuklids 239Pu. Ab einem Abbrand von ca. 45 MWd/kg nimmt dessen Masse wieder geringfügig ab.
Würde man die Ordinate nach unten auf einen Massenanteil von mindestens 1 g pro eingesetzter Tonne Schwermetall herabsetzen, kämen auf der Abbildung ab einem Abrand von ca. 45 MWd/kg das Nuklid 242m1Am und ab einem Abrand von ca. 60 MWd/kg das Nuklid 243Cm hinzu.
Zusammengefasst: In einem Druckwasserreaktor mit Uran-Brennelementen (ohne MOX-Brennelemente) werden aus den ursprünglich vorhandenen Actinoid-Nukliden 235U und 238U (und einem geringen Anteil 234U) maximal 13 synthetische Actinoid-Nuklide innerhalb der üblichen Betriebszeiten gebildet, deren Anteil größer als 1 g je Tonne Startmasse Schwermetall (SM) ist, also 1 ppm.[19] Das sind die Nuklide 236U, 237Np, 238Pu, 239Pu, 240Pu, 241Pu, 242Pu, 241Am, 242m1Am, 243Am, 242Cm, 243Cm und 244Cm. Nuklide der Elemente Berkelium und Californium werden in einem Kernreaktor ebenfalls, aber nur in sehr geringen Mengen gebildet.
Die Actinoide können, wie erwähnt, durch chemische Aufarbeitung von entladenem Brennstoff extrahiert werden. Der Massenanteil von Curium zum Beispiel beträgt ca. 0,00024 bei einem Abbrand von 60 MWd/kg:
- ,
wobei die Masse des Curiums und die Startmasse des Schwermetalls bedeuten. In einem Leistungsreaktor beträgt die anfängliche Schwermetallmasse[11] ca. , verteilt auf 193 Brennelemente. Angenommen, alle Brennelemente seien entladen worden, die diesen Abbrandzustand erreicht haben. Folglich ist die Masse des Curiums
- .
Im gesamten Reaktor sind bei diesem mittleren Abbrand im Brennstoff ca. 24 kg Curium entstanden.
Anzumerken ist, dass Leistungsreaktoren nicht betrieben werden, um Actinoide zu gewinnen, sondern um möglichst viele Actinoide zu spalten und Energie freizusetzen. Die Gesamtmasse aller Actinoide verringert sich durch Kernspaltung, und zwar bei einem mittleren Abbrand von 60 MWd/kg um insgesamt nur ca. 6 %. Diese findet sich im Wesentlichen in der Masse der Spaltprodukte wieder. Obwohl sämtliche freigesetzte Energie auf dem Massendefekt basiert, ist dessen Effekt auf die Gesamtmasse vernachlässigbar.
Eigenschaften
Nukleare Eigenschaften
Die hervorgehobene Stellung der Actinoide, man denke an ihre Bedeutung zur nuklearen Energiefreisetzung und an Kernwaffen, werden durch die Eigenschaften ihrer Atomkerne determiniert.
- Alle Actinoid-Nuklide sind radioaktiv.
- Alle Actinoid-Nuklide sind neutroneninduziert spaltbar,[3] wenn auch mit sehr unterschiedlichen Wirkungsquerschnitten, die außerdem sehr stark von der kinetischen Energie der Neutronen abhängen.
- Thermische Neutronen haben eine höhere Wahrscheinlichkeit überhaupt mit den Nukliden zu interagieren während bei schnellen Neutronen die Kernspaltung wahrscheinlicher ist, wenn es überhaupt zu einer Interaktion zwischen Kern und Neutron kommt. Alle Actinoid-Isotope sind durch schnelle Neutronen spaltbar, aber nur einige durch thermische Neutronen.
- Die vier Actinoid-Nuklide 232Th, 234U, 235U und 238U kommen natürlich vor. Ihre Quadrate sind in der obigen Nuklidkarte durch eine dickere Umrandung hervorgehoben. Mit Ausnahme von 234U sind es primordiale Nuklide, also Nuklide, die schon bei der Entstehung der Erde vorhanden waren und noch nicht vollständig zerfallen sind. Das natürlich vorkommende, extrem seltene primodiale Plutonium-Nuklid 244Pu spielt im Kernreaktor keine Rolle. Sein Massenanteil in einigen Erzen liegt bei 10−18.
- Im Jahr 2000 waren mehr als 200 synthetisch erzeugte Actinoid-Nuklide bekannt.[19] Die meisten besitzen kurze Halbwertszeiten. Nur 45 haben Halbwertszeiten T1/2 > 40 d.
- Von 41 Actinoid-Nukliden wird angenommen, dass sie zu einer sich selbsterhaltenden Kettenreaktion fähig sind.[19] Andere Quellen gehen von weniger Actinoid-Nukliden aus, für die es eine kritische Masse gibt.
- Für die sechs Actinoid-Nuklide 233U, 235U, 238U, 239Pu, 240Pu und 241Pu sind die Wirkungsquerschnitte relativ genau bekannt, für alle anderen sind die Nukleardaten weniger genau.[19] Auf Kritikalitätsberechnungen wirken sich diese Ungenauigkeiten aber kaum aus. Je weniger Masse eines Nuklids sich im Kernreaktor befindet, desto geringer ist die Auswirkung fehlerhafter Wirkungsquerschnitte auf solche Berechnungen.
Klassische physikalische Eigenschaften
Einige physikalische Eigenschaften der Actinoid-Elemente findet man unter dem Stichwort der Namen der Elemente. Die Voraussetzung dafür, dass klassische physikalische Eigenschaften, zum Beispiel Kristallstruktur, Massendichte, Schmelzpunkt, Siedepunkt oder elektrische Leitfähigkeit gemessen werden können, ist es, dass das Element in wägbaren Mengen gewonnen werden kann. Die Anzahl der tatsächlich gemessenen physikalischen Eigenschaften nimmt mit wachsender Ordnungszahl des Elements schnell ab. Zum Beispiel ist Californium das letzte Actinoid-Element, von dem die Massendichte gemessen werden konnte.
Zur Atomphysik der Actinoide ist anzumerken:
- Alle Actinoide sind, wie oben erwähnt, Schwermetalle.
- Einige Actinoide sind in feinverteiltem Zustand pyrophor.
- Actinoide gehören wie die Lanthanoide zu den inneren Übergangselementen oder f-Block-Elementen, da in diesen Reihen die f-Unterschalen mit Elektronen aufgefüllt werden.
Chemische Eigenschaften
Alle Actinoide bilden dreifach geladene Ionen, sie werden wie das Actinium als Untergruppe der 3. Nebengruppe aufgefasst. Die „leichteren“ Actinoide (Thorium bis Americium) kommen in einer größeren Anzahl von Oxidationszahlen vor als die entsprechenden Lanthanoide.[20]
Farben der Actinoid-Ionen in wässriger Lösung
| Oxidationszahl[21][22] | 89 | 90 | 91 | 92 | 93 | 94 | 95 | 96 | 97 | 98 | 99 | 100 | 101 | 102 | 103 |
| +3 | Ac3+ farblos |
(Th3+) tiefblau |
(Pa3+) blauschwarz |
U3+ purpurrot |
Np3+ purpurviolett |
Pu3+ tiefblau |
Am3+ gelbrosa |
Cm3+ farblos |
Bk3+ gelbgrün |
Cf3+ grün |
Es3+ blassrosa |
Fm3+ |
Md3+ |
No3+ |
Lr3+ |
| +4 | Th4+ farblos |
Pa4+ blassgelb |
U4+ smaragdgrün |
Np4+ gelbgrün |
Pu4+ orangebraun |
Am4+ gelbrot |
Cm4+ blassgelb |
Bk4+ beige |
Cf4+ grün |
||||||
| +5 | PaO2+ farblos |
UO2+ blasslila |
NpO2+ grün |
PuO2+ pink |
AmO2+ gelb |
||||||||||
| +6 | UO22+ gelb |
NpO22+ rosarot |
PuO22+ altrosé |
AmO22+ zitronengelb |
|||||||||||
| +7 | NpO23+ tiefgrün |
PuO23+ blaugrün |
(AmO65−) dunkelgrün |
Verbindungen
Die Eigenschaften beziehen sich auf das häufigste bzw. stabilste Isotop.
Oxide
Die vierwertigen Oxide der Actinoide kristallisieren im kubischen Kristallsystem; der Strukturtyp ist der CaF2-Typ (Fluorit) mit der Raumgruppe Fm3m (Raumgruppen-Nr. 225) und den Koordinationszahlen An[8], O[4].
| Dioxide der Actinoide[23] | |||||||||
| Name | Thorium(IV)- oxid |
Protactinium(IV)- oxid |
Uran(IV)- oxid |
Neptunium(IV)- oxid |
Plutonium(IV)- oxid |
Americium(IV)- oxid |
Curium(IV)- oxid |
Berkelium(IV)- oxid |
Californium(IV)- oxid |
| CAS-Nummer | 1314-20-1 | 12036-03-2 | 1344-57-6 | 12035-79-9 | 12059-95-9 | 12005-67-3 | 12016-67-0 | 12010-84-3 | 12015-10-0 |
| Summenformel | ThO2 | PaO2 | UO2 | NpO2 | PuO2 | AmO2 | CmO2 | BkO2 | CfO2 |
| Molare Masse | 264,04 g·mol−1 | 263,04 g·mol−1 | 270,03 g·mol−1 | 269,05 g·mol−1 | 276,06 g·mol−1 | 275,06 g·mol−1 | 279,07 g·mol−1 | 279,07 g·mol−1 | 283,08 g·mol−1 |
| Schmelzpunkt | 3390 °C | 2878 °C | 2600 °C | 2400 °C | 1000 °C (Zers.) | 380 °C (Zers.) | |||
| Siedepunkt | 4400 °C | 2800 °C | |||||||
| Strukturformel | 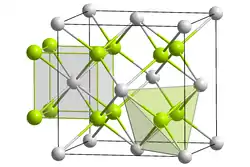 __ An4+ __ O2− __ An4+ __ O2− | ||||||||
| Raumgruppe | Fm3m (Nr. 225) | ||||||||
| Koordinationszahlen | An[8], O[4] | ||||||||
| Gitterkonstanten | 550,5 pm | 547 pm | 543 pm | 540 pm | 533 pm | 536 pm | 533 pm | 531 pm | |
Halogenide
Die dreiwertigen Chloride der Actinoide kristallisieren im hexagonalen Kristallsystem. Die Struktur des Uran(III)-chlorids ist die Leitstruktur für eine Reihe weiterer Verbindungen. In dieser werden die Metallatome von je neun Chloratomen umgeben. Als Koordinationspolyeder ergibt sich dabei ein dreifach überkapptes, trigonales Prisma, wie es auch bei den späteren Actinoiden und den Lanthanoiden häufig anzutreffen ist. Es kristallisiert im hexagonalen Kristallsystem in der Raumgruppe P63/m (Raumgruppen-Nr. 176) und zwei Formeleinheiten pro Elementarzelle.[24]
| Dreiwertige Chloride der Actinoide[23] | |||||||
| Name | Uran(III)-chlorid | Neptunium(III)- chlorid |
Plutonium(III)- chlorid |
Americium(III)- chlorid |
Curium(III)- chlorid |
Berkelium(III)- chlorid |
Californium(III)- chlorid |
| CAS-Nummer | 10025-93-1 | 20737-06-8 | 13569-62-5 | 13464-46-5 | 13537-20-7 | 13536-46-4 | 13536-90-8 |
| Summenformel | UCl3 | NpCl3 | PuCl3 | AmCl3 | CmCl3 | BkCl3 | CfCl3 |
| Molare Masse | 344,39 g·mol−1 | 343,41 g·mol−1 | 350,32 g·mol−1 | 349,42 g·mol−1 | 353,43 g·mol−1 | 353,43 g·mol−1 | 357,44 g·mol−1 |
| Schmelzpunkt | 837 °C | 800 °C | 767 °C | 715 °C | 695 °C | 603 °C | 545 °C |
| Siedepunkt | 1657 °C | 1767 °C | 850 °C | ||||
| Strukturformel | 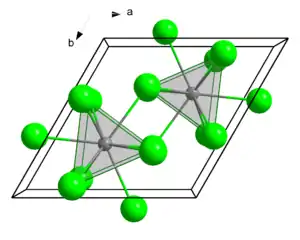 __ An3+ __ Cl− __ An3+ __ Cl− | ||||||
| Raumgruppe | P63/m (Nr. 176) | ||||||
| Koordinationszahlen | An[9], Cl[3] | ||||||
| Gitterkonstanten[24] | a = 745,2 pm c = 432,8 pm | a = 740,5 pm c = 427,3 pm | a = 739,4 pm c = 424,3 pm | a = 738,2 pm c = 421,4 pm | a = 726 pm c = 414 pm | a = 738,2 pm c = 412,7 pm | a = 738 pm c = 409 pm |
Einzelnachweise
- Wolfgang Liebscher, Ekkehard Fluck: Die systematische Nomenklatur der anorganischen Chemie. Springer, Berlin 1999, ISBN 3-540-63097-X.
- Neil G. Connelly (Red.): Nomenclature of inorganic chemistry – IUPAC recommendations 2005. Royal Society of Chemistry, Cambridge 2005, ISBN 0-85404-438-8.
- Janis 4 – Java-based Nuclear Data Information System.
- Norman N. Greenwood, Alan Earnshaw: Chemistry of the elements. 2. ed., repr. Elsevier Butterworth-Heinemann, Amsterdam, Heidelberg 2005, ISBN 0-7506-3365-4, S. XXII, 1341, S. 1250 ff. (englisch).
- Ida Noddack: Das Periodische System der Elemente und seine Lücken, in: Angewandte Chemie, 1934, 47 (20), S. 301–305 (doi:10.1002/ange.19340472002).
- E. McMillan, P. H. Abelson: Radioactive Element 93, in: Physical Review, 1940, 57, S. 1185–1186 (doi:10.1103/PhysRev.57.1185.2).
- B. B. Cunningham, L. B. Werner: The First Isolation Of Plutonium. In: Journal of the American Chemical Society. 71 (5), 1949, S. 1521–1528 (doi:10.1021/ja01173a001).
- Matthew W. Francis et al.: Reactor fuel isotopics and code validation for nuclear applications. ORNL/TM-2014/464, Oak Ridge, Tennessee 2014, S. 11 (xv, 89 S., ornl.gov [PDF; abgerufen am 18. November 2017]).
- High Flux Isotope Reactor, Oak Ridge National Laboratory; abgerufen am 18. November 2017.
- Albert Ghiorso: Einsteinium and Fermium, Chemical & Engineering News, 2003.
- Die Schwermetallmasse ist nicht für jeden Leistungsreaktor leicht zu finden. Im Artikel Kernkraftwerks Emsland wird die Schwermetallmasse mit 103 t angegeben, verteilt auf 193 Brennelemente. Das dürfte auch auf die anderen Leistungsreaktoren der Bauform Konvoi näherungsweise zutreffen.
- Audi, G., F. G. Kondev, M. Wang, B. Pfeiffer, X. Sun, J. Blachot, and M. MacCormick: The NUBASE2012 evaluation of nuclear and decay properties. In: Chinese Physics C. Band 36, Nr. 12, 2012, S. 1157–1286.
- M. J. Bell: ORIGEN - The ORNL Isotope Generation and Depletion Code. Oak Ridge National Laboratory, Oak Ridge, Tenn. 1973 (148 S.).
- S. M. Bowman, I. C. Gauld: OrigenArp Primer: How to perform isotopic depletion and decay calculations with SCALE/ORIGEN. ORNL/TM-2010/43, Oak Ridge, Tennessee 2010 (ornl.gov [PDF; abgerufen am 18. November 2017]).
- Bradley T. Rearden: SCALE Code System. Oak Ridge, Tennessee 2016 (2712 S., ornl.gov [PDF; abgerufen am 18. November 2017]).
- Stamm'ler, Rudi J. J. et al.: HELIOS Methods: Version 1.8. Studsvik Scandpower 2003 (192 S.).
- RK: PWR-Calculations with the Code-System HELIOS 1.8, Studsvik 2005 International User’s Group Meeting, Charlotte, NC, USA, June 1-3, 2005.
- Paul Reuss: Neutron physics. EDP Sciences, Les Ulis, France 2008, ISBN 978-2-7598-0041-4, S. 325 (xxvi, 669 S., eingeschränkte Vorschau in der Google-Buchsuche [abgerufen am 18. November 2017]).
- R. Q. Wright, W. C. Jordan, R. M. Westfall: Critical Masses of Bare Metal Spheres Using SCALE/XSDRN. In: Proceedings of the Annual Meeting of the American Nuclear Society. 2000, S. 167. Die Zusammenfassung findet sich im INIS Repository https://inis.iaea.org/search/search.aspx?orig_q=RN:31056505
- Guttmann, Hengge: Anorganische Chemie. VCH, Weinheim / New York / Basel / Cambridge 1990.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1956.
- dtv-Atlas zur Chemie 1981, Teil 1, S. 224.
- Die Werte der atomaren und physikalischen Eigenschaften sind, wenn nicht anders angegeben, aus www.webelements.com entnommen.
- Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements: Bd. 3, 2006, Springer, ISBN 1-4020-3555-1.
Literatur
- Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements. Springer, Dordrecht 2006, ISBN 1-4020-3555-1:
- Harold W. Kirby, Lester R. Morss: Actinium, S. 18–51; doi:10.1007/1-4020-3598-5_2.
- Mathias S. Wickleder, Blandine Fourest, Peter K. Dorhout: Thorium, S. 52–160; doi:10.1007/1-4020-3598-5_3.
- Boris F. Myasoedov, Harold W. Kirby, Ivan G. Tananaev: Protactinium, S. 161–252; doi:10.1007/1-4020-3598-5_4.
- Ingmar Grenthe, Janusz Drożdżynński, Takeo Fujino, Edgar C. Buck, Thomas E. Albrecht-Schmitt, Stephen F. Wolf: Uranium, S. 253–698; doi:10.1007/1-4020-3598-5_5.
- Zenko Yoshida, Stephen G. Johnson, Takaumi Kimura, John R. Krsul: Neptunium, S. 699–812; doi:10.1007/1-4020-3598-5_6.
- David L. Clark, Siegfried S. Hecker, Gordon D. Jarvinen, Mary P. Neu: Plutonium, S. 813–1264; doi:10.1007/1-4020-3598-5_7.
- Wolfgang H. Runde, Wallace W. Schulz: Americium, S. 1265–1395; doi:10.1007/1-4020-3598-5_8.
- Gregg J. Lumetta, Major C. Thompson, Robert A. Penneman, P. Gary Eller: Curium, S. 1397–1443; doi:10.1007/1-4020-3598-5_9.
- David E. Hobart, Joseph R. Peterson: Berkelium, S. 1444–1498; doi:10.1007/1-4020-3598-5_10.
- Richard G. Haire: Californium, S. 1499–1576; doi:10.1007/1-4020-3598-5_11.
- Richard G. Haire: Einsteinium, S. 1577–1620; doi:10.1007/1-4020-3598-5_12.
- Robert J. Silva: Fermium, Mendelevium, Nobelium, and Lawrencium, S. 1621–1651; doi:10.1007/1-4020-3598-5_13.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1948–1976.
- James E. Huheey: Anorganische Chemie. de Gruyter, Berlin 1988, ISBN 3-11-008163-6, S. 873–900.
- Norman N. Greenwood, Alan Earnshaw: Chemie der Elemente. 1. Auflage. VCH, Weinheim 1988, ISBN 3-527-26169-9, S. 1601–1641.
- dtv-Atlas zur Chemie, Teil 1. 1981, S. 222–229.