Hauptgruppe
In der Chemie bezeichnet man als Hauptgruppen diejenigen Gruppen des Periodensystems, die zum s- und p-Block des Periodensystems gehören.
| IUPAC-Gruppe | Hauptgruppe | Inhalt |
|---|---|---|
| 1 | I | Alkalimetalle und Wasserstoff |
| 2 | II | Erdalkalimetalle |
| 13 | III | Borgruppe |
| 14 | IV | Kohlenstoff-Silicium-Gruppe |
| 15 | V | Stickstoff-Phosphor-Gruppe |
| 16 | VI | Chalkogene |
| 17 | VII | Halogene |
| 18 | VIII | Edelgase |
Die Anordnung der chemischen Elemente im Periodensystem wurde so vorgenommen, dass Elemente mit ähnlichen Eigenschaften jeweils in einer Gruppe untereinander stehen, d. h. die Spalten im Periodensystem enthalten Elemente mit ähnlichen chemischen Eigenschaften. Die Übereinstimmung ist dabei bei den Hauptgruppen am größten. Das Periodensystem der Elemente besteht aus acht Haupt- und zehn Nebengruppen. Die Hauptgruppe gibt an, wie viele Elektronen sich auf der äußersten Schale eines Atoms befinden.
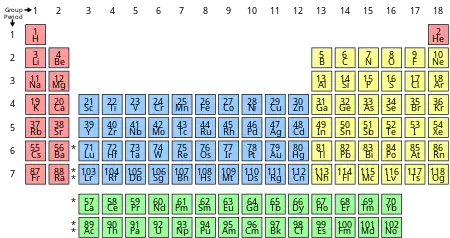
Besonders deutlich ist die Übereinstimmung der Eigenschaften bei den Alkalimetallen, Erdalkalimetallen, den Halogenen und den Edelgasen:
Die Elemente der Alkalimetalle sind Lithium, Natrium, Kalium, Rubidium, Caesium und Francium. Wasserstoff befindet sich zwar in derselben Hauptgruppe, kann aber aufgrund seiner physikalischen und chemischen Eigenschaften nicht zu den Alkalimetallen gezählt werden. Die Alkalimetalle haben eine geringe Schmelztemperatur, reagieren schnell und heftig mit Wasser (unter Bildung von Wasserstoffgas und der entsprechenden Lauge) und Sauerstoff, haben niedrige Dichten, sind allesamt brennbare Leichtmetalle und zeigen charakteristische Flammenfärbungen. Die Alkalimetalle kommen in der Natur nicht elementar, sondern nur in Verbindungen vor. Die elementaren Metalle von Lithium bis Kalium werden in oder unter Petroleum aufbewahrt und sind weiche Metalle, die man schneiden kann. Rubidium und Caesium werden in Ampullen aufbewahrt und schmelzen weitgehend bei Handwärme. Ihre Salze zeigen, wie die elementaren Metalle, in der Brennerflamme charakteristische Farben.
Die Erdalkalimetalle zeigen ein ähnliches Verhalten wie die Alkalimetalle, sind aber in allen Eigenschaften abgeschwächt. Zu dieser Gruppe gehören Beryllium, Magnesium, Calcium, Strontium, Barium und Radium. Im Unterschied zu den Alkalimetallen bilden sie jedoch (mit Ausnahme von Beryllium und Magnesium) schwerlösliche Carbonate und Sulfate.
Die Elemente der Halogene, die auch Salzbildner genannt werden, sind Fluor, Chlor, Brom, Iod, Astat und Tenness. Auch diese Elemente kommen in der Natur nur in Verbindungen vor und reagieren heftig mit Wasserstoffgas (zu Säuren), Metallen (zu Salzen) und sind zudem farbig und gesundheitsschädlich bis giftig. Da Fluor und Chlor recht schnell und aggressiv an der Luft reagieren, sollte man bei Versuchen mit ihnen vorsichtig sein.
Die Elemente der Edelgase sind Helium, Neon, Argon, Krypton, Xenon und Radon. Sie kommen in der Natur nur elementar vor. Die Edelgase sind geruchlos, farblos und gasförmig. Sie sind in der Luft nur in geringer Menge vorhanden und reagieren so gut wie nicht mit anderen Stoffen; eine Eigenschaft, die sie mit den Edelmetallen gemeinsam haben. Deshalb nennt man sie Edelgase. Über den Edelgascharakter des in derselben Gruppe stehenden künstlichen Elements Oganesson ist nichts bekannt, da bisher nur wenige Atome hergestellt wurden, es könnte aber aufgrund relativistischer Effekte von den typischen Edelgasen abweichen.
Die Tatsache, dass die Elemente der Hauptgruppen ähnliche Eigenschaften haben, hängt mit dem Aufbau der Atome zusammen. Die Hauptgruppenelemente versuchen durch Reaktionen mit anderen Stoffen eine Edelgaskonfiguration der Elektronenhülle zu erreichen. Elemente in derselben Hauptgruppe müssen gleich viele Elektronen abgeben oder aufnehmen, um dies zu erreichen; daher resultieren die gleichen Eigenschaften.
Weblinks
Literatur
- Charles E. Mortimer, Ulrich Müller, Johannes Beck: Chemie: das Basiswissen der Chemie. 12., korrigierte und aktualisierte Auflage. Georg Thieme Verlag, Stuttgart, New York 2015, ISBN 978-3-13-484312-5.