Alphastrahlung
Alphastrahlung oder α-Strahlung ist eine ionisierende Strahlung, die beim Alphazerfall, einer Art des radioaktiven Zerfalls von Atomkernen, auftritt. Ein radioaktives Nuklid, das diese Strahlung aussendet, wird als Alphastrahler bezeichnet. Der Name stammt von der auf Rutherford zurückgehenden Einteilung der Strahlen aus radioaktiven Stoffen in Alpha-, Beta- und Gammastrahlen (in der Reihenfolge zunehmenden Durchdringungsvermögens). Alphastrahlung ist eine Teilchenstrahlung, denn der zerfallende Atomkern (Mutterkern) sendet einen Helium-4-Atomkern aus, der in diesem Fall Alphateilchen genannt wird, und wird dadurch zum Tochterkern.
|
α-Teilchen | |
|---|---|
| Eigenschaften [1] | |
| elektrische Ladung | +2 e |
| Masse | 4,001 506 179 127(63) u 6,644 657 3357(20) · 10−27 kg 7294,299 541 42(24) me |
| Ruheenergie | 3727,379 4066(11) MeV |
| SpinParität | 0+ |
| Isospin | 0 (Iz = 0) |
| mittlere Lebensdauer | stabil |

Der α-Zerfall tritt nur in Nukliden mit hoher Massenzahl auf. Das Formelzeichen für das Alphateilchen ist der kleine griechische Buchstabe α (alpha).
Physik des Alphazerfalls
Zerfallsvorgang
Das Alphateilchen ist der Atomkern eines Helium-4-Atoms, es ist ein zweiwertiges Kation von Helium. Es besteht aus zwei Protonen und zwei Neutronen. Die Massenzahl des Kerns nimmt beim Alphazerfall um vier Einheiten ab, die Kernladungszahl um zwei Einheiten. Bezeichnet X das Mutter- und Y das Tochternuklid, die beim Zerfall freiwerdende Energie, und werden wie üblich Massenzahlen oben und Ordnungszahlen unten angeschrieben, gilt für den Alphazerfall allgemein:
- .
Ein konkretes Beispiel ist:
- .
Das Alphateilchen verlässt den Kern mit einer Austrittsgeschwindigkeit zwischen etwa 10.000 km/s und 20.000 km/s, entsprechend einer kinetischen Energie von einigen MeV. Der anfängliche Elektronenüberschuss des entstehenden Tochteratoms baut sich durch den Rückstoß des Zerfalls und Wechselwirkung (Ladungsausgleich) mit der umgebenden Materie ab.
Energiespektrum
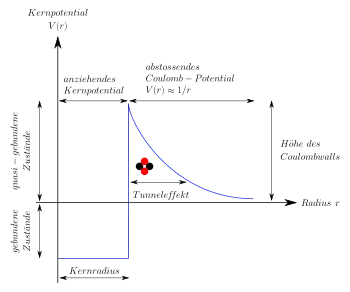
Wie bei jedem radioaktiven Zerfall wird durch den Alphazerfall eine wohldefinierte Energiemenge frei. Sie entspricht nach der Masse, die als Massendefekt durch den Vorgang verloren geht. Diese Energie zeigt sich als kinetische Energie des Alphateilchens und des Tochterkerns; in manchen Fällen kann auch ein Teil der Energie zunächst als angeregter Zustand des Tochterkerns verbleiben und dann anschließend als Gammastrahlung abgebaut werden. Die kinetische Energie verteilt sich auf die beiden Teilchen im umgekehrten Verhältnis ihrer Massen (siehe Kinematik (Teilchenprozesse)). Die von einem gegebenen Nuklid emittierten Alphateilchen haben deshalb, anders als beispielsweise beim Betazerfall, nur ganz bestimmte Werte der kinetischen Energie, d. h., ihr Energiespektrum ist ein Linienspektrum. Dieses Spektrum ist charakteristisch für das jeweilige Radionuklid. Seine Messung kann also zur Bestimmung dieses Nuklids dienen.
Coulombwall, Tunneleffekt
Das Alphateilchen wird einerseits durch die starke Wechselwirkung vom Kern angezogen, aber zugleich aufgrund gleichnamiger Ladungen elektrisch abgestoßen. Die stärkere Kernkraft hat eine kurze, die schwächere elektrostatische Abstoßung eine lange Reichweite. Daher bildet das Potential eine Art Barriere, den Coulombwall. Der Wall ist höher als die für das Alphateilchen verfügbare kinetische Energie. Das Alphateilchen wäre daher nach der klassischen Physik stabil im Kern gebunden; mittels des quantenmechanischen Tunneleffekts kann es ihn jedoch verlassen. Die Wahrscheinlichkeit pro Zeiteinheit dafür kann sehr klein sein. Sie bestimmt die Halbwertszeit des Zerfalls. Der beobachtete Zusammenhang zwischen der Halbwertszeit und der Energie der emittierten Alphateilchen wird durch die Geiger-Nuttall-Regel beschrieben.
Radionuklide mit Alphazerfall
Alphazerfall tritt nur bei schweren Nukliden auf, beginnend mit einigen wenigen der Neutronenzahl 84, deren Tochterkerne somit 82 Neutronen haben, eine der „magischen Zahlen“, bei denen Kerne besonders stabil sind. Dominierend wird der α-Zerfall oberhalb der „magischen“ Neutronenzahl 126. Typische in der Natur vorkommende Alphastrahler sind Uran und Thorium sowie deren Zerfallsprodukte Radium und Radon.
Die kinetische Energie eines Alphateilchens liegt typischerweise in der Größenordnung von 2 bis 5 MeV. Alphateilchen aus künstlich erzeugten Nukliden können aber Energien von über 10 MeV besitzen. Die Alpha-Energien und Halbwertszeiten der einzelnen Nuklide können in der Liste der Isotope nachgeschlagen werden und sind in Nuklidkarten angegeben.
Der Alphazerfall ergibt rechnerisch nach der Bethe-Weizsäcker-Massenformel für alle Nuklide ab Massenzahl 165 eine positive Energiefreisetzung, denn die so berechnete Summe der Massen des Alphateilchens und des Tochterkerns ist kleiner als die Masse des Mutterkerns. Dennoch wurde bei vielen schweren Nukliden ein Alphazerfall bisher nie beobachtet. Allerdings sind in den letzten Jahrzehnten einige früher als stabil geltende Nuklide als extrem langlebige Alphastrahler „entlarvt“ worden, zum Beispiel 149Sm, 152Gd und 174Hf. Erst in den 2000er Jahren konnte dann auch bei 180W[2] und 209Bi[3] Alphazerfall mit Halbwertszeiten von einigen Trillionen Jahren nachgewiesen werden.
Nachweis
Zum Nachweis von Alphastrahlung, beispielsweise zu Strahlenschutzzwecken, eignen sich im Prinzip alle Teilchendetektoren. Allerdings muss die Strahlung das Innere des Detektors, das empfindliche Volumen, erreichen können; ein Zählrohr muss dazu ein genügend dünnes Folienfenster haben. Geeignet sind z. B. die üblichen Kontaminationsnachweisgeräte. Für genaue Messungen, etwa zur Bestimmung des Energiespektrums der Strahlung, müssen sich Strahlenquelle und Detektor in einem gemeinsamen Vakuum befinden. Dabei wird meist ein Halbleiterdetektor verwendet.
Wechselwirkung mit Materie
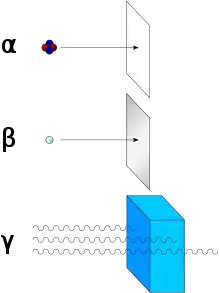
Eindringtiefe, Reichweite
Aufgrund ihrer elektrischen Ladung und relativ großen Masse von 4 u haben Alphateilchen nur eine sehr geringe Eindringtiefe in Materie.
Die Reichweite ist neben der jeweiligen Energie wesentlich abhängig von der Dichte des jeweils umgebenden Mediums. Sie beträgt in Luft bei Normaldruck ungefähr 10 cm (bei 10 MeV) und ist umgekehrt proportional zum Luftdruck. In der Hochatmosphäre der Erde beträgt sie hunderte Kilometer. Ursache ist die Druckabhängigkeit der freien Weglänge der Alphateilchen, d. h. des Abstandes zwischen den Stoßpartnern (Moleküle), an die die Alphateilchen ihre kinetische Energie sukzessive abgeben.
Die Ionisation von Alphateilchen ist dichter – d. h. die Anzahl Ionen, die das Teilchen pro Längeneinheit seiner Wegstrecke erzeugt, ist viel höher – als etwa bei Beta- oder Gammastrahlung. In einer Nebelkammer sehen deshalb die durch Alphastrahlung erzeugten Bahnspuren, verglichen mit denen von Betastrahlen ähnlicher Energie, kürzer und dicker aus. Die Eindringtiefe eines 5,5-MeV-Alphateilchens in Wasser oder organischem Material beträgt dementsprechend nur etwa 45 μm. Ein etwas kräftigeres Blatt Papier oder einige Zentimeter Luft reichen somit im Allgemeinen schon aus, um Alphastrahlung vollständig abzuschirmen.[4]

Biologische Wirkung
Alphastrahlung, die von außen den menschlichen Körper trifft, ist relativ ungefährlich, da die Alphateilchen aufgrund ihrer geringen Eindringtiefe überwiegend nur in die oberen toten Hautschichten eindringen und dort verbleiben. Ein im Organismus durch Einatmen oder sonst wie eingelagerter (inkorporierter) Alphastrahler ist dagegen sehr schädlich, da seine Strahlung lebende Zellen schädigt. Insbesondere bei Anreicherung eines Alphastrahlers in einem Organ wirkt die Strahlendosis sich auf kleinem Raum, also konzentriert, und u. U. auf wichtige Körperzellen aus. Der Strahlungswichtungsfaktor für Alphastrahlung wurde auf 20 festgelegt, während er für Beta- und Gammastrahlung lediglich 1 beträgt. Für gleichen Energieeintrag wird also bei Alphastrahlung die 20-fache Schadwirkung angenommen.
In der Radonbalneologie wird eine heilende Wirkung gering dosierter Alphastrahlung durch den Radongehalt mancher Heilbäder (z. B. Badgastein) angenommen.
Auf Grund der großen Masse des Alphateilchens erhält beim Alphazerfall auch der Tochterkern einen merklichen Teil der freiwerdenden Energie. Dies wurde 1909 von Lise Meitner und Otto Hahn entdeckt und entspricht der Kinematik des Zwei-Teilchen-Zerfalls. Die Tochterkern-Energien betragen bis zu etwa 200 keV. Damit tragen bei inkorporierten Alphastrahlern auch die Rückstoßkerne zur Schädigung des Gewebes bei.
Anwendungen
Isotopenbatterie

Alphastrahler (hauptsächlich Transurane) mit relativ kurzer Halbwertszeit können sich durch ihren eigenen Alphazerfall bis zur Rotglut erhitzen. Dies ist möglich, weil nahezu alle bei ihrem Zerfall erzeugten energiereichen Alphateilchen von ihren schweren Atomen noch in ihrem Innern aufgehalten werden und ihre Bewegungsenergie als Wärme an sie abgeben. Wenn sie außerdem nur wenig Gammastrahlung erzeugen und ihre Halbwertszeit (meistens einige Jahre bis Jahrzehnte) lang genug ist, kann die abgegebene Wärme in Radionuklidbatterien zur Gewinnung elektrischer Energie genutzt werden.
Rauchmelder
Außerdem werden Alphastrahler in Ionisationsrauchmeldern verwendet. Diese erkennen den Rauch durch die Messung der Leitfähigkeit der durch Alphastrahlen ionisierten Luft, da Rauchpartikel die Leitfähigkeit verändern.
Endprodukt Helium
Haben Alphateilchen nach vielen Stößen in Materie den Großteil ihrer kinetischen Energie abgebaut, sind sie so langsam, dass sie Elektronen einfangen können. Dadurch entsteht das Edelgas Helium, und zwar das bei weitem häufigste Heliumisotop Helium-4.
Das aus im Erdinneren emittierter Alphastrahlung entstandene Helium diffundiert relativ leicht durch Mineralien. In Erdgasblasen erreicht es Konzentrationen von einigen Prozent, so dass einzelne Erdgasquellen auch ökonomisch rentabel zur Heliumgewinnung genutzt werden.
In der Atmosphäre befindliches Helium steigt aufgrund seiner geringen Dichte weiter auf; in Höhen zwischen 700 und 1700 km ist Helium das häufigste Gas. Ein zwar winziger, aber eben nicht mehr zu vernachlässigender Teil seiner Atome erreicht die Fluchtgeschwindigkeit der Erde und entkommt für immer dem Gravitationsfeld der Erde.
„Alphastrahlen“ aus anderen als radioaktiven Quellen
Mit dem Ausdruck Alphateilchen bezeichnet man in der Physik üblicherweise jeden vollständig ionisierten Helium-4-Kern, auch wenn er nicht aus einem radioaktiven Zerfall stammt. Zum Beispiel sind etwa 12 % aller Teilchen der galaktischen kosmischen Strahlung solche Alphateilchen.[5] Dies ist nicht überraschend, da Helium eines der häufigsten Elemente im Universum ist. Allerdings erreicht dieser Teil der kosmischen Strahlung nie den Erdboden.
Alphateilchen können auch künstlich aus Heliumgas in einer Ionenquelle erzeugt werden. Werden sie in einem Teilchenbeschleuniger beschleunigt, wird dessen Strahlenbündel dementsprechend manchmal auch Alphastrahl genannt.
Forschungsgeschichte
Alphastrahlung war die erste nachgewiesene Form von Radioaktivität. Antoine Henri Becquerel entdeckte sie 1896 durch die Schwärzung von lichtdicht verpackten Fotoplatten durch Uransalze. Weitere Forschungen von Marie Curie und Pierre Curie führten unter anderem zur Isolation der Uran-Zerfallsprodukte Radium und Polonium und dem Nachweis, dass diese ebenfalls Alphastrahler sind. Die drei Forscher erhielten für diese Leistungen 1903 den Nobelpreis für Physik.
Ernest Rutherford zeigte 1898 die Unterscheidbarkeit verschiedener Arten ionisierender Strahlung durch ihr unterschiedliches Durchdringungsvermögen und prägte dabei die Bezeichnungen α- und β-Strahlung.[6] 1899 demonstrierten Stefan Meyer, Egon Schweidler und Friedrich Giesel die Unterscheidbarkeit durch verschiedene Ablenkung im magnetischen Feld.
Durch Beobachtung der Spektrallinien bei Gasentladung konnte Rutherford 1908 die Identität der Alphateilchen als Heliumkerne nachweisen.[7]
1911 benutzte Rutherford Alphastrahlen für seine Streuexperimente, die zur Aufstellung des Rutherfordschen Atommodells führten.
1913 stellten Kasimir Fajans und Frederick Soddy die radioaktiven Verschiebungssätze auf, die das beim Alphazerfall entstehende Nuklid bestimmen.
Mit Alphastrahlen, die auf Stickstoffatomkerne trafen, konnte Rutherford 1919 erstmals eine künstliche Elementumwandlung beobachten: es entstand Sauerstoff in der Kernreaktion 14N(α,p)17O oder, ausführlicher geschrieben,
- .
1928 fand George Gamow die quantenmechanische Erklärung des Alphazerfalls durch den Tunneleffekt[8], siehe dazu auch Gamow-Faktor.
Literatur
- Werner Stolz: Radioaktivität. Grundlagen – Messung – Anwendungen. 5. Auflage. Teubner, Wiesbaden 2005, ISBN 3-519-53022-8.
Kernphysik
- Theo Mayer-Kuckuk: Kernphysik. 6. Auflage. Teubner, 1994, ISBN 3-519-03223-6.
- Klaus Bethge: Kernphysik. Eine Einführung (mit 24 Tabellen, 89 Übungen mit ausführlichen Lösungen sowie Kästen zur Erläuterung und einem historischen Überblick über die Entwicklung der Kernphysik). Springer, Berlin 1996, ISBN 3-540-61236-X.
- Jean-Louis Basdevant, James Rich, Michael Spiro: Fundamentals in Nuclear Physics: From Nuclear Structure to Cosmology. Springer, New York 2005, ISBN 0-387-01672-4.
Forschungsgeschichte
- Milorad Mlađenović: The History of Early Nuclear Physics (1896–1931). World Scientific 1992, ISBN 981-02-0807-3.
Strahlenschutz
- Hanno Krieger: Grundlagen der Strahlungsphysik und des Strahlenschutzes. Teubner, Wiesbaden 2007, ISBN 978-3-8351-0199-9.
- Claus Grupen: Grundkurs Strahlenschutz. Praxiswissen für den Umgang mit radioaktiven Stoffen. Springer 2003, ISBN 3-540-00827-6.
- James E Martin: Physics for Radiation Protection. John Wiley & Sons, New York 2006, ISBN 0-471-35373-6.
Medizin
- Günter Goretzki: Medizinische Strahlenkunde. Physikalisch-technische Grundlagen. Urban & Fischer, 2004, ISBN 3-437-47200-3.
- Thomas Herrmann, Michael Baumann, Wolfgang Dörr: Klinische Strahlenbiologie – kurz und bündig. Elsevier, Urban und Fischer, München 2006, ISBN 3-437-23960-0.
Weblinks
- Literatur von und über Alphastrahlung im Katalog der Deutschen Nationalbibliothek
- Das „Glossar Strahlenschutz“ des Forschungszentrums Jülich erläutert viele Begriffe rund um ionisierende Strahlen (Alpha-, Beta-, Gammastrahlung, Regelwerke, Strahlenschutz etc.).
Video
Einzelnachweise
- Die Angaben über die Teilcheneigenschaften der Infobox sind, wenn nicht anders angegeben, entnommen aus der Veröffentlichung der CODATA Task Group on Fundamental Constants: CODATA Recommended Values. National Institute of Standards and Technology, abgerufen am 4. Juli 2019 (englisch). Die eingeklammerten Ziffern bezeichnen die Unsicherheit in den letzten Stellen des Wertes, diese Unsicherheit ist als geschätzte Standardabweichung des angegebenen Zahlenwertes vom tatsächlichen Wert angegeben.
- Cristina Cozzini et al.: Detection of the natural ? decay of tungsten. Physical Review C (2004), preprint.
- Pierre de Marcillac et al.: Experimental detection of alpha-particles from the radioactive decay of natural bismuth, Nature 422, S. 876–878 (24. April 2003), Ergebnistabelle.
- Harvard Natural Sciences Lecture Demonstrations: α, β, γ Penetration and Shielding. Abgerufen am 20. Februar 2020 (englisch).
- C. Grupen: Astroparticle Physics, Springer 2005, ISBN 3-540-25312-2, S. 78.
- Uranium Radiation and the Electrical Conduction Produced by It. In: Philosophical Magazine. 5. Folge, Band 47, Nummer 284, 1899, S. 116 (doi:10.1080/14786449908621245).
- Ernest Rutherford, T. Royds: The Nature of the α Particle from Radioactive Substances. Phil. Mag. 17 (1909), S. 281–286 (Online).
- George Gamow: Zur Quantentheorie des Atomkernes. Zeitschrift für Physik 51 (1928), S. 204.