Halogene
Die Halogene [halogeːnə] („Salzbildner“, von altgriechisch ἅλς háls „Salz“ und γεννᾶν gennãn „erzeugen“) bilden die 7. Hauptgruppe oder nach neuer Gruppierung des Periodensystems die Gruppe 17 im Periodensystem der Elemente, die aus folgenden sechs Elementen besteht: Fluor, Chlor, Brom, Iod, dem äußerst seltenen radioaktiven Astat und dem 2010 erstmals künstlich erzeugten, sehr instabilen Tenness[1]. Die Gruppe der Halogene steht am rechten Rand des Periodensystems zwischen den Chalkogenen (6. Hauptgruppe) und Edelgasen (8. Hauptgruppe).
|
Lage im Periodensystem
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe | 17 |
| Hauptgruppe | 7 |
| Periode | |
| 2 | 9 F |
| 3 | 17 Cl |
| 4 | 35 Br |
| 5 | 53 I |
| 6 | 85 At |
| 7 | 117 Ts |
Diese Nichtmetalle sind im elementaren Zustand sehr reaktionsfreudig (Fluor kann unter Feuererscheinung reagieren), farbig und reagieren mit Metallen zu Salzen (Namensherkunft) und mit Wasserstoff unter Normalbedingung zu Halogenwasserstoffen (gasförmige, einprotonige Säuren).
Fluor, Chlor, Brom und Iod spielen wichtige Rollen in Chemie, Biologie und Medizin. Astat dient in organischen Verbindungen in der Nuklearmedizin zur Bestrahlung von bösartigen Tumoren.[2]
Vorkommen

Halogene kommen in der Natur vor allem als einfach negativ geladene Anionen in Salzen vor. Das zugehörige Kation ist meist ein Alkali- oder Erdalkalimetall, insbesondere die Natriumsalze der Halogene sind häufig anzutreffen. Aus diesen können dann die Halogene mittels Elektrolyse gewonnen werden. Ein nicht unbeträchtlicher Teil der Halogenide ist im Meerwasser gelöst.
Wichtige Halogenid-Verbindungen:
- Natriumfluorid, NaF
- Calciumfluorid, CaF2 (Flussspat)
- Natriumhexafluoridoaluminat (ein Komplexsalz), Na3[AlF6] (Kryolith)
- Natriumchlorid, NaCl (Kochsalz)
- Kaliumchlorid, KCl
- Natriumbromid, NaBr
- Kaliumbromid, KBr
- Natriumiodid, NaI
Im Gegensatz zu den anderen Halogenen kommt Iod auch in der Natur als Iodat vor. Astat, das seltenste natürlich vorkommende Element, ist Zwischenprodukt der Uran- und Thoriumzerfallsreihen. Die Gesamtmenge in der Erdkruste beträgt lediglich 25 g.
Gewinnung der Reinelemente
Fluorgas F2 lässt sich nur durch elektrochemische Vorgänge gewinnen, da es kein Element und keine Verbindung gibt, die ein größeres Redox-Potential als Fluor hat und dieses oxidieren könnte (Oxidation, weil Elektronenabgabe von 2 F− zu F2, andere Halogene analog).
Alle anderen Halogene lassen sich neben der elektrochemischen Darstellung (z. B. Chloralkalielektrolyse) auch mit Oxidationsmittel wie MnO2 (Braunstein), KMnO4 (Kaliumpermanganat) herstellen.
Eine weitere Möglichkeit zur Gewinnung von Brom oder Iod ist das Einleiten von Chlorgas als Oxidationsmittel in konzentrierte Bromid- bzw. Iodidlösungen:
Hier sei zur Gewinnung von Chlor auch das Deacon-Verfahren erwähnt (Redoxreaktion von Salzsäuregas mit Luft als Oxidationsmittel zu Wasser und Chlorgas):
Eigenschaften
Physikalische Eigenschaften
Halogen Molekül Struktur Modell d(X–X) / pm
(Gasphase)d(X–X) / pm
(Feststoff)Fluor F2 

143 149 Chlor Cl2 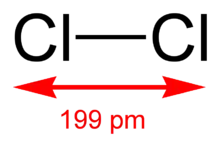

199 198 Brom Br2 

228 227 Iod I2 

266 272
Elementare Halogene sind farbige, leicht flüchtige bis gasförmige Substanzen, die in Wasser löslich sind (Fluor reagiert). Ihre Farbintensität, Siedepunkte und Dichte nehmen mit der Ordnungszahl zu. Sie liegen in Form von zweiatomigen Molekülen der Form X2 vor (z. B. F2 und Cl2) und sind daher Nichtleiter (Isolatoren).
- Die Farbintensität im gasförmigen Aggregatzustand steigt mit zunehmender Ordnungszahl.
- Dichte, Schmelz- und Siedepunkt nehmen aufgrund der Zunahme der Molmasse von oben nach unten zu. Bei Standardbedingungen sind Fluor und Chlor Gase, Brom ist eine Flüssigkeit und Iod fest.
| Element | Fluor | Chlor | Brom | Iod |
|---|---|---|---|---|
| Schmelzpunkt (1013 hPa)[3] | 53,53 K (−219,62 °C) |
171,6 K (−101,5 °C) |
265,8 K (−7,3 °C) |
386,85 K (113,70 °C) |
| Siedepunkt (1013 hPa)[3] | 85,15 K (−188 °C) |
238,5 K (−34,6 °C) |
331,7 K (58,5 °C) |
457,2 K (184 °C) |
| Kritischer Punkt[3] |
|
|
|
|
| Tripelpunkt[3] |
|
|
| |
| Dichte (0 °C, 1013 hPa)[3] | 1,6965 kg/m3 | 3,215 kg/m3 | 3,12 g/cm3 | 4,94 g/cm3 |
| Atommasse | 18,998 u | 35,45 u | 79,904 u | 126,904 u |
| Elektronegativität | 4,0 | 3,16 | 2,96 | 2,66 |
| Struktur | 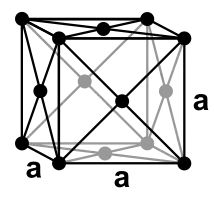 |
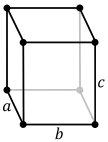 |
 |
 |
| Kristallsystem | kubisch | orthorhombisch | orthorhombisch | orthorhombisch |
Chemische Eigenschaften
Halogene sind sehr reaktionsfreudige Nichtmetalle, da ihnen nur noch ein einziges Valenzelektron zur Vollbesetzung der Valenzschale fehlt. Da die Halogen-Halogen-Bindung nicht sehr stabil ist, reagieren auch Halogenmoleküle heftig. Die Reaktivität nimmt, wie die Elektronegativität, von Fluor zu Iod ab. Gleichzeitig steigt die 1. Ionisierungsenergie nach oben hin an. Die Eigenschaften von Astat sind jedoch größtenteils unerforscht, wahrscheinlich ist es aber aus chemischer Sicht dem Iod sehr ähnlich.
- Halogene reagieren exotherm mit Wasserstoff unter Bildung von Halogenwasserstoffen, die, in Wasser gelöst, mehr oder weniger starke Säuren sind. Die Heftigkeit der Reaktion nimmt von Fluor zu Iod ab.
- Beispiel: Chlorknallgasreaktion:
- Die Wasserlöslichkeit der Halogene nimmt von Fluor zu Iod ab, wobei Fluor mit Wasser unter Bildung von Fluorwasserstoff und Sauerstoff reagiert.
- Chlor reagiert mit Wasser zu Chlorwasserstoff und Hypochloriger Säure.
- Ebenso reagiert Brom mit Wasser zu Bromwasserstoff und Hypobromiger Säure.
- Iod ist kaum löslich in Wasser und reagiert nicht.
- Die Halogene sind von Iod zu Fluor zunehmend giftig.
Verwendung
In der organischen Chemie werden sie zur Synthese von Halogenverbindungen verwendet. Das Verfahren wird allgemein als Halogenierung bezeichnet.
Durch Zugabe von Halogenen in Glühlampen wird durch den Wolfram-Halogen-Kreisprozess deren Lebensdauer und Lichtausbeute erhöht. Man spricht dann auch von Halogenlampen.
Verbindungen
Halogenide
_iodide.jpg.webp)
Ionische Halogenverbindungen wie z. B. die Fluoride, Chloride, Bromide und Iodide sind salzartige Stoffe. Dementsprechend haben sie hohe Schmelzpunkte, sind spröde und elektrische Nichtleiter außer in Schmelze und Lösung. Die meisten Halogenide sind wasserlöslich (wie z. B. Kochsalz, Natriumchlorid. Wasserunlöslich sind Blei-, Quecksilber- und Silberhalogenide (siehe Salzsäuregruppe) sowie Kupfer(I)-halogenide. Viele Halogenide kommen in der Natur in Form von Mineralien vor.
Halogenwasserstoffe
- Fluorwasserstoff siedet trotz der geringen Molmasse durch die Bildung von starken Wasserstoffbrückenbindungen erst bei 19,5 °C. Die wässrige Lösung wird Flusssäure genannt.
- Chlorwasserstoff siedet bei −85 °C. Er löst sich in Wasser und reagiert als sehr starke Säure. Die wässrige Lösung wird Salzsäure genannt.
- Bromwasserstoff siedet bei −67 °C. Er löst sich in Wasser und reagiert als eine der stärksten Säuren. Die wässrige Lösung wird Bromwasserstoffsäure genannt.
- Iodwasserstoff siedet bei −35 °C. Er löst sich in Wasser und reagiert als die stärkste bekannte sauerstofffreie Säure. Die wässrige Lösung wird Iodwasserstoffsäure genannt.
Halogensauerstoffsäuren
Mit Ausnahme von Fluor, dessen einzige Sauerstoffsäure die instabile Hypofluorige Säure ist, bilden die Halogene vier Arten von Sauerstoffsäuren, die wie folgt benannt werden:
- HXO: Hypohalogenige Säure (Beispiel: Hypochlorige Säure)
- HXO2: Halogenige Säure (Beispiel: Chlorige Säure)
- HXO3: Halogensäure (Beispiel: Chlorsäure)
- HXO4: Perhalogensäure (Beispiel: Perchlorsäure)
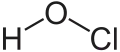 Hypochlorige Säure
Hypochlorige Säure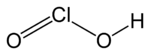 Chlorige Säure
Chlorige Säure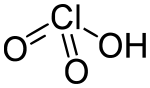 Chlorsäure
Chlorsäure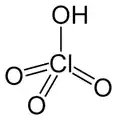 Perchlorsäure
Perchlorsäure
Die Säurestärke wächst mit steigender Zahl der Sauerstoffatome, ebenso die oxidierende Wirkung. Die meisten Sauerstoffsäuren der Halogene sind sehr instabil und zersetzen sich exotherm.
Interhalogenverbindungen
| Cl | ClF, ClF3, ClF5 | ||
|---|---|---|---|
| Br | BrF, BrF3, BrF5 | BrCl | |
| I | IF, IF3, IF5, IF7 | ICl, (ICl3)2 | IBr, IBr3 |
| F | Cl | Br |
Interhalogenverbindungen sind Verbindungen der Halogene untereinander. Es gibt folgende Arten (Y ist das elektronegativere Element):
- XY: alle möglichen Kombinationen existent
- XY3: Y ist Fluor, Chlor oder Brom
- XY5: Y ist immer Fluor
- XY7: nur IF7 bekannt
Interhalogenverbindungen sind bei Standardbedingungen instabil oder äußerst reaktiv.
Es existieren auch Interhalogenidionen wie beispielsweise BrF6− und IF6−. Auch Sauerstoffsäurehalogenide wie z. B. Perchlorylfluorid ClO3F oder Iodoxipentafluorid IOF5 sind bekannt.
Einzelnachweise
- Spiegel Online: Ordnungszahl 117, Physiker erzeugen neues chemisches Element
- M. J. Willhauck, B. R. Samani, I. Wolf, R. Senekowitsch-Schmidtke, H. J. Stark, G. J. Meyer, W. H. Knapp, B. Göke, J. C. Morris, C. Spitzweg: The potential of 211Astatine for NIS-mediated radionuclide therapy in prostate cancer. In: Eur. J. Nucl. Med. Mol. Imaging. 35, Nr. 7, Juli 2008, S. 1272–1281. doi:10.1007/s00259-008-0775-4. PMID 18404268.
- P. Häussinger, R. Glatthaar, W. Rhode, H. Kick, C. Benkmann, J. Weber, H.-J. Wunschel, V. Stenke, E. Leicht, H. Stenger: Noble Gases. In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim 2006 (doi:10.1002/14356007.a17_485).
Literatur
- M. Binnewies, M. Jäckel, H. Willner: Allgemeine und Anorganische Chemie. Spektrum Akademischer Verlag, 2004, ISBN 3-8274-0208-5.
