Tributylzinnhydrid
Tributylzinnhydrid (TBTH) ist eine metallorganische Verbindung des Zinns und eine Tributylzinn-Verbindung.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
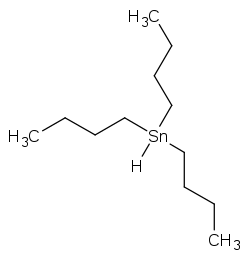 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Tributylzinnhydrid | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C12H28Sn | |||||||||||||||||||||
| Kurzbeschreibung |
farblose bis gelbliche Flüssigkeit[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 291,04 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||||||||
| Dichte |
1,10 g·cm−3 (20 °C)[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
112–114 °C (11 hPa)[2] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit |
in Wasser Zersetzung[2] | |||||||||||||||||||||
| Brechungsindex |
1,4715 (25 °C)[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
0,004 ml·m−3[5] | |||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Gewinnung und Darstellung
Die Verbindung kann durch Umsetzung von Tributylzinnchlorid mit Natriumborhydrid in einer Stickstoffatmosphäre gewonnen werden[3]:
Eigenschaften
Tributylzinnhydrid ist eine farblose, giftige Flüssigkeit. Die Sn–H-Bindung im TBTH ist mit 310 kJ/mol recht schwach, so dass sie leicht homolytisch gespalten werden kann.
Verwendung
Synthetische Anwendung
Mit Azobis(isobutyronitril) (AIBN) als Radikalstarter wird TBTH in der Barton-McCombie-Reaktion und der Barton-Decarboxylierung eingesetzt. Diese beiden vom englischen Nobelpreisträger Derek H. R. Barton entdeckten Reaktionen ermöglichen die Umsetzung von Alkoholen, bzw. Säurehalogeniden in ihre entsprechenden Alkane.
Eine weitere interessante Reaktion ist die reduktive Dehalogenierung von Halogenalkanen, die auch oft in Verbindung mit einer anschließenden intramolekularen radikalischen Cyclisierung des gebildeten Alkylradikals synthetischen Nutzen findet.
TBTH wird auch oft zur Synthese der zur Stille-Kupplung benötigten Zinn-Organyle verwandt.
Nachweis
Organozinnhydride wie TBTH lassen sich im Infrarotspektrum einfach an einer ausgeprägten Sn-H-Bande im Bereich von 1800 bis 1880 cm−1 identifizieren.[3]
Literatur
- Heinz Rüdel, Jürgen Steinhanses, Josef Müller, Christa Schröter-Kermani: Retrospektives Monitoring von Organozinnverbindungen in biologischen Proben aus Nord- und Ostsee – sind die Anwendungsbeschränkungen erfolgreich? Umweltwissenschaften und Schadstoff-Forschung 21(3), 2009, S. 282–291, doi:10.1007/s12302-009-0039-3.
Einzelnachweise
- Eintrag zu Tributylzinnhydrid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. September 2014.
- Datenblatt Tributylzinnhydrid zur Synthese (PDF) bei Merck, abgerufen am 19. Januar 2011.
- Ernest R. Birnbaum and Paul H. Javora: Organotin hydrides – A. Tri-n-butyltin hydride. In: Robert W. Parry (Hrsg.): Inorganic Syntheses. Band 12. McGraw-Hill Book Company, Inc., 1970, ISBN 07-048517-8 (defekt), S. 45–57 (englisch).
- Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Tributylzinnverbindungen, soweit in diesem Anhang nicht gesondert aufgeführt im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 9. Januar 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Tributylstannan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)


