Tetraphenylzinn
Tetraphenylzinn ist eine chemische Verbindung aus der Gruppe der zinnorganischen Verbindungen.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
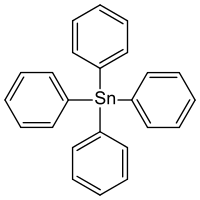 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Tetraphenylzinn | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C24H20Sn | |||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff mit charakteristischem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 427,10 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
1,49 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
424 °C[1] | |||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (0,041 mg·l−1 bei 20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Tetraphenylzinn kann durch Reaktion von Phenylmagnesiumbromid mit Zinntetrachlorid gewonnen werden.[3] Das Phenylmagnesiumbromid wird dazu zunächst in situ aus Brombenzol und Magnesium in Dekalin hergestellt und dann direkt mit dem Zinnhalogenid umgesetzt:
Eigenschaften
Tetraphenylzinn ist ein brennbarer weißer Feststoff, der praktisch unlöslich in Wasser ist. Im 13C-Kernresonanzspektrum (NMR) zeigt es folgende Signale:[4]
| Sn–C1– | –C2 | –C3 | –C4 | |
|---|---|---|---|---|
| ppm | 138,3 | 137,7 | 129,0 | 129,4 |
| J(13C–119Sn) | 530 | 37,0 | 50,7 | 11,1 |
Im 119Sn–NMR liefert es ein Signal bei −127 ppm.[4]
Verwendung
Tetraphenylzinn kann zur Stabilisierung von Kunststoffen eingesetzt werden.[5] Es dient aber in erster Linie dazu, andere zinnorganische Verbindungen herzustellen.[5] So werden durch die Kocheshkov-Umlagerung Diphenyl- und Triphenyl-Verbindungen hergestellt[6]:
Einzelnachweise
- Eintrag zu Tetraphenylzinn in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- Datenblatt Tetraphenyltin, 97% bei Sigma-Aldrich, abgerufen am 27. Dezember 2017 (PDF).
- Luise Ellinghaus, Christine Kropf, Ernst Langer, Peter Müller, Heidi Müller-Dolezal, Renate Stoltz, Hanna Söll: Houben-Weyl Methods of Organic Chemistry Vol. XIII/6, 4th Edition: Organogermanium- and -tin Compounds. Georg Thieme Verlag, 14 May 2014, ISBN 978-3-13-180734-2, S. 215.
- Cathrin Zeppek, Johann Pichler, Ana Torvisco, Michaela Flock, Frank Uhlig: Aryltin chlorides and hydrides: Preparation, detailed NMR studies and DFT calculations. In: Journal of Organometallic Chemistry. Band 740, September 2013, S. 41–49, doi:10.1016/j.jorganchem.2013.03.012.
- Joachim Voigt: Die Stabilisierung der Kunststoffe gegen Licht und Wärme. Springer-Verlag, 9. März 2013, ISBN 978-3-642-52097-6, S. 370–.
- Alwyn George Davies: Organotin chemistry. Band 1. Wiley-VCH Verlag GmbH & Co. KGaA, 2004, ISBN 3-527-31023-1 (Seite 167 in der Google-Buchsuche).

