Nachweisreaktion
Ein Nachweis ist eine Methode der Analytischen Chemie, die dazu dient, eine Stoffprobe (den Analyten) qualitativ zu untersuchen. Davon zu unterscheiden sind quantitative Bestimmungsmethoden und Methoden der Strukturanalytik.

-Ionen1.jpg.webp)
Die Nachweisreaktion ist eine chemische Reaktion des jeweils eingesetzten Nachweisreagenz, die das Vorhandensein eines Analyten anzeigt. Die Bilder rechts zeigen beispielsweise eine Niederschlagsbildung im Reagenzglas als Nachweisreaktion für Chlorid-Anionen mit Hilfe von Silbersalzlösung und Ammoniakwasser, darunter zwei Nachweise von Kupfersalzen als Kupfertetramminkomplex (tiefblaue Lösung, Komplexbildungsreaktion) und als Kupferhexacyanidoferrat-II (brauner Niederschlag, Fällungsreaktion). Weitere als typische Nachweisreaktionen nutzbare Arten von Stoffumwandlungen sind Redoxreaktionen und Säure-Base-Reaktionen.
Mit dem Nachweis (der Nachweisreaktion) kann eine Probe ohne oder mit relativ einfachen apparativen Mitteln untersucht werden auf:
- in ihr enthaltene Einzelkomponenten (qualitativ),
- deren ungefähre Menge oder Konzentration (halbquantitativ) sowie
- auf strukturelle Besonderheiten, z. B. funktionelle Gruppen
- Spezies, in denen ein Element vorliegt (z. B. Chlor als Chlorid oder Hypochlorit oder elementar)
So werden chemische Elemente, eventuell vorhandener Ionen und funktionelle Gruppen mit Hilfe vieler „Schnelltests“ (Teststreifen oder nasschemische Nachweisreaktionen) in der Probe identifiziert. Von zentraler Bedeutung ist dabei neben diversen Messmethoden vor allem die Sinneswahrnehmung, während zur Konzentrationsanalytik und Strukturanalytik (in Forschung, Produktion (Analytik) und Chemieunterricht) Methoden der instrumentellen Analytik eingesetzt werden. Hierzu zählen z. B. instrumentelle Bestimmungsmethoden der Chromatographie, Spektrometrie, Photometrie, Osmometrie, Refraktometrie, Volumetrie, Gravimetrie und elektroanalytische Methoden.
Methodologie
Die Methoden umfassen Fällungsreaktionen, Redoxreaktionen, Verdrängungsreaktionen, Komplexbildungsreaktionen und Flammproben. Gegebenenfalls ist die Probe vor Durchführung der Nachweisreaktion aufzubereiten oder von störenden Begleitstoffen zu reinigen.
In der anorganisch-analytischen Chemie geschieht das qualitative Nachweisen von Stoffen in Stoffproben z. B. in Form der Durchführung des Kationentrennganges (vgl. unter Qualitative Analyse und im folgenden Artikelabschnitt).
Anwendungsgebiete und Geschichte
Quantitative Bestimmungen von Stoffen werden oft mit ähnlichen Nachweisreaktionen durchgeführt, zielen aber darauf ab, Gehaltsangaben für die zuvor qualitativ nachgewiesenen Stoffe zu ermitteln (vgl. unter: Quantitative Nachweise). Diese kommen oft nur in Spuren vor (<1 %), knapp oberhalb der Grenzkonzentration (GK) oder der Erfassungsgrenze (EG) der Nachweisreaktion, so dass physikalische Analysemethoden eingesetzt werden müssen (Gaschromatografie, Atomabsorptionsspektroskopie usw.). So lassen sich heutzutage auch Spurenstoffe im ppb-Bereich erfassen (1 ppb = 1:109; siehe unter: Quantitative Analyse, Instrumentelle Analytik, Analytische Chemie).
Qualitative sowie quantitative Nachweise auch von nur in Spuren vorhandenen Stoffen durchführen zu können, war früher von großer Bedeutung in der Chemie. Das Beispiel des Arsens zeigt diese Bedeutung im Hinblick auf die Kriminalistik: Die Marshsche Probe ist eine Nachweisreaktion in der Chemie und Gerichtsmedizin für Arsen, die 1832 von dem englischen Chemiker James Marsh entwickelt wurde. Vor der Entdeckung der Marshschen Probe war Arsen ein beliebtes Mordgift, da es sich nur schwer nachweisen ließ. Ein anderer Arsennachweis ist die Bettendorfsche Probe (über Zinn(II)-chlorid).
Durch die Instrumentelle Analytik und ihre Methoden wie z. B. die spektroskopischen Verfahren hat die Bedeutung von Nachweisreaktionen in der Analytik abgenommen. Für die Vermittlung fachspezifischer Inhalten und Methoden sind sie jedoch nach wie vor von didaktischer Bedeutung (vgl. unter: Chemieunterricht).
Nachweisreaktionen
Die Nachweisreaktion ist also vor allem eine Voruntersuchung zur quantitativen Bestimmung oder zur Strukturaufklärung. Sie hat in der Regel die Funktion eines Schnelltests, der gewisse Hinweise zur Probenbeschaffenheit liefert.
Nachweise von Ionen
%252C(III).JPG.webp)
Nachweisreaktionen für Ionen können in Form von Redoxreaktionen, Säure-Base-Reaktionen, Komplexbildungsreaktionen oder Fällungsreaktionen ablaufen.
Einige Salze sind z. B. nur sehr schlecht wasserlöslich. Dies nutzt man zum Nachweis von Ionen durch Ausfällung. Dazu mischt man sowohl eine wässrige Lösung der Untersuchungssubstanz (Probe, Analyt) als auch eine Referenzlösung (Probelösung) mit dem Nachweismittel. Die in der Vergleichslösung enthaltenen Ionen reagieren mit dem Nachweismittel, ebenso die gegebenenfalls in der Probelösung enthaltenen Ionen. Reagiert die Probelösung wie die Vergleichslösung, so ist der Nachweis positiv. So fallen z. B. Eisen-II-Kationen bei Zugabe einer wässrigen Lösung des roten Blutlaugensalzes als schwer wasserlösliches, intensiv blaues Salz aus.
Man unterscheidet vom Analyten her in der Anorganik:
Nachweise von Gasen
Nachweisreaktionen existieren nicht nur für Anionen und Kationen, sondern auch für Gase:
Wasserstoff
Für den Nachweis von Wasserstoff eignet sich die Knallgasprobe. Das unbekannte Gas wird entzündet. Vernimmt man hierbei einen Knall oder ein lautes Pfeifen, handelte es sich um Wasserstoff:
Sauerstoff
Sauerstoff kann mit der Glimmspanprobe nachgewiesen werden. Ein glimmender Holzspan glüht in einem Gasgemisch mit hohem Sauerstoffanteil deutlich auf.
Kohlenstoffdioxid
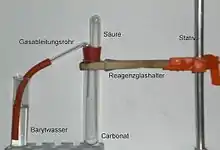
Für den Nachweis von Kohlenstoffdioxid verwendet man eine Calciumhydroxidlösung. Dazu leitet man das Gas in gesättigtes Kalkwasser oder Barytwasser und ein farbloser Feststoff (Calciumcarbonat) fällt aus, wenn Kohlenstoffdioxid enthalten ist.
oder :
Ammoniak
Für den Nachweis von Ammoniak verwendet man gasförmigen Chlorwasserstoff bzw. konzentrierte Salzsäure. Dabei entsteht Ammoniumchlorid, der als weißer auffälliger Nebel sichtbar wird.
Nachweise für Säuren und Basen

Ein Säure-Base-Indikator ist ein Stoff, der durch eine Farbveränderung pH-Wert-Änderungen durch Säuren oder Basen anzeigt. Am häufigsten werden Säure-Base-Indikatoren daher bei Titrationen verwendet (siehe unter Säure-Base-Titration).
Säuren und Basen enthalten in wässriger Lösung Oxonium- bzw. Hydroxidionen. Diese lassen sich beispielsweise mit Universalindikator nachweisen. Hierbei ändert der Indikator abhängig vom pH-Wert der Probesubstanz seine Farbe. Andere Säure-Base-Indikatoren sind zum Beispiel Phenolphthalein und Bromthymolblau.
Nachweis von Wasser
Wasser entsteht zum Beispiel als Kondensat gasförmigen Wasserdampfes oder als Reaktionsprodukt aus der Neutralisation von Säuren und Laugen. Man weist es mit wasserfreiem Kupfer(II)-sulfat nach: wasserfreies, weißes Kupfersulfat färbt sich bei Zugabe von Wasser hellblau. Es entsteht ein Kupferpentahydrat-Komplex, bei dem vier Wassermoleküle als Liganden des Zentralions auftreten:
Dabei handelt es sich um eine Komplexbildungsreaktion.
Ein weiterer sehr empfindlicher Wassernachweis auf der Grundlage von Komplexbildung ist die Rosafärbung von blauem (also wasserfreiem) Cobaltchlorid, dies wird zur Herstellung von Wasserteststreifen aus blauem Cobaltchloridpapier genutzt.
Siehe auch
Literatur
- Michael Wächter: Chemielabor. Verlag Wiley-VCH, Weinheim 2011, S. 215–241, ISBN 978-3-527-32996-0
- Gerhart Jander, E. Blasius: Einführung in das anorganisch-chemische Praktikum. S. Hirzel Verlag, Stuttgart 2005 (in 15. Aufl.), ISBN 3-7776-1364-9
- Gerhart Jander, E. Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie. S. Hirzel Verlag, Stuttgart 2002 (in 15. Aufl.), ISBN 3-7776-1146-8
- Michael Wächter: Stoffe, Teilchen, Reaktionen. Verlag Handwerk und Technik, Hamburg 2000, S. 154–169, ISBN 3-582-01235-2
- Bertram Schmidkonz: Praktikum Anorganische Analyse. Verlag Harri Deutsch, Frankfurt 2002, ISBN 3-8171-1671-3
- Eberhard Gerdes: Qualitative Anorganische Analyse. Ein Begleiter für Theorie und Praxis. Springer, Berlin 2001 (2. Aufl.), ISBN 3-540-67875-1
- Thomas Bitter (Redaktion): Elemente Chemie I – Unterrichtswerk für Gymnasium. Ernst Klett Schulbuchverlag GmbH, Stuttgart 1986 (1. Aufl.), ISBN 3-12-759400-3