Tributylzinnchlorid
Tributylzinnchlorid (kurz TBTC) ist eine metallorganische Verbindung des Zinns. TBTC ist bei Raumtemperatur eine farblose bis gelbliche, nahezu wasserunlösliche giftige Flüssigkeit. Die toxische Wirkung beruht auf der Inhibierung von V-ATPasen durch zinnorganische Verbindungen.[7]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
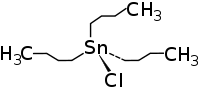 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tributylzinnchlorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C12H27ClSn | ||||||||||||||||||
| Kurzbeschreibung |
farblose bis gelbliche Flüssigkeit [1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 325,49 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,20 g·cm−3 (20 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser (17 mg·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
Zur Darstellung werden Zinntetrachlorid SnCl4 und Tri-n-butylaluminium nBu3Al umgesetzt:
Durch partielle Hydrolyse mit Wasser und einer Base wie Pyridin oder Triethylamin kann aus dem Tributylzinnchlorid Bis(tributylzinn)oxid hergestellt werden.
Eigenschaften
TBTC ist eine farblose, oft durch Verunreinigungen gelblich gefärbte Flüssigkeit, die sich nur geringfügig (17 mg·l−1 bei 20 °C [1]) in Wasser löst. Die Verbindung ist weitgehend stabil gegenüber hydrolytischen und oxidativen Einflüssen. Es hat in Benzol ein Dipolmoment von 3,31 Debye.[8]
Verwendung
Tributylzinnverbindungen wie TBTC, Tributylzinnhydrid (TBT) und Bis(tributylzinn)oxid (TBTO) und andere Zinnorganische Verbindungen werden als Desinfektionsmittel gegen Befall mit Pilzen und Milben bei Textilien, Leder, Papier und Holz sowie als Saatbeizmittel verwendet. Auch bei Schiffsanstrichen werden sie zugesetzt, um in Antifoulingfarben Algen und Schnecken zu bekämpfen.[9] In Deutschland und der EU wird auf den Einsatz zinnorganischer Verbindungen weitgehend verzichtet. Teilweise gilt ein Verwendungsverbot.
Weitere wichtige Verwendungen von Tributylzinnchlorid sind der Einsatz bei Synthesen in der Pharmachemie und als Zusatz zu Styrol-Butadien-Kautschuk zur Verminderung des Reibungswiderstands von Autoreifen. In beiden Fällen gelangen keine zinnorganischen Verbindungen in die Umwelt, weshalb der Einsatz erlaubt bleibt.[10]
Toxikologie
Wegen des geringen Dampfdrucks der Flüssigkeit ist eine Aufnahme über die Atemwege unwahrscheinlich; die dermale und orale Resorption ist jedoch hoch. Die Toxizität gegenüber Säugetieren liegt bei LD50 (oral – Ratte) = 220 mg·kg−1.[11] Auf Schleimhäute und Haut wirkt die Substanz stark reizend bis ätzend und erzeugte im Tierversuch Nekrosen, ein reduziertes Körpergewicht, Dämpfung der Reflexe, Entkräftung und Krämpfe.[1] Auf Wasserlebewesen besitzt Tributylzinnchlorid eine sehr hohe Toxizität. Bei Schnecken bewirken Zinnorganika das Imposex-Phänomen, wobei die Purpurschnecke (Haustellum brandaris) schon ab einer Konzentration von 1,2 ng/l Auswirkungen zeigte.[10]
Einzelnachweise
- Eintrag zu Tributylzinnchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Tributylzinnverbindungen, soweit in diesem Anhang nicht gesondert aufgeführt im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Nippon Eiseigaku Zasshi. Japanese Journal of Hygiene. Vol. 46, Pg. 297, 1991.
- Eintrag zu Tributylchlorostannane in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 17. August 2021.
- Yakkyoku. Pharmacy. Vol. 30, Pg. 505, 1979.
- Prehled Prumyslove Toxikologie; Organicke Latky. Marhold, J., Prague, Czechoslovakia, Avicenum, Pg. 1250, 1986.
- Wissenschaft-Online-Lexika: Eintrag zu V-ATPasen im Lexikon der Biochemie. Abgerufen am 15. September 2009
- Jörg Lorberth, Heinrich Nöth: Dipolmomente einiger Organozinnchloride. In: Chemische Berichte. Band 98, Nr. 3, März 1965, S. 969, doi:10.1002/cber.19650980342.
- Eintrag zu Tributylzinn-Verbindungen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 21. November 2021.
- Dietrich Klingmüller, Burkard Watermann (Hrsg.): TBT - Zinnorganische Verbindungen - eine wissenschaftliche Bestandsaufnahme (PDF; 2,1 MB). Umweltbundesamt Berlin, März 2003, ISSN 0722-186X
- Bernard Jousseaume: Organometallic Synthesis and Chemistry of Tin and Lead Compounds. In: Mikrochimica acta. Band 109, Nr. 1–4, 1992, S. 5–12, doi:10.1007/BF01243203 (englisch).


