Zinn(IV)-bromid
Zinn(IV)-bromid ist eine anorganische chemische Verbindung des Zinns aus der Gruppe der Bromide.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
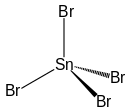 | |||||||||||||||||||
| Keile zur Verdeutlichung der räumlichen Struktur | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Zinn(IV)-bromid | ||||||||||||||||||
| Andere Namen |
Zinntetrabromid | ||||||||||||||||||
| Summenformel | SnBr4 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 438,33 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
3,34 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
202 °C[1] | ||||||||||||||||||
| Löslichkeit |
leicht löslich in Wasser[2] | ||||||||||||||||||
| Brechungsindex |
1,6628 (31 °C)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
Zinn(IV)-bromid-tetrahydrat kann durch Reaktion von Zinn(IV)-oxid mit Bromwasserstoffsäure gewonnen werden. Das Anhydrat kann durch Reaktion der Elemente gewonnen werden.[4]
Eigenschaften
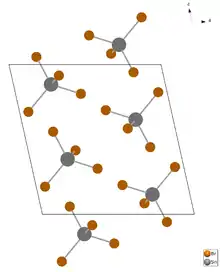
Zinn(IV)-bromid ist ein farbloser, an Luft rauchender Feststoff, der leicht löslich in Wasser ist.[2] Es besitzt eine monokline Kristallstruktur mit der Raumgruppe P21/c (Raumgruppen-Nr. 14), a = 1037,1 pm, b = 700,6 pm, c = 1047,0 pm, β = 102,56°, Z = 4.[5][6]
Verwendung
Zinn(IV)-bromid wird als Ausgangsmaterial für Zinn(IV)-oxid durch laserunterstützte chemische Gasphasenabscheidung (engl. laser-assisted CVD) verwendet und besitzt dabei eine höhere Effizienz als andere Ausgangsstoffe wie zum Beispiel Dibutylzinndiacetat.[1] Er wird auch zur Trennung von Mineralien verwendet.[2]
Einzelnachweise
- Datenblatt Tin(IV) bromide, 99.999% trace metals basis bei Sigma-Aldrich, abgerufen am 23. Juli 2013 (PDF).
- Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. Taylor & Francis, 2011, ISBN 1-4398-1462-7, S. 483 (eingeschränkte Vorschau in der Google-Buchsuche).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Index of Refraction of Inorganic Liquids, S. 4-140.
- Anil Kumar De: A Text Book of Inorganic Chemistry. New Age International, 2007, ISBN 81-224-1384-6, S. 379 (eingeschränkte Vorschau in der Google-Buchsuche).
- Roger Blachnik (Hrsg.): Taschenbuch für Chemiker und Physiker. Band III: Elemente, anorganische Verbindungen und Materialien, Minerale. begründet von Jean d’Ans, Ellen Lax. 4., neubearbeitete und revidierte Auflage. Springer, Berlin 1998, ISBN 3-540-60035-3, S. 1389 (eingeschränkte Vorschau in der Google-Buchsuche).
- H. Reuter, R. Pawlak: Zinnhalogenverbindungen. II. Die Molekül- und Kristallstrukturen von Zinn(IV)-bromid und -iodid. In: Zeitschrift für Kristallographie. 216, 2001, S. 34–38, doi:10.1524/zkri.216.1.34.18992.

