Indiumnitrid
Indiumnitrid (InN) ist eine anorganische chemische Verbindung des Indiums aus der Gruppe der Nitride.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
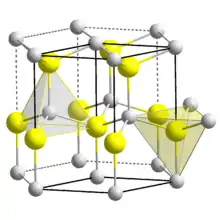 | ||||||||||||||||
| _ In3+ _ N3− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Indiumnitrid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | InN | |||||||||||||||
| Kurzbeschreibung |
schwarzer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 128,83 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Dichte |
6,89 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt |
1100 °C[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Indiumnitrid kann durch Reaktion von Ammoniumhexafluoroindat mit Ammoniak bei 580 bis 600 °C gewonnen werden.[1]
Eigenschaften
Indiumnitrid ist ein schwarzer, luftbeständiger Feststoff. Er wird von Natronlauge und von konzentrierter Schwefelsäure aufgelöst, von den anderen Mineralsäuren dagegen nicht. Er besitzt eine Kristallstruktur vom Wurtzit-Typ (a = 353,3 pm, c = 569,3 pm).[1] Die Verbindung ist ein III-V-Verbindungshalbleiter, der aus Indium und Stickstoff gebildet ist. Potenzielle zukünftige Anwendungen dieses Werkstoffes liegen in Kombinationen mit Galliumnitrid im Bereich von Solarzellen.[4]
Der temperaturabhängige Bandabstand von InN beträgt bei 300 K ca. 0,7 eV und liegt im infraroten Spektralbereich.[5][6] Indiumnitrid bildet mit Galliumnitrid den ternären Verbindungshalbleiter Indiumgalliumnitrid, dessen Bandlücke im Herstellungsprozess durch das Verhältnis der beiden Komponenten über einen sehr weiten Bereich von 0,7 bis 3,4 eV wählbar ist.
Dünne polykristalline Strukturen von Indiumnitrid zeigen bei Temperaturen unter Tc=3,3 K supraleitende Eigenschaften, die auch unter dem Einfluss von hohen magnetischen Flussdichten bestehen bleiben.[7]
Literatur
- Timothy David Veal, Christopher F. McConville, William J. Schaff: Indium Nitride and Related Alloys. CRC Press, 2011, ISBN 1-4398-5961-2 (eingeschränkte Vorschau in der Google-Buchsuche).
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 872.
- Datenblatt Indium(III) nitride, 99.9% trace metals basis bei Sigma-Aldrich, abgerufen am 29. März 2014 (PDF).
- William M. Haynes: CRC Handbook of Chemistry and Physics, 93rd Edition. CRC Press, 2012, ISBN 1-4398-8049-2, S. 4–67 (eingeschränkte Vorschau in der Google-Buchsuche).
- T. D. Veal, C. F. McConville, and W. J. Schaff (Eds), Indium Nitride and Related Alloys (CRC Press, 2009)
- V. Yu. Davydov: Absorption and Emission of Hexagonal InN. Evidence of Narrow Fundamental Band Gap (PDF; 86 kB), Phys. Stat. Solidi (b) 229 (2002) R1 (engl.)
- EL-ELA, FMABOU and EL-ASSY, BM: Electron transport in wurtzite InN. In: Pramana. Band 79, 2012, S. 125, doi:10.1007/s12043-012-0294-5.
- T. Inushima: Electronic structure of superconducting InN, in Sci. Techn. Adv. Mater. 7, 2006, Seiten 112; doi:10.1016/j.stam.2006.05.009.