Nuklearmedizin
Nuklearmedizin ist die Anwendung von offenen Radionukliden zu diagnostischen und therapeutischen Zwecken.[1] Sie umfasst zudem die Anwendung weiterer radioaktiver Substanzen und kernphysikalischer Verfahren zur Funktions- und Lokalisationsdiagnostik und den Strahlenschutz mit seinen physikalischen, biologischen und medizinischen Grundlagen.
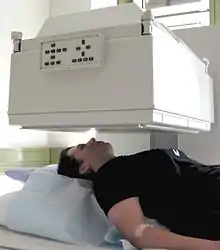
„In-vivo“-Verfahren
In-vivo-Verfahren sind Messverfahren, bei denen ein Radiopharmakon („Tracer“) in den Körper eingebracht wird, dessen Gammastrahlung oder Vernichtungsstrahlung von außerhalb des Körpers sehr genau gemessen werden kann. (Zusätzliche Information über Organfunktionen liefern fallweise auch Radioaktivitätsmessungen von Blutproben oder Ausscheidungen.)
Ein Radiopharmakon ist ein Radionuklid oder die chemische Verbindung eines Radionuklids mit anderen Stoffen. Wie ein Radiopharmakon in der Nuklearmedizin verwendet wird, hängt wesentlich von zwei Eigenschaften ab:
- Radioaktivität (Zerfallsverhalten und entstehende Strahlung)
- Pharmakokinetik (Verteilung im Organismus, Teilnahme an Körperfunktionen, Eliminierung).
Diagnostik
Die bildgebenden Verfahren Szintigrafie, Positronen-Emissions-Tomographie (PET) und SPECT (single photon emission computed tomography) bilden nach dem Tracer-Prinzip vorwiegend die Funktion eines Organs oder Organsystems ab, im Gegensatz zu den morphologischen bildgebenden Verfahren, die hauptsächlich die Struktur zeigen. Zum Beispiel verwendet man in der Skelettszintigrafie ein Radiopharmakon (99mTechnetium-Methylendiphosphonat), das bevorzugt von knochenbildenden Zellen (Osteoblasten) aufgenommen wird. Normales Knochengewebe zeigt im resultierenden Szintigramm niedrige Aktivität, die von physiologischen Umbauprozessen herrührt. Zonen erhöhter Aktivität lassen dagegen auf verstärkten Knochenumbau und damit auf krankhafte Vorgänge schließen, die an den entsprechenden Stellen im Skelett ablaufen. Dabei kann es sich um Kontusionen, heilende Frakturen, Krebs, gutartige Knochentumore, Arthrosen oder Knochenentzündungen handeln.
Dynamische Untersuchungen sind ein weiteres Beispiel für den funktionellen Charakter der Nuklearmedizin. Etwa wird bei der Nierenfunktionsszintigrafie eine Reihe von Bildern in Intervallen zwischen einer und 60 Sekunden über einen Zeitraum von 20 bis 40 Minuten aufgezeichnet. So lässt sich die Anreicherung und Ausscheidung des Radiopharmakons in verschiedenen Organen als Kurven aufzeichnen. Dies ermöglicht zum Beispiel die Beurteilung der Ausscheidungsleistung einer Niere im Verhältnis zur anderen.
Ebenfalls zum Gebiet der Nuklearmedizin gehören Nachweis und medizinische Beurteilung von Radioaktivität, die bei Strahlenunfällen in den Körper gelangt ist oder des natürlichen Kalium-40, das der Muskelmasse proportional ist. Dafür stehen nicht-bildgebende Messmethoden (Szintillationsdetektor, Halbleiterdetektor, Ganzkörperzähler und Ausscheidungsmessungen) zur Verfügung.
Die häufigsten nuklearmedizinischen Untersuchungsverfahren sind die Schilddrüsenszintigrafie, Skelettszintigrafie, Myokardszintigrafie, Nierenfunktionsszintigrafie und Lungenszintigrafie sowie die Positronen-Emissions-Tomografie. Für viele weitere physiologische Vorgänge existieren nuklearmedizinische Untersuchungen.
Als von ionisierenden Strahlen unabhängige Untersuchungsmethoden, die kernphysikalische Effekte ausnutzen, um Bilder vom Inneren des Körpers zu erzeugen und die Zusammensetzung von Geweben zu analysieren, stehen die Magnetresonanztomographie (auch Kernspintomographie genannt) und die Magnetresonanzspektroskopie zur Verfügung. Deren Aussagemöglichkeiten liegen aber nicht so ausgeprägt auf funktionellem Gebiet wie die der klassischen Nuklearmedizin, sondern mehr auf anatomischem, wobei vornehmlich der Wasserstoffgehalt von Geweben zusätzliche, eben funktionelle, Aufschlüsse gibt. Diese Methode wird von dazu berechtigten Radiologen und seltener auch Nuklearmedizinern ausgeübt.
Da nuklearmedizinische Untersuchungen oft zu anatomisch nicht eindeutigen Befunden führen (d. h., der Untersucher sieht zwar eine Abweichung von der Norm, kann sie aber nicht genau einer speziellen Körperstruktur, etwa einer Lymphknotengruppe, zuordnen) werden seit etwa dem Jahr 2000 mehr und mehr Kombinationsgeräte angeboten und aufgestellt, bei denen eine nuklearmedizinische Gammakamera oder ein PET-Scanner mit einem mechanisch fest verbundenen Computertomographen kombiniert wird. Dabei können in einem Gang ohne Umlagerung sowohl funktionelle, als auch anatomische Daten erhoben werden und in einem Bildersatz fusioniert werden. Dies verbessert die Anschaulichkeit und in verschiedenen kritischen Fällen auch die Richtigkeit der Diagnose. Solche Geräte nennt man SPECT-CT beziehungsweise PET-CT; an vollintegrierten Lösungen wird gearbeitet, auch gibt es heute (2012) erste – noch überwiegend in der Forschung eingesetzte – PET-MRT-Geräte. Der klinische Wert der PET-MRT ist noch nicht zu beurteilen.
Therapie
In der nuklearmedizinischen Therapie werden Radiopharmaka eingesetzt, die Beta- oder seltener Alphastrahlung abgeben. Diese Strahlungsarten zeichnen sich durch eine geringe Durchdringungstiefe (wenige Millimeter bei Betastrahlung, einige µm bei Alphastrahlung) aus. Dadurch entfalten sie ihre Wirkung am Ort der Anreicherung im Organismus. Die Kinetik des Radiopharmakons bestimmt, wo diese Anreicherung stattfindet. So zielt beispielsweise die Radiojodtherapie auf die Schilddrüse. Das Radiopharmakon wird vorzugsweise von hormonproduzierenden Follikelzellen aufgenommen und zerstört lokal überschüssiges oder bösartiges Gewebe (siehe auch Hyperthyreose, Schilddrüsenkarzinom). Radiojod wird gewöhnlich in Form einer Therapiekapsel oral verabreicht.
Eine weitere Möglichkeit besteht in der Verabreichung künstlich hergestellter, mit einem geeigneten Radionuklid versehener monoklonaler Antikörper oder Peptide (kleine Eiweißmoleküle). Ein solches Radiopharmakon kann intravenös injiziert werden und findet „von selbst“ sein Zielorgan.
Wenn das Zielorgan räumlich gut abgegrenzt und zugänglich ist, bietet sich die direkte Einbringung des therapeutischen Radionuklids an (Endoradiotherapie). Ein solches Verfahren ist die Radiosynoviorthese, die zunehmend bei der chronischen Polyarthritis, aktivierten Arthrose oder anderen Gelenkerkrankungen durchgeführt wird. Dabei wird Yttrium-90 oder ein anderer Betastrahler in den Gelenkspalt injiziert, um die Gelenkinnenhaut zu veröden. Als nicht invasive Anwendung gilt die epidermale Radioisotopentherapie, welche bei der Behandlung von Basaliomen oder Spinaliomen der Haut zum Einsatz kommt. Dabei wird Rhenium-188, ein Betastrahler, direkt auf einer Folie über der zu behandelnden Läsion aufgebracht.[2]
Die Anwendung der Gammastrahlung aus umschlossenen radioaktiven Substanzen, die Brachytherapie, wird nicht zu den nuklearmedizinischen Verfahren gezählt.
„In-vitro“-Verfahren
Als In-vitro-Verfahren werden Labormethoden wie der Radioimmunoassay (RIA) bezeichnet. Bei diesen Verfahren können Substanzkonzentration in aus dem Körper gewonnenem Probenmaterial mittels immunologischer Reaktionen besonders genau bestimmt werden, da ein Reaktionspartner zuvor radioaktiv markiert wurde.
Der Facharzt für Nuklearmedizin
Um nach einem absolvierten Medizinstudium in Deutschland als Facharzt für Nuklearmedizin tätig zu werden, bedarf es einer fünfjährigen Weiterbildung,
- davon ein Jahr in der stationären Patientenversorgung,
- wovon 6 Monate in einem anderen Gebiet abgeleistet werden können
- ein Jahr in der Radiologie kann angerechnet werden.
Die Weiterbildungsordnung schreibt bestimmte Mindestzahlen für Untersuchungen und Therapien vor. Vor der Facharztprüfung müssen außerdem noch spezielle Kurse im Strahlenschutz absolviert werden.
Literatur
- H. Götte, G. Kloss: Nuklearmedizin und Radiochemie. In: Angew. Chem., 85. Jahrg., Nr. 18, 1973, S. 793.
- Michael Feld: Nuklearmedizin. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. de Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 1058–1060.
Weblinks
- Deutsche Gesellschaft für Nuklearmedizin e. V.
- Österreichische Gesellschaft für Nuklearmedizin
- Schweizerische Gesellschaft für Nuklearmedizin
- Nuclear Medicine Information (englisch)
- Muster-Weiterbildungsordnung 2003 (in der Fassung vom 25. Juni 2010). (Memento vom 21. Januar 2012 im Internet Archive; PDF, 742 kB) bei der deutschen Bundesärztekammer
Einzelnachweise
- Erich Oberhausen u. a.: Technik der Nuklearmedizin. 4. Auflage. Deutscher Ärzte-Verlag, Köln 1990, ISBN 3-7691-1089-7, S. 9.
- Paolo Castellucci, F. Savoia, A. Farina, G. M. Lima, A. Patrizi: High dose brachytherapy with non sealed 188Re (rhenium) resin in patients with non-melanoma skin cancers (NMSCs): single center preliminary results. In: European Journal of Nuclear Medicine and Molecular Imaging. 2. November 2020, ISSN 1619-7089, doi:10.1007/s00259-020-05088-z.