Suspension (Chemie)
Eine Suspension (lateinisch suspendere ‚aufhängen‘, ‚in der Schwebe lassen‘) ist ein heterogenes Stoffgemisch aus einer Flüssigkeit und darin fein verteilten Festkörpern (Partikeln). Eine Suspension ist eine grobdisperse Dispersion und tendiert zur Sedimentation und Phasentrennung. Die Feststoffe sind in der flüssigen Phase „suspendiert“.

Suspensionen in Wasser bezeichnet man in der Materialwissenschaft oder bei natürlichen Vorkommen auch als Aufschlämmung oder (aus dem Englischen) Slurry. Sie werden unterteilt in „grobe“ Suspensionen (Teilchengröße 0,1 mm bis 1 mm, z. B. Kreideschlamm) und „feine“ Suspensionen (Teilchengröße 1 µm bis 100 µm, z. B. Kalkmilch). Noch feiner dispergierte Teilchen (kleiner als 1 µm) sind Dispersionen, kleiner 1 nm Molekulardispersionen.[1]
Suspensionen oder Dispersionen in der Polymerchemie sind feinstdispergierte Polymerprodukte, die durch Suspensionspolymerisation gewonnen werden, beispielsweise Polyacrylate oder Vinylacetate.
Sedimentation
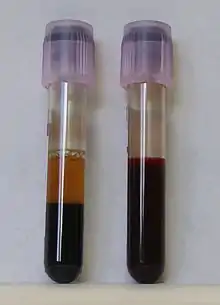
Lässt man eine Suspension stehen, so sinkt (im Gegensatz zu einer Lösung) ein Feststoff mit größerer Dichte als die reine Flüssigkeit bei nicht zu kleiner Partikelgröße langsam auf den Boden und bildet ein Sediment (Sedimentation). Die überstehende Flüssigkeit kann abgegossen (dekantiert) und somit der Feststoff (Sediment) von der Flüssigkeit (Dekantat) getrennt werden. Durch die Zugabe von sogenannten Thixotropiermitteln oder grenzflächenaktiven Substanzen kann die Sedimentation verlangsamt, durch Zugabe von Flockungsmitteln beschleunigt werden.
Die Stabilität einer Suspension kann mit einem Sedigraphen definiert werden. Dieser misst nach dem Gesetz von Stokes die Sinkgeschwindigkeit unterschiedlicher Teilchen.
Je kleiner ein Partikel ist, je geringer seine Dichte und je höher die Viskosität der Flüssigkeit ist, desto langsamer geht die Sedimentation vonstatten. Auch Form und Struktur der Partikel und andere Eigenschaften von Partikel und Flüssigkeit beeinflussen die Sedimentation.
Die Sedimentation lässt sich durch Zentrifugieren beschleunigen.
Eine Methode zur Ermittlung der Stoffeigenschaften oder der Partikelgröße und deren Verteilung ist die Ultraschalldämpfungsspektroskopie.
Beispiele
Beispiele für Suspensionen sind:
- Aufschlämmungen von Sand in Meerwasser, Schwebstoffe, oder Treibsand
- Mörtel oder Beton (mineralische Suspensionen)
- Suspensionen aus Siliciumcarbid und Polyethylenglycol, die gleichzeitig abrasiv und kühlend wirken, werden in der Photovoltaik-Industrie und in der Halbleiter-Industrie dazu verwendet, um Reinsilizium zu Wafern zu zerschneiden.[2]
- Deckfarbe, Anstrichmittel (Pigmentsuspensionen, in Unterscheidung zu Farbstoffen, die in Lösung gehen)
- Blut
- die lichtempfindliche fotografische Schicht auf Film oder Fotopapier. Sie wird in der Fachsprache (fälschlicherweise) als „Emulsion“ bezeichnet, da ursprünglich eine Silbernitratlösung und Kaliumbromidlösung in flüssiger Gelatine emulgiert auf Glasplatten oder Fotopapier aufgetragen wurde; Silbernitrat und Kaliumbromid reagieren dabei aber zu wasserunlöslichem lichtempfindlichen Silberbromid, was im Flüssig- und Gelzustand eine Suspension in Gelatine ergibt.
- Pollen in wässrigen Honiglösungen, die für die mikroskopische Palynologie hergestellt werden
- Hefeweizenbier
- Orangensaft
- Bohrspülung
Der flüssige Anteil der Suspension ist oft kein Reinstoff, sondern seinerseits ein Gemisch: Die Trägerflüssigkeit kann auch eine Lösung, eine Emulsion oder eine unsedimentierte Dispersion sein. Beispiel: Bei gezuckertem Milchkakao sind Partikel von Kakaobestandteilen in einer Flüssigkeit suspendiert, die eine wässrige Zuckerlösung und zugleich eine wässrige Fettemulsion ist. Ein gezuckertes Kakaogetränk ist deshalb eine „Dispersion in einer Zuckerlösung“.
Kuhmilch ist eine Dispersion von Milchfett und Eiweiß in Wasser. Auch andere Suspensionen, die „milchig“ aussehen, werden als „-milch“ bezeichnet, beispielsweise
- Gletschermilch, eine Aufschlämmung von Gesteinsabrieb in Gletscherwasser,
- Kalkmilch, eine Aufschlämmung von Löschkalk in Wasser,
- Scheuermilch, mehlfeine Scheuermittel in Tensidlösungen oder Lösungsmitteln eingemischt.
Suspensionen als pharmazeutische Formulierung
Für medizinische Suspensionen werden unlösliche Pulver wie Arzneistoffe in Trägerflüssigkeiten dispergiert. Die Nichtmischbarkeit der Bestandteile kann, anders als bei einer echten Lösung, zur Entmischung durch Absinken der Festteilchen infolge der Gravitation führen. Suspensionen sind daher makroskopisch gesehen nur dann homogen, wenn sie leicht und rasch aufschüttelbar sind.
Suspensionen sind für viele Anwendungsarten möglich: äußerlich (beispielsweise auf der Haut, am Auge), innerlich (zum Einnehmen), zum Einbringen in Körperöffnungen oder auch parenteral (etwa intramuskulär).
Einteilung im Schema der chemischen Stoffe
| Schematische Einteilung der Stoffe | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Siehe auch
Einzelnachweise
- Gerhart Jander, Ewald Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie. Mit Ausnahme der quantitativen Analyse. 12. Auflage. 1983, ISBN 3-7776-0439-9, S. 91.
- Nutzung von gebrauchtem Slurry beim Drahtsägen ohne Wiederaufarbeitung..