Kryolith
Kryolith ist ein eher selten vorkommendes Mineral aus der Mineralklasse der Halogenide mit der idealisierten chemischen Zusammensetzung Na2NaAlF6 und damit Natriumhexafluoroaluminat(III).
| Kryolith | |
|---|---|
 | |
| Allgemeines und Klassifikation | |
| Andere Namen | |
| Chemische Formel | |
| Mineralklasse (und ggf. Abteilung) |
Halogenide |
| System-Nr. nach Strunz und nach Dana |
3.CB.15 (8. Auflage: III/B.03) 11.06.01.01 |
| Ähnliche Minerale | Anhydrit, Fluorit, Halit[7] |
| Kristallographische Daten | |
| Kristallsystem | monoklin |
| Kristallklasse; Symbol | monoklin-prismatisch; 2/m |
| Raumgruppe | P21/n (Nr. 14, Stellung 2)[8][5] |
| Gitterparameter | a = 5,4024 Å; b = 5,5959 Å; c = 7,7564 Å β = 90,278°[8] |
| Formeleinheiten | Z = 2[8] |
| Häufige Kristallflächen | {100}, {010}, {001}, {101}, {101}, {011}, {110}, {111}, {112} |
| Zwillingsbildung | häufig, Durchdringungs-, Wiederholungs- und polysynthetische Zwillinge[9] |
| Physikalische Eigenschaften | |
| Mohshärte | 2,5 bis 3[10]; Vickershärte VHN50=286-412 kg/mm² |
| Dichte (g/cm3) | gemessen: 2,96 bis 2,98[11]; berechnet: 2,973[9] |
| Spaltbarkeit | keine; Absonderungen nach {001} und {110}[12] |
| Bruch; Tenazität | muschelig[10] bis uneben[12]; spröde[12] |
| Farbe | wasserklar-farblos bis weißlich und schneeweiß, auch rötlich, ziegelrot, bräunlich, grau, schwarz[10][9] |
| Strichfarbe | weiß[12] |
| Transparenz | durchsichtig bis durchscheinend[10] |
| Glanz | feuchter Glasglanz bis Fettglanz, Perlmuttglanz auf {001}[10] |
| Kristalloptik | |
| Brechungsindizes | nα = 1,339[11] nβ = 1,339[11] nγ = 1,340[11] |
| Doppelbrechung | δ = 0,001[11] |
| Optischer Charakter | zweiachsig positiv[11] |
| Achsenwinkel | 2V = 43°[11] |
| Pleochroismus | keiner |
| Weitere Eigenschaften | |
| Chemisches Verhalten | schon in der Kerzenflamme schmelzbar (Schmelzpunkt: 1012 °C.)[13]; in konzentrierter H2SO4 löslich; wird bereits von atmosphärischer Feuchtigkeit angelöst[10] |
| Besondere Merkmale | schwache Thermolumineszenz; intensive gelbe Fluoreszenz im kurzwelligen UV-Licht mit gelber Phosphoreszenz[9] |
Kryolith kristallisiert im monoklinen Kristallsystem und entwickelt entweder pseudokubische Kristalle oder massige Aggregate von weißer, brauner, grauer, braun-schwarzer oder rötlicher Farbe. Das Mineral bildet sich typischerweise im Pegmatitstadium und findet sich in Granit-Pegmatiten und in der Grundmasse einiger fluorreicher, topashaltiger Rhyolithe. Es wird unter anderem von Aegirin, Chabasit, Eudialyt, Fluorit, Kryolithionit, Mikroklin, Natrolith, Pachnolith, Phenakit, Quarz, Siderit, Sodalith, Sphalerit, Thomsenolith, Topas, Villiaumit und Weberit begleitet.
Die Typlokalität des Kryoliths ist der extrem fluorreiche Granit-Pegmatit der Ivigtut Mine (Koordinaten der Kryolith-Lagerstätte Ivigtut) bei der wüstgefallenen Siedlung Ivittuut (nach alter Rechtschreibung Ivigtût, auch Ivigtut) am Südufer des Ilorput (Arsukfjords) im Distrikt Ivittuut in der Kommuneqarfik Sermersooq im autonomen Teil Grönland des Königreichs Dänemark. Sie war der einzige Ort weltweit, wo das Mineral Kryolith lagerstättenbildend auftrat und gewinnbringend abgebaut wurde.
Etymologie und Geschichte


Das Mineral war den Grönländern bereits zu Beginn des 18. Jahrhunderts bekannt. Sie beschwerten damit ihre Zelte und Fischernetze und mischten es in pulverisierter Form ihrem Schnupftabak bei.[14] Erste Proben des Minerals kamen durch Missionare und/oder Grönlandfahrer nach Dänemark, wo sie 1795 erstmals vom Militärchirurgen und Assistenzprofessor einer naturforschenden Gesellschaft zu Kopenhagen Heinrich Christian Friedrich Schumacher – allerdings irrtümlich als Schwerspat – beschrieben wurde.[14] Als Typpublikation gilt die kurze Notiz von Peter Christian Abildgaard (1740–1801) im von Alexander Nicolaus Scherer herausgegebenen Allgemeinen Journal der Chemie von 1799:
„In der ordentlichen Versammlung der königl. Gesellschaft der Wissenschaften am 1. Februar dieses Jahres stattete Hr. Prof. Abildgaard einen Bericht […] ab. Zugleich theilte er auch eine Nachricht von einer vor wenigen Jahren aus Grönland nach Dänemark gebrachten besonders weißen spatartigen Miner mit. Einer damit angestellten Untersuchung zu folge bestand sie aus Thonerde und Flußspathsäure. Eine Verbindung, von welcher noch kein ähnliches Beyspiel im Mineralreich vorgekommen ist. Sie hat den Namen Chryolith erhalten, weil sie vor dem Löthrohre wie gefrorne Salzlauge schmilzt.“
Ein Jahr später erschien eine Übersetzung ins Französische im französischen Wissenschaftsmagazin Annales de Chimie.[15]
Abildgaard benannte das Mineral aufgrund seiner leichten Schmelzbarkeit nach altgriechisch κρύος krýos, deutsch ‚Frost, Kälte‘, und altgriechisch λίθος líthos, deutsch ‚Stein‘, als Kryolith. Der deutsche Trivialname „Eis-Stein“ – entstanden aufgrund des charakteristischen Aussehens wie massiges Eis – ist einer Fehlübersetzung des griechischen Wortes κρύος geschuldet, welches nicht „Eis“, sondern „Frost“ bedeutet. Das griechische Wort für Eis ist κρύσταλλος krýstallos.[10] Die Grönländer aus Ivittuut und Umgebung bezeichneten das Mineral als Orsugisat – aufgrund seiner äußerlichen Ähnlichkeit mit Seehundspeck, dessen Name „Orsok“ lautet.[3]
Es ist kein (Typ)-Material erhalten geblieben, welches in Zusammenhang mit den ersten Untersuchungen und Beschreibungen steht. Verschiedene Quellen[11][9] geben an, dass sich das Typmaterial für Kryolith in der Universität Kopenhagen in Kopenhagen in Dänemark befindet. Der Typmineralkatalog der International Mineralogical Association (IMA) verweist allerdings darauf, dass das Typmaterial (Cotypen) für Kryolith in der Sammlung des Muséum national d’histoire naturelle (deutsch Nationales Naturkundemuseum) in Paris in Frankreich und dort in der Galerie Nationale de Minéralogie et de Géologie aufbewahrt wird, wobei keine Katalognummern angegeben sind.[16] Aufgrund der Entdeckung und Erstbeschreibung vor 1959 (vor über 220 Jahren) zählt der Kryolith zu den anerkannten Mineralen mit Bestandsschutz, die von der IMA als Grandfathered bezeichnet werden[16][4] und keine eigentliche IMA-Nummer besitzen.
Klassifikation
Bereits in der veralteten 8. Auflage der Mineralsystematik nach Strunz gehörte der Kryolith zur Mineralklasse der „Halogenide“ und dort zur Abteilung der „Doppelhalogenide“, wo er zusammen mit Elpasolith die „Kryolith-Elpasolith-Gruppe“ mit der System-Nr. III/B.03 und den weiteren Mitgliedern Chukhrovit, Creedit, Gearksutit, Jarlit, Kryolithionit, Tikhonenkovit, Usovit und Yaroslavit sowie dem 2006 diskreditierten Boldyrevit bildete.
Im zuletzt 2018 überarbeiteten und aktualisierten Lapis-Mineralienverzeichnis nach Stefan Weiß, das sich aus Rücksicht auf private Sammler und institutionelle Sammlungen noch nach dieser alten Form der Systematik von Karl Hugo Strunz richtet, erhielt das Mineral die System- und Mineral-Nr. III/B.03-30. In der „Lapis-Systematik“ entspricht dies ebenfalls der Abteilung „Doppelhalogenide“, wobei in den Gruppen III/B.01 bis 03 die Doppelhalogenide mit [BF4]1−, [SiF6]2− und [AlF6]3− eingeordnet sind. Kryolith bildet hier zusammen mit Bøgvadit, Calcjarlit, Colquiriit, Elpasolith, Fluornatrocoulsellit, Jarlit, Jørgensenit, Kryolithionit und Simmonsit eine eigenständige, aber unbenannte Gruppe.[6]
Die seit 2001 gültige und von der IMA verwendete 9. Auflage der Strunz’schen Mineralsystematik ordnet den Kryolith ebenfalls in die Klasse der „Halogenide“, dort allerdings in die Abteilung der „Komplexen Halogenide“ ein. Diese ist zudem weiter unterteilt nach der Art der Kristallstruktur, so dass das Mineral entsprechend seinem Aufbau in der Unterabteilung „Insel-Aluminofluoride (Neso-Aluminofluoride)“ zu finden ist, wo es als alleiniger Namensgeber die „Kryolithgruppe“ mit der System-Nr. 3.CB.15 und den weiteren Mitgliedern Elpasolith und Simmonsit bildet.
Auch die vorwiegend im englischen Sprachraum gebräuchliche Systematik der Minerale nach Dana ordnet den Kryolith in die Klasse der „Halogenide“ und dort in die Abteilung „Komplexe Halogenide – Aluminiumfluoride“ ein. Auch hier ist er namensgebend in der „Kryolithgruppe“ mit der System-Nr. 11.06.01 innerhalb der Unterabteilung „Komplexe Halogenide - Aluminiumfluoride mit verschiedenen Formeln“ zu finden.
Chemismus
Die erste qualitative Analyse des Kryoliths stammt von Abildgaard[1], der „Thonerde und Flußspathsäure“, also Aluminium (eigentlich Al2O3!) und HF, fand. Die erste quantitative nasschemische Analyse führte Martin Heinrich Klaproth aus, der im Kryolith das von den früheren Bearbeitern (Abildgaard, José Bonifácio de Andrada e Silva, Louis-Nicolas Vauquelin) übersehen Natrium („Natrum“) nachwies:
„Ganz unerwartet hatte ich also hier, neben den bereits von Hrn. Prof. Abildgaard angezeigten beiden Bestandtheilen des Kryoliths, auch noch das Natrum, als dessen dritten wesentlichen Bestandtheil, aufgefunden, welche Entdeckung mir um so viel mehr Vergnügen gewährte, da es das erste mir vorgekommene Beispiel vom Dasein des Natrum, als Bestandtheil eines festen steinartigen Fossils, ist.“
Die erste genaue Analyse führte Jöns Jakob Berzelius[18][19] aus; er erhielt 54,07 % F, 13,00 % Al und 32,93 % Na (Summe 100,00 %).
Mittelwerte aus neun Mikrosonden-Analysen an Kryolith von der Typlokalität lieferten 33,31 % Na; 13,96 % Al und 53,97 % F (Summe 101,25 %).[20] Auf der Basis von sechs Fluoratomen wurde daraus die empirische Formel Na3,06Al1,09F6 ermittelt, die zu Na3,00Al1,00F6,00 vereinfacht werden kann.[20] Berücksichtigt man die unterschiedliche strukturelle Position der Na-Atome, entspricht diese Formel auch der offiziellen Formel (Na2NaAlF6) der IMA für Kryolith.[4]
Die alleinige Elementkombination Na–Al–F, wie sie der offiziellen Formel der IMA für den Kryolith zu entnehmen ist, weisen unter den derzeit bekannten Mineralen (Stand 2022) nur Chiolith, Na5Al3F14 und der ungenügend charakterisierte, möglicherweise mit Chiolith identische Khodnevit, Na2AlF5, auf.[21]
Hinsichtlich der chemischen Zusammensetzung ist Kryolith das Na2-dominante Analogon zum K2-dominierten Elpasolith, K2NaAlF6, das Na-dominante Analogon zum Li-dominierten Simmonsit, Na2LiAlF6, und das Na2-Na-dominante Analogon zum Ca-Li-dominierten Colquiriit, CaLi[AlF6]. Eine mögliche Mischkristallbildung zwischen Kryolith und Elpasolith wurde bisher noch nicht nachgewiesen.[22]
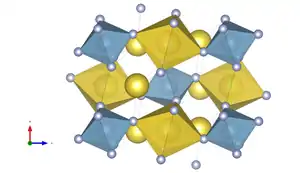
Kristallstruktur
Kryolith kristallisiert im monoklinen Kristallsystem in der Raumgruppe P21/n (Raumgruppen-Nr. 14, Stellung 2) mit den Gitterparametern a = 5,4024 Å; b = 5,5959 Å, c = 7,7564 Å und β = 90,278 ° sowie zwei Formeleinheiten pro Elementarzelle.[8] Hierbei kommt es zu einer Gitterverzerrung.[23]
Die Kristallstruktur des Kryoliths besteht aus isolierten, extrem regelmäßigen AlF6-Oktaedern, die von zwei kristallographisch unterschiedlichen, [6]- und [8]-koordinierten Na-Atomen umgeben sind. Na(1) zeigt eine ziemlich regelmäßige oktaedrische Koordination durch Fluor, und diese Oktaeder besitzen gemeinsame Ecken mit den AlF6-Oktaedern. Na(2) wird von acht Fluoratomen koordiniert, die in einem stark verzerrten kubischen Antiprisma angeordnet sind. Der große Bindungslängenbereich des Na(2)-Atoms resultiert aus den Anforderungen an die Bindungsstärke der Fluoranionen. Die AlF6- und NaF6-Oktaeder bilden ein dreidimensionales Gerüst, in dessen großen Hohlräumen die Na[8]-koordinierten Atome sitzen.[8][5]
Obwohl Kryolith eine monokline Symmetrie aufweist, ist er pseudokubisch mit einer Superzellmultiplizität von 2. Aus dieser Superzelle können die Zellen aller homotypischen Alkalimetallhexafluoride wie zum Beispiel die tetragonalen Polymorphe von K3AlF6, Rb3AIF6 und Cs3AlF6 abgeleitet werden. Der komplexe Polymorphismus dieser Verbindungen kann mit den Koordinationserfordernissen der großen Alkalimetallkationen zusammenhängen. Der Komplexitätsgrad des Polymorphismus der M+3AlF6-Verbindungen nimmt mit abnehmendem Ionenradius des Alkalikations zu.[8]
Die kubische Hochtemperaturform des β-Kryoliths besitzt ein flächenzentriertes Gitter mit vier Formeleinheiten pro Elementarzelle. Die Umwandlung von β-Kryolith zu α-Kryolith, dem eigentlichen Kryolith, verläuft ähnlich wie die zwischen Hoch- und Tiefquarz spontan und reversibel bei einer Temperatur von 560 °C.[24][5]
Im Gegensatz zu allen erwähnten Arbeiten haben Hexiong Yang und Kollegen[25] im Verlauf einer Hochtemperatur-Einkristall-Röntgenbeugungsstudie im Bereich 295 bis 900 K Hinweise darauf erhalten, dass im verwendeten Kryolith-Einkristall bei T0 ≈ 885 K ein fluktuationsinduzierter Phasenübergang erster Ordnung von monokliner zu orthorhombischer Symmetrie stattfindet – im Gegensatz zu den Ergebnissen früherer Studien, die – wie oben erwähnt – davon ausgehen, dass Kryolith bei ≈ 823 K in eine kubische Hochtemperatur-Modifikation übergeht.[25]
Eigenschaften
Morphologie
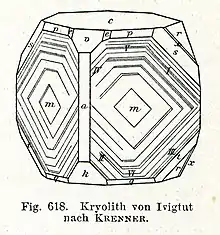
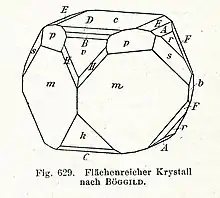
Kryolith bildet bis zu 4 cm große Kristalle[14], in deren Tracht ca. 30 verschiedene Flächenformen nachgewiesen wurden.[10][26] Zu den wichtigsten und verbreitetsten zählen das vordere Pinakoid a {100}, das seitliche Pinakoid b {010} und das Basispinakoid c {001}; die Pinakoide parallel zur b-Achse v {101} und k {101}; das Prisma parallel zur a-Achse r {011}; das Prisma parallel zur c-Achse m {110} sowie die Prismen allgemeiner Lage p {111} und s {121}.[24] Der größte Teil der im Atlas der Krystallformen von Victor Mordechai Goldschmidt abgebildeten Kristallzeichnungen des Kryoliths stammt von József Sándor Krenner und Ove Balthasar Bøggild.[27][28]
- Tracht und Habitus von Kryolith-Kristallen (gleiche Farben bedeuten gleiche Flächenformen)
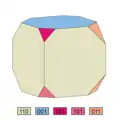 1. isometrisch und flächenarm
1. isometrisch und flächenarm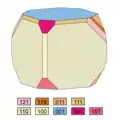 2. wie 1, aber deutlich flächenreicher
2. wie 1, aber deutlich flächenreicher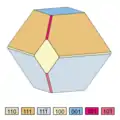 3. pseudokubisch, oktaederähnlich
3. pseudokubisch, oktaederähnlich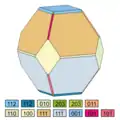 4. ähnlich wie 3, aber flächenreicher
4. ähnlich wie 3, aber flächenreicher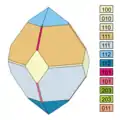 5. wie 4, durch Wegfall von {001} spindelförmig
5. wie 4, durch Wegfall von {001} spindelförmig 6. pseudokubisch, oktaederähnlich, flächenarm
6. pseudokubisch, oktaederähnlich, flächenarm 7. kurzprismatisch, extrem flächenreich
7. kurzprismatisch, extrem flächenreich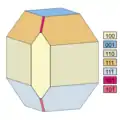 8. kurzprismatisch flächenarm
8. kurzprismatisch flächenarm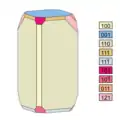 9. langprismatisch, flächenarm
9. langprismatisch, flächenarm 10. langprismatisch, flächenreich
10. langprismatisch, flächenreich
Die Kristalle bilden zwei verschiedene Habitusvarianten. Sie sind entweder würfelähnlich-pseudokubisch mit {110} und {001} und zeigen oft „gebrochene Kanten“ durch das Auftreten des vorderen Pinakoids {100} und des Prismas {111} sowie abgestumpfte Ecken durch das Pinakoid {101} und die Prismen {011} und {121} (vgl. dazu die Nummer 2 der nebenstehenden Kristallzeichnungen). Die Flächen des Prismas {110} weisen charakteristische Streifungen parallel zu [111], [111] und [110] auf. Die zweite Habitusvariante sind nach der c-Achse [001] kurzprismatische Kristalle (vgl. dazu die Nummern 9 und 10 der nebenstehenden Kristallzeichnungen).[24][9]
Die Kristalle sind häufig nach einem oder gleichzeitig nach mehreren (bis zu 5 oder mehr) von 13 unterschiedlichen Gesetzen verzwillingt, was zu Durchdringungs-, Wiederholungs- und polysynthetischen Zwillingen führt.[9] Zu diesen zählen:[12]
- Durchdringungszwillinge nach [110] durch Rotation um 90° oder 270° (häufig)
- Wiederholungszwillinge nach [110] durch Rotation um 180° (weniger häufig)
- Zwillinge nach [021] durch Rotation um 120° (häufig), Zusammensetzung Oberfläche unregelmäßig; vor allem in körnigem Material, als feine Lamellen und wohl immer sekundär
- Wiederholungszwillinge nach [111] durch Rotation um 180° (selten); nicht in körnigem Material
- Zwillinge nach (001) oder nach [100] durch Rotation um 180°, Verwachsungsfläche (001)
- Zwillinge nach (100) oder nach [001] durch Rotation um 180°, Verwachsungsfläche (100)
- Zwillinge nach (112), Verwachsungsfläche (112)
- Zwillinge nach (112), Verwachsungsfläche (112)
- Zwillinge nach (110), Verwachsungsfläche (110)
- Zwillinge nach [111] durch Rotation um 180°
- Zwillinge nach (211)
Im Gegensatz zu den seltenen Kristallen tritt Kryolith wesentlich häufiger massiv-derb oder in spätigen bis grobkörnig-dichten Aggregaten auf. Die Kristalle sind dann auf den Oberflächen dieser Aggregate flach und parkettartig aufgewachsen (vgl. die Kristallzeichnung nach József Sándor Krenner 1883).[12][24] Die derben, sehr grobkörnigen Aggregate des Kryoliths an der Typlokalität erreichten Größen von bis zu 6 m.[14]
In dem Karbonatitstock in den Chibinen, Russland, bildete Kryolith in einem Sideritgang mit Burbankit, Dawsonit und Pyrit clusterartige Aggregate bis zu 1 cm Durchmesser aus kleinen farblosen Kristallen bis zu 1 mm Größe. Die Kristalle weisen einen pseudokubischen Habitus auf und zeigen gekrümmte Flächen des Prismas {110} und des Basispinakoids {001}. In anderen Dawsonit-Kryolith-Gängchen innerhalb des Karbonatitstocks fanden sich wasserklar-durchsichtige, isometrische, bis zu 3 cm große Kryolith-Aggregate unter schneeweißem faserigem Dawsonit in Begleitung von Neighborit, Fluorit, Siderit, Burbankit, Pyrit, Galenit und Sphalerit.[29]
Physikalische Eigenschaften


Kryolith-Kristalle sind wasserklar-farblos bis weißlich und schneeweiß, können aber auch rötlich, ziegelrot, bräunlich, grau, braun-schwarz oder schwarz gefärbt sein.[10][9] Die schwarze Farbe soll durch Gehalte an organischen Stoffen bedingt sein, da so gefärbter Kryolith nach Erhitzen bis zur Rotglut weiß wird.[30][31] Ihre Strichfarbe wird mit weiß angegeben.[12] Die Oberflächen des durchsichtigen bis durchscheinenden[10] Kryoliths zeigen einen feuchten, glasartigen Glanz, gelegentlich auch Fettglanz.[10] Auf den Flächen des Basispinakoids {001} weist das Mineral hingegen Perlmuttglanz auf.[10] Kryolith besitzt eine diesem Glanz entsprechende geringe Lichtbrechung (nα = 1,339; nβ = 1,339; nγ = 1,340)[11] und eine kaum vorhandene Doppelbrechung (δ = 0,001).[11] Aufgrund dieser niedrigen Lichtbrechung, welche mit der des Wassers nahezu identisch ist (Wasser hat für Tageslicht mit einer Wellenlänge von λ = 589 nm einen Brechungsindes von 1,33300), verschwindet farbloser Kryolith scheinbar im Wasser.[11] Unter dem Polarisationsmikroskop ist der zweiachsig positive[11] Kryolith im durchfallenden Licht farblos und nicht pleochroitisch.[9][29]
Kryolith besitzt keine Spaltbarkeit, die Teilbarkeit mit Absonderungen nach {001} und {110} ruft aber einer der Spaltbarkeit ähnelnden Effekt hervor.[12] Da der Winkel zwischen den beiden Absonderungsflächen 88° beträgt, wird dadurch eine würfelähnliche Absonderung erzeugt.[32] Das Mineral bricht aufgrund seiner Sprödigkeit[12] ähnlich wie Quarz oder Amblygonit, wobei die Bruchflächen muschelig[10][29] (wie beim Quarz) oder uneben[12] (wie beim Amblygonit) ausgebildet sind. Kryolith weist für massives Material eine Mohshärte von 2,5 bis 3[10] und für Kristalle eine Mohshärte von 3 bis 3,5[33][11] auf und gehört damit zu den mittelharten Mineralen, die sich ähnlich gut wie das Referenzmineral Calcit mit einer mit Kupfermünze ritzen lassen. Die Vickershärte des Minerals wurde auf der Fläche (001) mit VHN50 = 346 (286–412) kg/mm² bestimmt.[33] Die gemessene Dichte für Kryolith beträgt je nach Bearbeiter 2,96 bis 2,98 g/cm³[11], die berechnete Dichte 2,973 g/cm³.[9]
Das Mineral hat schwache thermolumineszente Eigenschaften und fluoresziert im kurzwelligen UV-Licht intensiv gelb bei gelber Phosphoreszenz sowie im langwelligen UV-Licht blassgelb.[9] Anderen Angaben zufolge fluoresziert Kryolith jeweils nur selten und sehr schwach im kurzwelligen UV-Licht (254 nm) pinkfarben, bläulichweiß, orangerot, violettrot, violetrosa oder lachsrosa und im langwelligen UV-Licht (365 nm) bläulichweiß, violettrot und violettrosa. Am intensivsten fluoresziert danach Kryolith aus Ivittuut (rotorange im kurzwelligen, violettrot im langwelligen UV-Licht). Wichtigster Aktivator ist Eu2+.[34] Kryolith färbt sich bei längerer Einwirkung von Elektronenstrahlen schwarz, entfärbt sich jedoch bereits nach einigen Minuten wieder.[10]
Chemische Eigenschaften
Kryolith ist sehr leicht – schon in der Kerzenflamme – schmelzbar; sein Schmelzpunkt liegt bei 1012 °C.[13] Vor dem Lötrohr schmilzt er zu einem weißen Email und färbt die Flamme rötlichgelb. Beim Glühen im offenen Glasröhrchen entwickelt sich Fluorwasserstoff (HF). Auf Kohle schmilzt er zu einer klaren Perle, die beim Erkalten undurchsichtig wird. Die Schmelzperlen überziehen sich beim Erkalten mit Kristallskeletten von zunächste kubischem β-Kryolith (der Hochtemperaturmodifikation). Nach dem Glühen auf Kohle bleibt eine Kruste zurück, die durch Kobaltnitratlösung blau gefärbt wird.
Kryolith wird bereits von atmosphärischer Feuchtigkeit angelöst und kavernös; er löst sich leicht in Wasser (ein Teil in 2730 Teilen H2O bei 12 °C).[30][31] Ferner löst er sich leicht in einer Lösung aus Aluminiumchlorid (AlCl3). Feines Pulver zersetzt sich beim Erwärmen mit konzentrierter wässriger Oxalsäure (C2H2O4) unter Entwicklung von HF. Kryolith löst sich gleichfalls unter Entwicklung von HF in konzentrierter Schwefelsäure (H2SO4) vollständig, in Salzsäure (HCl) dagegen nur teilweise.[10]
Bildung und Fundorte
Kryolith ist ein im Pegmatitstadium gebildetes Mineral und tritt typischerweise eingewachsen in Granit-Pegmatiten oder aufgewachsen in Drusenhohlräumen von Pegmatiten auf. Ferner tritt er in Drusen von Alkaligesteinen, als Nebengemengteil von zinnführenden Alkali-Graniten und als aus der Dampfphase gebildetes Mineral auf Klüften und in der Grundmasse einiger fluorreicher, topashaltiger Rhyolithe auf. In Form von Schmitzen (geringmächtige, nach den Seiten auskeilende Einlagerungen[35]) in Karbonatit-Gängen, die durch einen fenitisierten Biotit-Gneis setzen, und als seltene authigene Komponente in den Mergelsteinen und Schiefern der Green-River-Formation.[9] Sekundär entsteht Kryolith hydrothermal und aus Verwitterungslösungen in Drusen und Spalten in primären, Kryolith führenden Mineralvergesellschaftungen.[24]
Kryolith wandelt sich leicht in andere Aluminiumfluoride wie Pachnolith, Thomsenolith, Gearksutit, Kryolithionit, Weberit, Jarlit und Prosopit um. Die Veränderung beginnt gewöhnlich mit dem Eindringen entlang der Teilbarkeien und führt zu zelligen oder porösen Massen, die mit Kristallen der sekundären Minerale ausgekleidet sind. Einige der Alterationen wurden auch künstlich nachvollzogen.[12] In einem Biotit-Nephelin-Sodalith-Orthoklas-Gang in Hornfelsen am Berg Partomtschorr in den Chibinen wird Kryolith von Nephelin verdrängt. In Foyaiten am Berg Judytschwumtschorr wird er durch Albit ersetzt.[29] Im Ringkomplex Liruei (auch Ririwai) auf dem Jos-Plateau im nigerianischen Bundesstaat Plateau enthält die dritte Granitphase (der Kaffo-Valley-Albit-Riebeckit-Granit) bis zu 6 % Kryolith.[36]
Charakteristische Begleitminerale sind Pachnolith, Thomsenolith, Gearksutit, Kryolithionit, Weberit, Jarlit, Prosopit, Chiolith, Mikroklin, Quarz, Fluorit, Siderit, Sphalerit und Topas (Ivigtut Mine, Grönland); Topas, Chiolith, Fluorit und Phenakit (Ilmengebirge, Russland) bzw. Sodalith, Villiaumit, Eudialyt, Lovozerit, Natrolith, Chabasit und Aegirin (Mont Saint-Hilaire, Kanada).[9]
_Greenland._The_cryolite_quarry_at_Ivittuut_(12049891056).jpg.webp)
Die Typlokalität des Kryoliths ist der extrem fluorreiche Granit-Pegmatit der Ivigtut Mine (Koordinaten der Kryolith-Lagerstätte Ivigtut) bei der wüstgefallenen Siedlung Ivittuut am Südufer des Ilorput (Arsukfjords) im Distrikt Ivittuut in der Kommuneqarfik Sermersooq im autonomen Teil Grönland des Königreichs Dänemark. Sie wurde erst von Carl Ludwig Giesecke auf seiner von 1806 bis 1813 dauernden Grönlandreise aufgefunden und anschließend kurz beschrieben.[37] Gieseckes Tagebuch wurde allerdings erst wesentlich später – im Jahre 1878, lange nach Gieseckers Tod – von Frederik Johnstrup herausgegeben.[38] Im Jahre 1910 erschien eine zweite, vervollständigte Ausgabe.[39]
Die Ivigtut Mine ist die einzige Lokalität weltweit, in der Kryolith lagerstättenbildend auftrat und ab 1854 auch kommerziell gewonnen wurde. Im Jahre 1865 wurde die Kryolith Mine og Handels Selskabet in Kopenhagen gegründet.[10] Jahrzehntelang produzierte die Ivigtut Mine jährlich rund 30000 Tonnen Kryolith.[7] Die Lagerstätte ist seit 1962, als man den Abbau nach 106 Jahren einstellte, erschöpft – im Jahre 1987 endete auch der Abtransport des aufgehaldeten Kryoliths.[14]


Weltweit konnte Kryolith bisher (Stand: 2022) an rund 50 Fundorten nachgewiesen werden.[40][41][36] Dazu gehören:
- In Europa:
- die Zinnlagerstätte (Quarz-Kassiterit-Wolframit-Stockwerk) des Huber-Stocks bei Boží Dar (Gottesgab), Okres Karlovy Vary, Karlovarský kraj, und Krupka im ehemaligen Okres Teplice, Ústecký kraj, beide in Tschechien, sowie die Zinn-Wolfram-Lithium-Lagerstätte Zinnwald-Cínovec beiderseits der deutsch-tschechischen Grenze auf dem Kamm des Erzgebirges (Krušné hory)
- kleine Aufschlüsse/Straßeneinschnitte im Ekerit am Fluss Gjerdingselva neben der unbefestigten Straße vom Gjerdingen-See zum Bahnhof Stryken, Kommune Lunner, Fylke Viken, Norwegen
- die brennende Kohlehalde der Grube Marcel, Radlin, Powiat Wodzisławski, Rybniker Kohlenrevier (Rybnicki Okręg Węglowy) im Oberschlesischen Industriegebiet (Górnośląskie Zagłębie Węglowe), Woiwodschaft Schlesien (Województwo śląskie), Polen
- das Oktjabrski (Mariupolski) Massiv (russisch Октябрьский (Мариупольский) массив) bei Mariupol in der Oblast Donezk, und Vorkommen und Lagerstätten („Kammerpegmatite“) im Rajon Korostyschiw (ukrainisch Коростишівський район, ehemals Rajon Wolodarsk-Wolynskyj) und die Beryllium-Lagerstätte Perga (russisch месторождение Перга) im Erzfeld Pershanskoe (russisch Пержанское рудное поле), beide in der Oblast Schytomyr, alle in der Ukraine
- der cancrinitführende Nephelinsyenit bei Ditrău, Kreis Harghita, Region Siebenbürgen, Rumänien
- der Karbonatitstock in der Nähe der Tulilucht-Bucht (russisch залива Тульилухт) des Sees Umbosero, Chibinen-Massiv, der im August 2002 entdeckte Pegmatit Palitra (russisch пегматит Палитра) in der Grube Karnasurt, Grubenbereich Kedyk, Lowosero-Tundren im Rajon Lowozero, und der Berg Alluaiw (russisch гора Аллуайв), Rajon Lowozero, alle in der Oblast Murmansk, Halbinsel Kola, Russland
- der Pit No. 69 (G.I. Gasberg’s Topas-Kryolith-Bruch), Ilmengebirge, Oblast Tscheljabinsk, Föderationskreis Ural, Russland
- In Asien:
- agpaitische Alkali-Granite des Verkhnee-Espe-Massivs in den Akzhaylyautas-Bergen im Tarbagataigebirge, Ostkasachstan, Kasachstan
- das ca. 100 km nordöstlich der Nordspitze des Baikalsees liegende Alkaligesteinsmassiv Burpala (russisch Бурпала массив) am Fluss Maigunda im Becken der Mama, Burjatien, Föderationskreis Ferner Osten, Russland
- der Erzdistrikt Wosnessenski (russisch Вознесенский рудный район) nördlich von Wladiwostok, Region Primorje, Föderationskreis Ferner Osten, Russland
- die Seltenmetall-Nb-Ta-Zr-Lagerstätte Ulug-Tansek (russisch Улуг-Танзек) im Erzin-Massiv, Koschuun Kaa-Chemski, Tuwa, Russland
- die Ta-Nb-Lagerstätte Katugin (Katuginskoe, russisch Катугин) auf dem Aldan-Schild, Rajon Kalarski, Region Transbaikalien, Föderationskreis Ferner Osten, Russland
- In Afrika:
- der Granitkomplex Timedjelalen, Cercle de Tessalit, Region Kidal, Mali
- die Aris Quarries bei Aris, circa 25 km südlich Windhoek im Wahlkreis Windhoek-Land (englisch Windhoek Rural) in der Region Khomas, der Kalkfeld-Komplex bei Kalkfeld unweit Otjiwarongo, Omatako, und die Okorusu Mine bei Otjiwarongo, beide in der Region Otjozondjupa, alle in Namibia
- der Ringkomplex Afu im Bundesstaat Nassarawa sowie die Ringkomplexe Amo, Jos Plateau, Liruei, Ropp und Shere auf dem Jos-Plateau im Bundesstaat Plateau, alle in Nigeria
- das Auftreten in Form von gelben warzigen fumarolischen Krusten auf trachyandesitischer Lava von der Inselgruppe Tristan da Cunha, St. Helena, Ascension und Tristan da Cunha

- In Nordamerika:
- Nellusivik, Kangerlussuaq, (Søndre Strømfjord), Qeqqata Kommunia, Grönland
- der Steinbruch Poudrette im Mont-Saint-Hilaire-Komplex, Regionale Grafschaftsgemeinde La Vallée-du-Richelieu, Montérégie, der Steinbruch Demix-Varennes im Saint-Amable-Sill, Varennes & Saint-Amable, Regionale Grafschaftsgemeinde Marguerite-D’Youville (früher Lajemmerais), Montérégie, und der Steinbruch Francon Quarry in Montréal, alle in Québec, Kanada
- die Little Three Mine bei Ramona im Ramona Mining District, San Diego County, Kalifornien, USA
- die Inexco Mine im Jamestown Mining District, Boulder County, Colorado, USA
- Eureka Shaft und St Peters Dome (mit den Einzelfundstellen 30-4 Pegmatite, Cryolite Mine (65-2 Pegmatite) und Eureka tunnel (1-15 Pegmatite)) sowie die Stove Mountain Mineral Locality, alle im Cheyenne Mining District (St. Peters Dome Mining District) an der südlichen Basis des Pikes Peak im El Paso County, Colorado, USA
- der Goldie-Karbonatit und der gangförmige McClure-Gulch-Karbonatit am McClure Mountain im Iron Mountain Complex, beide im Fremont County, sowie das Piceance Basin im Garfield County und Rio Blanco County, alle in Colorado, USA
- die Green-River-Formation im Grenzgebiet der Bundesstaaten Colorado, Wyoming und Utah, welche Gebiete in tertiären lakustrinen, kerogenreichen Schiefern umfasst
- der Zapot-Pegmatit in der Gillis Range im Fitting Mining District, Mineral County, Nevada, USA
- der Steinbruch Point of Rocks, Point of Rocks Mesa (Pecks Mesa) bei Springer, Colfax County, New Mexico, USA
- die Round Top Prospects, Sierra Blanca Peaks, Hudspeth County, Texas, USA
- ein Vorkommen im südlichen Teil des Emery County, Utah, USA, etwa zwischen Cidar City und Grand Junction
- der aluminiumfluoridhaltige Pegmatit der Morefield Mine bei Winterham im Amelia County, Virginia, USA
- der McGuire Pit (Salzman Quarry) im Nine Mile Pluton innerhalb des Wausau Intrusive Complex’, Marathon County, Wisconsin, USA
- der Yellowstone-Nationalpark, USA
- In Südamerika:
- die Sn-Nb-Ta-T-(Y,REE,Li)-Lagerstätte der an den Madeira-A-Typ-Granit gebundenen Pitinga Mine bei der Gemeinde Presidente Figueiredo, Amazonas, und der 30 km Durchmesser aufweisende Karbonatit-Komplex von Lages, Santa Catarina, beide in Brasilien
Synthetische Herstellung
Da die Vorräte der einzigen Kryolith-Lagerstätte für den Bedarf der Aluminiumverhüttung nicht ausreichten, wird die Phase Natriumhexafluoroaluminat(III) künstlich hergestellt. Die Synthese erfolgt aus Hexafluoridokieselsäure, Natrium- und Aluminiumhydroxid.[42]
Verwendung

„Kryoliten har stor praktisk Interesse, da den er det eneste Mineral, der for Tiden er Genstand for Brydning i Grønland og det eneste, som nogen Sinde har givet noget større Udbytte.“
„Der Kryolith ist von großem praktischem Interesse, da er das einzige Mineral ist, das derzeit in Grönland abgebaut wird und das einzige, das jemals einen größeren Ertrag erbracht hat.“
Die Grönländer Kryolithlagerstätte wurde seit 1854 im Steinbruchbetrieb abgebaut, wobei bis 1901 insgesamt 307.731 Tonnen Kryolith gefördert worden sind. Im Jahre 1901 betrug die Produktion 8.125 Tonnen, wobei man 5.089 Tonnen nach Amerika und 2.954 Tonnen nach Europa exportierte. Die Jahreshöchstproduktion innerhalb der ersten 50 Jahre fällt in das Jahr 1897 und betrug 13.361 Tonnen.[3] Mitte des 20. Jahrhunderts bis zum Ende der Förderung im Jahre 1962 wurden jährlich etwa 30.000 Tonnen Kryolith produziert.[7] Insgesamt lieferte die Lagerstätte 3,7 Millionen Tonnen Erz mit einem Kryolithgehalt von 58 %.[44] Der grönländische Kryolith war längere Zeit das wichtigste Aluminiumerz und diente daneben der Sodafabrikation. Etwa ab dem Beginn des 20. Jahrhunderts fand er noch Verwendung zur Aluminiumherstellung (siehe unten) und zur Herstellung von Opalglas und von Emaille[45] für Eisenwaren.[3]
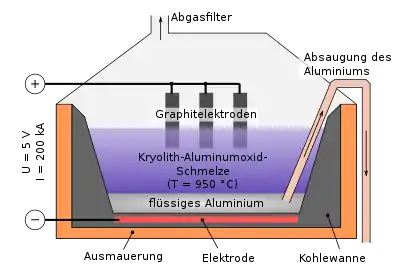
Eine großtechnische Anwendung von Kryolith wurde die Schmelzflusselektrolyse zur Gewinnung von Aluminium (der seit 1886/87 etablierte Hall-Héroult-Prozess), wobei etwa seit dem Ende des 19. Jahrhunderts und spätestens seit 1987 nur noch künstlich aus Fluorit erzeugter Kryolith zur Anwendung kommt. Dabei wird die Eigenschaft des relativ niedrigen Schmelzpunktes von Kryolith (1012 °C) genutzt. Aluminiumoxid (Korund), der Ausgangsstoff der Elektrolyse, hat eine Schmelztemperatur von 2050 °C. Für die Schmelzflusselektrolyse wird die eutektische Mischung verwendet. Sie besteht aus 18,5 % Al2O3 und 81,5 % Na3[AlF6].[46] Der Schmelzpunkt des Eutektikums liegt dann bei 960 °C. Erst diese relativ niedrige Arbeitstemperatur ermöglicht die großtechnische Anwendung der Schmelzflusselektrolyse.
Kryolith wird weiter in der Gießereiindustrie eingesetzt. Dem Formstoff beim Gießen kann Kryolith beigemischt werden. Dieses Beimischen kann jedoch die Oberflächenqualität des Werkstücks negativ beeinflussen.
Synthetisch hergestellter Kryolith findet in der Hülle von Schweißelektroden als Flussmittel Verwendung.
Kryolith wird außerdem als schleifaktive Substanz in kunstharzgebundenen Schleifmitteln sowie in Schleifmitteln auf Unterlagen genutzt. Aufgrund der hohen Temperaturen, die beim Schleifen an der Spitze des Schleifkorns auftreten, schmilzt der Kryolith. Dabei korrodiert der geschmolzene Kryolith den abgeschliffenen Stahlspan und verhindert damit ein Zusetzen des Schleifkörpers.
Problematisch ist das Auftreten von Kryolith bei der Zinkphosphatierung von zum Beispiel Aluminium-Automobilkarossen oder feuerverzinkten Oberflächen. Aluminium wird hierbei im Phosphatierbad als Kryolith ausgefällt und muss wieder herausgefiltert werden.
Kryolith wird auch zur Herstellung optisch hochreflektiver Oberflächen verwendet. Er wird dabei in dünnen Schichten abwechselnd mit einem anderen Stoff, zum Beispiel Zinkselenid, im Vakuum aufgedampft (Vielschichtspiegel in der Lasertechnik).
Im Kryolithglas, das zur Herstellung von Augenprothesen verwendet wird, sorgt Kryolith als Trübungsmittel für eine milchig-weiße Trübung des Glases.[42]
Trotz der Weichheit und der „verschwommenen Erscheinung“ sind farblose transparente monokline Kristalle gelegentlich verschliffen worden.[47]
Der bei einer Temperatur von etwa 560 °C erfolgende Modifikationswechsel von kubischem β-Kryolith zu monoklinem α-Kryolith wird als ein wichtiges geologisches Thermometer zur Klärung der Bildungsbedingungen von Gesteinen genutzt.[7]
Daneben wird die gelbe Farbe bei der Feuerwerkerei nicht nur durch Natriumoxalat und Natriumnitrat, sondern auch durch Natriumhexafluoroaluminat(III) und damit künstlichen Kryolith hervorgerufen.[48]
Vorsichtsmaßnahmen
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Name |
Natriumhexafluoroaluminat, Kryolith | ||||||||
| CAS-Nummer | |||||||||
| |||||||||
Das Mineral bzw. die chemische Verbindung wird als gesundheitsgefährdend und umweltgefährlich eingestuft. Gesundheitsschädlich ist vor allem das Einatmen und Verschlucken von Kryolithteilchen, die akut zu Beschwerden im Atemtrakt mit funktioneller Dyspnoe (erschwerte Atemtätigkeit) und schließlich Lungenemphysem (Überblähung der Lungenbläschen) führen können. Des Weiteren sind Appetitlosigkeit, Übelkeit, Erbrechen und Verstopfung die Folge.[49]
Längerfristig hat Kryolith eine toxische Wirkung auf Knochen, Zähne und Nieren.[49]
Literatur
- Carl Hintze: Kryolith. AlFl3·3NaFl = Na3AlFl6. In: Handbuch der Mineralogie von Dr. Carl Hintze. Erster Band. Elemente – Sulfide – Oxyde – Haloide – Carbonate –Sulfate – Borate – Phosphate : Zweite Abtheilung. Oxyde und Haloide. 1. Auflage. Band 1. Veit & Comp., Leipzig 1915, S. 2507–2505.
- Charles Palache, Harry Berman, Clifford Frondel: Cryolite. In: The System of Mineralogy. of James Dwight Dana and Edward Salisbury Dana Yale University 1837–1892. 7. Auflage. II (Halides Nitrates, Borates, Carbonates, Sulfates, Phosphates, Arsenates, Tungstates, Molybdates etc.). John Wiley & Sons, New York 1951, ISBN 0-471-19272-4, S. 110–113 (englisch, Erstausgabe: 1892).
- Friedrich Klockmann: Klockmanns Lehrbuch der Mineralogie. Hrsg.: Paul Ramdohr, Hugo Strunz. 16. Auflage. Enke, Stuttgart 1978, ISBN 3-432-82986-8, S. 490–491 (Erstausgabe: 1891).
- Hans Jürgen Rösler: Lehrbuch der Mineralogie. 4. durchgesehene und erweiterte Auflage. Deutscher Verlag für Grundstoffindustrie (VEB), Leipzig 1987, ISBN 3-342-00288-3, S. 357–358.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1140.
- Cryolite. In: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Hrsg.): Handbook of Mineralogy, Mineralogical Society of America. 2001 (englisch, handbookofmineralogy.org [PDF; 99 kB; abgerufen am 23. Januar 2022]).
- David Dolejš, Don R. Baker: Phase transitions and volumetric properties of cryolite, Na3AlF6: Differential thermal analysis to 100 MPa. In: American Mineralogist. Band 91, Nr. 1, 2006, S. 97–103, doi:10.2138/am.2006.1772.
- Erwin Riedel, Christoph Janiak: Anorganische Chemie. 8. Auflage. de Gruyter, Berlin 2011, ISBN 978-3-11-022566-2, S. 594 (eingeschränkte Vorschau in der Google-Buchsuche).
Weblinks
- Kryolith. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 10. Januar 2022.
- Eintrag zu Kryolith bei mindat.org, abgerufen am 10. Januar 2022.
- David Barthelmy: Cryolite Mineral Data. In: webmineral.com. Abgerufen am 10. Januar 2022 (englisch).
- Cryolite search results. In: rruff.info. Database of Raman spectroscopy, X-ray diffraction and chemistry of minerals (RRUFF), abgerufen am 10. Januar 2022 (englisch).
- American-Mineralogist-Crystal-Structure-Database – Cryolite. In: rruff.geo.arizona.edu. Abgerufen am 10. Januar 2022 (englisch).
- Datenblatt Kryolith (PDF) bei Merck, abgerufen am 23. Februar 2010.
Einzelnachweise
- Peter Christian Abildgaard: Norwegische Titanerze und andre neue Fossilien. In: Allgemeines Journal der Chemie. Band 2, 1799, S. 502 (rruff.info [PDF; 500 kB; abgerufen am 23. Januar 2022]).
- Ernst Friedrich Glocker: Handbuch der Mineralogie : Zweyte Abtheilung, die specielle Oryktognosie und die Geognosie enthaltend. 1. Auflage. Johann Leonhard Schrag, Nürnberg 1831 (eingeschränkte Vorschau in der Google-Buchsuche).
- Alfred Wilhelm Stelzner, Alfred Bergeat: Die Erzlagerstätten : 1. Hälfte. 1. Auflage. Arthur Felix, Leipzig 1904, S. 71–72 (470 S., online verfügbar bei archive.org – Internet Archive).
- Malcolm Back, Cristian Biagioni, William D. Birch, Michel Blondieau, Hans-Peter Boja und andere: The New IMA List of Minerals – A Work in Progress – Updated: January 2022. (PDF; 3,7 MB) In: cnmnc.main.jp. IMA/CNMNC, Marco Pasero, Januar 2022, abgerufen am 23. Januar 2022 (englisch).
- Hugo Strunz, Ernest H. Nickel: Strunz Mineralogical Tables. Chemical-structural Mineral Classification System. 9. Auflage. E. Schweizerbart’sche Verlagsbuchhandlung (Nägele u. Obermiller), Stuttgart 2001, ISBN 3-510-65188-X, S. 161 (englisch).
- Stefan Weiß: Das große Lapis Mineralienverzeichnis. Alle Mineralien von A – Z und ihre Eigenschaften. Stand 03/2018. 7., vollkommen neu bearbeitete und ergänzte Auflage. Weise, München 2018, ISBN 978-3-921656-83-9.
- Friedrich Klockmann: Klockmanns Lehrbuch der Mineralogie. Hrsg.: Paul Ramdohr, Hugo Strunz. 16. Auflage. Enke, Stuttgart 1978, ISBN 3-432-82986-8, S. 490–491 (Erstausgabe: 1891).
- Frank C. Hawthorne, Rob B. Ferguson: Refinement of the crystal structure of cryolite. In: The Canadian Mineralogist. Band 13, Nr. 4, 1975, S. 377–382 (englisch, rruff.info [PDF; 505 kB; abgerufen am 10. Januar 2022]).
- Cryolite. In: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Hrsg.): Handbook of Mineralogy, Mineralogical Society of America. 2001 (englisch, handbookofmineralogy.org [PDF; 99 kB; abgerufen am 10. Januar 2022]).
- Carl Hintze: Kryolith. AlFl3•3NaFl = Na3AlFl6. In: Handbuch der Mineralogie von Dr. Carl Hintze. Erster Band. Elemente – Sulfide – Oxyde – Haloide – Carbonate –Sulfate – Borate – Phosphate : Zweite Abtheilung. Oxyde und Haloide. 1. Auflage. Band 1. Veit & Comp., Leipzig 1915, S. 2507–2505.
- Eintrag zu Cryolite (Kryolith) bei mindat.org, abgerufen am 23. Januar 2022.
- Charles Palache, Harry Berman, Clifford Frondel: Colemanite. In: The System of Mineralogy. of James Dwight Dana and Edward Salisbury Dana Yale University 1837–1892. 7. Auflage. II (Halides Nitrates, Borates, Carbonates, Sulfates, Phosphates, Arsenates, Tungstates, Molybdates etc.). John Wiley & Sons, New York 1951, ISBN 0-471-19272-4, S. 110–113 (englisch, Erstausgabe: 1892).
- Eintrag zu Kryolith. In: Römpp Online. Georg Thieme Verlag, abgerufen am 6. Februar 2022.
- Ole V. Petersen, Karsten Secher: Grönland : Mineralien, Geologie, Geschichte. In: Magma. Band 1984, Nr. 6, 1984, S. 32–42 (Artikel: Die Kryolith-Lagerstätte Ivigtut).
- Peter Christian Abildgaard: Sur plusieurs pierres nouvelles envoyées de Norwège. In: Annales de Chimie. Band 32, 1800, S. 194 (französisch, eingeschränkte Vorschau in der Google-Buchsuche – als Chryolithe).
- Catalogue of Type Mineral Specimens – C. (PDF; 312 kB) Commission on Museums (IMA), 9. Februar 2021, abgerufen am 10. Januar 2022.
- Martin Heinrich Klaproth: Chemische Untersuchung des Kryoliths. In: Der Gesellschaft Naturforschender Freunde zu Berlin Neue Schriften. Band 3, 1801, S. 322–328 (eingeschränkte Vorschau in der Google-Buchsuche).
- Jöns Jakob Berzelius: Undersökning af flusspatssyran och dess märkvärdigste föreningar. In: Kongl. Vetenskaps-Academiens Handlingar under förra hälften för år 1823. Band 1823, 1823, S. 315 (schwedisch, 66 S., online verfügbar bei archive.org – Internet Archive).
- Jöns Jakob Berzelius: Untersuchungen über die Flußspatsäure und deren merkwürdigsten Verbindungen. In: Annalen der Physik und Chemie. Band 1, Nr. 1, 1824, S. 41 (48 S., Digitalisat).
- Cryolite RRUFF ID R050287. In: rruff.info. Database of Raman spectroscopy, X-ray diffraction and chemistry of minerals (RRUFF), abgerufen am 23. Januar 2022 (englisch).
- Minerals with Na–Al–F. In: mindat.org. Hudson Institute of Mineralogy, abgerufen am 10. Januar 2022 (englisch).
- Roger H. Mitchell, Mark D. Welch, Anton R. Chakhmouradian: Nomenclature of the perovskite supergroup: A hierarchical system of classification based on crystal structure and composition. In: Mineralogical Magazine. Band 81, Nr. 3, 2017, S. 431–432, doi:10.1180/minmag.2016.080.156 (englisch, rruff.info [PDF; 2,2 MB; abgerufen am 5. Oktober 2021]).
- Ulrich Müller: Anorganische Strukturchemie. 6., aktualisierte Auflage. Vieweg+Teubner, Wiesbaden 2008, ISBN 978-3-8348-0626-0, S. 298.
- Karl Ludwig Weiner, Rupert Hochleitner: Steckbrief Kryolith. In: Lapis. Band 5, Nr. 12, 1980, S. 5–7.
- Hexiong Yang, Subrata Ghose, Dorian M. Hatch: Ferroelastic phase transition in cryolite, Na3AlF6, a mixed fluoride perovskite: High temperature single crystal X-ray diffraction study and symmetry analysis of the transition mechanism. In: Physics and Chemistry of Minerals. Band 19, Nr. 8, 1993, S. 528–544, doi:10.1007/BF00203053 (englisch, online verfügbar bei af.booksc.eu [PDF; 1,6 MB; abgerufen am 23. Januar 2022]).
- Victor Mordechai Goldschmidt: Kryolith. In: Atlas der Krystallformen von Victor Goldschmidt. Tafeln. 1. Auflage. Band V. Kainit – Margarosanit. Carl Winters Universitätsbuchhandlung, Heidelberg 1918, S. Tafel 28–31.
- József Sándor Krenner: Die grönlandischen Minerale der Kryolithgruppe. In: Mathematisch-naturwissenschaftliche Berichte aus Ungarn. Band 1, 1883, S. 1–24.
- Ove Balthasar Bøggild: Krystalform og Tvillingdannelser hos Kryolit, Perovskit og Boracit (Kristallform und Zwillingsformationen in Kryolith, Perowskit und Boracit). In: Meddelelser om Grønland. Commissionen for Ledelsen af de geologiske og geografiske Undersøgelser i Grønland. 1. Auflage. Band 50. Reitzel, København 1912, S. 1–72 (online verfügbar bei Dansk Geologisk Forening [PDF; 30,4 MB; abgerufen am 23. Januar 2022]).
- Victor N. Yakovenchuk, Gregory Yu. Ivanyuk, Yakov A. Pakhomovsky, Yuri P. Men’shikov: Khibiny. Hrsg.: Frances Wall. 1. Auflage. Laplandia Minerals, Apatity 2005, ISBN 5-900395-48-0, S. 102 (englisch, researchgate.net [PDF; 47,3 MB; abgerufen am 26. April 2021]).
- Johannes Frederik Johnstrup: Kryolitens Forekomst i Grønland. In: 12te Skandinaviska naurforskaremötets Förhandlingar Stockholm 1883. 1883, S. 234–252 (dänisch).
- Hjalmar Sjögren: P. Johnstrup: Über das Vorkommen des Kryoliths in Grönland. (Förhandl. vid de skandinaviska naturforskarnes 12te möte i Stockholm. 1880. 231—252. Stockholm 1883.). In: Neues Jahrbuch für Mineralogie, Geologie und Palaeontologie I. Band 1886, 1886, S. 28–31 (zobodat.at [PDF; 13,2 MB; abgerufen am 10. Januar 2022]).
- Helmut Schröcke, Karl-Ludwig Weiner: Mineralogie. Ein Lehrbuch auf systematischer Grundlage. de Gruyter, Berlin; New York 1981, ISBN 3-11-006823-0, S. 330–332.
- Hans Pauly: Hardness of cryolite, chiolite, cryolithionite and other fluorides from Ivigtut, South Greenland. In: Meddelelser fra Dansk Geologisk Forening (Bulletin of the Geological Society of Denmark). Band 34, Nr. 3-4, 1985, S. 145–150 (englisch, 2dgf.dk [PDF; 450 kB; abgerufen am 10. Januar 2022]).
- Gerard Barmarin: Cryolite. In: fluomin.org. Luminescent Mineral Database, abgerufen am 10. Januar 2022 (englisch, Fluoreszenzdaten für Kryolith).
- Hans Murawski, Wilhelm Meyer: Geologisches Wörterbuch. 12. Auflage. Spektrum Akademischer Verlag, Heidelberg 2010, ISBN 978-3-8274-1810-4, S. 147.
- John C. Bailey: Formation of cryolite and other aluminofluorides: A petrologic review. In: Bulletin of the Geological Society of Denmark. Band 29, 1980, S. 1–45 (englisch, online verfügbar bei Dansk Geologisk Forening [PDF; 3,3 MB; abgerufen am 23. Januar 2022]).
- Carl Ludwig Giesecke: On Cryolite. In: The Edinburgh Philosophical Journal. Band 6, Nr. XI, 1822, S. 141–144 (englisch, Digitalisat bei biodiversitylibrary.org [abgerufen am 23. Januar 2022]).
- Carl Ludwig Giesecke: Bericht einer mineralogisches Reise in Grönland, in Form eines Tagebuchs, gehalten von Dr. Karl Ludwig Giesecke, Königl. Preuss. Bergrath, 1806–1813. Hrsg.: Frederik Johnstrup. 1. Auflage. Bianco Lunos Bogtrykkeri, København 1878, S. 1–332 (332 S., Digitalisat).
- Carl Ludwig Giesecke: Mineralogisches Reisejournal über Grönland, gehalten von Karl Ludwig Giesecke, Kön. Pr. Bergrath. In: Knud Johannes Vogelius Steenstrup (Hrsg.): Meddelelser om Grønland. Commissionen for Ledelsen af de geologiske og geografiske Undersøgelser i Grønland. 2., vollst. Auflage. Band 35. Reitzel, København 1910, S. 1–478 (478 S., online verfügbar bei archive.org – Internet Archive).
- Localities for Cryolite. In: mindat.org. Hudson Institute of Mineralogy, abgerufen am 23. Januar 2022 (englisch).
- Fundortliste für Kryolith beim Mineralienatlas (deutsch) und bei Mindat, abgerufen am 23. Januar 2022.
- Erwin Riedel, Christoph Janiak: Anorganische Chemie. 8. Auflage. de Gruyter, Berlin 2011, ISBN 978-3-11-022566-2, S. 594 (eingeschränkte Vorschau in der Google-Buchsuche).
- Ove Balthasar Bøggild: Mineralogia Groenlandica (Systematisk Fortegnelse over Mineralerne). In: Meddelelser om Grønland. Commissionen for Ledelsen af de geologiske og geografiske Undersøgelser i Grønland. 1. Auflage. Band 32. Reitzel, Kjøbenhavn 1905, S. 108–115 (archive.org [PDF; 33,1 MB; abgerufen am 23. Januar 2022] Beschreibung von Kryolith auf den Seiten 108–115).
- Exploration and mining in Greenland, Fact Sheet No. 2 : Greenland Mineral Resources. In: geus.dk. Geological Survey of Denmark and Greenland (GEUS), abgerufen am 10. Januar 2022 (englisch).
- Julius Grünwald: Chemische Technologie des Kryoliths und der Kryolithersatzmittel, wie Kieselfluornatrium und über die Rolle des Kryoliths in der Emailfabrikation. In: Julius Grünwald (Hrsg.): Chemische Technologie der Emailrohmaterialien. 1. Auflage. Springer, Wien 1922, S. 87–127, doi:10.1007/978-3-7091-5899-9_6 (276 S.).
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1140.
- Cryolite. In: gemdat.org. Hudson Institute of Mineralogy, abgerufen am 10. Januar 2022 (englisch).
- Anne Marie Helmenstine: The Chemistry of Firework Colors. In: thoughtco.com. Abgerufen am 23. Januar 2022 (englisch).
- Eintrag zu Natriumhexafluoroaluminat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Januar 2022. (JavaScript erforderlich)