Chlorwasserstoff
Chlorwasserstoff (Summenformel HCl, systematisch auch als Wasserstoffchlorid oder Hydrogenchlorid bezeichnet) ist ein farbloses, stechend riechendes Gas, das sich sehr leicht in Wasser löst. Wässrige Lösungen von Chlorwasserstoff werden Salzsäure oder Chlorwasserstoffsäure genannt. Beim Einatmen des Gases entsteht in der Lunge Salzsäure, was zu schweren Verätzungen führt, da Chlorwasserstoffsäure eine sehr starke Säure ist.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemeines | ||||||||||||||||
| Name | Chlorwasserstoff | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | HCl | |||||||||||||||
| Kurzbeschreibung |
farbloses, stechend riechendes Gas[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 36,46 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||
| Dichte |
1,64 kg·m−3 (Gasdichte, 0 °C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
−85,0 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| pKS-Wert |
−6,2[3] | |||||||||||||||
| Löslichkeit |
leicht in Wasser (720 g·l−1 bei 20 °C)[2] | |||||||||||||||
| Dipolmoment | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−92,3 kJ/mol (gasförmig)[7] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Es wurde von Humphry Davy 1808 dargestellt.
Gewinnung und Darstellung
Hergestellt wird Chlorwasserstoff im Labor aus konzentrierter Schwefelsäure und Natriumchlorid:
- Natriumchlorid und Schwefelsäure reagieren zu Natriumsulfat und Chlorwasserstoff
Statt der Schwefelsäure kann auch Natriumhydrogensulfat (NaHSO4) benutzt werden. Dazu wird ein Gemisch aus Natriumchlorid und Natriumhydrogensulfat trocken erhitzt. Um die Reaktion in Gang zu halten, muss das hierbei entstehende Chlorwasserstoffgas abgeführt werden.
In der chemischen Industrie fällt Chlorwasserstoff hauptsächlich als Nebenprodukt bei der Chlorierung organischer Verbindungen an oder wird mit der Chlorknallgasreaktion (Zündung eines Gemisches aus Wasserstoff und Chlor beispielsweise durch Belichtung) gewonnen.
- Wasserstoff und Chlor reagieren zu Chlorwasserstoff
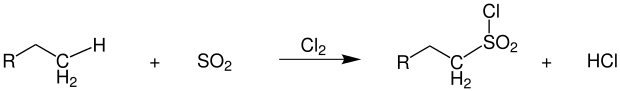
Bei der Photochlorierung oder Sulfochlorierung von Kohlenwasserstoffen fällt Chlorwasserstoff als Koppelprodukt an:
Eigenschaften
Die systematische Bezeichnung Wasserstoffchlorid bringt mit der Silbe -chlorid zum Ausdruck, dass das Chloratom in der Molekülverbindung eine negative Partialladung trägt, ähnlich wie nach Chloridionen, die eine negative Ionenladung besitzen.
Chlorwasserstoff hat eine etwas höhere Dichte als Luft. In einem Liter Wasser lösen sich bei 0 °C unter Erwärmung 520 l, das entspricht 850 g HCl-Gas. Bei 20 °C lösen sich in einem Liter Wasser 442 Liter Chlorwasserstoff. An feuchter Luft bildet HCl-Gas Nebel aus feinen Salzsäure-Tröpfchen. Chlorwasserstoff löst sich in Alkoholen ähnlich gut wie in Wasser. Er ist in Ethern noch gut und in Kohlenwasserstoffen oder Chlorkohlenwasserstoffen nur gering löslich.[8]
| Löslichkeiten von Chlorwasserstoff in organischen Lösungsmitteln (gemessen bei 101,3 kPa)[8] | ||||||||||||
| Temperatur in °C | 0 | 10 | 15 | 20 | 25 | 27 | 30 | 40 | 50 | 102 | 177 | |
| Löslichkeit in g·kg−1 Lösungsmittel | ||||||||||||
| Methanol | 1092 | 877 | 688 | |||||||||
| Ethanol | 838 | 756 | 681 | 610 | ||||||||
| Tetrahydrofuran | 584 | |||||||||||
| 1,4-Dioxan | 433 | |||||||||||
| Diisopropylether | 349 | |||||||||||
| Dibutylether | 250 | |||||||||||
| n-Hexan | 7,1 | |||||||||||
| n-Hexadecan | 3,9 | 2,2 | 1,6 | |||||||||
| Benzol | 20 | 12,5 | ||||||||||
| Toluol | 21,3 | |||||||||||
| Chloroform | 8,5 | 6,9 | ||||||||||
| Tetrachlormethan | 6,0 | 3,9 | ||||||||||
Seine spezifische Wärmekapazität cp beträgt 799 J/(kg K).
Verwendung
Neben der vielfältigen Verwendung als Säure findet reiner Chlorwasserstoff Verwendung als Chlorierungsmittel in der Oxychlorierung von Ethen zu Vinylchlorid.
Sicherheitshinweise
Chlorwasserstoff ist ätzend und in hohen Konzentrationen giftig. Vergiftungen sind jedoch sehr selten. Beim Einatmen können Reizungen und Verätzungen der Schleimhäute und der Atemwege auftreten, die zu einer akuten Bronchitis oder Lungenentzündung führen können. Bei Kontakt mit Haut und Kleidung lässt sich die Säure mit Wasser gut und restlos auswaschen.
Weblinks
Einzelnachweise
- Eintrag zu HYDROCHLORIC ACID in der CosIng-Datenbank der EU-Kommission, abgerufen am 21. März 2020.
- Eintrag zu Chlorwasserstoff, wasserfrei in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- Robert Anthony Robinson, Roger G. Bates: Dissociation constant of hydrochloric acid from partial vapor pressures over hydrogen chloride-lithium chloride solutions. In: Analytical Chemistry, 43(7), 1971, S. 969–970.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Dipole Moments, S. 9-51.
- Eintrag zu Hydrogen chloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 7647-01-0 bzw. Chlorwasserstoff), abgerufen am 2. November 2015.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-22.
- S. Austin; A. Glowacli: Hydrochloric Acid, in: Ullmanns Enzyklopädie der Technischen Chemie, Wiley-VCH Verlag, Weinheim 2012; doi:10.1002/14356007.a13_283.


