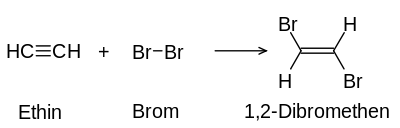Halogenierung
Als Halogenierung wird in der Chemie die Überführung eines Elementes oder einer Verbindung in ein Halogenid, eine salzartige oder kovalent aufgebaute Verbindung mit einem Halogen, bezeichnet. Dies ist sowohl für anorganische als auch organische Verbindungen möglich. Je nach Halogen wird zwischen Fluorierung, Chlorierung, Bromierung oder Iodierung unterschieden.
Additionsreaktionen
Halogen, Halogenwasserstoff oder hypohalogenige Säure reagieren mit ungesättigten Verbindungen.
Addition von Halogenen an Alkene oder Alkine
Aus Alkenen entstehen durch die Umsetzung mit Halogenmolekülen vicinale Dihalogenalkane. Alkine addieren Halogen schrittweise. Es entstehen Tetrahalogenalkane.[1] Hier am Beispiel der Reaktion von Br2 mit Ethin dargestellt:
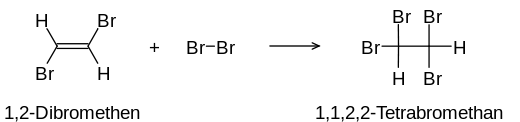
Der erste Schritt ist die Bildung des vicinalen Dihalogenalkens (hier 1,2-Dibromethen).
Im zweiten Schritt entsteht das Tetrahalogenalkan (hier 1,1,2,2-Tetrabromethan).
Addition von Halogenwasserstoff an Alkene oder Alkine
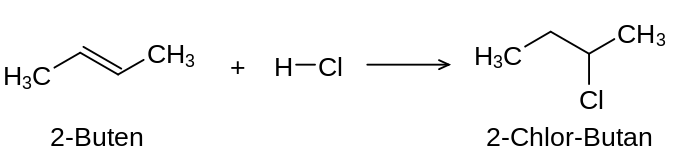
Die Addition von Halogenwasserstoff an ein Alken liefert ein Monohalogenalkan. Alkine reagieren mit Halogenwasserstoff zu einem Monohalogenalken, wobei das Halogenatom an eines der zwei sp2-hybridisierten Kohlenstoffatomorbitale der Kohlenstoff-Kohlenstoff-Doppelbindung addiert wird.[2] Ein Beispiel für die Addition von Halogenwasserstoffen an Alkene ist die Chlorwasserstoffaddition an 2-Buten:
Addition von hypohalogeniger Säure an Alkene
Die Addition von hypohalogeniger Säure an Alkene liefert Halogenhydrine, d. h. beide sp2-hybridisierten Kohlenstoffatome im Edukt wandeln sich in sp3-hybridisierte Kohlenstoffatome im Produkt um, in dem an eines dieser Kohlenstoffatome ein Hydroxy-Rest und an das andere ein Halogenatom gebunden wird.[3]
Addition von Halogenen an freie Radikale
Wegen der leichten homolytischen Spaltung von Halogenmolekülen reagieren diese spontan mit freien organischen Radikalen.
Substitutionsreaktionen
Halogenierung von Aromaten
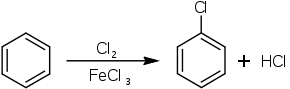
Eine Variante um Aromaten zu halogenieren ist die elektrophile aromatische Substitution. Hierbei greifen aktivierte Halogenide das aromatische System elektrophil an. Ein Beispiel hierfür ist die Chlorierung von Benzol:
Lässt man Chlor in Gegenwart einer Lewis-Säure mit Benzol reagieren, entstehen Chlorbenzol und Chlorwasserstoff. Eisen(III)-chlorid oder auch Aluminiumtrichlorid fungiert dabei meist als Lewis-Säure und dient der Aktivierung von Chlor, das andernfalls nicht mit Benzol reagieren würde. Die Reaktion mit Brom würde analog verlaufen.[4][5]
Halogenierung von Alkanen
Die Halogenierung von Alkanen läuft radikalisch ab und führt zu Halogenalkanen.[6]
- Radikalische Substitution von Ethan mit Cl2
Halogenierung in der Allyl-Stellung oder Benzyl-Stellung
Die Halogenierung von Alkenen in Allyl-Stellung[7] oder von Alkylaromaten in der Benzyl-Stellung[8] läuft radikalisch ab und führt unter Substitution zu halogenierten Alkenen bzw. in der Seitenkette halogenierten Alkylaromaten:
Bruttoreaktion am Beispiel des Cyclohexen.
Halogenierung von Ketonen und Aldehyden
Die Halogenierung von Ketonen ist formal eine elektrophile Substitutionsreaktion mit einem Proton als Abgangsgruppe. Sie verläuft jedoch nicht nach einem derartigen Mechanismus, sondern über das Enol des betreffenden Ketons und es entstehen α-halogenierte Ketone.[9] Die Halogenierung von Aldehyden verläuft analog.[10][11]
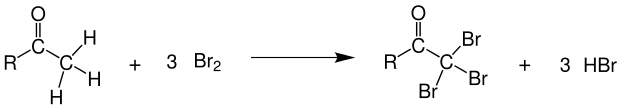
R bezeichnet ein Wasserstoffatom für ein Aldehyd und einen organischen Rest für ein Keton.
Mechanismus der Halogenierung von Aldehyden und Ketonen
Die Halogenierung von Carbonylgruppen, wie sie an Aldehyden und Ketonen vorhanden sind, kann entweder säure- oder basenkatalysiert ablaufen. Im Folgenden wird der Mechanismus exemplarisch anhand einer säurekatalytischen Bromierung von Aceton demonstriert:
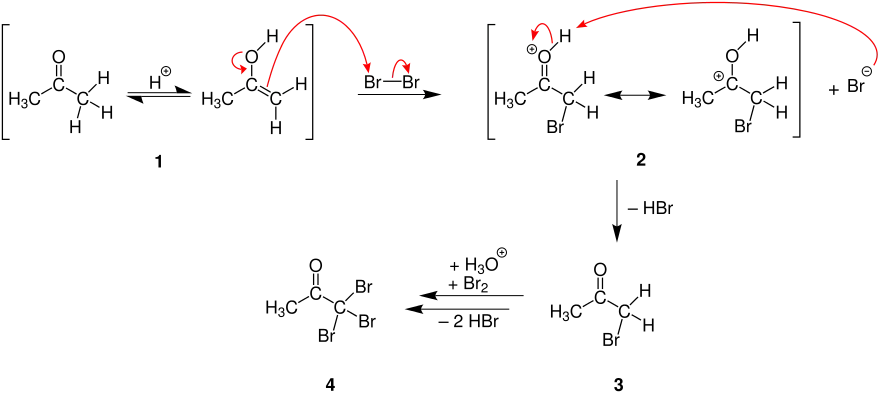
Mechanismus der Halogenierung von Carbonylverbindungen; R bezeichnet ein Wasserstoffatom für ein Aldehyd und einen organischen Rest für ein Keton.[10]
Das eingesetzte Aceton (1) steht mit seiner Enolform über die Keto-Enol-Tautomerie im Gleichgewicht. Setzt man nun Brom hinzu, so lagert sich dieses wie beschrieben an die Enolform an und es bildet sich das Oxoniumion 2, welches eine weitere mesomere Grenzstruktur besitzt. Außerdem bildet sich ein Bromion, welches im folgenden Schritt das Oxoniumion 2 deprotoniert. Dadurch erhält man einfach bromiertes Aceton 3. Wiederholt man diese Schritte zweimal für dieses bromierte Aceton 3, so kann man ein dreifach bromiertes Aceton 4 erhalten. Man spricht dann von einem α,α,α-trihalogeniertem Aceton.
Der geschwindigkeitsbestimmende Schritt bei dieser Reaktion ist die Bildung des Enols. Die Reaktionsgeschwindigkeit nimmt mit jedem dem Molekül zugefügten Halogen ab, da die Halogene elektronenziehend sind. Dadurch erschweren sie die Umlagerung von Elektronen im Molekül zur Enolform. Man sagt auch, dass die Enolisierbarkeit der Verbindung gesenkt wurde.[10]
Halogenierung von Carbonsäuren
Carbonsäuren lassen sich durch Umsetzung mit Thionylchlorid in Carbonsäurechloride umwandeln. Andere Chlorierungsmittel, wie z. B. Phosphortrichlorid oder Phosphorpentachlorid können ebenfalls eingesetzt werden.[12]
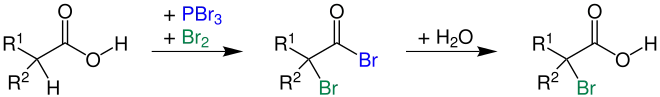
- Beispiel einer Bromierung nach Hell-Volhard-Zelinsky
Halogenierung von Ethern
Ether sind bei tiefen Temperaturen zu α-Chlor- und α,α'-Dichlorethern chlorierbar.[13]
Substitution von Hydroxygruppen
Hydroxygruppen in Alkoholen können mittels Chlorwasserstoff durch Chlor bzw. mittels Bromwasserstoff durch Brom substituiert werden.[13] Insbesondere für primäre und sekundäre Alkohole wird häufig Thionylchlorid (SOCl2) zur Chlorierung oder Phosphortribromid (PBr3) zur Bromierung verwendet. Um Hydroxygruppen durch Iod zu substituieren wird neben Iodwasserstoff im Labor auch Phosphortriiodid verwendet, welches in situ aus Phosphor und Iod hergestellt werden muss.
Primäre und sekundäre Alkohole können auch mittels der Appel-Reaktion chloriert oder bromiert werden. Die Reaktion ist stereoselektiv, führt aber zu einer Inversion der Konfiguration.[14]
Substitution des Sauerstoffs von Carbonylgruppen
Beim Erhitzen von Aldehyden oder Ketonen mit Phosphortrichlorid oder Phosphortribromid entstehen geminale Dichloride bzw. Dibromide.[15]
Substitution von stickstoffhaltigen Gruppen durch Halogen
Reaktion von Diazoniumsalzen unter Bildung von organischen Halogenverbindungen. Neben der Sandmeyer-Reaktion ist hier die Balz-Schiemann-Reaktion von Bedeutung.[15]
Halogenierung am Stickstoffatom von Carbonsäureamiden
Carbonsäureamide, die am Amidstickstoffatom mindestens ein Wasserstoffatom tragen, reagieren mit Hypohalogeniten. Es entstehen N-Halogencarbonsäureamide. Ein Beispiel ist N-Bromsuccinimid (NBS), das man in wässeriger Lösung aus Succinimid und je einem Äquivalent einer Base und Brom erhält.[16]
Halogenierung in der anorganischen Chemie
In der anorganischen Chemie spielt die Halogenierung unter anderem zur Bildung von Salzen, Halogenwasserstoffen und Halogensauerstoffsäuren eine Rolle.
Literatur
- Marye Anne Fox, James K. Whitesell: Organische Chemie, Grundlagen, Mechanismen, bioorganische Anwendungen, Spektrum, Akad. Verl., 1995, ISBN 3-86025-249-6.
Einzelnachweise
- Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 517.
- Hans Beyer und Wolfgang Walter: Organische Chemie, S. Hirzel Verlag, Stuttgart, 1984, S. 73, ISBN 3-7776-0406-2.
- Siegfried Hauptmann: Reaktion und Mechanismus in der organischen Chemie, B. G. Teubner, Stuttgart, 1991, S. 113, ISBN 3-519-03515-4.
- K. Peter C. Vollhardt, Neil E. Schore, "Organische Chemie", Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, 2005, 4. Auflage, H. Butenschön, ISBN 3-527-31380-X, S. 779–783.
- Paula Yurkanis Bruice: Organic Chemistry. 4. Auflage, Prentice-Hall, 2003, ISBN 0-13-141010-5, S. 607–609.
- Ivan Ernest: Bindung, Struktur und Reaktionsmechanismen in der organischen Chemie, Springer-Verlag, 1972, S. 297–306, ISBN 3-211-81060-9.
- Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 240, ISBN 3-342-00280-8.
- Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 297, ISBN 3-342-00280-8.
- Siegfried Hauptmann: Reaktion und Mechanismus in der organischen Chemie, B. G. Teubner, Stuttgart, 1991, S. 95–96 und S. 136, ISBN 3-519-03515-4.
- K. Peter C. Vollhardt, Neil E. Schore: Organische Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, 2005, 4. Auflage, H. Butenschön, ISBN 3-527-31380-X, S. 921–922.
- Paula Yurkanis Bruice: Organic Chemistry. 4. Auflage, Prentice-Hall, 2003, ISBN 0-13-141010-5, S. 797.
- Hans Beyer und Wolfgang Walter: Organische Chemie, S. Hirzel Verlag, Stuttgart, 1984, Seite 238–239, ISBN 3-7776-0406-2.
- Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 518.
- Substitutionsreaktionen an Aliphaten. EPF Lausanne, abgerufen am 2. November 2011.
- Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 519.
- Allinger, Cava, de Jongh, Johnson, Lebel, Stevens: Organische Chemie, Walter de Gruyter & Co., 1980, S. 898, ISBN 3-11-004594-X.