Additionsreaktion
Die chemische Addition (v. lat.: addere = dazugeben), auch als Additionsreaktion oder Anlagerungsreaktion bezeichnet, ist eine der typischen Reaktionen in der organischen Chemie. Bei dieser Reaktion werden mindestens zwei Moleküle zu einem vereinigt, wobei eine oder mehrere Mehrfachbindungen aufgespalten werden. Die Atomökonomie der Additionsreaktionen ist durchgängig hervorragend.
Die Addition ist die Umkehrung der Eliminierung, bei der von einem Molekül, z. B. unter Bildung von Mehrfachbindungen, Moleküle abgespalten werden.
Bei der Addition wird beispielsweise an einem ungesättigten Kohlenwasserstoff (Alken und Alkin), Carbonsäurederivat, Aldehyd oder Keton unter Aufspaltung ein symmetrisches (beispielsweise H–H, F–F) oder unsymmetrisches (beispielsweise H–Cl) Molekül an eine Kovalente Bindung mit Doppel- oder Dreifachbindung angelagert.
Eine besondere Form der Addition ist die Polyaddition, bei der mehrere Additionen nacheinander ablaufen und zu einer Bildung kettenförmiger größerer Moleküle – bis hin zu Makromolekülen – führen, die ggf. auch räumlich vernetzt sind.
Beispiel Kohlenwasserstoffe
Für die von den Kohlenstoffatomen nicht genutzten Elektronenpaare bilden die Alkene und Alkine Doppel- und Dreifachbindungen. Sie sind nun stabil, aber haben nicht an jedem Kohlenstoffatom die maximale Anzahl Wasserstoffatome gebunden. Sie werden daher als ungesättigt bezeichnet.
Ungesättigte Kohlenwasserstoffe sind zwar stabil, aber energetisch ungünstiger als gesättigte Kohlenwasserstoffe. Deshalb ist es leicht möglich, die Mehrfachbindungen der ungesättigten Kohlenwasserstoffe unter Aufhebung einer π-Bindung (siehe Doppelbindung und kovalente Bindung) in die nächste niedrigere Stufe umzuwandeln, beispielsweise ein Alken in ein Alkan.
Addition von Wasserstoff an ein Alkin
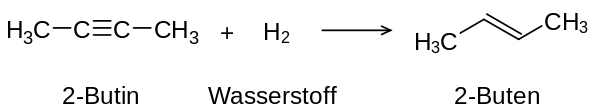
Die Addition von Wasserstoff wird auch als Hydrierung bezeichnet.[1] Für die Reaktion wird in der Regel ein Katalysator verwendet, als heterogener Katalysator bietet sich hier Palladium (dispergiert auf Aktivkohle: Pd/C) an, der die Aktivierung des Wasserstoffs durch dessen Bindung auf der Metalloberfläche übernimmt. Bei der heterogenen Katalyse entsteht bevorzugt oder ausschließlich ein cis-Alken.
Addition von Chlorwasserstoff an ein Alken
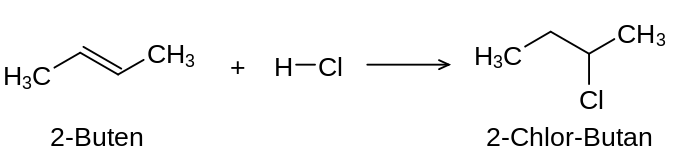
Beispiel Aldehyde (Acetalbildung)
Aldehyde reagieren – meist säurekatalysiert – mit Alkoholen zu Halbacetalen, die dann mit einem weiteren Molekül des entsprechenden Alkohols durch Wasserabspaltung zu den Vollacetalen weiterreagieren können.[2]
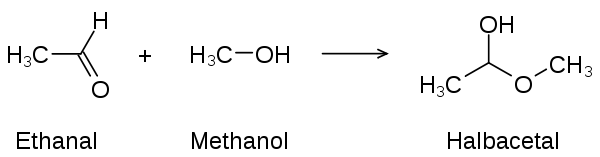
Anwendungen
Nachweis für Mehrfachbindungen
Mittels Additionsreaktion kann man Mehrfachbindungen in Molekülen organischer Stoffe mit Brom nachweisen: Das normalerweise rötlich-braune, in Wasser gelöste Brom („Bromwasser“), entfärbt sich, da das Brom die Mehrfachbindungen aufspaltet und sich anlagert und somit seine Farbe verliert.
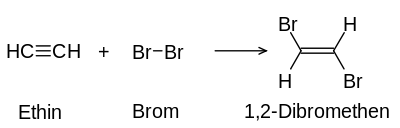
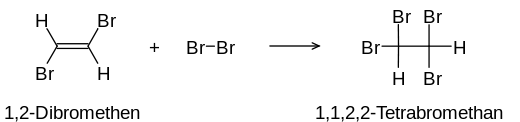
Beide Reaktionen laufen so lange ab, bis entweder alle Brommoleküle angelagert oder keine Mehrfachbindungen mehr vorhanden sind (bei der Nachweisreaktion nicht erwünscht). Das positive Ergebnis des Nachweises ist im Idealfall eine farblose Lösung. Normalerweise hat die Lösung jedoch eine leicht gelbliche Färbung durch kaum vermeidbare Verunreinigungen.
Arten von Additionsreaktionen
Weitere Reaktionen der organischen Chemie
Weitere Anwendungen
Siehe auch
Einzelnachweise
- Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 203, ISBN 3-342-00280-8.
- Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 358, ISBN 3-342-00280-8.