Dünger
Dünger oder Düngemittel ist ein Sammelbegriff für Reinstoffe und Stoffgemische, die in der Land- und Forstwirtschaft sowie im Gartenbau und in Privatgärten dazu benutzt werden, das Nährstoffangebot für die angebauten Kulturpflanzen zu ergänzen. Pflanzen benötigen für ihr Wachstum neben Wärme, Licht, Luft und Wasser zusätzlich auch Nährstoffe. Diese sind notwendig, um das Wachstum und die Entwicklung der Pflanzen zu steuern und zu unterstützen.


Die Nährstoffe liegen im Boden oft nicht in der optimal verwertbaren Form und Menge vor. Sie werden durch Auswaschung im Boden verlagert oder diesem durch die Ernteprodukte in beträchtlichen Mengen entzogen. Erst die Zufuhr von Pflanzennährstoffen durch die Düngung ermöglicht es, diese Nährstoffentzüge zu ersetzen.
Mit der Düngung wird die Ernährung der Pflanze verbessert, das Pflanzenwachstum gefördert, der Ertrag erhöht, die Qualität der Ernteprodukte verbessert und letztlich die Bodenfruchtbarkeit erhalten und gefördert.
Die Pflanzennährstoffe werden von verschiedenen Pflanzen in unterschiedlichen Mengen benötigt. Deshalb unterscheidet man Makronährstoffe (Hauptnährstoffe) und Mikronährstoffe (Spurennährstoffe).
Zu den Makronährstoffen gehören Stickstoff, Kalium, Phosphor (siehe auch Phosphatdünger), Magnesium, Schwefel und Calcium. Von diesen benötigen die landwirtschaftlichen Kulturpflanzen im Laufe ihrer Entwicklung je nach Nährstoff etwa 20–350 Kilogramm pro Hektar (entspricht im Hausgarten Gramm pro 10 Quadratmeter).
Von den Mikronährstoffen sind es lediglich etwa 5–1000 Gramm pro Hektar. Zu dieser Nährstoffgruppe zählen Bor, Chlor, Kupfer, Eisen, Mangan, Molybdän, Nickel und Zink. Mikronährstoffe übernehmen vielfältige Funktionen in Pflanzen, so zum Beispiel als Bestandteile von Enzymen, bei Stoffwechselreaktionen und im Hormonhaushalt.[1][2][3] Die Düngung der Pflanze oder des Bodens soll angepasst an den Pflanzenbedarf und abgestimmt auf die Nährstoffverhältnisse im Boden erfolgen.
Einflüsse auf Pflanzen wurden auch für folgende chemische Elemente nachgewiesen:[4] Aluminium, Arsen, Cer, Chrom, Fluor, Gallium, Germanium, Jod, Kobalt, Lanthan, Lithium, Mangan, Natrium, Rubidium, Selen, Silizium, Titan, Vanadium und weitere.
Klassifizierung von Düngemitteln
Es gibt verschiedene Möglichkeiten, wie Düngemittel unterschieden oder klassifiziert werden können, beispielsweise nach Herkunft, Entstehung oder chemischer Verbindung. Dementsprechend gibt es vielfältige Bezeichnungen, mit denen Düngemittel beschrieben werden. Nachfolgende Gruppierungen und Begriffserklärungen wurden nach diesen Unterscheidungen erstellt (nach[5]). Dies soll zum besseren Verständnis und einer klareren Abgrenzung beitragen – eine eindeutige Zuordnung in diese Gruppierungen ist allerdings nicht immer möglich.
Nach der Herkunft oder Entstehung
Ausgehend von ihrem Urzustand werden die Rohstoffe in verschiedenen Aufbereitungsverfahren in eine besser pflanzenverfügbare Form überführt.
- Handelsdünger
- Düngemittel, die im Handel und in Gartencentern verkauft werden.
- Naturdünger
- Dünger, der in der anfallenden Form unverarbeitet verwendet wird. Beispiele sind Naturprodukte wie Guano, Chilesalpeter und Gesteinsmehle.
- Sekundärrohstoffdünger
- Sammelbezeichnung für Düngemittel, die vorwiegend aus organischen Abfällen (Bioabfall) und Reststoffen, das heißt aus sekundären Rohstoffen hergestellt werden. Mit diesem Begriff sind so unterschiedliche Erzeugnisse wie Komposte, Gärrestprodukte, Fleischknochenmehle, Klärschlammprodukte, aber auch Gemische mit z. B. landwirtschaftlicher Gülle zusammengefasst.
- Wirtschaftsdünger
- Entstehen im landwirtschaftlichen Betrieb. Hierzu zählen Stallmist, Jauche, Gülle, Stroh, Gärreste aus Biogasanlagen.
- Synthetische Düngemittel
- Düngemittel, die unter hohem Energieaufwand in technischen Aufbereitungsverfahren natürlicher Rohstoffe hergestellt werden. Sie werden als Einzel- oder Mehrfachnährstoffdünger im Handel angeboten.[6]
Nach zeitlicher Verfügbarkeit
- Schnell wirkende Dünger
- Enthalten die Nährstoffe in sofort pflanzenverfügbarer Form. Sie wirken unmittelbar nach der Anwendung, Beispiele: Amid-, ammonium- und nitrathaltige Stickstoffdünger, wasserlösliche Phosphate, Kalisalze, Branntkalk.
- Langsam wirkende Dünger
- Die Wirkung bzw. Verfügbarkeit der Nährstoffe tritt erst nach Umsetzung im Boden ein. Beispiele: Durch Kunststoffumhüllung[7] aufbereitete Stickstoffdünger und auch Harnstoff, Rohphosphate, kohlensaure Kalke, Komposte, Hornspäne
Nach chemischer Verbindung

- Organische Dünger
- Enthalten organische Verbindungen beispielsweise aus Pflanzenteilen oder tierischen Ausscheidungen. Ein wechselnder Anteil der Nährstoffe ist in organischen Verbindungen gebunden. Aufgrund ihres Kohlenstoffanteils tragen diese zum Erhalt des Humusgehaltes in den Böden bei. Im Gegensatz zu Mineraldüngern sind die Nährstoffe in wechselnder Zusammensetzung, Pflanzenverfügbarkeit und Menge enthalten. Beispiele: Stallmist, Gülle, Gärreste, Stroh, Kompost, Hornspäne.
- Mineraldünger
- Sie bestehen aus mineralischen Salzen. Die Nährstoffe sind zum Beispiel als Oxide, Chloride, Sulfate, Carbonate etc. gebunden. Je nach Düngertyp sind die jeweiligen Nährstoffe in definierten pflanzenverfügbaren Formen und exakt festgelegten Mengen enthalten. Somit kann die Düngung je nach Bedarf genau kalkuliert und gezielt durchgeführt werden (siehe auch Precision Farming).
Nach Anzahl der Nährelemente
- Einzelnährstoffdünger
- Enthalten nur einen Nährstoff. So gibt es Stickstoff-, Phosphat- oder Kalium-Einzeldünger. Auch Kalkdünger zählen zu dieser Gruppierung. Geringe Mengen von anderen Nährstoffen sind möglich.
- Mehrnährstoffdünger
- Werden auch als Komplexdünger bezeichnet. Sie enthalten mehrere Nährstoffe in unterschiedlicher Zusammensetzung. Gängige Beispiele sind Phosphat-Kalium- (PK-Dünger) und Stickstoff-Phosphat-Dünger (NP-Dünger) als Zweinährstoffdünger; oder NPK-Dünger (Volldünger), die bis zu fünf Hauptnährstoffe plus Spurennährstoffe enthalten. Zu unterscheiden sind hier auch die Mehrnährstoffdünger industrieller Produktion und Mischdünger. Mehrnährstoffdünger aus der Industrie werden als Marken vertrieben. Mischdünger werden in speziellen Mischanlagen beim Landhandel und Genossenschaften hergestellt. Sie werden in der Regel aus Einzelnährstoffdüngern gemischt.
Auch Wirtschaftsdünger und organische Dünger können als Mehrnährstoffdünger bezeichnet werden, da sie mehrere Nährstoffe enthalten.
Nach Mengenbedarf der Pflanze
- Makronährstoffdünger
- Enthalten die Hauptnährstoffe für Pflanzen, die in großen Mengen benötigt werden. Dies sind vor allem Stickstoff, Phosphor und Kalium. Außerdem die Nährstoffe Schwefel, Magnesium und Calcium; diese drei werden in der Fachliteratur und in Rechtsvorschriften teilweise als Sekundärnährstoffe bezeichnet.[8] In der Regel werden Makronährstoffdünger über den Boden gedüngt.
- Mikronährstoffdünger
- Enthalten Spurennährstoffe, die in geringen Mengen von den Pflanzen benötigt werden (z. B. Zink, Mangan, Bor und Eisen). Sie werden in geringer Menge über den Boden oder über das Blatt appliziert.
Nach Applikationsart
- Bodendünger
- Werden auf oder in den Boden eingebracht, dienen hauptsächlich zur Versorgung mit Makronährstoffen eingesetzt und verbessern vorrangig die Nährsubstrate (Erden, Substrate im Gartenbau, Boden in der Landwirtschaft). Die Pflanze profitiert indirekt bzw. erst nach Umsetzung der Substanzen. Beispiele sind Kalke und Komposte.
- Pflanzendünger
- Sind dazu bestimmt, direkt von der Pflanze aufgenommen zu werden. Sie enthalten Nährstoffe in pflanzenverfügbaren Bindungsformen. Hierzu gehören die meisten Handelsdünger und auch Wirtschaftsdünger wie Jauche und Gülle.
- Fertigation (Nährstofflösung als Pflanzendünger)
- Der Begriff Fertigation ist ein Schachtelwort aus Düngung (engl. fertilization) und Bewässerung (engl. irrigation). Die Nährstoffe werden dem Bewässerungswasser zugegeben.
- Blattapplikation
- Bei der Blattapplikation werden in Wasser gelöste Nährstoffe auf die Blätter gespritzt und von diesen zügig aufgenommen. Bislang wird die Blattdüngung meist nur unterstützend zur Bodendüngung eingesetzt und dient vor allem bei der Spurennährstoffversorgung.
Nach Aggregatzustand
- Feste Dünger
- Düngergranulate oder -salze
- Flüssige Dünger
- Düngerlösungen und -suspensionen.
Nach speziellen Pflanzengruppen, für besondere Nährstoffansprüche und gegen Nährstoffmängel
- Dünger für Blattpflanzen und Rasen (bei N-P-K-Dünger mehr Stickstoffdünger)
- Dünger um mehr Blüten zu erreichen (bei N-P-K-Dünger mehr Kaliumanteile), beispielsweise Balkonblumendünger
- Dünger für höheren Fruchtertrag (bei N-P-K-Dünger mehr Phosphatanteile), beispielsweise "Tomatendünger" oder (kalkarmer) "Beerenobstdünger" oder Dünger für Obstgehölze
- Rhododendrondünger, kalkfrei und im pH-Wert sauer
- Wasserpflanzendünger, enthält wenig Phosphate (die starken Algenwuchs im Wasser bewirken)
- Zitruspflanzendünger, enthält mehr gut lösliche Eisensalze (Chelate)
- Hydrokulturdünger (Nitrate anstelle von Ammoniumsalzen, Eisendünger mit Komplexbildnern)
- Dünger für Koniferen, meist mit Schwefel (der von Bakterien zu pflanzenverfügbaren Sulfaten umgebaut wird; siehe dazu Schwefelkreislauf), Eisen und mehr Magnesium
- Dünger zur Bekämpfung von Chlorose (Gelbfärbung von Blättern)
- Dünger zur Förderung der Bewurzelung von Stecklingen mit stark erhöhten Phosphatanteilen und Bewurzelungshormonen
Geschichte

Seit spätestens 3100 v. Chr. wurden landwirtschaftlich genutzte Felder zur Steigerung der Ernte mit tierischen und menschlichen Fäkalien bestreut. Bereits die Römer und auch die Kelten begannen kohlensauren Kalk und Mergel als Dünger zu verwenden.
Um 1840 konnte der Chemiker Justus von Liebig die wachstumsfördernde Wirkung von Stickstoff, Phosphaten und Kalium nachweisen. Stickstoff erhielt man zum Beispiel in Form von Nitraten zunächst vor allem durch den Einsatz von Guano, einer Substanz, die sich aus den Exkrementen von Seevögeln bildet. Da die natürlichen Vorräte an mineralischem Dünger begrenzt sind und größtenteils aus Südamerika eingeführt werden müssen, sann man nach einer Methode, Stickstoffverbindungen synthetisch zu erzeugen.
Zwischen 1905 und 1908 entwickelte der Chemiker Fritz Haber die katalytische Ammoniak-Synthese. Dem Industriellen Carl Bosch gelang es daraufhin, ein Verfahren zu finden, das die massenhafte Herstellung von Ammoniak ermöglichte. Dieses Haber-Bosch-Verfahren bildete die Grundlagen der Produktion von synthetischem Stickstoff-Dünger.
Einen weiteren Prozess zur Produktion von Düngemitteln erfand Erling Johnson 1927 im Schmelzwerk Odda (Odda Smelteverk); er wurde 1932 patentiert und als Odda-Prozess bekannt.[9]
Seit dem Zweiten Weltkrieg brachte die Industrie vermehrt Düngemittel mit unterschiedlicher Zusammensetzung auf den Markt. Im letzten Viertel des 20. Jahrhunderts geriet der mineralische Dünger jedoch zunehmend in die Kritik, da seine übermäßige Verwendung oft ökologische Schäden verursacht. Durch die Entdeckung des Edaphons und der Funktionen des Humus gab es die Möglichkeit, nach Alternativen in Form einer organischen Düngung zu suchen. Seit etwa 1985 sinkt der Verbrauch von mineralischen Düngemitteln zum Beispiel in Deutschland. Allerdings blieb der Einsatz von Dünger angesichts der rasant wachsenden Weltbevölkerung immer im Fokus der Diskussion.
Zunehmender Wohlstand in Ländern wie China, Brasilien und Indien führte zu einer Veränderung der Ernährungsgewohnheiten, einem erhöhten Fleischkonsum und steigendem Düngemitteleinsatz in einigen Ländern.[10]
Rechtsgrundlagen
Herstellung, Inverkehrbringen und Anwendung von Düngemitteln sind in einigen Staaten durch mehrere Rechtsvorschriften (Düngemittelgesetz, Düngemittelverordnung, Düngeverordnung sowie angrenzende Rechtsbereiche) geregelt. Derzeit gibt es bezüglich der Anforderungen an Düngemittel sowie für ihr Inverkehrbringen sowohl nationale wie auch europäische Vorschriften: Ein Düngemittel kann also nach nationalem Recht oder nach EU-Recht zugelassen werden.
Anforderungen
Grundsätzlich dürfen in Deutschland und auf EU-Ebene Düngemittel nur dann in Verkehr gebracht werden, wenn sie genau definierten Düngemitteltypen entsprechen (Positivliste). Diese Typenlisten können auf Antrag um neue Typen ergänzt werden, soweit keine negativen Auswirkungen auf die Gesundheit von Menschen und Tieren sowie auf den Naturhaushalt zu erwarten sind und alle Anforderungen der jeweiligen Rechtsvorschrift erfüllt werden.
In Deutschland regelt die Düngemittelverordnung (Verordnung über das Inverkehrbringen von Düngemitteln, Bodenhilfsstoffen, Kultursubstraten und Pflanzenhilfsmitteln – DüMV),[8] welche Düngemittel gehandelt werden dürfen. Sie definiert die Düngemitteltypen und legt fest, welche Mindestgehalte für die einzelnen Nährstoffe einzuhalten sind. Zudem bestimmt sie Kennzeichnungsschwellen und Obergrenzen für Schadstoffe, etwa für Schwermetalle. Außerdem bestimmt sie, welche Informationen für eine ordnungsgemäße Kennzeichnung sowie für eine sachgerechte Lagerung und Anwendung aufzuführen sind.
Auf europäischer Ebene schreibt die EU-Verordnung 2003/2003/EG über Düngemittel[11] vor, welche Anforderungen mineralische EU-Düngemittel erfüllen müssen, um handelsfähig zu sein. Auch die EU-Verordnung legt Mindestnährstoffgehalte für die verschiedenen, aufgeführten Düngemitteltypen fest. Die Verordnung bestimmt ebenfalls Einzelheiten zur ordnungsgemäßen Kennzeichnung.
Anwendung
Bei der Anwendung von Düngemitteln durch die Landwirte sind vor allem die „gute fachliche Praxis“ aber auch mögliche negative Auswirkungen auf die Böden sowie Oberflächengewässer und Grundwasser zu berücksichtigen.
Auf europäischer Ebene ist die sogenannte Nitratrichtlinie[12] von wesentlicher Bedeutung. Sie dient dem Schutz der Gewässer vor Verunreinigung durch Nitrat aus landwirtschaftlichen Quellen. Zu diesem Zweck müssen die Mitgliedsstaaten gefährdete Gebiete definieren, Regelungen zur guten fachlichen Praxis erlassen und Aktionsprogramme mit verschiedenen Maßnahmen durchführen, um Gewässer zu schützen.
Ihre nationale Umsetzung in Deutschland erfolgt zu einem wesentlichen Teil durch die Düngeverordnung (DüV).[13] Die DüV definiert die gute fachliche Praxis bei der Anwendung von Düngemitteln auf landwirtschaftlich genutzten Flächen und soll die stofflichen Risiken beim Einsatz von Düngemitteln begrenzen.
Die Düngeverordnung geriet zunehmend in Kritik. Laut Beurteilung der Europäischen Kommission setzte Deutschland die Nitratrichtlinie nur unzureichend um. Sie eröffnete deswegen ein Vertragsverletzungsverfahren vor dem Europäischen Gerichtshof. Das federführende Bundesministerium für Ernährung und Landwirtschaft erarbeitete deshalb eine Novelle der Düngeverordnung, die am 2. Juni 2017 in Kraft trat.[14]
Mit dem European Green Deal wurde das Ziel gesetzt, der Einsatz von Düngemitteln bis 2030 um mindestens 20 % zu reduzieren.[15]
Düngerarten
Man unterscheidet Dünger allgemein nach der Art, wie der düngende Stoff gebunden ist. Weitere Unterscheidungsarten sind die Form des Düngers (Feststoffdünger und Flüssigdünger) und deren Wirkung (schnellwirkender Dünger, Langzeitdünger, Depotdünger). Unsachgemäßer Düngereinsatz führt zur Überdüngung (Eutrophierung) angrenzender Flächen und Gewässer und damit zum Artenrückgang.
Mineraldünger

Im anorganischen Dünger oder Mineraldünger liegen die düngenden Bestandteile meist in Form von Salzen vor. Mineraldünger werden in Granulat-, Pulver- oder in flüssiger Form (Flüssigdünger) eingesetzt.
Mineraldünger haben einen großen Produktivitätsfortschritt in der Landwirtschaft ermöglicht und werden heute sehr häufig eingesetzt. Problematisch sind einige der meist synthetischen anorganischen Dünger zum Beispiel in Anbetracht des hohen Energieaufwandes bei der Herstellung. In der Anwendung spielt die Wasserlöslichkeit eine große Rolle. Im Vergleich dazu führen organische Dünger mit entsprechenden Anbaumethoden zu einem höheren Humusgehalt und zu einer höheren Bodenqualität (siehe Humus).[16][17][18]
Phosphate wurden zunächst über das Naturprodukt Guano zugeführt, werden jedoch heutzutage überwiegend aus dem Bergbau gewonnen. Der Rückgang bzw. das Zur-Neige-Gehen abbauwürdiger Phosphorvorkommen ist ein Nachhaltigkeitsproblem. Phosphaterze enthalten Schwermetalle wie Cadmium und Uran, die über mineralische Phosphatdünger auch in die Nahrungskette gelangen können.[19] Jährlich werden mit Phosphordünger in der deutschen Landwirtschaft u. a. ca. 160 Tonnen Uran ausgebracht.[20]
Stickstoffdünger sind Ammoniumnitrat, Ammoniumsulfat, Kaliumnitrat und Natriumnitrat. Sie werden meist aus Luftstickstoff hergestellt, zum Beispiel über das Haber-Bosch-Verfahren und Ostwaldverfahren. Die Herstellung von Stickstoffdünger ist sehr energieintensiv: Der gesamte Energiebedarf für die Düngung mit 1 Tonne Stickstoff einschließlich Herstellung, Transport und Ausbringung entspricht dem Energiegehalt von etwa 2 Tonnen Erdöl.[21]
Kalisalze werden im Salzbergwerk gewonnen, aufbereitet oder zu Kaliumsulfat umgesetzt. Die herkömmliche Kalidüngerherstellung verursacht große Mengen kochsalzhaltiger Ablaugen oder Deponien.
Gasförmiger Dünger
Die Düngung mit Kohlenstoffdioxid (CO2) ist wichtig im Unterglasgartenbau. Grund ist der durch den photosynthetischen Verbrauch entstehende CO2-Mangel bei ungenügendem Nachschub an Frischluft, besonders im Winter bei geschlossener Lüftung. Pflanzen benötigen Kohlenstoff als Grundsubstanz.[22]
Das Kohlenstoffdioxid wird entweder als Flüssiggas zugekauft oder als Verbrennungsprodukt aus Propan oder Erdgas eingebracht (Kopplung von Düngung und Heizung). Die mögliche Ertragssteigerung ist abhängig davon, wie stark der Mangel an CO2 ist und wie hoch das Lichtangebot für die Pflanzen ist.
Organischer Dünger


Bei den organischen Düngern sind die düngenden Bestandteile meist an kohlenstoffhaltige Verbindungen gebunden. Sind diese bereits wie etwa im Kompost teilweise oxidiert, so sind die düngenden Mineralien an den Abbauprodukten (Huminsäuren) etc. adsorbiert. Somit entfalten sie ihre Wirkung langzeitiger und werden in der Regel weniger schnell ausgewaschen als mineralische Dünger. Organische Dünger sind meist Abfallstoffe aus der Landwirtschaft (Wirtschaftsdünger).[23] Dazu gehören vor allem Gülle und Stallmist. Daneben wird häufig aber auch Klärschlamm verwendet.
Eine Kennzahl für die Wirkgeschwindigkeit ist das Verhältnis zwischen Kohlenstoff und Stickstoff: der C/N-Quotient. Organische Dünger sind normalerweise tierischen oder pflanzlichen Ursprungs, können aber auch synthetisiert werden.
| N | P2O5 | K2O | CaO | MgO | |||
|---|---|---|---|---|---|---|---|
| gesamt | im 1. Jahr wirksam | ||||||
| Rindermist | kg/t | 5 | 2 | 3 | 7 | 4 | 2 |
| Schweinemist | 8 | 3 | 8 | 5 | 7 | 2 | |
| Hühnertrockenmist | 30 | 21 | 20 | 15 | 40 | 4 | |
| Putenmist | 20 | 11 | 23 | 23 | 0 | 5 | |
| Hähnchenmist | 24 | 15 | 21 | 30 | 0 | 6 | |
| Pferdemist | 4 | 2 | 3 | 11 | 0 | 1 | |
| Champignonsubstrat | 9 | <1 | 9 | 14 | 27 | 3 | |
| Biogassubstrat (Mais/Gülle) | 5 | 2 | 2 | 4 | n.n. | n.n. | |
| Biogassubstrat (Pellets) | 25 | 9 | 30 | 55 | 25 | 15 | |
| Feinkompost (Laub und Grünschnitt) | 6 | <1 | 2 | 4 | 6 | 1 | |
Düngerverbrauch
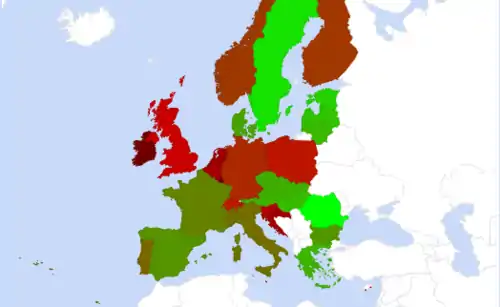
Der weltweite Verbrauch an Düngemitteln betrug 1999 141,4 Mio. Tonnen.[25]
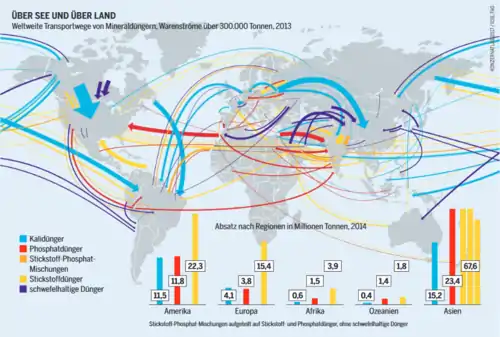
Die größten Verbraucher-Länder waren (2012 in Mio. Tonnen):
| China | 36,7 |
| Vereinigte Staaten: | 19,9 |
| Indien: | 18,4 |
| Brasilien: | 5,9 |
| Frankreich: | 4,8 |
| Deutschland: | 3,0 |
| Pakistan: | 2,8 |
| Indonesien: | 2,7 |
| Kanada: | 2,6 |
| Spanien: | 2,3 |
| Australien: | 2,3 |
| Türkei: | 2,2 |
| England: | 2,0 |
| Vietnam: | 1,9 |
| Mexiko: | 1,8 |
| Niederlande: | 1,4 |
Diese Zahlen geben keinen Aufschluss über den Pro-Kopf- bzw. Pro-Hektar-Verbrauch. Dieser kann jedoch für ausgewählte Staaten und Regionen aus der Grafik abgelesen werden.
In Deutschland beträgt der Inlandsabsatz an Düngemittel wie folgt:
| Düngemittelsorte | Tonnen Nährstoff | 1993/1994[26] | 2000/2001[27] | 2010/2011[28] | 2020/2021[29] |
|---|---|---|---|---|---|
| Stickstoff-Dünger, insgesamt | N | 1.612.215 | 1.847.581 | 1.786.485 | 1.265.477 |
| Kalkammonsalpeter | N | 992.752 | 896.647 | 728.379 | 476.836 |
| Ammonnitrat, Harnstoff-Lösung | N | 205.690 | 231.793 | 199.730 | 133.395 |
| Harnstoff | N | 162.809 | 292.056 | 377.326 | 172.636 |
| Andere Einnährstoffdünger | N | 31.934 | 206.676 | 325.389 | 380.299 |
| NP-Dünger | N | 54.404 | 64.819 | 76.514 | 52.237 |
| NK- und NPK-Dünger | N | 164.626 | 153.590 | 79.147 | 49.074 |
| Phosphat-Dünger, insgesamt | P2O5 | 415.433 | 351.337 | 286.348 | 192.182 |
| Superphosphat | P2O5 | 29.981 | 28.545 | 19.569 | 21.626 |
| Andere Phosphatdünger | P2O5 | 19.934 | 9.637 | 9.092 | 4.207 |
| PK-Dünger | P2O5 | 80.565 | 57.598 | 29.026 | 16.779 |
| NP-Dünger | P2O5 | 137.164 | 131.863 | 169.282 | 111.014 |
| NPK-Dünger | P2O5 | 147.789 | 123.694 | 59.379 | 38.556 |
| Kali-Dünger, insgesamt | K2O | 644.700 | 544.017 | 433.743 | 446.396 |
| Kalirohsalz | K2O | 27.493 | 11.809 | 11.823 | 5.202 |
| Kaliumchlorid | K2O | 286.771 | 248.455 | 253.021 | 333.068 |
| Kaliumsulfat | K2O | 19.257 | 21.929 | 26.735 | 27.596 |
| PK-Dünger | K2O | 127.425 | 95.023 | 59.120 | 32.860 |
| NK- und NPK-Dünger | K2O | 183.754 | 166.801 | 83.044 | 47.670 |
| Kalk-Dünger, insgesamt | CaO | 1.560.338 | 2.171.061 | 2.074.889 | 2.673.260 |
| Kohlensaurer Kalk | CaO | 1.087.003 | 1.529.578 | 1.483.359 | 2.065.800 |
| Branntkalk | CaO | 120.861 | 112.277 | 66.880 | 74.455 |
| Konverterkalk | CaO | 115.656 | 151.510 | 185.445 | 185.859 |
| Andere Kalkdünger | CaO | 236.818 | 377.696 | 339.205 | 347.146 |
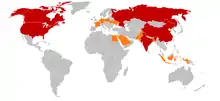
Die größten Düngerproduzenten
Das bedeutendste Herstellerland stickstoffhaltiger Düngemittel ist China, gefolgt von Indien und den USA. In Europa sind die wichtigsten Produzenten Russland und Ukraine, gefolgt von Polen, Niederlande, Deutschland und Frankreich.
| Rang | Land | Produktion (in Mio. t) |
Rang | Land | Produktion (in Mio. t) |
|---|---|---|---|---|---|
| 1 | China | 23,6 | 9 | Ägypten | 1,5 |
| 2 | Indien | 10,6 | 10 | Saudi-Arabien | 1,3 |
| 3 | USA | 9,4 | 11 | Polen | 1,2 |
| 4 | Russische Föd. | 6,0 | 12 | Bangladesch | 1,1 |
| 5 | Kanada | 3,8 | 13 | Niederlande | 1,1 |
| 6 | Indonesien | 2,9 | 14 | Deutschland | 1,0 |
| 7 | Ukraine | 2,3 | 15 | Frankreich | 1,0 |
| 8 | Pakistan | 2,2 |
Man nimmt an, dass der weltweite Markt für Düngemittel bis zum Jahr 2019 ein Volumen von über 185 Milliarden US-Dollar erreicht haben wird.[10]
Nährstoffaufnahme

Nährstoffaufnahme der Pflanzen
Bei der Nährstoffaufnahme aus dem Boden ist zwischen der Ernährung von Sommer- und Winterarten sowie von mehrjährigen Pflanzen zu unterscheiden:
- Bei Sommerarten (z. B. Kartoffeln) steigt der Bedarf an Nährstoffen nach dem Auflaufen je nach der Länge der Wachstumszeit schnell bis zu einem bestimmten Punkt vor der Reife an und fällt dann ab oder hört ganz auf.
- Bei Winterarten (z. B. Wintergetreide oder -raps) unterbricht die winterliche Wachstumsruhe (Frost) die Nährstoffaufnahme.
- Mehrjährige Pflanzen mit ausdauernden unterirdischen Organen, z. B. Gräser, Kleearten, Hopfen und Wein, speichern in den Wurzeln Nährstoffe und beschleunigen mit diesen Reservestoffen die Entwicklung im folgenden Frühjahr.
Nährstoffaufnahme aus der Bodenlösung
Die Pflanze nimmt die Nährstoffe über die Wurzeln aus der wässrigen Bodenlösung auf. Die meisten Nährstoffe liegen in der Bodenlösung als elektrisch geladene Teilchen (Ionen) vor. Zusätzlich können im Boden vorliegende Pflanzennährstoffe wie Eisen, Mangan, Kupfer und Zink mit organischen Stoffen wasserlösliche Chelatverbindungen eingehen und in dieser Form von den Pflanzen aufgenommen werden. Von den 16 unentbehrlichen Elementen deckt die Pflanze ihren Bedarf an Kohlenstoff, Wasserstoff und Sauerstoff vorrangig aus dem Kohlenstoffdioxid der Luft und Wasser aus dem Boden. Es werden aber auch (beispielsweise aus mit anorganischen Schadstoffen belasteten Böden) für Mensch und Tier giftige Metallionen in die Pflanzen eingelagert (z. B. Cadmium). Ein Pflanzennährstoff wird verstärkt von den Wurzeln aufgenommen und in den Pflanzenorganen über den Bedarf hinaus angereichert (Luxuskonsum), wenn er durch starke Mineralisierung (z. B. Stickstofffreisetzung in humosen Böden) oder einseitig hohe Düngergaben in größeren Mengen in der Bodenlösung enthalten ist. Die mengenmäßige Nährstoffaufnahme der Pflanze hängt von der Leistung der Wurzelatmung ab. Leicht erwärmbare Böden bieten mit günstigem Luft-Wasser-Haushalt im Krumenbereich die besten Bedingungen für die Aufnahme.
Nährstoffaufnahme durch das Blatt
Auch die Blätter können Wasser und die darin gelösten Nährstoffe durch Kleinporen aufnehmen. Theoretisch könnte man die Pflanze vollständig durch die Blätter ernähren. Im integrierten Pflanzenbau gewinnt die gezielte Mineralstoffzufuhr (Spritz- oder Sprühverfahren) in bestimmten Wachstumsabschnitten mit verdünnten Düngersalzlösungen als Blattdüngung zunehmende Bedeutung. Durch die Blattdüngung wird mit geeigneten Ausbringungsgeräten ein mengenmäßig geringer, aber hochwirksamer Mineralstoffbelag auf die grünen Pflanzenteile aufgebracht. Seit Jahren bewährt sich im praktischen Anbau vorrangig die ergänzende Versorgung mit Stickstoff, Magnesium und Spurenmineralstoffen durch das Blatt. Der Vorteil dieses Verfahrens einer gezielten Nährstoffzufuhr besteht im hohen Ausnutzungsgrad, der Nachteil in der nur begrenzt möglichen Mineralstoffmenge mit einer Gabe. Um entwicklungshemmende Blattverbrennungen zu vermeiden, sind bei der Blattdüngung die richtige Konzentration der Lösung und eine Rücksichtnahme auf empfindliche Wachstumsperioden des Pflanzenbestandes zu beachten. Blattdüngung erfolgt heute vorrangig, wenn eine kurzfristige Nährstoffsbedarfsdeckung in einem bestimmten Wachstumsstadium notwendig ist, die aus der Boden-Nachlieferung nicht ohne weiteres zu befriedigen ist (N-Spätdüngung bei Weizen, P-Zufuhr zu Mais oder Behebung plötzlich auftretender Nährstoffmangelerscheinungen z. B. durch Bor-Spritzung gegen Herz- und Trockenfäule bei Zuckerrüben). (Siehe hierzu auch den Abschnitt Stoffaustausch über die Oberfläche im Artikel Blatt.)
Vorteile des Düngens
Das Minimumgesetz der Pflanzenernährung besagt, dass das genetische Ertragspotential einer Nutzpflanze durch das Hauptnährelement begrenzt wird, das nicht in ausreichender Menge zum Bedarfszeitpunkt der Pflanzen zur Verfügung steht. Der erforderliche Düngebedarf wird in aller Regel durch Bodenuntersuchungen und Düngefenster festgestellt. Bei Unterernährung der Pflanzenbestände kommt es zu Mangelerscheinungen mit Mindererträgen und gelegentlich sogar zum Totalverlust eines Nutzpflanzenbestandes.
Nachteile des Düngens
Wird mehr Dünger als benötigt ausgebracht, führt dies zur Belastung von Grundwasser und Oberflächenwasser. Auch wird darauf verwiesen, dass stark gedüngte Kulturen einen höheren Wassergehalt haben können und das Verhältnis von Kohlenhydraten zu Vitaminen und Mineralstoffen ungünstiger sei, wenngleich dies überwiegend eine Frage der angebauten Pflanzenart ist.
Im Boden wandeln Bakterien Stickstoffverbindungen in Lachgas (N2O) um – ein 300-mal potenteres Treibhausgas als Kohlendioxid (CO2).[31] Für den menschengemachten Lachgasausstoß ist vor allem der Einsatz von stickstoffhaltigen Düngemitteln in der Landwirtschaft verantwortlich.[32][33]
Zugleich mit Phosphatdünger gelangt Uran in die Böden und ausgewaschen ins Trinkwasser. Auf deutschen Böden landen insgesamt 100 Tonnen Uran pro Jahr. Laut Bundesforschungsamt für Landwirtschaft (Julius Kühn-Institut) beträgt der Uraneintrag im Mittel 15,5 g Uran pro Hektar.[34] Bei Bodenuntersuchungen an 1000 Standorten fand sich in ackerbaulich genutzten Flächen gegenüber Forstböden eine Anreicherung um im Mittel 0,15 mg Uran/kg. Ein Hinweis auf die „schleichende Anreicherung von Uran“ im Ackerboden.[35]


auf einem Blatt
Bei zu starker Ausbringung von Düngern besteht die Gefahr, dass der Boden überdüngt und damit die Bodenfauna nachteilig verändert wird, was wiederum zu Lasten der Erträge und der Qualität der Ernte geht. In Extremfällen kann es zur Abtötung der Pflanzen durch Plasmolyse kommen.
Die negative Folge für die Umwelt (Eutrophierung) muss unterschieden werden von den negativen Folgen einer Überdüngung auf die Qualität der erzeugten Produkte für die menschliche und die Tierernährung bereits vor dem Rückgang der Erträge: Insbesondere durch hohe Stickstoffgaben kommt es auch in den Pflanzen zu einer hohen Nitratkonzentration. Diese Nitrate werden im Darm von Mensch und Tier zu gesundheitlich nachteiligen Nitriten reduziert. In nicht frischem überdüngtem Gemüse sowie bereits im Boden bilden sich Nitrite als Zwischenstufe bei der Oxidation der Bestandteile von Stickstoffdünger, Gülle oder anderen stickstoffhaltigen Stoffen.
Überdies werden die nicht von den Pflanzen aufgenommenen Düngerbestandteile in das Grundwasser ausgeschwemmt und können dadurch dessen Qualität gefährden. Zudem führt Niederschlagswasser auf den gedüngten Böden, wenn es in Oberflächengewässer gelangt, zu einem Überangebot an Nährstoffen (Eutrophierung), was zu Algenblüten führen kann und so Sauerstoffmangel im Tiefenwasser von Seen verursacht.
Dieses Problem besteht vor allem in Gebieten intensiver landwirtschaftlicher Nutzung mit hohem Viehbesatz (z. B. im Münsterland und in Südwestniedersachsen) und stellt die Wasserversorgung dort vor erhebliche Probleme. Zweck des Ausbringens von Gülle und Mist ist hier weniger die Steigerung des Ertrags, als eine Entsorgung der tierischen Exkremente in den Mastbetrieben.
Werden die Kulturen zu stark gedüngt, können die Erträge sinken. Es gilt also die Pflanzen optimal mit Nährstoffen zu versorgen. Anhand der Bodenuntersuchungen, die Landwirte vornehmen lassen, kann die Düngung an die Bedürfnisse der jeweiligen Kulturpflanze angepasst werden. Auch eine Düngeranalyse ist dazu sinnvoll.
Düngungseinfluss auf den Boden
Die Bestandteile des Düngers haben folgende Einflüsse auf den Boden:
- Stickstoff: Förderung des Bodenlebens
- Phosphor: Förderung der Krümelbildung; Bodenstabilisator; Brücken zwischen Humusteilchen
- Kalium: K+ Ionen wirken in hoher Konzentration krümelzerstörend, weil sie Ca2+-Ionen verdrängen (Antagonismus)
- Magnesium: Wie Ca, Förderung der Krümelstabilität durch Verdrängung der Hydroniumionen von Austauscherplätzen
- Calcium: Stabilisiert Krümelstruktur/Förderung des Bodenlebens/pH-Regulierung
- Schwefel: Förderung des Bodenlebens
Einflüsse auf chemische und physikalische Bodeneigenschaften
Einige Düngemittel (insbesondere N-Düngemittel) tragen zur Bodenversauerung bei. Dies kann ohne Ausgleichsmaßnahme zu einer Beeinträchtigung der Strukturverhältnisse im Boden führen. Durch planvolle Düngungsmaßnahmen (z. B. Kalkung) kann jedoch einem Absinken des pH-Wertes entgegengewirkt werden, so dass nachteilige Auswirkungen auf Nährstoffdynamik, Bodenlebewesen und Bodenstruktur nicht zu befürchten sind.
Tonminerale im Boden sind negativ geladen und können positiv geladene Teilchen binden (z. B. Kalium [K+]- oder Ammonium [NH4+]-Ionen, Ammonium-Fixierung in tonigen bindigen Böden), wodurch die Stickstoff-Verfügbarkeit nach einer Düngemittelgabe eingeschränkt werden kann. Die Bindung ist reversibel.
Einfluss auf Bodenlebewesen
Die Absenkung des pH-Wertes und eine überhöhte Salzkonzentration können das Bodenleben beeinträchtigen. Außerdem geht mit steigender N-Düngung die Aktivität N-bindender Bakterien zurück. Insgesamt fördert eine ausreichende Bodenversorgung mit organischen und mineralischen Düngern die Menge und Vielfalt der Bodenlebewesen. Diese beeinflussen entscheidend die Bodenfruchtbarkeit. Bei ordnungsgemäßer mineralischer Düngung bleibt die Regenwurmdichte weitgehend stabil. Durch wirtschaftseigene organische Dünger wird der Regenwurmbesatz gefördert.
Bei einer 21-jährigen Studie wurde zusammenfassend festgestellt: „Um die Effektivität landwirtschaftlicher Anbausysteme zu beurteilen, bedarf es eines Verständnisses der Agrarökosysteme. Eine 21-jährige Studie ergab 20 Prozent geringere Erträge bei ökologischen Anbausystemen gegenüber konventionellen, obgleich der Einsatz von Düngemitteln und Energie um 34 bis 53 % und der von Pestiziden um 97 % geringer war. Wahrscheinlich führen die erhöhte Bodenfruchtbarkeit und die größere biologische Vielfalt in den ökologischen Versuchsparzellen dazu, dass diese Systeme weniger auf Zufuhr von außen angewiesen sind“.[36]
Anreicherung mit Metallen
Über die Anreicherung des Bodens mit Schwermetallen durch mineralische Düngung gibt es zahlreiche Untersuchungen. Von den in der Landwirtschaft und im Gartenbau verwendeten Mineraldüngern enthalten viele Phosphatdünger einen natürlichen Gehalt an Uran[37] und Cadmium. Diese Schadstoffe können sich im Boden anreichern und auch in das Grundwasser gelangen.[38]
Die Folgen der Verwendung von Phosphatdünger und der Zusammenhang erhöhter Urangehalte in Mineral- und Trinkwässern mit der Geologie der Grundwasserspeichergesteine wurden im Jahr 2009 erstmals bundesweit untersucht.[39] Dabei stellte sich heraus, dass erhöhte Urangehalte vorwiegend an Formationen wie Buntsandstein oder Keuper gebunden sind, die selbst geogen erhöhte Urangehalte aufweisen. Allerdings sind örtlich auch bereits Urangehalte aus landwirtschaftlicher Phosphatdüngung in das Grundwasser durchgeschlagen. Denn Rohphosphate enthalten 10–200 mg/kg Uran, das sich im Aufbereitungsprozess zum Dünger zu noch höheren Konzentrationen anreichert. Bei der üblichen Düngung mit mineralischem Phosphatdünger führt dies zu jährlichen Einträgen von 10–22 g Uran pro Hektar. Organische Düngemittel wie Gülle und Mist (Wirtschaftsdünger) weisen niedrigere Urangehalte von häufig unter 2 mg/kg und dementsprechend geringe Uran-Einträge auf. Der Urangehalt von Klärschlamm liegt zwischen diesen Extremen. Über Wirtschaftsdünger können jedoch, auf Grund von Futtermittelzusatzstoffen, die Schwermetalle Zink und Kupfer in intensiv genutzten Böden angereichert werden[40].
Zu einer unerwünschten Anreicherung mit Metallen kann auch langjährige, intensive Düngung mit Sekundärrohstoffen führen. Aus diesem Grunde müssen bei Klärschlammausbringung auf landwirtschaftliche Flächen sowohl der Klärschlamm als auch der Boden untersucht werden. Die Einflüsse der Düngung auf die chemischen und physikalischen Bodeneigenschaften sind durch bestimmte acker- und pflanzenbauliche Maßnahmen korrigierbar. Im Vergleich dazu ist eine Anreicherung mit Metallen unveränderbar, da Metalle kaum ausgewaschen werden und der Entzug durch die Pflanzen nur gering ist. Durch zu hohe Metallgehalte im Boden wird die Bodenfruchtbarkeit langfristig geschädigt.
Düngungseinfluss auf das Wasser
.jpg.webp)
Eine Verschlechterung der Wassergüte durch Düngung kann erfolgen bei:
- Nitratanreicherung des Grundwassers durch N-Auswaschung,[41]
- Mineralstoffanreicherung, insbesondere Phosphatanreicherung, in Oberflächengewässern z. B. durch Abschwemmung von Boden (Bodenerosion, mit der Folge einer Eutrophierung des Gewässers)
Nitratbelastung des Grundwassers
Nitrat (NO3−) ist im Trinkwasser unerwünscht, weil es unter bestimmten Umständen in das gesundheitlich bedenkliche Nitrit umgewandelt wird. Es kann mit sekundären Aminen (Ammoniakbase), die in der Nahrung vorkommen oder bei der Verdauung entstehen, Nitrosamine bilden. Von diesen zählen einige zu den krebserregenden Stoffen. Um die gesundheitlichen Risiken weitgehend auszuschließen, sollen die Nitratgehalte im Trinkwasser möglichst niedrig sein. Der Grenzwert für den Nitratgehalt im Trinkwasser wurde 1991 mit der EG-Richtlinie 91/676/EWG auf 50 mg NO3−/Liter festgesetzt. Dieser Grenzwert kann bei unsachgemäßer Düngung, insbesondere auf leichten, durchlässigen Böden überschritten werden. Grundwasser enthält von Natur aus meistens weniger als 10 mg NO3−/Liter. Als Ursache für die in der Nachkriegszeit z. T. stark angestiegenen Nitratgehalte sind u. a. zu nennen:
- Dichtere Besiedlung mit zunehmenden Abwassermengen aus Haushaltungen, Gewerbe und Industrie und Mängel in der Abwasserkanalisation.
- Intensive landwirtschaftliche Bodennutzung; hier sind wirtschaftseigene Dünger (Gülle, Jauche) kritischer zu werten als Mineraldünger, da sie oftmals nicht so gezielt wie Mineraldünger eingesetzt werden und damit der Stickstoffausnutzungsgrad schlechter ist. Hinzu kommt, dass regional durch Aufstockung der Tierbestände, u. U. auch durch Konzentration der Tierhaltung, das Problem der Nitratauswaschung verschärft wurde. Allerdings ist die N-Auswaschung, festzustellen mit Lysimeteranlagen oder Tiefbohrungen, nicht automatisch eine Folge steigender Düngemengen. Die angewendeten Düngemengen sind in den letzten Jahren deutlich zurückgegangen. Die Ursache ist vielmehr in der unsachgemäßen Anwendung von Düngern zu suchen.
Folgende Maßnahmen zur Verminderung der Nitratbelastung sind zu empfehlen:
- N-Vorrat des Bodens bei der Düngung berücksichtigen. Im Frühjahr können je nach Fruchtfolge, Bodenart, Bodentyp, organischer Düngung und Herbst- bzw. Winterwitterung sehr unterschiedliche Mengen an mineralisiertem, d. h. pflanzenverfügbarem Stickstoff, im Boden vorhanden sein. Sie können durch die Nmin-Methode erfasst und bei der Ermittlung des N-Düngebedarfs berücksichtigt werden.
- N-Mengen dem Mineralstoffbedarf der Pflanzen anpassen. Überdüngung bei Sonderkulturen, wie Wein, Hopfen und Gemüse, aber auch bei anspruchsvollen Ackerfrüchten wie Mais, vermeiden.
- Düngung zur rechten Zeit und wenn nötig Aufteilung der Düngemenge in Teilgaben
- Gezielter Einsatz der Wirtschaftsdünger
- N-Bindung durch möglichst ganzjährigen Pflanzenbewuchs, damit der durch die Vorfrucht nicht verbrauchte sowie der durch Mineralisierung freigesetzte Stickstoff biologisch gebunden wird. So soll bei hohen N-Spätdüngungsgaben zur Erzeugung von Qualitätsweizen oder beim Anbau von Körnerleguminosen durch pflanzenbauliche Maßnahmen, wie Fruchtfolgegestaltung, Zwischenfruchtanbau oder Strohdüngung, die N-Auswaschung vermindert werden.
- Umbruch von mehrjährigen Futterschlägen mit Leguminosen (Kleegras, Luzernegras) nicht im Herbst, sondern im Frühjahr vornehmen.
Phosphatbelastung der Oberflächengewässer

Eutrophierung bezeichnet einen Zustand von stehenden Gewässern, der durch hohen Nährstoffgehalt und ein dadurch verursachtes üppiges Auftreten von Wasserpflanzen und Algen gekennzeichnet ist. Meistens ist die Eutrophierung durch hohe Phosphatzufuhr bedingt, da Phosphat natürlicherweise in Oberflächengewässer kaum vorhanden ist. Eine starke P-Zufuhr steigert das Wachstum von Algen und Wasserpflanzen. Der Abbau der abgestorbenen Algen- und Pflanzenmasse verbraucht übermäßig viel Sauerstoff des Wassers. Deshalb kann es infolge Sauerstoffmangels zum Fischsterben kommen.
Phosphate gelangen in Oberflächengewässer durch
- Abwasser aus dem Siedlungsbereich (Waschmittel); jedoch besitzen viele Kläranlagen inzwischen eine Reinigungsstufe zur Phosphorelimination
- Auswaschung von Phosphat bzw. Abschwemmung von Boden und Düngern
Da Düngerphosphat meist im Boden gebunden wird, kann die Auswaschung von Phosphat auf Lehm- und Tonböden praktisch vernachlässigt werden. Anders ist die P-Abschwemmung zu bewerten:
- im Zusammenhang mit dem Bodenabtrag durch Wassererosion
- bei unsachgemäßem Einsatz von wirtschaftseigenen Düngern
Hier kann es schnell zu erheblichen Zufuhren an P in die Gewässer kommen.
Düngungseinfluss auf die Luft
.jpg.webp)
Nach der Ausbringung organischer (Stallmist, Gülle) und anorganischer (Mineraldünger) Dünger können erhebliche gasförmige Stickstoffverluste als Ammoniak auftreten.
Organische Dünger
Die Höhe der Ammoniakverluste ist von der Art und Zusammensetzung des organischen Düngers, dessen Behandlung, wie z. B. Einarbeitung in den Boden, und von der Witterung bei der Ausbringung abhängig. Folgende Reihenfolge bei der Höhe der Ammoniakverluste ergibt sich hinsichtlich
- der Art der Wirtschaftsdünger: Tiefstallmist < Rottemist < Normalgülle (Schweinegülle < Rindergülle) < Biogasgülle bzw. Frischmist;
- des TS- (Trockensubstanz-) Gehaltes: wasserreiche Gülle < Gülle mit hohem TS-Gehalt
In Abhängigkeit vom TS-Gehalt der Gülle, dem Zeitpunkt der Einarbeitung, der Tierart und der Witterung ist mit Verlusten von ca. 1 % (bei Gülle-Injektion) und nahezu 100 % (Stoppelgabe ohne Einarbeitung) des in der Gülle vorhandenen Ammoniumstickstoffs zu rechnen. Neben der Art der Lagerung und Ausbringung hat der Zeitpunkt der Einarbeitung großen Einfluss auf die Höhe der Verluste. Sofortige Einarbeitung mindert die Ammoniakverluste ganz erheblich.
Mineralischer Feststoffdünger
Die Ammoniakverluste stickstoffhaltiger Mineraldünger steigen wie folgt: Kalkammonsalpeter < Mehrnährstoffdünger < Diammonphosphat < Harnstoff < Kalkstickstoff < Ammoniumsulfat.
An den gesamten Ammoniakstickstoffverlusten der Landwirtschaft ist der Anteil der mineralischen Dünger gering.
Siehe auch
Literatur
- Johannes Kotschi, Kathy Jo Wetter: Düngemittel: Zahlende Konsumenten, intrigante Produzenten. In: Heinrich-Böll-Stiftung, u. a.(Hrsg.): Bodenatlas. Daten und Fakten über Acker. Land und Erde, Berlin 2015, S. 20–21.
- Arnold Finck: Dünger und Düngung – Grundlagen und Anleitung zur Düngung der Kulturpflanzen. Zweite, neubearbeitete Auflage. VCH, Weinheim; New York; Basel; Cambridge 1992, ISBN 3-527-28356-0, S. 488.
- Sven Schubert: Pflanzenernährung – Grundwissen Bachelor. Verlag Eugen Ulmer, Stuttgart, ISBN 3-8252-2802-9.
- Günther Schilling: Pflanzenernährung und Düngung (= UTB. Band 8189). Ulmer, Stuttgart (Hohenheim) 2000, ISBN 3-8252-8189-2.
- Udo Rettberg: Alles, was sie über Rohstoffe wissen müssen. Erfolgreich mit Kaffee, Gold & Co. FinanzBuch-Verlag, München 2007, ISBN 978-3-89879-309-4.
Weblinks
Einzelnachweise
- Müfit Bahadir, Harun Parlar, Michael Spiteller: Springer Umweltlexikon. Springer-Verlag, 2013, ISBN 978-3-642-97335-2, S. 301 (eingeschränkte Vorschau in der Google-Buchsuche).
- Guido A. Reinhardt: Energie- und CO2-Bilanzierung Nachwachsender Rohstoffe Theoretische Grundlagen und Fallstudie Raps. Springer-Verlag, 2013, ISBN 978-3-322-84192-6, S. 78 (eingeschränkte Vorschau in der Google-Buchsuche).
- Hartmut Bossel: Umweltwissen Daten, Fakten, Zusammenhänge. Springer-Verlag, 2013, ISBN 978-3-642-95714-7, S. 165 (eingeschränkte Vorschau in der Google-Buchsuche).
- Nährstoffe, private Website des verstorbenen Agrarjournalisten Rainer Maché.
- Arnold Finck: Dünger und Düngung – Grundlagen und Anleitung zur Düngung der Kulturpflanzen 1992.
- Jonas Stoll: Düngemittel. 27. Mai 2013, abgerufen am 15. Februar 2019.
- Alfons Deter: 13.000 t Plastik pro Jahr landen in unseren Böden. In: topagrar.com. 1. Juni 2021, abgerufen am 1. Juni 2021.
- Düngemittelverordnung (DüMV) auf juris.
- Elisabeth Bjørsvik: The Ticcih Section for hydroelectricity and the electrochemical industry: Industrial heritage in Norway as an example. In: Le patrimoine industriel de l’électricité et de l’hydroélectricité. Hrsg. Denis Varaschin und Yves Bouvier, Universität Savoyen, Dezember 2009, ISBN 978-2-915797-59-6, S. 112–115.
- Ceresana: Marktstudie Düngemittel, Mai 2013.
- Verordnung (EG) Nr. 2003/2003 (PDF) über Düngemittel.
- Richtlinie 91/676/EWG (PDF) (Nitratrichtlinie).
- Düngeverordnung (DüV); im Juni 2017 durch neue Vorschrift ersetzt.
- Düngeverordnung (DüV); seit Juni 2017 geltende Neufassung.
- Agriculture, forestry and fishery statistics — 2020 edition. (PDF; 16,1 MB) Eurostat, 17. Dezember 2020, abgerufen am 19. Dezember 2020 (englisch).
- Christine von Buttlar, Marianne Karpenstein-Machan, Roland Bauböck: Anbaukonzepte für Energiepflanzen in Zeiten des Klimawandels Beitrag zum Klimafolgenmanagement in der Metropolregion Hannover-Braunschweig-Göttingen-Wolfsburg. ibidem-Verlag / ibidem Press, 2014, ISBN 978-3-8382-6525-4 (eingeschränkte Vorschau in der Google-Buchsuche).
- Organische Düngung und reduzierte Bodenbearbeitung als Steuerungsfaktoren für die C-, N-, P- und S-Speicherung von Mikroorganismen. kassel university press GmbH, 2010, ISBN 978-3-86219-033-1, S. 86 (eingeschränkte Vorschau in der Google-Buchsuche).
- Franz Schinner, Renate Sonnleitner: Bodenbewirtschaftung, Düngung und Rekultivierung. Springer-Verlag, 2013, ISBN 978-3-642-80184-6, S. 179 (eingeschränkte Vorschau in der Google-Buchsuche).
- Sylvia Kratz: Uran in Düngemitteln. (Memento vom 13. April 2014 im Internet Archive) (PDF) Uran-Umwelt-Unbehagen: Statusseminar am 14. Oktober 2004, Bundesforschungsinstitut für Landwirtschaft (FAL), Institut für Pflanzenernährung und Bodenkunde, 2004.
- Dethlev Cordts: Uran im Trinkwasser (Dokumentation) NDR, 45 min., November 2010.
- Eckhard Jedicke, Wilhelm Frey, Martin Hundsdorfer, Eberhard Steinbach (Hrsg.): Praktische Landschaftspflege. Grundlagen und Maßnahmen. 2. verbesserte und erweiterte Auflage. Ulmer, Stuttgart (Hohenheim) 1996, ISBN 3-8001-4124-8, S. 80.
- A. Fangmeier, H.-J. Jäger: Wirkungen erhöhter CO2-Konzentrationen. Institut für Pflanzenökologie der Justus-Liebig-Universität Gießen, 2001, abgerufen am 7. Mai 2014.
- Ulrich Gisi: Bodenökologie. Georg Thieme Verlag, 1997, ISBN 978-3-13-747202-5, S. 265 (eingeschränkte Vorschau in der Google-Buchsuche).
- Arbeitstagebuch 2014 der OVA Jork, S. 210.
- FAO
- Statistisches Bundesamt (Hrsg.): Düngemittelversorgung. Fachserie 4, Reihe 8.2, 1995 (statistischebibliothek.de).
- Statistisches Bundesamt (Hrsg.): Düngemittelversorgung. Fachserie 4, Reihe 8.2, 2001 (statistischebibliothek.de).
- Statistisches Bundesamt (Hrsg.): Düngemittelversorgung. Fachserie 4, Reihe 8.2, 2011 (statistischebibliothek.de).
- Statistisches Bundesamt (Hrsg.): Düngemittelversorgung. Fachserie 4, Reihe 8.2, 2001 (destatis.de [PDF]).
- Die Welt in Zahlen. In: Handelsblatt (2005)
- Atlant Bieri: Dünger für den Klimawandel. (168 kB; PDF) In: Medienmitteilung vom 4. Februar 2010 der Forschungsanstalt Agroscope Reckenholz-Tänikon (ART). Eidgenössisches Volkswirtschaftsdepartement EVD, S. 1, abgerufen am 7. September 2010: „im Boden wandeln beispielsweise Bakterien die Stickstoffverbindungen in Lachgas (N2O) um – ein 300-mal potenteres Klimagas als Kohlendioxid“.
- Jörg Staude: Lachgas heizt die Erde mittlerweile mit. In: Klimareporter.de. 10. Oktober 2020, abgerufen am 11. Oktober 2020 (deutsch).
- Eliza Harris et al.: Denitrifying pathways dominate nitrous oxide emissions from managed grassland during drought and rewetting. In: Sci. Adv. 2021, doi:10.1126/sciadv.abb7118 (uibk.ac.at [abgerufen am 7. Februar 2021]).
- Tickende Zeitbombe – Uran im Dünger, bei umweltinstitut.org
- Uran in Boden und Wasser, Claudia Dienemann, Jens Utermann, Umweltbundesamt, Dessau-Roßlau, 2012, S. 15.
- Paul Mäder, Andreas Fließbach, David Dubois, Lucie Gunst, Padruot Fried und Urs Niggli: Bodenfruchtbarkeit und biologische Vielfalt im ökologischen Landbau. ÖKOLOGIE & LANDBAU 124, 4/2002 orgprints.org (PDF; 300 kB).
- Uwe Leiterer: Giftiges Uran in Gartendüngern (Memento vom 11. Mai 2012 im Internet Archive), bei ndr.de
- Dünger: 16 Prozent enthalten zu viel Cadmium. In: schweizerbauer.ch. 21. Juli 2021, abgerufen am 21. Juli 2021.
- Friedhart Knolle: Ein Beitrag zu Vorkommen und Herkunft von Uran in deutschen Mineral- und Leitungswässern. 2009, abgerufen am 12. Februar 2010 (TU Braunschweig, Dissertation).
- Nationalen Bodenbeobachtung (NABO) 1985–2009. (PDF; 2,3 MB) Zustand und Veränderungen der anorganischen Schadstoffe und Bodenbegleitparameter. Agroscope, 2015, abgerufen am 29. Dezember 2020.
- Tamara Kolbe, Jean-Raynald de Dreuzy u. a.: Stratification of reactivity determines nitrate removal in groundwater. In: Proceedings of the National Academy of Sciences. 116, 2019, S. 2494, doi:10.1073/pnas.1816892116.
