Alkohole
Alkohole (arabisch الكحول, DMG al-kuḥūl) sind organische chemische Verbindungen, die eine oder mehrere an unterschiedliche aliphatische Kohlenstoffatome gebundene Hydroxygruppen (–O–H) besitzen.[1]

Der Unterschied zwischen Alkoholen und anderen Verbindungen mit OH-Gruppen (z. B. Enole, Halbacetale oder Carbonsäuren) als Teil der funktionellen Gruppe ist, dass in Alkoholen jedes Kohlenstoffatom, das eine OH-Gruppe trägt, sp3-hybridisiert sein muss und außer der Hydroxygruppe nur noch an Kohlenstoff- oder Wasserstoffatomen gebunden sein darf. Nur dieser Bindungszustand entspricht dem Oxidationszustand eines normalen Alkanols.[2]
Wenn die Hydroxygruppe an ein nicht-sp3-hybridisiertes Kohlenstoffatom gebunden ist, das Teil eines aromatischen Ringes ist, so werden diese Verbindungen als Phenole bezeichnet[3] und zählen nicht zu den Alkoholen.[4][5]
Während Alkohole schwächer sauer sind als Wasser und mit einem pKS-Wert von ca. 16 zu den „sehr schwachen Säuren“ zählen, gehören normale Phenole mit einem pKS-Wert von 10 bereits zu den „schwachen Säuren“.
Etymologie
Das Wort „Alkohol“ stammt vom arabischen „kuhl“ (arabisch: الكحل, romanisiert: al-kuḥl), einem Puder, das als Eyeliner verwendet wird. „Al-“ ist der arabische bestimmte Artikel, äquivalent zu „the“ im Englischen. Alkohol wurde ursprünglich für das sehr feine Pulver verwendet, das durch die Sublimation des natürlichen Minerals Stibnit zu Antimontrisulfid Sb2S3 entsteht. Es wurde als die Essenz oder den „Geist“ dieses Minerals betrachtet und als Antiseptikum, Eyeliner und Kosmetikum verwendet. Die Bedeutung von Alkohol wurde im Laufe der Zeit auf destillierte Substanzen im Allgemeinen ausgedehnt und dann wieder auf Ethanol eingeengt, als „Spiritus“ ein Synonym für harter Schnaps war.[6]
Bartholomäus Traheron führt in seiner Übersetzung von Giovanni da Vigo aus dem Jahr 1543 das Wort als erster als einen von „barbarischen“ Autoren verwendeten Begriff für „feines Pulver“ ein. Vigo schrieb: „the barbarous auctours use alcohol, or (as I fynde it sometymes wryten) alcofoll, for moost fine poudre.“ Arabische Chemiker verwendeten den Begriff al-kuhl auch für andere Substanzen wie Essenzen, die durch Destillation gewonnen wurden – eine Bedeutung, die erstmals im 17. Jahrhundert im englischen für Alkohol verwendet wurde.[6][7]
Das Lexicon Chymicum von William Johnson aus dem Jahr 1652 glossiert das Wort als antimonium sive stibium und bezog sich damit auf jede Flüssigkeit, die durch Destillation gewonnen wurde, einschließlich „Weinalkohol“, der destillierten Essenz von Wein.[8] Libavius in Alchymia (1594) bezieht sich auf vini alcohol vel vinum alcalisatum.[9] Johnson glossiert alcohol vini als quando omnis superfluitas vini a vino separatur, ita ut accensum ardeat donec totum consumatur, nihilque fæcum aut phlegmatis in fundo remaneat.[8] Die Bedeutung des Wortes wurde im 18. Jahrhundert auf „Weingeist“ (die heute als Ethanol bekannte Chemikalie) beschränkt. Doch noch im 18. Jahrhundert wurde Alkohol oft zuerst als Pulver feinster Form und erst in zweiter Linie als Weingeist definiert.[10] In der organischen Chemie wurde das Wort bis 1808 auf die Klasse der gleichartigen Verbindungen ausgedehnt (in einer Übersetzung von Lavoisiers „Elemente der Chemie“ von 1790 steht alkoholisches Gas für „die Verbindung von Alkohol mit Kalorik“).[11]
Nomenklatur und Einteilung
Der Name einfacher Alkohole ergibt sich als Zusammensetzung aus dem Namen des ursprünglichen Alkans und der Endung „-ol“. Zusätzlich wird die Position der OH-Gruppe durch eine vorangestellte Zahl verdeutlicht, zum Beispiel Propan-2-ol. Eine veraltete, bis 1957 gültige Bezeichnung für Alkohole ist – nach einem Vorschlag von Hermann Kolbe – Carbinole.[12]
Die Stoffgruppe der Alkohole wird nach verschiedenen Kriterien (Zahl der Nichtwasserstoffnachbarn, Wertigkeit, Vorhandensein von Doppel-/Dreifachbindungen und Kettenlänge) eingeteilt.
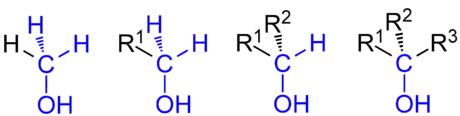
Zahl der Nichtwasserstoffnachbarn
Man unterscheidet Alkohole nach der Zahl der C- und H-Atome an dem C-Atom der funktionellen Gruppe, an das auch die Hydroxygruppe gebunden ist. Bei primären Alkoholen sind an dieses C-Atom neben einem C-Atom zwei H-Atome, bei sekundären Alkoholen neben zwei C-Atomen ein H-Atom und bei tertiären Alkoholen neben drei C-Atomen kein Wasserstoffatom gebunden. Ein Sonderfall ist der Alkohol mit nur einem C-Atom, das Methanol, das neben der Hydroxygruppe nur drei Wasserstoffatome am C-Atom der funktionellen Gruppe trägt.
Wertigkeit der Alkohole
Ist mehr als eine Hydroxygruppe an verschiedenen C-Atomen in einem Alkoholmolekül vorhanden, wird deren Anzahl durch Einfügen einer der Anzahl der Hydroxygruppen entsprechenden griechischen Silbe (-di-, -tri- usw.) vor der Endung -ol angegeben und man spricht von mehrwertigen Alkoholen. Ein Alkandiol ist das Ethan-1,2-diol (Trivialname Ethylenglycol), ein Alkantriol das Propan-1,2,3-triol (Trivialname Glycerin). Die Zahl vor der Endung -ol gibt die Position der funktionellen Gruppe(n) an. Dies gilt auch für einwertige Alkohole, zum Beispiel Propan-2-ol (Trivialname Isopropanol).
 Strukturformel des Ethanols
Strukturformel des Ethanols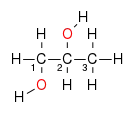 Strukturformel Propan-1,2-diol
Strukturformel Propan-1,2-diol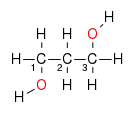 Strukturformel Propan-1,3-diol
Strukturformel Propan-1,3-diol
Doppel- bzw. Dreifachbindungen
In Bezug auf das Vorhandensein von Doppel- bzw. Dreifachbindungen in der Kette der C-Atome unterscheidet man Alkanole (abgeleitet von Alkanen), Alkenole (abgeleitet von Alkenen) und Alkinole (abgeleitet von Alkinen). Für den Fall, dass die OH-Gruppe an ein sp2-hybridisiertes Kohlenstoffatom gebunden ist, hat man es mit einem anderen Oxidationszustand und damit mit einer anderen Stoffgruppe zu tun, nämlich mit den meist instabilen Enolen.
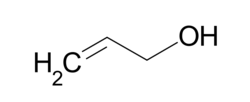 Strukturformel des Allylalkohols (2-Propen-1-ol)
Strukturformel des Allylalkohols (2-Propen-1-ol)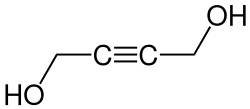 Strukturformel des Butindiols
Strukturformel des Butindiols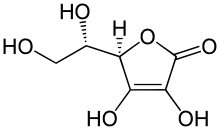 Strukturformel der Ascorbinsäure, eines Endiols
Strukturformel der Ascorbinsäure, eines Endiols
Kettenlänge
Über die Kettenlänge werden Alkohole ebenfalls unterschieden. Die Bezeichnung Fettalkohole verwendet man für Alkohole mit endständiger primärer –OH-Gruppe mit gerader Kette und einer Länge von sechs (Hexanol) bis hin zu 22 (Behenylalkohol) Kohlenstoffatomen.[13] Sie werden meist durch Reduktion der –COOH-Gruppe aus Fettsäuren gewonnen. Die höheren primären Alkohole mit 24 bis 36 Kohlenstoffatome bezeichnet man als Wachsalkohole.[14]
Physikalische Eigenschaften
Niedrigmolekulare Alkohole sind Flüssigkeiten, die einen charakteristischen Geruch und einen brennenden Geschmack besitzen. Höhere Alkohole sind meist feste Verbindungen mit nur schwach ausgeprägtem Geruch. Aufgrund von intermolekularen Wasserstoffbrückenbindungen besitzen die Alkohole im Vergleich zu Kohlenwasserstoffen gleicher Molekülmasse relativ hohe Schmelz- und Siedepunkte.[15] Wichtigstes gemeinsames Merkmal der Alkohole ist die Hydrophilie. Diese Eigenschaft nimmt mit zunehmender Länge des Alkylrestes ab und mit der Anzahl der Hydroxygruppen zu. Besonders die kurzkettigen Alkohole werden aufgrund ihres amphiphilen Charakters oft als Lösungsmittel verwendet.
Hohe Siedepunkte
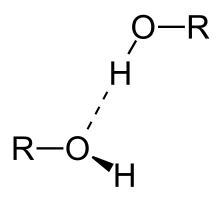
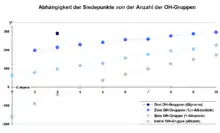
Sauerstoff ist elektronegativer als Wasserstoff und Kohlenstoff, d. h., er zieht Elektronen stärker an als diese. Das führt zu einer unsymmetrischen Verteilung der Elektronen entlang der C–O–H-Bindung, man spricht von einer polaren Bindung, es bildet sich ein molekularer Dipol aus. Diese Dipole können untereinander Wasserstoffbrückenbindungen ausbilden, die die Anziehung der einzelnen Moleküle untereinander drastisch verstärken. Dies führt für Alkohole zu relativ hohen Siedepunkten gegenüber den um eine Methyleneinheit verlängerten Homologen ihrer Stammverbindung, die eine annähernd gleiche molarer Masse besitzen. So hat beispielsweise das unpolare Ethan (C2H6) (M = 30) einen Siedepunkt von −89 °C, während Methanol (CH3OH) (M = 32) diesen erst bei 65 °C erreicht.
Zusammenfassend:
- Im Vergleich zu Alkanen mit einer vergleichbaren molaren Masse haben Alkohole einen höheren Schmelz- und Siedepunkt, da die Hydroxygruppe (OH-Gruppe) Wasserstoffbrückenbindungen ausbildet.
- Je mehr Hydroxygruppen ein Molekül aufweist, desto mehr Wasserstoffbrückenbindungen können ausgebildet werden und desto höher ist der Siedepunkt.
- Zwischen den Alkylresten bilden sich zusätzlich Van-der-Waals-Kräfte aus. Deswegen steigt der Siedepunkt mit der Länge des Alkylrestes
- Da die Stärke der Van-der-Waals-Wechselwirkungen nicht nur von der Größe des Alkylrestes, sondern auch von dessen Oberfläche abhängig ist, weisen stark verzweigte, eher kugelförmige Moleküle mit einer mittelständigen Hydroxygruppe einen niedrigeren Siedepunkt als unverzweigte, langgestreckte, primäre Alkohole auf.
Hydrophilie
Die OH-Gruppe ist ebenfalls in der Lage, Wasserstoffbrückenbindungen mit Wasser einzugehen. Sie erhöht damit die Hydrophilie, die Wasserlöslichkeit, der Verbindung. Organische Alkylreste selbst sind nicht wasserlöslich, also hydrophob. Die Wasserlöslichkeit sinkt daher mit der Größe des organischen Anteils und steigt mit der Zahl der Hydroxygruppen. Die Propanole und tert-Butanol sind bei Raumtemperatur noch in jedem Verhältnis mit Wasser mischbar, alle langkettigeren Alkohole lösen sich nur noch in zunehmend kleinen Mengen. Größere Mengen gelöster anorganischer Salze können auch bei den kurzkettigen Alkoholen eine Phasentrennung bewirken („Salzfracht“).
Zusammenfassend:
- Die Hydroxygruppe eines Alkohols ist aufgrund der ungleichen Ladungsverteilung polar. Somit ist die Fähigkeit derselben, auch zu ebenfalls polaren Wassermolekülen Wasserstoffbrückenbindungen ausbilden zu können, für die gute Löslichkeit vor allem kurzkettiger Alkohole verantwortlich.
- Je mehr Hydroxygruppen ein Alkohol aufweist, desto mehr Wasserstoffbrücken können diese mit dem Wasser ausbilden. Daher steigt mit wachsender Anzahl der hydrophilen Hydroxygruppen die Wasserlöslichkeit.
- Diesem Effekt wirkt allerdings der hydrophobe, also wasserabweisende, unpolare Alkylrest entgegen: Je länger er ist, desto geringer ist die Wasserlöslichkeit des Alkohols.
Acidität und Deprotonierung
Mit einem pKS-Wert (Säurestärke) von etwa 16 sind Alkohole schwächer sauer als Wasser und reagieren somit in wässriger Lösung näherungsweise neutral. Die Acidität von Alkoholen nimmt in der Reihe von Methanol über primäre, sekundäre und tertiäre Alkohole ab. Es ist möglich, Alkohole mit starken Basen wie z. B. Hydridanionen oder durch Reaktion mit Natrium unter Entwicklung von Wasserstoff zu deprotonieren. Die dabei entstehenden Alkoholate können dann als stark nucleophile Anionen für weitere Reaktionen eingesetzt werden.
Es ist auch möglich, Alkohole in gewissem Umfang mit starken Säuren zu protonieren:
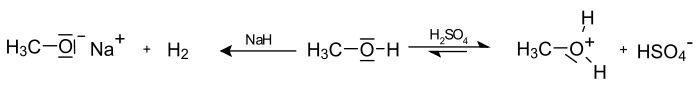
Spektroskopie
Im IR-Spektrum von Alkoholen ist deutlich die breite Bande der O–H-Valenzschwingung im Bereich von 3200–3650 cm−1 zu erkennen. Die Breite des Peaks wird durch Wasserstoffbrückenbindungen mit Wassermolekülen verursacht und ist in Spektren von wasserfreien Alkoholen in einem engeren Bereich von 3620–3650 cm−1 zu finden.
Chemische Eigenschaften
Reaktion mit konzentrierter Schwefelsäure
Unterhalb von 140 °C bildet sich der Ester der Schwefelsäure.
Bei etwa 140 °C findet die Kondensationsreaktion zu einem Ether statt.
Oberhalb von 170 °C werden primäre Alkohole zu Alkenen dehydratisiert. (Eliminierung)
Selenoxid-Eliminierung
Die Selenoxid-Eliminierung ist eine milde Variante der Eliminierung.
Veresterung
Mit Carbonsäuren reagieren Alkohole unter Wasserabgabe zu Estern, diese Reaktion wird auch Veresterung genannt. Diese Reaktion wird durch Säuren katalysiert.
Oxidation
Primäre Alkohole lassen sich zu Aldehyden und Carbonsäuren, sekundäre Alkohole zu Ketonen oxidieren. Tertiäre Alkohole lassen sich nicht weiter oxidieren, es sei denn unter Zerstörung des Kohlenstoffgerüsts.
| Oxidation von Alkoholen | ||||
| Alkohol | primär | sekundär | tertiär | |
| Oxidationsprodukt I | Aldehyd | Keton | keine Reaktion | |
| Oxidationsprodukt II | Carbonsäure | keine Reaktion | – | |
| Beispiel: Oxidationsprodukte der strukturisomeren Butanole | ||||
| Butanol | Butan-1-ol | 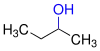 Butan-2-ol |  2-Methylpropan-2-ol | |
| Name | Butan-1-ol | Butan-2-ol | 2-Methylpropan-2-ol | |
| Oxidationsprodukt I | Butanal |  Butanon | keine Reaktion | |
| Name | Butanal (Butyraldehyd) | Butanon (Methylethylketon) | – | |
| Oxidationsprodukt II | Butansäure | keine Reaktion | – | |
| Name | Butansäure (Buttersäure) | – | – | |
| Die funktionellen Gruppen sind blau markiert. | ||||
Zur Oxidation von primären Alkoholen zur Carbonsäure können Chrom(VI)-haltige Oxidationsmittel eingesetzt werden, wie sie z. B. bei der Jones-Oxidation Anwendung finden. Als chromfreies, weniger giftiges Reagenz steht wässriges Rutheniumtetroxid zur Verfügung.
Die Oxidation eines primären Alkohols kann unter Verwendung bestimmter Chrom(VI)-Verbindungen wie dem Collins-Reagenz auch nur bis zur Stufe des Aldehyds erfolgen. Entscheidend ist, dass wasserfreie Lösungsmittel eingesetzt werden. Ist kein Wasser anwesend, kann keine Hydratisierung zum geminalen Diol des Aldehyds (Aldehydhydrate) stattfinden.[16]
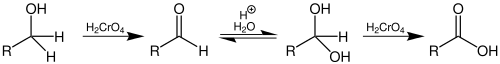
Da lösliche Chromate sehr giftig sind, sowie karzinogene und mutagene Eigenschaften besitzen, wurden alternative Methoden zur Oxidation von Alkoholen entwickelt. Eine häufig zur Anwendung kommende Methode ist die Swern-Oxidation mit aktiviertem Dimethylsulfoxid.[17] Fast alle Methoden eignen sich ebenfalls für die Oxidation sekundärer Alkohole zu Ketonen. Die folgende Aufzählung liefert eine Übersicht der wichtigsten Methoden.
Oxidation zur Carbonsäure/zum Keton:
- Jones-Oxidation (Chrom(VI)-oxid in Schwefelsäure unter Anwesenheit von Aceton)
- Kaliumdichromat in Schwefelsäure
- Rutheniumtetroxid
Oxidation zum Aldehyd/zum Keton:
- Collins-Reagenz (CrO3·py2 in Dichlormethan)
- Corey-Reagenz (Pyridiniumchlorochromat (PCC))
- Cornforth-Reagenz (Pyridiniumdichromat (PDC))
- Anelli-Oxidation (kat. TEMPO, stöch. NaOCl)
- Dess-Martin-Oxidation (Dess-Martin-Periodinan)
- Ley-Oxidation (kat. TPAP, stöch. NMO)
- Pfitzner-Moffatt-Oxidation (DMSO, DCC)
- Swern-Oxidation (DMSO, Oxalylchlorid, NEt3)
Acetalbildung
Mit Aldehyden reagieren Alkohole in Gegenwart saurer Katalysatoren zu Halbacetalen bzw. Acetalen.
Verwendung
Viele Alkohole sind wichtige Lösungsmittel, die sowohl in der Industrie, als auch im Haushalt eingesetzt werden; die mengenmäßig wichtigsten sind Methanol, Ethanol, 2-Propanol und n-Butanol. Im Jahr 2011 wurden weltweit etwa 6,4 Mio. Tonnen dieser alkoholischen Lösungsmittel nachgefragt.[18]
Nachweis
Alcotest
Der Umsatz von Alkoholen mit Dichromaten in schwefelsaurer Lösung ist geeignet, um Alkohole quantitativ nachzuweisen und wurde früher in den Alcotest-Röhrchen eingesetzt:
Das Nachweisprinzip beruht auf dem Farbumschlag von gelb-orange (saure Dichromatlösung) nach grün (Chrom(III)-Ionen) und kann spektralphotometrisch gemessen werden.[19]
Certest
Eine weitere Möglichkeit besteht in der Umsetzung mit Ammoniumcer(IV)-nitrat. Hierbei wird eine konzentrierte Lösung von Ammoniumcer(IV)-nitrat mit einer verdünnten Lösung der unbekannten Substanz versetzt. Enthält die unbekannte Substanz Alkohol-Gruppen, färbt sich das Gemisch rot (manchmal auch grün). Enthält die Substanz Phenole, fällt ein brauner Niederschlag aus. Der Grund für diese Farbreaktion ist eine Komplexbildung, genauer gesagt eine Ligandensubstitution, bei der ein Alkohol/Phenol mit dem Sauerstoffatom am Cer(IV) koordiniert. Durch die Veränderung der Ligandensphäre verändert sich die Farbe des Cer(IV) von hellgelb zu rot/grün/braun. Leicht oxidierbare Alkohole/Phenole können einen negativen Nachweis ergeben, indem sie das Cer(IV) zu Cer(III) reduzieren.
Lucas-Probe
Der Nachweis des Substitutionsgrades eines Alkohols, also ob es sich dabei um einen primären, sekundären oder tertiären Alkohol handelt, erfolgt über nucleophile Substitution der OH-Gruppe gegen Chlorid durch die Lucas-Probe. Die Substitution hat zur Folge, dass sich die entstehende Substanz nicht mehr in Wasser löst und damit eine eigene Phase ausbildet. Dabei ist die Geschwindigkeit dieser Phasenbildung entscheidend:
- Tertiäre Alkohole reagieren bei Raumtemperatur sofort.
- Sekundäre Alkohole reagieren nach etwa fünf Minuten.
- Primäre Alkohole reagieren ausschließlich unter Erwärmen.
Voraussetzung für diesen Test ist, dass sich der ursprüngliche Alkohol in Wasser löst. Auch darf keine andere unter den Reaktionsbedingungen substituierbare Gruppe vorliegen.
Spektroskopie und Derivatisierung
Die eindeutige Identifizierung eines unbekannten Alkohols erfolgt entweder spektroskopisch oder durch Synthese eines charakteristischen Derivates, das einen Schmelzpunkt hat, der von den Schmelzpunkten gleicher Derivate ähnlicher Alkohole gut zu unterscheiden ist. Oftmals werden sie über Ester der 4-Nitrobenzoesäure oder der 3,5-Dinitrobenzoesäure identifiziert. Hierzu wird die zu analysierende Substanz in Gegenwart geringer Mengen Schwefelsäure umgesetzt. Die Schmelzpunkte dieser Derivate sind in der Regel scharf.
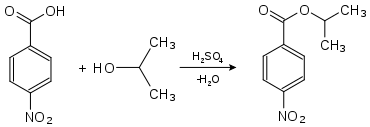 | 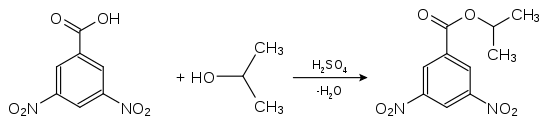 |
| Nachweis von Propan-2-ol (Isopropanol) als Derivat der 4-Nitrobenzoesäure: 4-Nitrobenzoesäure-2-propylester (Smp.: 100,5 °C[20]) | Nachweis von Propan-2-ol (Isopropanol) als Derivat der 3,5-Dinitrobenzoesäure: 3,5-Dinitrobenzoesäure-2-propylester (Smp.: 123 °C[20]) |
Die Derivate der 3,5-Dinitrobenzoesäure besitzen in der Regel höhere Schmelzpunkte als die der 4-Nitrobenzoesäure.[20] Sie werden dann bevorzugt gewählt, wenn der Schmelzpunkt mit der 4-Nitrobenzoesäure zu niedrig ist und keine genaue Bestimmung mehr möglich wird.
Liste wichtiger Alkohole mit Schmelz- und Siedepunkten
| Homologe Reihe der einwertigen, primären, linearen, unverzweigten Alkohole | ||||||
|---|---|---|---|---|---|---|
| C-Atome | Molare Masse g·mol−1 |
Systematischer Name | Trivialname | Schmelzpunkt °C |
Siedetemperatur °C |
Löslichkeit g·l−1 |
| 1 | 32,0 | Methanol | Holzgeist, Methylalkohol | −97,8 | 64,7[21] | ∞ |
| 2 | 46,1 | Ethanol | Alkohol, Ethylalkohol, Weingeist | −114,1 | 78,3[21] | ∞ |
| 3 | 60,1 | Propan-1-ol | n-Propylalkohol | −126,2 | 97,2[21] | ∞ |
| 4 | 74,1 | Butan-1-ol | n-Butylalkohol | −89,3 | 117,3[21] | 79 |
| 5 | 88,2 | Pentan-1-ol | n-Amylalkohol | −78,2 | 138[22] | 23 |
| 6 | 102,2 | Hexan-1-ol | n-Hexylalkohol | −48,6 | 157,5[23] | 6 |
| 7 | 116,2 | Heptan-1-ol | −34,0 | 176[24] | 2 | |
| 8 | 130,2 | Octan-1-ol | −14,9 | 194,5[23] | 0,5 | |
| 9 | 144,3 | Nonan-1-ol | −6 [25] | 214[25] | 0 | |
| 10 | 158,3 | Decan-1-ol | 7 [26] | 230[26] | 0 | |
| 11 | 172,3 | Undecan-1-ol | 15,9[27] | 243[27] | 0 | |
| 12 | 186,3 | Dodecan-1-ol | Laurylalkohol | 24 | 259[24] | 0 |
| 13 | 200,4 | Tridecan-1-ol | 31,7[28] | 274[28] | 0 | |
| 14 | 214,4 | Tetradecan-1-ol | Myristylalkohol | 39–40[29] | 289 | 0 |
| 15 | 228,4 | Pentadecan-1-ol | 44 | 270 | 0 | |
| 16 | 242,4 | Hexadecan-1-ol | Cetylalkohol | 50[30] | 344[30] | 0 |
| … | ||||||
| 18 | 270,5 | Octadecan-1-ol | Stearylalkohol | 56–59[31] | 336 | 0 |
| … | ||||||
| 26 | 382,7 | Hexacosan-1-ol | Cerylalkohol | 79–81 | 240 (13 Pa) | 0 |
| … | ||||||
| 30 | 438,8 | Triacontan-1-ol | Myricylalkohol | 88[32] | 0 | |
| Einwertige Alkohole: sekundär und tertiär, primär mit verzweigten Ketten | ||||||
| C-Atome | Molare Masse g·mol−1 |
Systematischer Name | Trivialname | Schmelzpunkt °C |
Siedetemperatur °C |
Löslichkeit g·l−1 |
| 3 | 60,1 | Propan-2-ol | Isopropylalkohol, Isopropanol | −88,5 | 82,3[21] | ∞ |
| 4 | 74,1 | Butan-2-ol | Sekundärer Butylalkohol | −114,7 | 99,5[33] | 125 |
| 4 | 74,1 | 2-Methylpropan-1-ol | Isobutylalkohol | −108 | 108[34] | 100 |
| 4 | 74,1 | 2-Methylpropan-2-ol | Tertiärer Butylalkohol, Trimethylcarbinol | 25,5[35] | 82,3[35] | ∞ |
| 5 | 88,2 | Pentan-2-ol | sek-n-Amylalkohol | −50 | 118,9[36] | 166 |
| 5 | 88,2 | Pentan-3-ol | Diethylcarbinol | −8 | 116,1[37] | 55 (30 °C) |
| 5 | 88,2 | 2-Methylbutan-1-ol | −70 | 129[38] | 36 | |
| 5 | 88,2 | 3-Methylbutan-1-ol | Isoamylalkohol | −117 | 130,8 | 20 |
| 5 | 88,2 | 2-Methylbutan-2-ol | −8,4 | 102[33] | ||
| 5 | 88,2 | 3-Methylbutan-2-ol | 112,9[33] | |||
| 5 | 83,2 | 2,2-Dimethylpropan-1-ol | neo-Pentylalkohol, tertiärer Amylalkohol | −12 | 102 | 125 |
| Mehrwertige Alkohole | ||||||
| C-Atome | Molare Masse g·mol−1 |
Systematischer Name | Trivialname | Schmelzpunkt °C |
Siedetemperatur °C |
Löslichkeit g·l−1 |
| 2 | 62,1 | Ethan-1,2-diol | Ethylenglycol, 1,2-Glycol | −15,6 | 197,2[21] | ∞ |
| 3 | 76 | Propan-1,2-diol | Propylenglycol | −68 | 188 | ∞ |
| 3 | 76 | Propan-1,3-diol | Trimethylenglycol | −32 | 215 | ∞ |
| 4 | 90 | Butan-1,2-diol | 1,2-Butylenglycol | −114 | 192 | ∞ |
| 4 | 90 | Butan-1,3-diol | 1,3-Butylenglycol | < −50 | 207,5 | ∞ |
| 4 | 90 | Butan-1,4-diol | Tetramethylenglycol | 16 | 230 | ∞ |
| 4 | 90 | Butan-2,3-diol | 2,3-Butylenglycol | 34 (meso) | 183 (meso) | ∞ |
| 5 | 104 | Pentan-1,5-diol | Pentamethylenglycol | −16 | 241 | ∞ |
| 6 | 118 | Hexan-1,6-diol | Hexamethylenglycol | 39–42 | 253–260 | 5000 |
| 8 | 146 | Octan-1,8-diol | Octamethylenglycol | 58–61 | 171–173 (27 hPa) | |
| 9 | 160 | Nonan-1,9-diol | Nonamethylenglycol | 45–46 | 288 | 9 |
| 10 | 174 | Decan-1,10-diol | Decamethylenglycol | 72 | 297 | 0,7 |
| 3 | 104 | Propan-1,2,3-triol | Glycerin, Glycerol | 18 | 290 | ∞ |
| Weitere Alkohole | ||||||
| C-Atome | Molare Masse g·mol−1 |
Systematischer Name | Trivialname | Schmelzpunkt °C |
Siedetemperatur °C |
Löslichkeit g·l−1 |
| 5 | 86,13 | Cyclopentanol | −19 | 141 | 13[39] | |
| 6 | 100,2 | Cyclohexanol | 25,2 | 161,5[21] | 36 | |
| 3= | 58 | Prop-2-en-1-ol | Allylalkohol | −129 | 97 | ∞ |
| 4= | 71 | But-2-en-1-ol | Crotylalkohol | −30 | 118 | 166 |
| 4 | 70,09 | 3-Butin-1-ol | −63 | 128,9 | ||
| 6 | 98,14 | 2-Hexin-1-ol | 66–67 | |||
| 6 | 98,14 | 3-Hexin-1-ol | 63–64 | |||
| 6 | 98,14 | 3-Hexin-2-ol | 79–80 | |||
| 6 | 98,14 | 5-Hexin-1-ol | 73–75 | |||
| 6 | 98,14 | 5-Hexin-3-ol | ||||
| 7 | 108,14 | Phenylmethanol, (Hydroxymethyl)benzol | Benzylalkohol | −15 | 205,4[21] | 39 |
| 7 | 114,19 | Cyclohexylmethanol | 19 | 187–188 | ||
| 8 | 126,20 | 3-Octin-1-ol | 880 | |||
| 8 | 126,20 | 7-Octin-1-ol | 70 | |||
| 8 | 122,14 | 1-Phenylethan-1-ol, (1-Hydroxyethyl)benzol (C6H5CH(OH)CH3) | α-Phenylethylalkohol | 21 | 205 | 0 |
| 8 | 122,14 | 2-Phenylethan-1-ol, (2-Hydroxyethyl)benzol (C6H5CH2CH2OH) | β-Phenylethylalkohol | −27 | 221 | 16 |
| 10 | 158,29 | 3-Decanol | 213 | |||
| 10 | 158,29 | 4-Decanol | −11 | 210–211 | ||
| 11 | 164,25 | 4-tert-Butylbenzylalkohol | 139–140 | |||
| 13 | 184,23 | Diphenylmethanol (C6H5)2CHOH | Diphenyltricarbinol, Benzhydrol | 69 | 298 | 0 |
| 19 | 260,33 | Triphenylmethanol (C6H5)3COH | Triphenylcarbinol | 162,5 | >360 | 0 |
| Zum Vergleich das Phenol und Alkohole mit ähnlichen molaren Massen | ||||||
| C-Atome | Molare Masse g·mol−1 |
Systematischer Name | Trivialname | Schmelzpunkt °C |
Siedetemperatur °C |
Löslichkeit g·l−1 |
| 6 | 94,1 | Phenol | Carbolsäure, Benzenol | 41 | 181,7[21] | 84 |
| 5 | 88,2 | Pentan-1-ol | n-Amylalkohol | −78,2 | 128,0 | 23 |
| 6 | 102,2 | Hexan-1-ol | n-Hexylalkohol | −48,6 | 157,1 | 6 |
| 5 | 86,13 | Cyclopentanol | −19 | 141 | 13 | |
| 6 | 100,2 | Cyclohexanol | 25,2 | 161,5[21] | 36 | |
Anmerkung:
- = Doppelbindungen
- * bei Siedepunkt: Die Substanz zersetzt sich vor Erreichen des Siedepunktes. Werte in Klammern geben den Siedepunkt bei 20 hPa Druck an.
- ∞ bei Löslichkeit: unbegrenzt mit Wasser mischbar.
Bei einzelnen Werten kann es in der Literatur zu Abweichungen kommen.
Siehe auch
Einzelnachweise
- Eintrag zu alcohols. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.A00204 – Version: 2.3.1.
- Clayden, Greeves Warren, Wothers: Organic Chemistry. Oxford University Press Inc, New York 2001, ISBN 978-0-19-850346-0, S. 35–36.
- Eintrag zu phenols. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.P04539 – Version: 2.3.1.
- Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag, Leipzig 1965, S. 44.
- Eintrag zu Alkohole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 23. Mai 2014.
- Thomas Nordegren: The A-Z Encyclopedia of Alcohol and Drug Abuse. Universal-Publishers, 2002, ISBN 978-1-58112-404-0, S. 38 (eingeschränkte Vorschau in der Google-Buchsuche).
- Church of England temperance society: The Church of England temperance chronicle [afterw.] The Temperance chronicle. 1884, S. 69 (eingeschränkte Vorschau in der Google-Buchsuche).
- William Johnson: Lexicon Chymicum Cum obscuriorum verborum et rerum hermeticarum ... 1652 (eingeschränkte Vorschau in der Google-Buchsuche).
- Henry Enfield Roscoe, Carl Schorlemmer: A Treatise on Chemistry: The chemistry of the hydrocarbons and their derivatives, or Organic chemistry. Appleton, 1884, S. 285 (eingeschränkte Vorschau in der Google-Buchsuche).
- Seth C. Rasmussen: The Quest for Aqua Vitae The History and Chemistry of Alcohol from Antiquity to the Middle Ages. Springer Science & Business, 2014, ISBN 978-3-319-06302-7, S. 8 (eingeschränkte Vorschau in der Google-Buchsuche).
- Online Etymology Dictionary: alcohol | Search Online Etymology Dictionary, abgerufen am 9. Januar 2021
- Science Vision, Jg. 3, Nr. 25, März 2000 (eingeschränkte Vorschau in der Google-Buchsuche).
- Eintrag zu Fettalkohole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. Januar 2013.
- Eintrag zu Wachsalkohole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 8. September 2014.
- Wissenschaft-Online-Lexika: Eintrag zu Alkanole/Alkohole im Lexikon der Chemie, abgerufen am 1. Juli 2008.
- Paula Yurkanis Bruice: Organische Chemie, Pearson Education Inc., 2007, 5. Auflage, S. 829, ISBN 978-3-8273-7190-4.
- Paula Yurkanis Bruice: Organische Chemie, Pearson Education Inc., 2007, 5. Auflage, S. 830–831, ISBN 978-3-8273-7190-4
- Ceresana: Markstudie Lösungsmittel, 2. Auflage (UC-3505), April 2012.
- Paula Yurkanis Bruice: Organische Chemie, Pearson Education Inc., 2007, 5. Auflage, S. 412, ISBN 978-3-8273-7190-4.
- CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, ISBN 3-342-00280-8, S. 312.
- Hans Beyer und Wolfgang Walter: Organische Chemie, S. Hirzel Verlag, Stuttgart, 22. Auflage, 1991, S. 120, ISBN 3-7776-0485-2.
- Hans Beyer und Wolfgang Walter: Organische Chemie, S. Hirzel Verlag, Stuttgart, 22. Auflage, 1991, S. 124, ISBN 3-7776-0485-2.
- Hans Rudolf Christensen: Grundlagen der organischen Chemie, Verlag Sauerländer Aarau, 1. Auflage, 1970, S. 166.
- Eintrag zu CAS-Nr. 143-08-8 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Dezember 2019. (JavaScript erforderlich)
- Eintrag zu CAS-Nr. 112-30-1 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Dezember 2019. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-517.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-496.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-507, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-301, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-496, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-355, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-169, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-446, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-447, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-396, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-397, ISBN 0-8493-0740-6.
- Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics, 1st Student Edition, 1988, CRC Press Baton Rouge, Florida, S. C-168, ISBN 0-8493-0740-6.
- Eintrag zu Cyclopentanol in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 25. März 2021.
Weblinks
- Schulversuche zum Thema Alkohole
- Lernzirkel Alkohole. (Nicht mehr online verfügbar.) In: ZUM-Wiki. Zentrale für Unterrichtsmedien im Internet e. V. [ZUM Internet e. V.], 28. Dezember 2009, archiviert vom Original am 28. Dezember 2009; abgerufen am 7. Februar 2010.
