Mangan(IV)-oxid
Mangan(IV)-oxid, auch Mangandioxid oder Braunstein, ist ein Oxid des Mangans mit der Summenformel MnO2. Mangan liegt hier in der Oxidationsstufe +4 vor. Aufgrund seines Aussehens (dunkelbraun, glänzt seidig, körnig bis erdig) wird es auch Magnesia nigra, schwarzes Magnesia, oder etwas unpräzise als Braunstein bezeichnet. Braunstein ist jedoch eine Gruppe von Mangan-Mineralien, deren Hauptbestandteil Mangandioxid ist.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
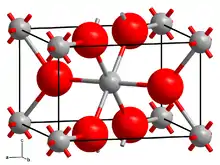 | ||||||||||||||||
| _ Mn4+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Mangan(IV)-oxid | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Verhältnisformel | MnO2 | |||||||||||||||
| Kurzbeschreibung |
schwarz-brauner Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 86,94 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
5,03 g·cm−3[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
0,5 mg·m−3[3] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Geschichte
Mangan(IV)-oxid wurde früher unter Handwerkern als „Glasmacherseife“ bezeichnet, da es durch Eisen(III)-silicate verfärbte Glasschmelzen entfärben konnte.[5] Schon in den Gläsern der alten Ägypter und Römer findet man etwa 2 % Manganoxide. Wahrscheinlich wurde schon zu dieser Zeit Braunstein zur Entfärbung der Gläser benutzt.
Vorkommen
Mangan(IV)-oxid findet man als orthorhombisch kristallisierten Ramsdellit, als tetragonal kristallisierten Pyrolusit (Weichmanganerz) und als hexagonal kristallisierenden Akhtenskit in großem Umfang im Südural und in Südafrika. Zusammen mit anderen Eisenverbindungen ist es oft ein Hauptbestandteil der Umbraerden und anderer brauner, dunkelfarbiger Erden.
Gewinnung und Darstellung
Mangan(IV)-oxid wird durch Mahlen von Pyrolusit oder durch das Erhitzen von Mangan(II)-nitrat an der Luft auf über 500 °C hergestellt.
Heute jedoch wird Mangan(IV)-oxid hauptsächlich durch Elektrolyse einer Lösung von Mangan(II)-sulfat gewonnen. Zweiwertige Manganionen (Mn2+) oxidieren an der Anode zu dreiwertigen Mn3+-Ionen, die anschließend zu Mn2+- und Mn4+-Ionen disproportionieren. Dabei lagert sich Braunstein an der Anode ab.
Eigenschaften

Mangan(IV)-oxid ist ein braunschwarzes Pulver, das in Wasser unlöslich ist. Außerdem findet keine Reaktion mit kalter Schwefel- oder Salpetersäure statt. Mangan(IV)-oxid kristallisiert normalerweise in der Rutilstruktur, wobei es auch in anderen Strukturen gefunden wird, wie im Artikel zu Braunstein beschrieben.
Reaktionen
Durch Erhitzen über 450 °C wird unter Sauerstoffabgabe Mangan(III)-oxid (Mn2O3) gebildet.
Durch Erhitzen über 600 °C wird unter Sauerstoffabgabe Mangan(II, III)-oxid (Mn3O4) gebildet; Mn3O4 enthält 72 % Mangan.
Das Erhitzen unter Zusatz von Schwefelsäure führt zur Abspaltung von Sauerstoff unter Bildung von Mangan(II)-sulfat.
Wasserstoffperoxid zersetzt sich in Anwesenheit von Mangandioxid unter Sauerstoffabgabe. Das Mangandioxid wirkt dabei als Katalysator.
Mit Salzsäure reagiert Mangandioxid unter Chlorentwicklung zu Mangan(II)-chlorid. Diese Umsetzung hatte als Weldon-Verfahren Bedeutung zur Gewinnung von Chlor.[6]
Verwendung

Aufgrund seiner oxidierenden Wirkung findet Mangandioxid häufig Anwendung als Oxidationsmittel. So wird es beispielsweise bei der organischen Synthese von Hydrochinon aus Anilin eingesetzt.[7] Mangandioxid ist der aktive Bestandteil der Härterpaste für Dichtstoffe auf der Basis von Polysulfiden und bewirkt die oxidative Verknüpfung über die SH-Gruppen des Polysulfidpräpolymers.[7] Es wird in europäischen Sicherheitsstreichhölzern als Brennratenkatalysator eingesetzt und ersetzt hier giftigere Stoffe wie Kaliumdichromat.[8] Auch in Feuerwerkskörpern wird es als Oxidationsmittel verwendet. Des Weiteren dient es im Labor zur Darstellung von Halogenen aus entsprechenden Halogenwasserstoffen.
Bekannt ist es auch als „Glasmacherseife“ bei der Glasherstellung. Glasschmelzen, die oft durch geringe Mengen an Eisen(III)-silikaten gelb-grün gefärbt sind, wird Mangandioxid in kleinen Mengen zugesetzt, um die Verfärbungen zu neutralisieren. Dabei werden Mangan(III)-silikate gebildet, deren Farbe violett ist. Gelbgrün und violett sind jedoch Komplementärfarben, weswegen der Schmelzfluss in einem neutralen Farbton (gräulich bis annähernd farblos) erscheint.[5][7]
In Batterien wird es als Kathodenmaterial verwendet. In Zink-Kohle- und Alkali-Mangan-Batterien wird entweder
- natürlich vorkommendes Mangandioxid („NMD“),
- chemisch hergestelltes Mangandioxid („CMD“) oder
- durch Elektrolyse hergestelltes Mangandioxid („EMD“) eingesetzt.
Weitere Verwendungen sind als Färbemittel für Ziegel[7], Teil der Gasreinigung in Atemschutzmasken und als Zusatzstoff bei der Herstellung von Firnissen und Sikkativen. Es wirkt auch katalytisch bei der Zersetzung von Wasserstoffperoxid und dient so der Dampf- und Sauerstoffherstellung.
Mangandioxidhydrat
-oxidhydroxid.jpg.webp)
Mangandioxidhydrat (Mangan(IV)-oxidhydroxid) erhält man durch oxidative Fällung aus Mangan(II)-salzlösungen mit Natronlauge und Wasserstoffperoxid oder mit Natriumperoxid als einen dunkelbraunen Niederschlag:
Bedeutung hat diese Verbindung, weil sie im Unterschied zum wasserfreien Mangandioxid eine größere Reaktionsfähigkeit als Oxidationsmittel aufweist.[9][10][11]
Einzelnachweise
- Eintrag zu MANGANESE DIOXIDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 22. Oktober 2021.
- Eintrag zu Mangandioxid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. November 2014.
- Eintrag zu Mangan(IV)-oxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- Eintrag zu Manganese dioxide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- arche-kurzmann.de: Das Märchen von der Entfärbung des Glases, abgerufen am 5. Februar 2013.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 436.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- Alexander P. Hardt: Pyrotechnics, Pyrotechnica Publications, Post Falls Idaho USA 2001, ISBN 0-929388-06-2, S. 74 ff.
- Heinrich Remy: Lehrbuch der Anorganischen Chemie Band II, Akademische Verlagsgesellschaft Geest & Portig Leipzig 1961, S. 258
- Jander-Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie, 5. Auflage, S. Hirzel, Stuttgart-Leipzig 1965, S. 209.
- Eberhard Schweda: Jander / Blasius, Anorganische Chemie I, 17. Auflage, 2012, S. 202

