Plutonium(III)-chlorid
Plutonium(III)-chlorid ist eine chemische Verbindung aus den Elementen Plutonium und Chlor. Es besitzt die Formel PuCl3 und gehört zur Stoffklasse der Chloride.
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
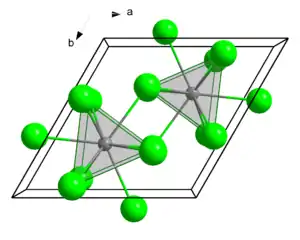 | ||||||||||
| _ Pu3+ _ Cl− | ||||||||||
| Kristallsystem | ||||||||||
| Raumgruppe |
P63/m (Nr. 176) | |||||||||
| Gitterparameter |
a = 739,4 pm | |||||||||
| Koordinationszahlen |
Pu[9], Cl[3] | |||||||||
| Allgemeines | ||||||||||
| Name | Plutonium(III)-chlorid | |||||||||
| Andere Namen |
Plutoniumtrichlorid | |||||||||
| Verhältnisformel | PuCl3 | |||||||||
| Kurzbeschreibung |
grüner Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 350,32 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
5,70 g·cm−3[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
1727 °C[1] | |||||||||
| Gefahren- und Sicherheitshinweise | ||||||||||

Radioaktiv | ||||||||||
| ||||||||||
| Thermodynamische Eigenschaften | ||||||||||
| ΔHf0 | ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Darstellung
Plutonium(III)-chlorid kann im durch Reaktion von Plutonium und Chlor im Vakuum oder einer Tetrachlorkohlenstoff-Argon-Atmosphäre gewonnen werden.[3]
Ebenfalls möglich ist die Herstellung aus Plutonium(IV)-oxid mit Tetrachlorkohlenstoff.[3]
Andere Herstellungsmethoden sind die Chlorierung einer Plutonium(IV)-hydroxid mit Chlorwasserstoff oder die Umsetzung von Plutonium mit Wasserstoff zu Plutoniumhydrid und dessen anschließende Chlorierung mit Chlorwasserstoff oder die Reaktion von Plutonium(III)-oxalat-Decahydrat mit Hexachlorpropen.[3]
Eigenschaften
Plutonium(III)-chlorid bildet grüne Kristalle mit einem Schmelzpunkt von 767 °C. In Wasser und in verdünnten Säuren ist es mit blauer Farbe löslich.[3] Es kristallisiert im hexagonalen Kristallsystem in der Raumgruppe P63/m (Nr. 176) mit den Gitterparametern a = 739 pm und c = 424 pm und zwei Formeleinheiten pro Elementarzelle. Seine Kristallstruktur ist isotyp mit Uran(III)-chlorid. In der Struktur werden die Plutoniumatome von je neun Chloratomen umgeben, als Koordinationspolyeder ergibt sich dabei ein dreifach überkapptes, trigonales Prisma.[4]
Mit Wasser bildet Plutonium(III)-chlorid ein Mono-, Tri- und Hexahydrat.[3]
Sicherheitshinweise
Einstufungen nach der CLP-Verordnung liegen nicht vor, obwohl die chemische Giftigkeit bekannt ist. Wichtig sind die auf der Radioaktivität beruhenden Gefahren, sofern es sich um eine dafür relevante Stoffmenge handelt.
Einzelnachweise
- Gmelins Handbuch der anorganischen Chemie, System Nr. 71, Transurane, Teil C, S. 129–135.
- Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieser Stoff entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 1301.
- John H. Burns, J. R. Peterson, J. N. Stevenson: „Crystallographic Studies of some Transuranic Trihalides: 239PuCl3, 244CmBr3, 249BkBr3 and 249CfBr3“, in: Journal of Inorganic and Nuclear Chemistry, 1975, 37 (3), S. 743–749 (doi:10.1016/0022-1902(75)80532-X).
Literatur
- David L. Clark, Siegfried S. Hecker, Gordon D. Jarvinen, Mary P. Neu: Plutonium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 813–1264 (doi:10.1007/1-4020-3598-5_7).