Methan
Methan ist eine chemische Verbindung mit der Summenformel CH4 und der einfachste Vertreter aus der Stoffgruppe der Alkane. Unter Normalbedingungen ist es ein farb- und geruchloses, brennbares Gas. Methan ist in Wasser unlöslich und bildet mit Luft explosive Gemische. Es verbrennt mit bläulich-heller Flamme in Gegenwart von ausreichend Sauerstoff zu Kohlenstoffdioxid und Wasser.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
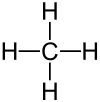 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Methan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | CH4 | ||||||||||||||||||
| Kurzbeschreibung |
farb- und geruchsloses Gas[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 16,04 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
gasförmig | ||||||||||||||||||
| Dichte |
0,72 kg·m−3 gasförmig, 0 °C, 1013 hPa 0,42 g·cm−3 flüssig am Siedepunkt[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
−162 °C[1] | ||||||||||||||||||
| pKS-Wert |
48[2] | ||||||||||||||||||
| Löslichkeit |
wenig löslich in Wasser (36,7 ml·l−1)[1] gut löslich in Ethanol und Diethylether[3] | ||||||||||||||||||
| Dipolmoment |
0[4] | ||||||||||||||||||
| Brechungsindex |
1,000444 (0 °C, 101,325 kPa)[5] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 10000 ml·m−3 oder 6700 mg·m−3[7] | ||||||||||||||||||
| Treibhauspotential |
28 (bezogen auf 100 Jahre)[8] | ||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−74,6 kJ/mol (gasförmig)[9] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Es kommt in der Natur unter anderem als Hauptbestandteil von Erdgas vor. Da es in Lagerstätten in großen Mengen existiert, ist es eine attraktive Energiequelle. Der Transport erfolgt durch Pipelines oder als tiefgekühlte Flüssigkeit mittels Tankschiffen. Des Weiteren kommt es als Methanhydrat gebunden am Meeresboden und in Permafrostgebieten vor, wobei die genaue Menge unbekannt ist. Methan dient als Heizgas und ist in der chemischen Industrie als Ausgangsstoff für technische Synthesen wie etwa der Methanolherstellung oder der Herstellung von halogenierten Methanderivaten von großer Bedeutung. Es wird weiterhin zur Herstellung von Wasserstoff im großindustriellen Maßstab verwendet.
Das Gas entsteht in beträchtlichen Mengen durch biotische Prozesse, entweder anaerob durch Mikroorganismen oder aerob durch Phytoplankton, Pflanzen und Pilze. Anthropogene Quellen sind indirekt etwa der Reisanbau und die Schaf- und Rinderzucht. Abiotische Quellen wie Waldbrände oder Vulkanausbrüche setzen ebenfalls Methan frei.
Methan ist der meist vertretene Kohlenwasserstoff in der irdischen Atmosphäre, wobei die Konzentration sowohl zwischen der Nord- und Südhalbkugel als auch jahreszeitlich schwankt. Als Treibhausgas besitzt Methan ein hohes Treibhauspotential. Es trug zur klimageschichtlichen Erderwärmung bei und beeinflusst die aktuelle globale Erwärmung. In der Erdatmosphäre wird es zu Wasser, Formaldehyd und schließlich zu Kohlenstoffdioxid oxidiert. Methan ist Bestandteil der Atmosphäre anderer Planeten und Monde und wurde sowohl in Kometen als auch im interstellaren Medium nachgewiesen.
Etymologie
Der Name Methan leitet sich von Méthylène her. Dies war der Name, den die französischen Chemiker Jean-Baptiste Dumas und Eugène-Melchior Péligot 1834 der Flüssigkeit, die heute als Methanol bezeichnet wird, gaben; er setzt sich seinerseits aus altgriechisch μέθυ (méthy) für „Wein, berauschendes Getränk“ und ὕλη (hýlē) für „Holz“ zusammen.[10] Der deutsche Chemiker August Wilhelm von Hofmann schlug 1866 in einer englischen Veröffentlichung erstmals eine systematische Nomenklatur vor, wonach der Name für das Gas sich von Methylene ableitete und Methane genannt werden sollte.[11] Daraus entstand die deutsche Form Methan. In alten Texten wurde Methan gelegentlich als Methylwasserstoff bezeichnet.
Geschichte
Altertum und Spätmittelalter

Methan speist als Bestandteil von austretendem Erdgas sogenannte „Ewige Feuer“. Diese wurden so genannt, da das Vorhandensein einer Flamme in historischen Aufzeichnungen über lange Zeiträume berichtet wurde.[12] Diese Feuer treten oft in erdölführenden Gebieten mit tektonischen Verwerfungen auf, etwa in Chimaira (Lykien). Bereits seit 2000 v. Chr. sind diese Feuer bekannt. Bei dem ewigen Feuer in Baba Gurgur im Irak handelt es sich möglicherweise um den Feuerofen, der bereits in der Bibel im Buch Daniel beschrieben ist und in den König Nebukadnezar Daniels Begleiter Shadrach, Meshach, und Abednego warf, weil sie sich weigerten, eine goldene Statue anzubeten (Dan 3,23 ).[13] Das Orakel von Delphi befand sich im Apollon-Tempel, der um etwa 1000 vor Christus über einer ewigen Flamme errichtet wurde. Möglicherweise erfolgten die Wahrsagungen der Pythia unter Einfluss der Inhalation von narkotisch wirkenden Gasen wie Methan, Ethan und Ethen, als Pneuma bezeichnet, die in Spuren in einer dort vorhandenen Quelle nachgewiesen wurden.[14]
Methan als Bestandteil des Erdgases wurde bereits im 4. Jahrhundert vor Christus in China energetisch zum Eindampfen von Salzsole verwendet. Zum Teil traten aus den Bohrlöchern sowohl Methan als auch Sole aus, zum Teil wurde das Gas mittels Bambuspipelines von sogenannten trockenen Bohrlöchern aus zur Soleverarbeitung herangeführt.[15] Die Natur des Gases war damals unbekannt, aber es war den Alchemisten im Mittelalter bekannt als Bestandteil von Fäulnisgasen, auch als „Sumpfluft“ bezeichnet. Das Auftreten von Schlagwettern, einem Gasgemisch aus Methan und Luft, war im Untertagebau schon früh als Gefahr bekannt, da eine Zündquelle eine Schlagwetterexplosion auslösen konnte.
17. bis 19. Jahrhundert

Im Februar 1659 untersuchte der Engländer Thomas Shirley bei Wigan eine Quelle mit brennbarem Wasser. Er konnte zeigen, dass nicht das Wasser, sondern ein Gas, das vom Boden des aufgestauten Wassers aufstieg, das Phänomen verursachte. Er vermutete, dass das Gas aus einer darunterliegenden Kohlelagerstätte stammte und dass es Grubengas war.[16]

Der Priester Carlo Giuseppe Campi wies im Herbst 1776 Alessandro Volta auf das Phänomen der „entflammbaren Luft“ hin, die an einer Biegung des Flusses Lambro aufstieg. Dieses Phänomen war bereits einige Jahre zuvor von Antoine Laurent de Lavoisier, Benjamin Franklin und Joseph Priestley untersucht und beschrieben worden. Volta versuchte in den Sümpfen des Lago Maggiore den Boden mit Hilfe eines Stocks umzurühren, wobei er Gasblasen aufsteigen sah. Er sammelte das Gas in Flaschen, welches er mittels eines von ihm entwickelten Eudiometers quantitativ untersuchte.
Volta entwickelte auch die sogenannte Volta-Pistole, ein Eudiometer, in dem eine Luft-Methan-Mischung gezündet werden konnte. Er schlug 1777 vor, die Volta-Pistole als eine Art Fernschreiber zu nutzen. Über eine Drahtleitung zwischen Mailand und Como sollte ein elektrischer Impuls ein Luft-Methan-Gemisch in Volta-Pistolen zur Explosion bringen, wobei eine Reihe solcher Entladungen einen alphanumerischen Code zur Informationsübertragung darstellen würde.[17] Seine Untersuchungen beschrieb Volta in als Buch herausgegebenen Briefen an Carlo Campi.[18]
Um 1800 begannen Versuche zur Verwendung von Stadtgas, einer Mischung aus Methan, Kohlenstoffmonoxid, Wasserstoff und Stickstoff, für die Straßenbeleuchtung. William Henry untersuchte zu dieser Zeit die Eigenschaften von Mischungen brennbarer Gase, etwa ihre Löslichkeit in Flüssigkeiten in Abhängigkeit vom Partialdruck. Diese Arbeiten führten zur Formulierung des Henry-Gesetzes. Er bestimmte die relative Leuchtkraft von Gasen und die Unterschiede ihrer Zusammensetzung. Seine Ergebnisse bestätigten die Vermutung John Daltons über die Zusammensetzung von Methan und Ethen und, dass Kohlenstoff und Wasserstoff nur in bestimmten Verhältnissen miteinander verbunden sind.[19]

Nach dem Grubenunglück von Felling (Tyne and Wear) im Jahr 1812, einem der größten Grubenunglücke der damaligen Zeit, stellte Humphry Davy fest, dass das gefürchtete Grubengas hauptsächlich aus Methan bestand. Der Verlust von 92 Menschenleben war eine der Triebfedern für die Entwicklung der Davy-Lampe mit Flammsieb.[20]
Um 1821 fand William Hart, der als „Vater des Erdgases“ gilt, in Fredonia die erste Erdgasquelle in den Vereinigten Staaten.[21] Das Gas wurde lokal für Beleuchtungszwecke genutzt. Hart gründete 1858 die erste US-amerikanische Erdgasgesellschaft, die Fredonia Gas Light Company.
20. Jahrhundert
Mit Beginn der Erdölförderung wurde Methan als Hauptbestandteil des gleichzeitig geförderten Erdgases meist am Bohrlochkopf abgefackelt. Eine der ersten großen Pipelines wurde im Jahr 1891 gebaut. Sie war 193 Kilometer lang und verband Erdgasbohrungen in Indiana mit Chicago. Zu Beginn des Ausbaus und intensiveren Nutzung der Erdgaspipelines in den 1930er Jahren wurde Methanhydrat in den Erdgaspipelines gefunden, das sich aus Methan und Wasser bildete und die Pipelines verstopfte. Erst nach dem Zweiten Weltkrieg erlaubten Fortschritte in der Pipelinetechnik den Ausbau einer Pipelineinfrastruktur und der Nutzung von Methan als Bestandteil der Erdgases zur industriellen Nutzung sowie zur privaten Nutzung zu Heiz- und Kochzwecken.[22] Mit steigendem globalem Energiebedarf wurde Methan ein stetig wachsender Faktor der Weltprimärenergieproduktion. Zwischen 1980 und 1990 stieg der Anteil von etwa 18 auf etwa 22 %.[23]
Vorkommen
Irdisch
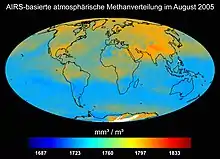
Methan war neben Ammoniak und Wasserdampf ein Hauptbestandteil der irdischen Uratmosphäre. Es kommt vielfältig vor und wird auf der Erde ständig neu gebildet, etwa bei technischen, biologischen oder geologischen Prozessen wie der Serpentinisierung.[25][26] Die Methankonzentration in der Erdatmosphäre hat sich vom Jahr 1750 bis zum Jahr 2018 von 0,73 auf 1,869 ppm mehr als verdoppelt und damit den höchsten Wert seit 800.000 Jahren erreicht.[27] Seit dem Ausfall des Envisat-Satelliten liefern der japanische Greenhouse Gases Observing Satellite (GOSAT) sowie das Tropomi-Spektrometer des Sentinel-5P-Satelliten Daten der globalen Verteilung der Methankonzentration in der Atmosphäre. Im Jahr 2023 ist der Beginn einer weiteren Sentinel-Mission zur Beobachtung der Atmosphärenzusammensetzung geplant.
In der Atmosphäre reagiert Methan mit Sauerstoff zunächst zu Formaldehyd und gegebenenfalls zu Ozon.[28] Durch weitere Oxidation entsteht schließlich Kohlenstoffdioxid.
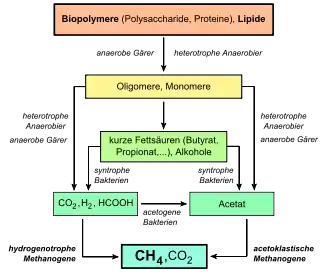
Mikroorganismen bilden einen großen Teil des terrestrischen Methans. Beim Faulen organischer Stoffe unter Luftabschluss in Sümpfen oder im Sediment auf dem Grund von Gewässern bildet sich Sumpfgas, ein Gemisch aus Methan und Kohlenstoffdioxid. Biogas enthält etwa 60 % Methan und etwa 35 % Kohlenstoffdioxid, neben geringeren Mengen Wasserstoff, Stickstoff und Schwefelwasserstoff.
Die Bildung erfolgt oberflächennah biotisch: einerseits anaerob im Zuge der Methanogenese vor allem aus Acetat, aber auch unter anderem aus Kohlenstoffdioxid, durch eine Gruppe von Archaeen, den Methanogenen. Sie nutzen einfache Verbindungen wie Kohlenstoffdioxid oder Methanol und reduzieren diese zu Methan, wobei sie – vor allem über die damit verbundene Oxidation von Reaktionspartnern – Energie gewinnen. Beispielsweise werden bei der Bildung von Methan und Wasser aus CO2 und Wasserstoff (H2) unter Standardbedingungen bei einem pH-Wert von sieben etwa 131 kJ/mol an Freier Enthalpie (Gibbs-Energie, ΔG0’) freigesetzt:[29]
Ein kleiner Teil der biotischen Entstehung basiert auf der aeroben Spaltung von Methylphosphonaten.[30][31]

Unterhalb der Oberfläche der Erde entsteht Methan im tieferen Untergrund bei hohen Temperaturen und Drücken und wird meist bei vulkanischen Aktivitäten frei. Als Bestandteil des Erdgases schwankt seine Konzentration je nach Lagerstätte zwischen 35 und 98 %. Andere Erdgasbestandteile können höhere Kohlenwasserstoffe, besonders Ethan sein, sowie Kohlenstoffdioxid und Stickstoff. Das meist zusammen mit Erdöl auftretende „Naßgas“ enthält Kohlenwasserstoffe wie Pentan, Hexan, Heptan und noch höhere Kohlenwasserstoffe, während „trockenes“ Erdgas Methan als Hauptbestandteil enthält. Das in Steinkohlelagern eingeschlossene Grubengas enthält hauptsächlich Methan.[32]
Es kann abiotisch thermal im Rahmen des Reifeprozesses von Kohle in der geochemische Phase der Inkohlung, sowie aus allen Typen von Kerogenen und Erdöl entstehen.[33] 2008 wurde nachgewiesen, dass Methan aus den Lost-City-Hydrothermalquellen geochemischen Ursprungs ist.[25]
Methan, das am Meeresgrund austritt, reagiert unter hohem Druck und niedriger Temperatur mit Wasser zu festem Methanhydrat, das auch als „Methaneis“ bezeichnet wird. Der Kohlenstoffgehalt der weltweiten Methanhydratvorkommen wurde Ende der 1980er Jahre etwa 11.000 Gigatonnen geschätzt, der Kohlenstoffgehalt der nachgewiesenen Erdgas, Kohle- und Ölreserven beträgt etwa 5000 Gigatonnen.[34] Neuere Schätzungen gehen von wesentlich geringeren Vorkommen aus, wobei die Vorkommen auf etwa 1800 Gigatonnen Kohlenstoff geschätzt werden.[35][36][37]
Außerirdisch
| Planet | Anteil |
|---|---|
| Erde | 1,86 ppm |
| Mars | 0,0105 ppm |
| Jupiter[38] | 2000 ppm |
| Saturn | 4500 ± 2000 ppm |
| Uranus[39] | 20–40.000 ppm |
| Neptun | 15.000 ± 5000 ppm |
Die Atmosphären der Planeten Mars, Jupiter, Saturn, Uranus, Neptun und des Zwergplaneten Pluto enthalten ebenfalls Methan, ebenso die Atmosphären von Monden wie Titan oder Enceladus.[40] Nach Wasserstoff und Helium ist Methan die dritthäufigste Komponente der Uranusatmosphäre. Durch dessen Absorptionsbanden im roten Bereich und im nahen Infrarot erscheint Uranus aquamarin oder cyanfarben. Die etwas helleren blauen Farbtöne des Saturns sind wahrscheinlich auf denselben Effekt zurückzuführen.[41]
Außerhalb unseres Sonnensystems ist Methan als erstes organisches Molekül auf dem Exoplaneten HD 189733 b vom Typ Hot Jupiter nachgewiesen worden.[42] Die Absorptionsspektren von kühlen Braunen Zwergen, die als Methan-T-Zwerge bezeichnet werden, werden von Methan und Wasser dominiert. Daneben gibt es heißere, sogenannte L-Zwerge, die ebenfalls Methanabsorptionsmerkmale aufweisen, die jedoch schwächer sind als die der T-Zwerge.[43]
Mars
2009 wurde über Methaneruptionen auf dem Mars berichtet; in der Atmosphäre des Mars wurde Methan nachgewiesen, etwa 10,5 ppb.[44] Da es sich normalerweise nicht in der Atmosphäre halten kann und es keine Hinweise auf Meteoriten als Quelle gibt, muss es auf dem Planeten neu gebildet worden sein, was ein Indiz für Leben auf dem Mars sein könnte.[45] Das Methan könnte vulkanischen Ursprungs sein, wofür auf dem Mars noch keine Hinweise gefunden wurden.
Eine methanreiche Ur-Atmosphäre auf dem Mars und der dadurch verursachte Treibhauseffekt könnte eine Erklärung für das Paradoxon der schwachen jungen Sonne bieten. Die in der Frühzeit geringe Strahlungsleistung der jungen Sonne steht im Widerspruch zu einer Oberflächentemperatur auf dem Mars über dem Gefrierpunkt von Wasser, für die es Hinweise durch Spuren von fließenden und stehenden Gewässern in der Urgeschichte des Mars gibt.[46]
Titan

Auf dem Saturnmond Titan herrscht bei −180 °C und etwa 1,6 Bar Atmosphärendruck fast der Tripelpunkt des Methans. Methan kann deshalb auf diesem Mond in allen drei Aggregatzuständen auftreten. Es gibt Wolken aus Methan, aus denen Methan regnet, das durch Flüsse, darunter der Vid Flumina, in Methanseen fließt, dort wieder verdunstet und so einen geschlossenen Methankreislauf bildet, analog zum Wasserkreislauf auf der Erde. Flüssiges Methan ist für Radarstrahlen durchsichtig, so konnte die Raumsonde Cassini die Tiefe des Sees Ligeia Mare zu 170 m bestimmen.[47]
Wahrscheinlich gibt es auf diesen Seen Eisberge aus Methan und Ethan. Diese schwimmen auf den Methanseen, wenn sie mindestens 5 % gasförmigen Stickstoff enthalten. Wenn die Temperatur nur geringfügig sinkt, zieht sich der Stickstoff soweit zusammen, dass das Eis zum Grund hinabsinkt. Steigt die Temperatur wieder, kann das Grundeis wieder zur Seeoberfläche aufsteigen. Bei bestimmten Temperaturen kann Oberflächen- und Grundeis gleichzeitig vorkommen.[48][49] Für den Ontario Lacus, einen See nahe dem Südpol des Titan, wurde als Hauptbestandteil Ethan nachgewiesen.
Enceladus
Enceladus stößt Eruptionssäulen von salzhaltigem Wasser aus, das mit Ammoniak und Spuren von Methan und höheren Kohlenwasserstoffen versetzt ist. Dies wird als Resultat hydrothermaler Aktivität in einem Ozean aus flüssigen Wasser unter der Oberfläche des Mondes gedeutet. Dort könnten ähnliche chemischen Reaktionen ablaufen, die das Leben in der Nähe von Hydrothermalquellen in der Tiefsee auf der Erde ermöglichen.[50] Molekularer Wasserstoff, der von methanogenen Mikroben verstoffwechselt werden kann, ist ebenfalls vorhanden.[51] Daher wurden mehrere Missionen vorgeschlagen, um Enceladus weiter zu erforschen und seine Bewohnbarkeit zu beurteilen.
Gewinnung und Darstellung
Gewinnung als Erdgas

Neben Methan kann Erdgas andere Gase wie Ethan, höhere Kohlenwasserstoffe, Sauergase wie Schwefelwasserstoff und Kohlenstoffdioxid sowie Inertgase wie Stickstoff, Helium und weitere Edelgase enthalten. Sogenannte „Trockene Erdgase“ enthalten etwa 75 bis 95 % Methan. Eine Abtrennung von anderen Kohlenwasserstoffkomponenten erfolgt meist nicht, Sauergase und Inertgase werden dagegen abgetrennt.
Im 19. Jahrhundert trat Methan als Bestandteil des Erdgases zunächst als unerwünschtes Nebenprodukt der Erdölförderung auf. Da es zu dieser Zeit keine genügenden Transport- und Speichermedien für die geförderten Mengen gab, wurde es meist einfach in Gasfackeln verbrannt. Diese Methode wird noch in der heutigen Zeit angewandt, falls es keine kommerziell einträglichen Alternativen gibt. Zum Teil wird das Gas wieder zurück in die Erde gepresst. Alternativ kann es durch Abkühlung verflüssigt werden und als Flüssigerdgas transportiert werden.[52]
Gewinnung als Biogas
Biogas ist ein Gasgemisch, das bei der mikrobiellen Zersetzung organischer Materie in Abwesenheit von Sauerstoff entsteht und zu etwa zwei Dritteln aus Methan und zu einem Drittel aus Kohlenstoffdioxid besteht.[53] Biogas wird von Methanbildnern durch Methanogenese von landwirtschaftlichen und Grünabfällen, Abwässern, Lebensmittelabfällen sowie Abfällen aus der Viehzuchtindustrie gebildet und gilt als erneuerbare Energiequelle. Das in Biogasanlagen erzeugte Methan kann etwa als Brennstoff verwendet werden.[54]
Gewinnung aus Methanhydrat
Eine Gewinnung des Methanhydrats könnte zur Lösung irdischer Energieprobleme beitragen, ist jedoch problematisch. Ein besonderes Problem besteht zum Beispiel darin, dass bei der Bergung viel Methan in die Erdatmosphäre gelangen würde und dort als sehr wirksames Treibhausgas zu einer weiteren Erwärmung und damit weiterer Freisetzung von Methan beitragen würde. Außerdem ist die Förderung von Methanhydrat nicht ungefährlich. Erste Förderversuche sind bereits im Gange. Die Folgen eines Raubbaus sind weitgehend ungeklärt; Forscher befürchten das Abrutschen der Kontinentalhänge, die zu großen Teilen aus Methaneis, das durch die Förderung instabil werden könnte, bestehen. Wegen der globalen Erwärmung und der damit verbundenen Meerwassererwärmung befürchten einige Forscher das Schmelzen und Verdampfen des Methanhydrats. Das würde zusätzlich Methan als Treibhausgas in die Erdatmosphäre bringen und den anthropogenen Treibhauseffekt verstärken. Die Freisetzung von Methan aus tauenden Permafrostböden ist ein weiteres Kippelement des Klimawandels.[55]
Methanisierung
Die Methanisierung oder Sabatier-Prozess ist ein Prozess zur Erzeugung von synthetischem Erdgas. Dabei werden Kohle oder andere Kohlenstoff-haltige Materialien durch Kohlevergasung in Kohlenstoffmonoxid oder Kohlenstoffdioxid konvertiert, welche mit Wasserstoff katalytisch zu Methan umgesetzt werden. Diese Reaktion wurde im 19. Jahrhundert durch den Franzosen und Nobelpreisträger Paul Sabatier entdeckt und nach ihm benannt.[56]
- .
- .
Die Reaktion wird nicht großtechnisch zur Herstellung von Methan eingesetzt, sie spielt jedoch eine Rolle beim Entfernen von Kohlenstoffmonoxid-Spuren, die in manchen Prozessen als Katalysatorgift wirken.
Laborsynthesen
Für die Herstellung aus Aluminiumcarbid gibt es zwei Methoden. Aluminiumcarbid kann dazu mit Wasser zu Aluminiumoxid und Methan umgesetzt werden, oder mit Chlorwasserstoff zu Aluminiumchlorid und Methan. Die Methoden werden meist nur im Labor eingesetzt.[57]
Eine weitere Quelle für die Darstellung im Labormaßstab bietet die thermische Zersetzung von Natriumacetat.
Eigenschaften
Physikalische Eigenschaften
Methan schmilzt bei −182,6 °C und siedet bei −161,7 °C. Aufgrund der unpolaren Eigenschaften ist es in Wasser kaum löslich, in Ethanol und Diethylether löst es sich jedoch gut. Die molare Schmelzenthalpie und die molare Verdampfungsenthalpie betragen 1,1 kJ/mol und 8,17 kJ/mol. Der Heizwert Hi liegt bei 35,89 MJ·m−3 beziehungsweise 50,013 MJ kg−1. Die Standardentropie beträgt 188 J·mol−1·K−1, die Wärmekapazität 35,69 J·mol−1·K−1. Der Tripelpunkt von Methan liegt bei 90,67 K und 0,117 bar, der kritische Punkt liegt bei 190,56 K und 45,96 bar.
Festes Methan existiert in mehreren Modifikationen, zurzeit sind neun verschiedene bekannt.[58] Bei der Abkühlung von Methan bei normalem Druck entsteht Methan I. Dabei handelt es sich um einen kubisch kristallisierenden Stoff Raumgruppe Fm3m (Raumgruppen-Nr. 225). Die Positionen der Wasserstoffatome sind nicht fixiert, das heißt, die Methanmoleküle können frei rotieren. Deshalb handelt es sich um einen plastischen Kristall.[59]
Molekulare Eigenschaften
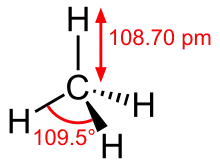
Das Methanmolekül besteht aus einem Kohlenstoffatom (C), an welches vier Wasserstoffatome (H) kovalent gebunden sind, was es zum einfachsten Vertreter der Alkane CnH2n+2 (mit n = 1) macht. Im Zentrum des Moleküls liegt das C-Atom, um das herum die H-Atome tetraedrisch im Abstand von 108,7 Picometer (pm) angeordnet sind. Die im Falle des Methanmoleküls optimal realisierte Tetraederstruktur mit einem zeitgemittelten H–C–H-Bindungswinkel von 109,5° ist für den Aufbau gesättigter Kohlenwasserstoffe grundlegend und steht daher meist am Beginn jeder Einführung in die Organische Chemie. Qualitativ lässt sich diese regelmäßige Anordnung der vier gleichen H-Atome um das zentrale C-Atom bereits im einfachen VSEPR-Bild verstehen, da auf diese Weise die H-Atome – und damit die entlang der C–H-Bindungsachsen erhöhten Elektronendichten – die größtmögliche Entfernung zueinander einnehmen, was Abstoßungseffekte minimiert. Die vier gleichlangen C–H-Bindungen lassen sich im Rahmen einer lokalisierten Valenzbindungstheorie mithilfe von Hybridorbitalen so beschreiben: Das C-Atom ist sp3-hybridisiert, die vier C–H-σ-Bindungen kommen durch paarweise Überlappung je eines der vier sp3-Hybridorbitale mit dem 1s-Orbital je eines H-Atoms zustande.[60] Dieses Modell mit vier energetisch äquivalenten Orbitalen ist jedoch nicht in der Lage, das experimentell ermittelte Elektronenspektrum von Methan zu erklären und widerspricht auch theoretischen Berechnungen.[61] Eine Beschreibung, die Theorie und Experiment in Einklang bringt, liefert die Molekülorbitaltheorie. So erhält man als Elektronenkonfiguration von Methan im Grundzustand (1a1)2(2a1)2(1t2)6, wobei das Molekülorbital 1a1 im Wesentlichen dem kernnahen 1s-Atomorbital des C-Atoms entspricht. Die beiden unterschiedlichen Energieniveaus für Valenzelektronen – das relativ energiearme 2a1-Orbital sowie das dreifach entartete t2-HOMO – entsprechen den gemessenen Ionisierungsenergien von 23 und 14 Elektronenvolt.[62] Aufgrund der Tetraedersymmetrie lassen sie sich im Rahmen eines LCAO-Ansatzes mit symmetrieadaptierten Linearkombinationen der H-1s-Orbitale entwickeln. Durch Überlagerung aller so formulierten Molekülorbitale erhält man auch hier wieder vier äquivalente C–H-Bindungen wie aus dem Hybridorbitalmodell.[63]
- Dichteplots im Grundzustand besetzter Molekülorbitale von Methan auf dem CCSD(T)/cc-pVQZ-Niveau
 1a1
1a1 2a1
2a1 1t2
1t2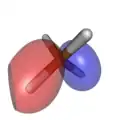 1t2
1t2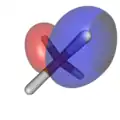 1t2
1t2
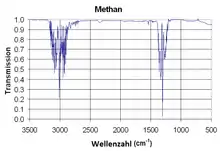
Die mittels Infrarot- und Raman-Spektroskopie gewonnenen Messergebnisse stimmen mit einer Tetraedersymmetrie überein. Es gibt vier Normalmoden für Molekülschwingungen bei etwa 2914, 1534, 3018 und 1306 cm−1, die mit ν1, ν2, ν3 und ν4 bezeichnet werden. Die Schwingungen ν2 (nur bei Wechselwirkungen mit anderen Molekülen, das heißt Symmetriestörung), ν3 und ν4 sind infrarotaktiv.[64][65] Das messbare Schwingungsspektrum setzt sich aus Linearkombinationen dieser Normalmoden zusammen, die im Bereich bis 4800 cm−1 zu jeweils einer Dyade[66] (zwei Kombinationen im Bereich 940–1850 cm−1), Pentade[67] (fünf Kombinationen im Bereich 2150–3350 cm−1) und Octade (acht Kombinationen im Bereich 3550–4800 cm−1) gruppiert werden können, zuzüglich einiger Übergänge zwischen angeregten Zuständen unterschiedlicher Polyaden (sog. hot bands).[68][69]
Chemische Eigenschaften
Im Vergleich zu anderen Alkanen weist die C-H-Bindung im Methan eine höhere Bindungsenergie auf. In Reaktionen mit radikalischer Abstraktion des Wasserstoffatoms ist Methan gewöhnlich das am wenigsten reaktive Alkan. Das Methylkation (CH3+) ist das instabilste Carbeniumion. Daher ist Methan in Reaktionen unter Hydrid-Abstraktion ebenfalls wenig reaktiv. In Elektronentransferreaktionen reagiert Methan aufgrund seines hohen Ionisierungspotentials meist träge.[23] Mit Eisen-, Kupfer- oder Aluminiumatomen reagiert photochemisch angeregtes Methan in einer Methanmatrix bei tiefen Temperaturen unter Insertion des Metalls in die H–C-Bindung unter Bildung eines Metallkomplexes wie etwa H–Fe–CH3.[70]
Methan ist stabil gegenüber herkömmlichen Säuren und Laugen. Mit Supersäuren wie Hexafluorantimonsäure lässt sich Methan zum Methaniumion (CH5+) protonieren. Der Name Methanium wurde in Analogie zum Ammoniumion gewählt.[71] Mit Oxidationsmitteln wie Kaliumpermanganat oder Kaliumdichromat lässt es sich nicht oxidieren. Mit Oxidationsmitteln wie Peroxodisulfaten oder Cer(IV)-Salzen bildet Methan in Schwefelsäure einen Monomethylester (CH3-OSO3H).[72]
Methan ist brennbar und verbrennt an der Luft mit bläulicher, nicht rußender Flamme. Aus der Reaktion eines Methanmoleküls mit zwei Sauerstoffmolekülen entstehen zwei Wasser- und ein Kohlenstoffdioxidmolekül. Es kann explosionsartig mit Sauerstoff oder Chlor reagieren, wozu eine Initialzündung (Zufuhr von Aktivierungsenergie) oder Katalyse erforderlich ist.
Mit Sauerstoff geht Methan unterschiedliche Reaktionen ein, je nachdem wie viel Sauerstoff für die Reaktion zur Verfügung steht. Nur bei genügend großem Sauerstoffangebot ist eine vollständige Verbrennung des Methans mit optimaler Energieausbeute möglich.[73]
Bei ungenügender Sauerstoffzufuhr hingegen entstehen Nebenprodukte wie Kohlenstoffmonoxid (CO) und Kohlenstoff (Ruß). Ferner ist in diesem Fall die Nutzenergie geringer.
Mit Chlor und Brom geht Methan unter Lichteinfluss Substitutionsreaktion ein, wobei die Wasserstoffatome durch Halogenatome ersetzt werden. Bei einer solchen Reaktion kommt es oft zu Mehrfachsubstitutionen, da das zunächst gebildete monohalogenierte Produkt tendenziell schwächere H-C-Bindungen aufweist als Methan selbst und daher selektiv weiter oxidiert wird. Iodverbindungen lassen sich durch Halogenaustausch herstellen.
Mit Dampf bildet sich bei hohen Temperaturen und unter Katalyse Wasserstoff, Kohlenstoffmonoxid und Kohlenstoffdioxid. Diese sogenannte Dampfreformierung ist der technische Prozess, mit dem technisch Wasserstoff und Synthesegas hergestellt werden.
Bei Temperaturen von etwa 2000 °C bildet sich bei schneller Abkühlung Ethin. Ohne Abkühlung zerfällt Methan ab etwa 1100 °C in die Elemente.[74] Bei einer Temperatur von etwa 1200 °C reagiert Methan mit Ammoniak zu Cyanwasserstoff und Wasserstoff.[75]
Verwendung
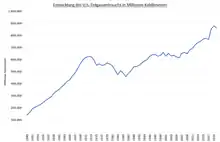
Methan wird vorwiegend als Heizgas zur Wärmeerzeugung und zum Betrieb von Motoren durch Verbrennung genutzt. Die Verwendung von Methan als Bestandteil von Erdgas stieg von 1950 bis 2020 etwa um den Faktor 5.[76] Neben Methan aus Erdgas wird zu diesem Zweck Biogas (Biomethan) mit einem Methangehalt von etwa 50 bis 70 % aus Mist, Gülle, Klärschlamm oder organischem Abfall gewonnen. Früher wurde Methan durch Pyrolyse von Holz gewonnen, bei der Holzgas entsteht (Holzvergasung). Holzgas, das unter anderem Methan enthält, diente wegen des Erdölmangels im Zweiten Weltkrieg zum Betrieb von zivilen Automobilen. Die aufheizenden Holzvergaser wurden meist außen angebaut. Rohes Biogas aus Abwasserreinigungsanlagen wird heute oft direkt mit Verbrennungsmotoren in Strom umgewandelt.
Verwendung als Brenn- und Kraftstoff
Durch das hohe Verhältnis von Wasserstoff zu Kohlenstoff im Methan wird bei der Verbrennung eine größere Menge an Energie pro freigesetztem Kohlenstoffdioxidmolekül geliefert als von flüssigen Kohlenwasserstoffen auf Basis von Erdöl, deren ungefähres Verhältnis von Wasserstoff zu Kohlenstoff etwa zwei beträgt oder von Kohle mit einem ungefähren Wasserstoff zu Kohlenstoffverhältnis von eins. Durch das hohe molare Verhältnis von Wasserstoff zu Kohlenstoff von 4 : 1 im Methan wird bei der Verbrennung von Methan eine größere Menge an Energie pro freigesetztem Kohlenstoffdioxidmolekül geliefert als bei allen anderen kohlenstoffhaltigen Energieträgern.
Bei Verwendung von Methan als alternativem Kraftstoff in Motoren werden etwa 2 % des Methans nicht verbrannt und müssen durch einen Fahrzeugkatalysator umgesetzt werden. Vor der Einführung einer Abgasnachbehandlung und schwefelfreien Kraftstoffs hatten methanbasierte Kraftstoffe ein geringeres Versauerungs- und Eutrophierungspotential sowie geringere Effekte auf die menschliche Gesundheit als die Verbrennung von Dieselkraftstoff. Dies war auf die geringeren Stickoxidemissionen bei der Verbrennung zurückzuführen.[78] In Fahrzeugen nach der aktuellen Abgasnorm sind die Emissionen nach der Abgasnachbehandlung unabhängig vom Kraftstoff auf ähnlichem Niveau.
Verwendung als Chemierohstoff
Methan dient als wichtiges Ausgangsprodukt für die technische Synthese von Ethin, Cyanwasserstoff, Schwefelkohlenstoff, Halogenalkane und vielen anderen organischen Verbindungen. Methan ist ein wichtiger Rohstoff für die Herstellung von Wasserstoff sowie Kohlenstoffmonoxid. Die Folgechemie von Wasserstoff-Kohlenstoffmonoxid-Gemischen ist vielfältig. Sie werden unter anderem zur Herstellung von Methanol oder in der Fischer-Tropsch-Synthese für die Herstellung von Alkanen genutzt.
Dampfreformierung und partielle Oxidation
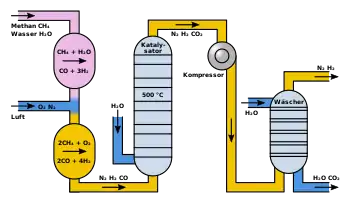
| Primärreformer | Sauerstoffeinspeisung |
| Sekundärreformer | CO-Konvertierung |
| Waschturm |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Folgeprodukte der Dampfreformierung von Methan (Auswahl). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Die Dampfreformierung, die partielle Oxidation und die Wassergas-Shift-Reaktion sind großtechnische durchgeführte Reaktionen. Das zunächst entstehende Produkt der Dampfreformierung ist ein als Synthesegas bezeichnetes Gasgemisch, das unter anderem für die Produktion von Methanol verwendet wird.
Die partielle Oxidation von Methan wird ebenfalls als katalytisches Verfahren durchgeführt. Dabei reagiert Methan mit Sauerstoff in einer exothermen Reaktion zu Kohlenstoffmonoxid und Wasserstoff. Der Energiebedarf der partiellen Oxidation ist daher geringer ist als bei der Dampfreformierung, erfordert jedoch den Einsatz von reinem Sauerstoff als Reaktand. Weiterhin besteht die Gefahr einer Explosion bei instabilen Prozessbedingungen.[79]
Eine Kombination beider Prozesse, bei der die partielle Oxidation den Energiebedarf der Dampfreformierung deckt, wird Autothermale Reformierung genannt.[79]
Ist Wasserstoff das Zielprodukt, wird das entstandene Kohlenstoffmonoxid mit weiterem Wasser in einem sogenannten Sekundärreformer einer Wassergas-Shift-Reaktion zu Kohlenstoffdioxid und weiterem Wasserstoff umgesetzt.[80] Als Katalysatoren dienen Eisen(III)-oxid-Kontakte.
Der im Jahr 2010 hergestellte Wasserstoff wurde zu 98 % durch Dampfreformierung hergestellt.[81] Die Folgeprodukte der Dampfreformierung und der partiellen Oxidation sind vielfältig. Je nach Kohlenstoffmonoxid zu Wasserstoffverhältnis wird das Synthesegas zur Methanolherstellung oder zur Hydroformylierung von Olefinen eingesetzt.[82][83] Reiner Wasserstoff wird zur Produktion von Ammoniak im Haber-Bosch-Verfahren oder für Hydrierungen eingesetzt.
Thermokatalytische Zersetzung
Bei den genannten drei Verfahren fällt entweder Kohlenstoffmonoxid oder Kohlenstoffdioxid als weiteres Produkt an.[81] Eine Kohlenstoffdioxid-freie Route zu Wasserstoff besteht in der thermischen oder thermokatalytischen Zersetzung von Methan in Kohlenstoff und Wasserstoff.[81] Die Herstellung von Wasserstoff aus Methan unter Abtrennung von Kohlenstoff bietet einen Weg, Energie aus Wasserstoff durch Verbrennung oder in Brennstoffzellen ebenfalls ohne Kohlenstoffdioxid zu erzeugen.
Als Katalysator dient Nickel, der entweder als Netz oder als Nickelsalz auf verschiedenen Trägern eingesetzt werden kann. Gegenüber dem rein thermischen Zerfall, der bei etwa 1200 °C stattfindet, liegt das Temperaturniveau der thermokatalytischen Zersetzung bei etwa 500 bis 600 °C.
Herstellung von Ethin
Für die Herstellung von Ethin aus Methan sind verschiedene Prozesse entwickelt worden, etwa die autotherme Verbrennung im Sachsse-Bartholomé-Verfahren.[84] Die Herstellung von Ethin gelingt weiterhin durch die thermische Spaltung von Methan im Lichtbogen bei Temperaturen von 2000 bis 3000 °C gemäß folgender Gleichung:[74]
Als Nebenprodukt fällt Ruß an. Die oxidative Kopplung von Methan zu Ethin durch die Reaktion mit Sauerstoff ist ebenfalls möglich, die Selektivität zu Ethin ist mit 20 % eher gering.[74]
Herstellung von Kohlenstoffdisulfid
Methan geht außer mit Sauerstoff noch vielfältige weitere Reaktionen ein, etwa mit Schwefel. Die Reaktion zu Kohlenstoffdisulfid läuft bei einer Temperatur von etwa 600 °C in Gegenwart von Kieselgel- oder Aluminiumoxidkatalysatoren ab:
Kohlenstoffdisulfid wird in großem Umfang zur Produktion von Kunstseide verwendet.[85]
Herstellung von Cyanwasserstoff
Beim Andrussow-Verfahren reagiert Methan mit Ammoniak in Gegenwart von Sauerstoff zu Cyanwasserstoff und Wasser.
Beim BMA-Verfahren der Degussa reagiert Methan mit Ammoniak in Gegenwart eines Platin-Katalysators bei Temperaturen von etwa 1200 °C direkt zu Cyanwasserstoff.
Cyanwasserstoff wird zur Herstellung von Adiponitril, einem Zwischenprodukt für die Herstellung von Nylon 6,6, durch Hydrocyanierung verwendet, der katalytischen Addition von Cyanwasserstoff an 1,3-Butadien.[86] Die Herstellung von Acetoncyanhydrin erfolgt durch die katalytische Addition von Cyanwasserstoff an Aceton. Weiterhin werden die α-Aminosäure DL-Methionin, die Verwendung in der Futtermittel-Supplementierung findet, sowie der Heterocyclus Cyanurchlorid aus Cyanwasserstoff hergestellt.
Herstellung von Halogenmethanen

Die Chlorierung von Methan kann katalytisch, thermisch oder photochemisch erfolgen. Bei der Chlorierung nach allen drei Prozessen entstehen neben Chlormethan auch die höhere chlorierten Produkte Dichlormethan, Chloroform und Tetrachlormethan. Die höher substituierten Produkte entstehen bereits zu Beginn der Reaktion, wenn noch genügend unreagiertes Methan vorliegt. Die Reaktion ist stark exotherm mit etwa 100 Kilojoule pro Substitutionsreaktion:[87]
- mit ΔRH = −103,5 kJ·mol−1
- mit ΔRH = −102,5 kJ·mol−1
- mit ΔRH = −99,2 kJ·mol−1
- mit ΔRH = −94,8 kJ·mol−1
Die Photochlorierung von Methan läuft bei Belichtung unter Beteiligung von Methyl- und Chlorradikalen als Kettenträger nach dem folgenden Schema ab:
Höherhalogenierte Produkte entstehen nach demselben Schema, wobei die gezielte Synthese von Chloroform bevorzugt über die Chlorierung von Aceton und die Synthese von Tetrachlormethan über die Chlorierung von Kohlenstoffdisulfid erfolgt.
Die chlorierten Methanderivate finden vielfältige industrielle Anwendung. Methylchlorid wird zur Herstellung von Methylzellulose verwendet, früher wurde es zur Herstellung von Tetramethylblei verwendet. Dichlormethan wird vor allem als Lösungsmittel verwendet. Brommethan wird in der Schädlingsbekämpfung zu Bodenbegasung und Begasung von Transportbehältern eingesetzt.
Biologische Bedeutung
Methanogene Archaeen

Die Methanogenese in Methanbildnern aus der Domäne der Archaeen oder Urbakterien ist eine Form der anaeroben Atmung. Als Kohlenstoffquelle dienen zum Beispiel Kohlenstoffdioxid, Essigsäure sowie C1-Verbindungen wie Methanol und Ameisensäure. Der überwiegende Teil des irdischen Methans stammt aus der biotischen Methanogenese durch die Reduktion von Kohlenstoffdioxid durch biologisch erzeugten Wasserstoff sowie durch den Zerfall von Essigsäure in Kohlenstoffdioxid und Methan durch Essigsäure-spaltende, acetoklastische Methanbildner.[88][89]
Methanotrophe Mikroben
Methan wird durch bestimmte methanotrophe Prokaryoten, etwa Methylococcus capsulatus, in Gewässern und Böden mit Sauerstoff zu Kohlenstoffdioxid und Wasser oxidiert. Es kann sich dabei um Bakterien oder Archaeen handeln, die unter aeroben oder anaeroben Bedingungen wachsen. Diese Umsetzung ist exergon und die Prokaryoten nutzen sie als Energiequelle. Diese sind oft in der Nähe von Methanquellen zu finden, etwa in Feuchtgebieten oder in aquatischen Umgebungen.[90] Aufgrund ihrer Rolle als Methansenke, welche die Freisetzung von Methan in die Atmosphäre reduziert, wird ihr möglicher positiver Einfluss auf die Reduktion der globalen Erwärmung untersucht.
In den Höhlen und unterirdischen Flüssen der Halbinsel Yucatán ist Methan die treibende Kraft für das dortige Leben. Das im Wasser gelöste Methan wird durch Bakterien umgewandelt und stellt somit die Grundlage des lokalen Nahrungsnetzes dar. Die dort lebenden Krebstiere beispielsweise beziehen bis zu 21 % ihrer Nahrung indirekt über methanotrophe Mikroben aus Methan.[91]
Die Umsetzung des Methans erfolgt unter anderem über das Enzym Methan-Monooxygenase, welches die Oxidation zu Methanol katalysiert. Die Methan-Monooxygenase liegt in einer löslichen Form mit zwei sauerstoffverbrückten Eisenatomen im aktiven Zentrum und einer unlöslichen Form vor, die ein Kupferatom im aktiven Zentrum enthält.[92]
Zoo- und Phytoplankton
Meeresalgen wie Emiliania huxleyi und andere Haptophyta produzieren im Ozean signifikante Mengen Methan: Versuche mit 13C-markierten Substraten wie Hydrogencarbonat, methylierten Schwefelverbindungen wie Dimethylsulfid, Dimethylsulfoxid und Methioninsulfoxid führten zur Bildung von 13C-angereichertem Methan. Feldstudien etwa im Pazifischen Ozean zeigten, dass die Methanproduktion durch Algen wahrscheinlich ein häufig ablaufender und wichtiger Prozess in marinen Oberflächengewässern ist.[93] Zooplankton setzt bei der Konsumtion von Algen ebenfalls Methan frei, das vermutlich im Verdauungstrakt gebildet wird. Ein möglicher Mechanismus ist Umsetzung neu gebildeter Methylamine wie Methylamin und Trimethylamin.[94]
Umweltrelevanz
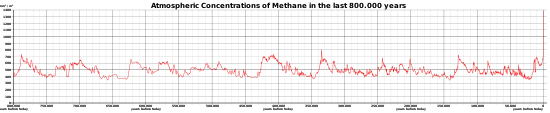
Methan könnte als Treibhausgas vor etwa 252 Mio. Jahren das größte Massenaussterben des Phanerozoikums mit verursacht haben. Der Anstieg seiner Konzentration in der Erdatmosphäre in der Moderne ist einer der Aspekte des Anthropozäns. Laut zweier Studien des Global Carbon Project stammten 2017 mehr als 60 % der Methan-Emissionen aus der menschlichen Wirtschaft.[95][96]
Atmosphärenchemie
Da das farb- und geruchlose Gas eine geringere Dichte als Luft aufweist, steigt es in die höheren Schichten der Erdatmosphäre auf. Dort wirkt es als Treibhausgas, wobei es 20- bis 30-mal wirkungsvoller ist als Kohlenstoffdioxid, wobei es in viel geringeren Mengen als dieses in der Atmosphäre vorkommt. In einer sauerstoffhaltigen Atmosphäre wird Methan langsam oxidiert, insbesondere durch Hydroxyl-Radikalen zu Kohlenstoffdioxid und Wasser. Dieser Prozess ist langsam, die Halbwertszeit wird auf 12 Jahre geschätzt.[8][97] Laut anderen Schätzungen beträgt die atmosphärische Verweildauer 8–15 Jahre und ist verglichen mit anderen Treibhausgasen kurz.[98]
Treibhauspotenzial
Sein Treibhauspotenzial ist dabei, auf einen Zeitraum von 100 Jahren bezogen, 28-mal höher als das der gleichen Gewichtsmenge Kohlenstoffdioxid. Nach einer neueren Untersuchung beträgt dieser Faktor 33, wenn Wechselwirkungen mit atmosphärischen Aerosolen berücksichtigt werden.[8][99] Auf einen Zeitraum von 20 Jahren bezogen steigt dieser Faktor auf 84. Methan trägt rund 20 bis 30 % zum anthropogenen Treibhauseffekt bei.[100] Nach Einschätzung des Umweltprogramms der Vereinten Nationen könnte mit Maßnahmen gegen Methan-Emissionen erreicht werden, dass die mittlere globale Temperatur bis 2045 um fast 0,3 °C langsamer anwächst als erwartet.[100] Im Vergleich zu Kohlendioxid hat Methan eine kürzere Verweildauer in der Erdatmosphäre (12 Jahre ggü. 5–200 Jahre).[101] Das UN-Umweltprogramm Unep hat im Oktober 2021 die Gründung einer Internationalen Beobachtungsstelle für Methanemissionen (IMEO) angekündigt, mit der die von den USA und der EU initiierte „Globale Methan-Verpflichtung“ ergänzt werden soll.[102][103]
Methanquellen

Die Methankonzentrationen stiegen zwischen 2000 und 2006 jährlich um etwa 0,5 ppb, seit 2006 mit einer mehr als zehnfach höheren Rate.[104] Damit ist weit mehr Methan in der Erdatmosphäre als jemals während der letzten 650.000 Jahre.[105] Eine im Februar 2020 erschienene Studie von Forschern der University of Rochester sieht starke Indizien dafür, dass rund zehnmal weniger Methan auf natürliche Weise aus geologischen Quellen austritt als bislang angenommen. Im Umkehrschluss hat die Förderung fossiler Energien (Öl, Gas und Kohle) einen deutlich höheren Anteil an den Methanemissionen.[106]
Jährlich werden auf der Erde etwa 600 Millionen Tonnen Methan emittiert. In Deutschland sank die Emission zwischen 1990 und 2018 von 121,2 Millionen Tonnen auf etwa 52,6 Millionen Tonnen CO2-Äquivalent.[107]
Anfang 2014 berichtete das Forschungsmagazin Science nach einer Meta-Studie von über 200 Studien, dass die US-amerikanische Umweltschutzbehörde Environmental Protection Agency (EPA) den Methangas-Ausstoß in den USA seit 20 Jahren zu gering angegeben habe. In den USA wurden jährlich 40 Millionen Tonnen mehr in die Atmosphäre emittiert als bisher offiziell angenommen, sowohl aus natürlichen Quellen wie auch aus der Viehhaltung von beispielsweise 88 Millionen Rindern im Land sowie aus Lecks in Förderanlagen und Pipelines. Basierend auf Daten aus Feldmessungen werden die jährlichen Methanemissionen aus der Öl- und Gaslieferkette auf etwa 13 Millionen Tonnen pro Jahr geschätzt und liegen damit 60 % über den Schätzungen der US-Umweltschutzbehörde. Bei der Öl- und Gasproduktion sind die gemessenen Emissionen sogar doppelt so hoch wie die behördlichen Schätzwerte. Mittels des Tropomi-Spektrometers wurden allein im Permian Basin in Texas 2018 eine jährliche Emission von 2,9 ±0,5 Millionen Tonnen gemessen.[108] Unklar ist bislang (2014), wieweit die fehlerhaften Angaben Einfluss auf die Rechenmodelle zur Entwicklung des Weltklimas haben.[109]
Hydraulic Fracturing
Der Ausstoß von Methan hat besonders in den Vereinigten Staaten signifikant zugenommen. Dieser könnte mit der Förderung von Schiefergas durch Hydraulic Fracturing (Fracking) zusammenhängen.[110][111] Es gibt erhebliche Unsicherheiten über das Ausmaß der Methanleckagen im Zusammenhang mit Hydraulic Fracturing und Hinweise darauf, dass die Leckagen die Vorteile der Verbrennung von Erdgas gegenüber anderen fossilen Brennstoffen zunichtemachen könnten. Laut einer 2020 veröffentlichten Studie emittieren Fracking-Anlagen doppelt so viel Methan wie zuvor geschätzt. Für die Hydraulic-Fracturing-Anlagen in Pennsylvania wird eine Leckagerate von etwa 10 % angenommen, die als repräsentativ für die Hydraulic-Fracturing-Industrie in den USA im Allgemeinen angesehen wird. Die Methanemissionen im Gebiet der Marcellus-Formation wurden pro Jahr zu etwa 0,67 Millionen Tonnen bestimmt.[112]
Permafrost
Die Freisetzung von Methan aus Permafrost und vom Meeresboden ist eine mögliche Folge und eine weitere Ursache für die globale Erwärmung.[113] Aus arktischen Permafrostböden wird Methan sowohl geologischen als auch biologischen Ursprungs freigesetzt, biogenes durch Umwandlung von Permafrost in Feuchtgebiete. Biogenes Methan wird in Abhängigkeit von den Wetterbedingungen wie Temperatur und Sonneneinfall freigesetzt, während Methan geologischen Ursprungs unabhängig davon freigesetzt wird.[114]
Öl- und Kohlegewinnung und Transport
Durch nicht bemerkte Lecks in Raffinerien und beim Transport von Öl und Gas durch Pipelines werden erhebliche Mengen Methan emittiert. Die Internationale Energieagentur (IEA) in Paris schätzt diese Menge Ende 2017 auf rund 75 Mio. Tonnen pro Jahr und damit 1,7 % der Gesamtfördermenge.[115]
Studien deuten darauf hin, dass die Methan-Emissionen aus Kohleminen stark unterschätzt wurden.[116] So wurde 2014 in der Gegend um Four Corners durch Satellitendaten eine gewaltige Methanemission aus nahe gelegenen Kohleabbaustätten detektiert.[117] Mit geschätzten 600.000 Tonnen Methan pro Jahr sind die Emissionen größer als die der gesamten britischen Öl-, Gas- und Kohleindustrie.[118]
Durch Leckagen in der Erdgasinfrastruktur kann es zu bedeutenden Freisetzungen von Methan kommen. So führte 2015 ein Leck in einer unterirdischen Speicheranlage im Aliso Canyon zu einer massiven Freisetzung von Erdgas, bei der etwa 100.000 Tonnen Methan freigesetzt wurden.[119] Bei einem Blowout in Ohio im Jahr 2018 wurden über einen Zeitraum von 20 Tagen etwa 57.000 Tonnen Methan emittiert.[120]
Reisanbau, Ziegen-, Schaf- und Rinderzucht
Etwa 70 % der mikrobiellen Methanemission der Erde ist auf menschliche Aktivitäten zurückzuführen. Die Methanemissionen in der Landwirtschaft und bei der Tierhaltung gehen zu 39 % auf die Rinderhaltung und zu 17 % auf den Nassreisanbau zurück. Die Ernährungs- und Landwirtschaftsorganisation der Vereinten Nationen (FAO) schrieb 2006 dem Viehwirtschaftssektor ein knappes Fünftel der vom Menschen verursachten Treibhausgasemissionen zu, etwas mehr als dem Transportsektor.[121] Viele Pflanzen produzieren ständig Methan und tragen so seit jeher zum Methangehalt der Atmosphäre bei.[122]
Die archaeellen Methanbildner im Pansen wiederkäuender Tiere sind für die ständige Neubildung von Methan verantwortlich. Ein Hausrind stößt täglich etwa 150 bis 250 Liter Methan aus, weil im Rindermagen Methanogene an der Zersetzung von Cellulose beteiligt sind. Die Senkung der Methanemission von Kühen durch Futterzusätze wird intensiv erforscht.[123][124][125][126][127] Möglicherweise können die Methanemissionen der Wiederkäuer durch spezielle Impfungen gesenkt werden.[128] Die Methanbildung reduziert auch die Energie, die den Tieren durch die Nahrungsaufnahme zur Verfügung gestellt wird und damit nicht für die Produktion von Milch, Fleisch oder Fasern zur Verfügung steht. Schätzungen gehen von einem Energieverlust von etwa 6 bis 10 % der Bruttoenergieaufnahme aus.[129]
Sicherheitsaspekte
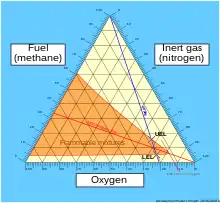
Methan ist hoch entzündlich, der Flammpunkt liegt bei −188 °C, die Zündtemperatur bei 595 °C.[1] Methan bildet bei einem Volumenanteil zwischen 4,4 und 16,5 % in Luft explosive Gemische.
Durch unbemerktes Ausströmen von Erdgas kommt es immer wieder zu folgenschweren Gasexplosionen, etwa die Explosion der New London School 1937. In Folge wurde die Beimengung von Methanthiol, Tetrahydrothiophen oder ähnlichen, leicht wahrnehmbaren Odoriermitteln zum Erdgas vorgeschrieben.[130] Methanbehälter sollen an gut belüfteten Orten aufbewahrt und von Zündquellen ferngehalten werden und es sollten Maßnahmen gegen elektrostatische Aufladung getroffen werden. Die gefürchteten Grubengasexplosionen in Kohlebergwerken, sogenannte Schlagwetter, sind auf Methan-Luft-Gemische zurückzuführen.
Methan wird, um die Dichte zu erhöhen, unter hohem Druck in Gasflaschen bei 200 bar aufbewahrt. Methan liegt in der handelsüblichen 50 Liter-Stahlflasche oder in Kraftfahrzeugtanks, oft mit Kohlenstofffasern verstärktes Epoxidharz über Aluminium-Liner, komprimiert auf 200 bar gasförmig vor, sogenanntes Compressed Natural Gas (CNG).[131]
Der Schifftransport in großen Mengen erfolgt in fast überdrucklosen Membrantanks, jedoch bei etwa −162 °C tiefkalt verflüssigt, sogenanntes Liquified Natural Gas (LNG).[132] Schiffe mit Rohr- und Kugeltanks transportieren Erdgas bei einem Druck von etwa 200 bis 300 bar und bei höherer Temperatur.[133]
Methan wird bei tiefen Temperaturen flüssig gelagert, weil die Dichte dadurch enorm erhöht werden kann. Aus diesem Grund kann es beim Austritt dieses gekühlten Methans leicht zu Erfrierungen kommen. Methan selbst ist ungiftig, durch Verdrängung von Sauerstoff aus der normalen Atemluft jedoch kann die Aufnahme von Methan zu erhöhter Atemfrequenz (Hyperventilation) und erhöhter Herzfrequenz führen, kurzzeitig niedrigen Blutdruck, Taubheit in den Extremitäten, Schläfrigkeit, mentale Verworrenheit und Gedächtnisverlust auslösen, alles hervorgerufen durch Sauerstoffmangel. Methan führt nicht zu bleibenden Schäden.[134] Wenn die Symptome auftreten, sollte das betroffene Areal verlassen und tief eingeatmet werden, falls daraufhin die Symptome nicht verschwinden, sollte die betroffene Person in ein Krankenhaus gebracht werden.
Nachweis
Der Nachweis von Methan kann mittels Infrarotspektroskopie erfolgen. Für den Nachweis extraterrestrischer Vorkommen ist der infrarotspektroskopische Nachweis etabliert.[135] Methan kann mittels Gaschromatographie und mit Gaschromatographie mit Massenspektrometrie-Kopplung nachgewiesen und quantifiziert werden.[136] Im Bergbau wurden früher zur Warnung vor Schlagwettern verschiedene qualitative Nachweismethoden eingesetzt, etwa die Davy-Lampe mit Flammsieb.
Literatur
- Enoch Durbin: Methane: Fuel for the Future. Plenum Press, New York, London, 1982, ISBN 978-1-4684-4342-4
- Reiner Wassman, Rhoda S. Lantin, Heinz-Ulrich Neue: Methane Emissions from Major Rice Ecosystems in Asia. Springer, 2000, ISBN 978-0-7923-6765-9
- Peter Pfeifer, Roland Reichelt (Hrsg.): H2O & Co. Organische Chemie. Oldenbourg, München 2003, ISBN 3-486-16032-X. (Extrakapitel über Methan und Informationen zu den anderen Alkanen)
- Pflanzen – eine vergessene Methanquelle. In: Bergbau. Heft 1/2007, S. 7–8. (Digitalisat, PDF-Datei, 72,2 kB)
Weblinks
Einzelnachweise
- Eintrag zu CAS-Nr. 74-82-8 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- D. H. Ripin, D. A. Evans: pKa's of Inorganic and Oxo-Acids. (PDF) Abgerufen am 15. Juli 2014 (englisch).
- S. Budavari u. a.: The Merck Index, 12. Auflage. MERCK & CO., 1996, S. 1018
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Permittivity (Dielectric Constant) of Gases, S. 6-188.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Index of Refraction of Gases, S. 10-254.
- Eintrag zu Methane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 74-82-8 bzw. Methan), abgerufen am 15. September 2019.
- G. Myhre u. a.: Anthropogenic and Natural Radiative Forcing. In: Climate Change 2013: The Physical Science Basis. Contribution of Working Group I to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge University Press, Cambridge/ New York 2013, S. 731, (PDF).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-26.
- George A. Olah, Alain Goeppert, G. K. Surya Prakash: Beyond oil and gas: the methanol economy. Verlag Wiley-VCH, 2009, ISBN 978-3-527-32422-4 (Anm.: 2018 erschien die 3. (erweiterte und aktualisierte) Auflage; ISBN 978-3527338030).
- August Wilhelm von Hofmann: On the action of trichloride of phosphorus on the salts of the aromatic monoamines. In: Proceedings of the Royal Society of London, Band 15, S. 55–62; Fußnoten: S. 57–58(online).
- Giuseppe Etiope, Agnieszka Drobniak, Arndt Schimmelmann: Natural seepage of shale gas and the origin of „eternal flames“ in the Northern Appalachian Basin, USA. In: Marine and Petroleum Geology, 43, 2013, S. 178–186, doi:10.1016/j.marpetgeo.2013.02.009.
- Mirella Galletti: Kirkuk: The Pivot of Balance in Iraq Past and Present. In: Journal of Assyrian Academic Studies, 19.2, 2005, S. 21–42.
- Henry A. Spiller, John R. Hale, Jelle Z. De Boer: The Delphic Oracle: A Multidisciplinary Defense of the Gaseous Vent Theory. In: Journal of Toxicology: Clinical Toxicology. 40, 2002, S. 189–196, doi:10.1081/CLT-120004410.
- David Curtis Wright: The history of China. Greenwood Press, Westport, 2001, ISBN 0-313-30940-X, S. 41.
- Thomas Shirley: The description of a well, and earth in Lanchashire, taking fire by a candle approached to it. In: Philosophical Transactions of the Royal Society of London. 2, 1666, S. 482–484, doi:10.1098/rstl.1666.0028.
- Anand Kumar Sethi: The European Edisons: Volta, Tesla, and Tigerstedt. Palgrave McMillan, 2016, ISBN 978-1-137-49220-3, S. 9–12.
- Alessandro Volta: Briefe über die natürlich entstehende entzündbare Sumpfluft. Wintherthur, bey Heinrich Steiner und Compagnie, 1778.
- Jaime Wisniak: William Henry: His Achievements and His Law. In: The Chemical Educator. 6, 2001, S. 62–68, doi:10.1007/s00897000449a.
- C. Morton: Observations on the Safety Lamp. In: Proceedings of the Yorkshire Geological Society. 1, 1839, S. 21–25, doi:10.1144/pygs.1.21.
- S. Faramawy, T. Zaki, A.A.-E. Sakr: Natural gas origin, composition, and processing: A review. In: Journal of Natural Gas Science and Engineering, 34, 2016, S. 34–54, doi:10.1016/j.jngse.2016.06.030.
- History, bei naturalgas.org, abgerufen am 17. Juli 2021.
- Robert H. Crabtree: Aspects of methane chemistry. In: Chemical Reviews, 95.4, 1995, S. 987–1007.
- X. Xiong, F. Weng, Q. Liu, E. Olsen: Space-borne observation of methane from atmospheric infrared sounder version 6: validation and implications for data analysis. In: Atmospheric Measurement Techniques Discussions. 8, 2015, S. 8563–8597, doi:10.5194/amtd-8-8563-2015.
- Giora Proskurowski, Martin D. Lilley, Jeffery S. Seewald, Gretchen L. Früh-Green, Eric J. Olson, John E. Lupton, Shean P. Sylva, Deborah S. Kelley: Abiogenic hydrocarbon production at Lost City Hydrothermal Field. In: Science, Band 319, 2008, S. 604–607
- William Martin: Alles hat einen Anfang, auch die Evolution: Hydrothermalquellen und der Ursprung des Lebens (PDF; 945 kB). In: Biologie in unserer Zeit. 3/2009(39), S. 166–173. doi:10.1002/biuz.200910391
- Bing Xie, Hua Zhang, Dong-Dong Yang, Zhi-Li Wang: A modeling study of effective radiative forcing and climate response due to increased methane concentration. In: Advances in Climate Change Research. 7, 2016, S. 241–246, doi:10.1016/j.accre.2016.12.001.
- Cristina Prados-Roman u. a.: Atmospheric formaldehyde at El Teide and Pic du Midi remote high-altitude sites. In: Atmospheric Environment. 234, 2020, S. 117618, doi:10.1016/j.atmosenv.2020.117618.
- U. Deppenmeier, V. Müller: Life close to the thermodynamic limit: how methanogenic archaea conserve energy. In: Günter Schäfer, Harvey S. Penefsky (Hrsg.): Bioenergetics: Energy Conservation and Conversion. Results and Problems in Cell Differentiation, Volume 45. Springer 2008, ISBN 978-3-540-78622-1, S. 123–152. PMID 17713742; doi:10.1007/400_2006_026.
- David M. Karl, Lucas Beversdorf u. a.: Aerobic production of methane in the sea. In: Nature Geoscience, 1, 2008, S. 473–478, doi:10.1038/ngeo234.
- Siddhesh S. Kamat, Howard J. Williams u. a.: The catalytic mechanism for aerobic formation of methane by bacteria. In: Nature, 497, 2013, S. 132–136, doi:10.1038/nature12061
- Fred N. Kissell u. a.: Handbook for methane control in mining. DHHS (NIOSH) Publication, No. 2006–127, NIOSH–Publications Dissemination, Cincinnati, S. 3–7.
- M. J. Hunt: Petroleum geochemistry and geology. 2. Auflage, W. H. Freeman and Company, New York 1995
- Keith A. Kvenvolden: Methane hydrate — A major reservoir of carbon in the shallow geosphere?. In: Chemical Geology. 71, 1988, S. 41–51, doi:10.1016/0009-2541(88)90104-0.
- C. D. Ruppel, J. D. Kessler: The interaction of climate change and methane hydrates. In: Reviews of Geophysics, 55, 2017, S. 126–168, doi:10.1002/2016RG000534.
- Bruce Buffett, David Archer: Global inventory of methane clathrate: sensitivity to changes in the deep ocean. In: Earth and Planetary Science Letters. 227, 2004, S. 185–199, doi:10.1016/j.epsl.2004.09.005.
- A. V. Milkov: Global estimates of hydrate-bound gas in marine sediments: how much is really out there? In: Earth-Science Reviews, Vol. 66, 2004, S. 183–197.
- Andrés Guzmán-Marmolejo, Antígona Segura: Methane in the Solar System. In: Boletín de la Sociedad Geológica Mexicana, 67, 3, 2015, S. 377–385.
- L.A. Sromovsky, E. Karkoschka, P.M. Fry, H.B. Hammel, I. de Pater, K. Rages: Methane depletion in both polar regions of Uranus inferred from HST/STIS and Keck/NIRC2 observations. In: Icarus. 238, 2014, S. 137–155, doi:10.1016/j.icarus.2014.05.016.
- J. H. Waite: Cassini Ion and Neutral Mass Spectrometer: Enceladus Plume Composition and Structure. In: Science. 311, 2006, S. 1419–1422, doi:10.1126/science.1121290.
- Jonathan I. Lunine: The Atmospheres of Uranus and Neptune. In: Annual Review of Astronomy and Astrophysics. 31, 1993, S. 217–263, doi:10.1146/annurev.aa.31.090193.001245.
- Astronomers Detect First Organic Molecule on an Exoplanet. auf: jpl.nasa.gov (englisch, 19. März 2008), abgerufen am 20. März 2008.
- S. K. Leggett u. a.: The missing link: Early methane (“T”) dwarfs in the Sloan Digital Sky Survey. In: The Astrophysical Journal Letters, 536.1, 2000, S. L35–L38.
- M. J. Mumma, G. L. Villanueva, R. E. Novak, T. Hewagama, B. P. Bonev, M. A. DiSanti, A. M. Mandell, M. D. Smith: Strong Release of Methane on Mars in Northern Summer 2003. In: Science. 323, 2009, S. 1041–1045, doi:10.1126/science.1165243.
- Kenneth Chang: NASA Rover on Mars Detects Puff of Gas That Hints at Possibility of Life, In: The New York Times, 22. Juni 2019, ISSN 0362-4331
- R. Wordsworth u. a.: Transient reducing greenhouse warming on early Mars. In: Geophysical Research Letters. 44, 2017, S. 665–671, doi:10.1002/2016GL071766.
- NASA's Cassini Spacecraft Reveals Clues About Saturn Moon. Auf: jpl.nasa.gov, 12. Dezember 2013, abgerufen am 27. Dezember 2013.
- Ralph-Mirko Richter: Eisschollen auf der Oberfläche der Titan-Seen? In: Raumfahrer.net. 13. Januar 2013, abgerufen am 11. Juni 2013
- Cassini Suggests Icing on a Lake. Auf: jpl.nasa.gov, 8. Januar 2013, abgerufen am 11. Juni 2013.
- Antonin Affholder u. a.: Bayesian analysis of Enceladus’s plume data to assess methanogenesis. In: Nature Astronomy, 6.2021, S. 2397, doi:10.1038/s41550-021-01372-6.
- J. Hunter Waite u. a.: Cassini finds molecular hydrogen in the Enceladus plume: Evidence for hydrothermal processes. In: Science. 356, 2017, S. 155–159, doi:10.1126/science.aai8703.
- Jinrui Zhang, Hans Meerman, René Benders, André Faaij: Comprehensive review of current natural gas liquefaction processes on technical and economic performance. In: Applied Thermal Engineering. 166, 2020, S. 114736, doi:10.1016/j.applthermaleng.2019.114736.
- H. Märkl, H. Friedmann: Biogasproduktion. In: Garabed Antranikian: Angewandte Mikrobiologie. Springer, Berlin, Heidelberg, 2006, ISBN 978-3-540-24083-9, S. 459–487.
- Anelli Petersson, Arthur Wellinger: Biogas upgrading technologies–developments and innovations. In: IEA bioenergy. 20, 2009, S. 1–19.
- Christian Gutt: Brennendes Eis: Methanhydrat—Energiequelle der Zukunft oder Gefahr fürs Klima? In: Physikalische Blätter. 57.9, 2001, S. 49–54.
- Paul Sabatier, Senderens: Compte Rendu Acad. Sci., Band 134, 1902, S. 689.
- Colin Campbell, Albert Parker: CXXXVI.—The preparation and analysis of methane. In: J. Chem. Soc., Trans.. 103, 1913, S. 1292–1297, doi:10.1039/CT9130301292.
- R. Bini, G. Pratesi: High-pressure infrared study of solid methane: Phase diagram up to 30 GPa. In: Physical Review. B, 55 (22), 1997, S. 14800–14809
- Visualisierung der Kristallstruktur von Methan als Feststoff
- J. Huheey, E. Keiter, R. Keiter: Anorganische Chemie: Prinzipien von Struktur und Reaktivität. Walter de Gruyter, Berlin/New York 2003, ISBN 3-11-017903-2, S. 174–179.
- Feng Wang: Molecular orbitals of methane: symmetry or hybridization? In: THEOCHEM, 2004, Band 678, Nr. 1–3, S. 105–111, doi:10.1016/j.theochem.2004.02.042.
- S. A. C. Clark, T. J. Reddish, C. E. Brion, E. R. Davidson, R. F. Frey: The valence orbital momentum distributions and binding energy spectra of methane by electron momentum spectroscopy: Quantitative comparisons using near Hartree-Fock limit and correlated wavefunctions. In: Chemical Physics, 1990, Band 143, Nr. 1, S. 1–10, doi:10.1016/0301-0104(90)85001-D.
- Catherine E. Housecroft, Alan G. Sharpe: Anorganische Chemie. Pearson, München u. a. 2006, ISBN 3-8273-7192-9, S. 125–126.
- E. K. Plyler, E. D. Tidwell, L. R. Blaine: Infrared Absorption Spectrum of Methane From 2470 to 3200 cm. In: Journal of Research of the National Bureau of Standards, Section A: Physics and Chemistry. Band 64A, Nummer 3, 1960 May-Jun, S. 201–212, doi:10.6028/jres.064A.021, PMID 32196187, PMC 5287146 (freier Volltext).
- Johann Weidlein, Ulrich Müller, Kurt Dehnicke: Schwingungsspektroskopie: Eine Einführung. 2., überarb. Auflage. Thieme, Stuttgart 1988, ISBN 3-13-625102-4, S. 134–135.
- C. Roche, J. P Champion: Analysis of dyad – dyad transitions of 12CH4 and 13CH4. In: Canadian Journal of Physics, 1991, Band 69, Nr. 1, S. 40–51, doi:10.1139/p91-007.
- J.-C. Hilico, J. P. Champion, S. Toumi, V. G. Tyuterev, S. A. Tashkun: New Analysis of the Pentad System of Methane and Prediction of the (Pentad-Pentad) Spectrum. In: Journal of Molecular Spectroscopy, 1994, Band 168, Nr. 2, S. 455–476, doi:10.1006/jmsp.1994.1293.
- Hans-Martin Niederer, Sieghard Albert, Sigurd Bauerecker, Vincent Boudon, Jean-Paul Champion, Martin Quack: Global Analysis of the Infrared Spectrum of 13CH4: Lines in the Region 0 to 3200 cm−1. In: Chimia, 2008, Band 62, Nr. 4, S. 273–276, doi:10.2533/chimia.2008.273.
- S. Albert, S. Bauerecker, V. Boudon, L. R. Brown, J.-P. Champion, M. Loëte, A. Nikitin, M. Quack: Global analysis of the high resolution infrared spectrum of methane 12CH4 in the region from 0 to 4800 cm−1. In: Chemical Physics, 2009, Band 356, Nr. 1–3, S. 131–146, doi:10.1016/j.chemphys.2008.10.019.
- Geoffrey A. Ozin, John G. McCaffrey, J. Mark Parnis: Photochemistry of Transition-Metal Atoms: Reactions with Molecular Hydrogen and Methane in Low-Temperature Matrices. In: Angewandte Chemie International Edition in English. 25, 1986, S. 1072–1085, doi:10.1002/anie.198610721.
- Clinton R. King u. a.: Supermetal: SbF5-mediated methane oxidation occurs by C–H activation and isobutane oxidation occurs by hydride transfer. In: Dalton Transactions, 48.45, 2019, S. 17029–17036.
- Ayusman Sen, Mark A. Benvenuto, Minren Lin, Alan C. Hutson, Naomi Basickes: Activation of Methane and Ethane and Their Selective Oxidation to the Alcohols in Protic Media. In: Journal of the American Chemical Society. 116, 1994, S. 998–1003, doi:10.1021/ja00082a022.
- Standardreaktionsenthalpie für die Verbrennung von Methan und diversen Erdölprodukten, vgl. S. 3 ff. in: Herbert Mayr: Vorlesung 9: Erdölverarbeitung. (PDF; 68 kB). LMU München: Physikalisch-organische Chemie, 2006
- Duy Khoe Dinh, Dae Hoon Lee, Young-Hoon Song, Sungkwon Jo, Kwan-Tae Kim, Muzammil Iqbal, Hongjae Kang: Efficient methane-to-acetylene conversion using low-current arcs. In: RSC Advances. 9, 2019, S. 32403–32413, doi:10.1039/c9ra05964d.
- F. Endter: Die technische Synthese von Cyanwasserstoff aus Methan und Ammoniak ohne Zusatz von Sauerstoff, Chemieingenieurtechnik, Nr. 30, 1958, S. 305–310, doi:10.1002/cite.330300506.
- Natural Gas Consumption, bei U.S. Energy Information Administration, abgerufen am 12. Juli 2021.
- Rudolph Hopp: Grundlagen der Chemischen Technologie: für Praxis und Berufsbildung. Wiley-VCH, Weinheim, 2001, ISBN 3-527-29998-X, S. 452.
- Selma K. Bengtsson, Erik Fridell, Karin E. Andersson: Fuels for short sea shipping: A comparative assessment with focus on environmental impact. In: Proceedings of the Institution of Mechanical Engineers, Part M: Journal of Engineering for the Maritime Environment. 228, 2013, S. 44–55, doi:10.1177/1475090213480349.
- L.S. Neiva: A Study on the Characteristics of the Reforming of Methane: A review. In: Brazilian Journal of Petroleum and Gas. 2010, S. 119–127, doi:10.5419/bjpg2010-0013.
- Trevor L. LeValley, Anthony R. Richard, Maohong Fan: The progress in water gas shift and steam reforming hydrogen production technologies – A review. In: International Journal of Hydrogen Energy. 39, 2014, S. 16983–17000, doi:10.1016/j.ijhydene.2014.08.041.
- Hazzim F. Abbas, W.M.A. Wan Daud: Hydrogen production by methane decomposition: A review. In: International Journal of Hydrogen Energy. 35, 2010, S. 1160–1190, doi:10.1016/j.ijhydene.2009.11.036.
- Martin Bertau, Heribert Offermanns, Ludolf Plass, Friedrich Schmidt, Hans-Jürgen Wernicke: Methanol: The Basic Chemical and Energy Feedstock of the Future: Asinger’s Vision Today, 750 Seiten, Verlag Springer; 2014, ISBN 978-3-642-39709-7, S. 52.
- Boy Cornils: Hydroformylierung (Oxo-Synthese). In: J. Falbe, U. Hasserodt: Katalysatoren, Tenside und Mineralöladditive, Georg Thieme Verlag, 1978, ISBN 3-13-552601-1, S. 108–111.
- Ernst Bartholomé: Probleme großtechnischer Anlagen zur Erzeugung von Acetylen nach dem Sauerstoff-Verfahren. In: Chemie Ingenieur Technik - CIT. 26, 1954, S. 253–258, doi:10.1002/cite.330260503.
- Manchiu D. S. Lay, Mitchell Sauerhoff, Donald R. Saunders: "Carbon Disulfide". In: Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2000, doi: 10.1002/14356007.a05_185.
- Dirk Steinborn: Grundlagen der metallorganischen Komplexkatalyse. Teubner, Wiesbaden 2007, ISBN 978-3-8351-0088-6, S. 261–263.
- Ivan Ernest: Bindung, Struktur und Reaktionsmechanismen in der organischen Chemie. Springer-Verlag, 1972, ISBN 3-211-81060-9, S. 297–306
- R. Conrad: Contribution of hydrogen to methane production and control of hydrogen concentrations in methanogenic soils and sediments. In: FEMS Microbiology Ecology. 28, 1999, S. 193–202, doi:10.1111/j.1574-6941.1999.tb00575.x.
- R. Hedderich, W. B. Whitman: Biogeochemistry of Methanogenesis. In: Salvator Eduardo Acevedo Monroy: The Prokaryotes. Volume 2: Ecophysiology and Biochemisty. Springer, New York, 2006, ISBN 978-0387-25492-0, S. 1052–1079.
- R. S. Hanson, T. E. Hanson: Methanotrophic bacteria. In: Microbiological Reviews. 60, 1996, S. 439–471, doi:10.1128/mr.60.2.439-471.1996.
- D. Brankovits u. a.: Methane- and dissolved organic carbon-fueled microbial loop supports a tropical subterranean estuary ecosystem. In: Nature Communications. 8, 2017, S. 1–12, doi:10.1038/s41467-017-01776-x.
- Matthew O. Ross, Amy C. Rosenzweig: A tale of two methane monooxygenases. In: JBIC Journal of Biological Inorganic Chemistry. 22, 2017, S. 307–319, doi:10.1007/s00775-016-1419-y.
- T. Klintzsch, G. Langer, G. Nehrke, A. Wieland, K. Lenhart, F. Keppler: Methane production by three widespread marine phytoplankton species: release rates, precursor compounds, and potential relevance for the environment. In: Biogeosciences, 16, 2019, S. 4129–4144, doi:10.5194/bg-16-4129-2019.
- Marie A. de Angelis, Cindy Lee: Methane production during zooplankton grazing on marine phytoplankton. In: Limnology and Oceanography. 39, 1994, S. 1298–1308, doi:10.4319/lo.1994.39.6.1298.
- R. B. Jackson, M. Saunois, P. Bousquet, J. G. Canadell, B. Poulter, A. R. Stavert, P. Bergamaschi, Y. Niwa, A. Segers, A. Tsuruta: Increasing anthropogenic methane emissions arise equally from agricultural and fossil fuel sources. In: Environmental Research Letters, 2020, Band 15, S. 071002, doi:10.1088/1748-9326/ab9ed2.
- Marielle Saunois u. a.: The Global Methane Budget 2000–2017. In: Earth System Science Data, 2020, Band 12, S. 1561–1623, doi:10.5194/essd-12-1561-2020
- Treibhausgase. Umweltbundesamt, 6. Juni 2019, abgerufen am 29. Februar 2020.
- A. V. Dzyuba, A. V. Eliseev, I. I. Mokhov: Estimates of changes in the rate of methane sink from the atmosphere under climate warming. In: Izvestiya, Atmospheric and Oceanic Physics. 48, 2012, S. 332–342, doi:10.1134/S0001433812020041.
- D. T. Shindell, G. Faluvegi, D. M. Koch, G. A. Schmidt, N. Unger, S. E. Bauer: Improved attribution of climate forcing to emissions. In: Science. 326, Nr. 5953, 2009, S. 716–718
- Joachim Wille: Der "mächtige Hebel" beim Klimaschutz. In: Klimareporter.de, 11. Mai 2021.
- Intergovernmental Panel on Climate Change: Technical Summary of the Working Group I Report, 2001, S. 38.
- Joachim Wille: Methan endlich im Fokus. In: Klimareporter. 31. Oktober 2021, abgerufen am 31. Oktober 2021 (deutsch).
- Klimakonferenz: Dutzende Staaten wollen Methan reduzieren. In: tagesschau.de. 2. November 2021, abgerufen am 3. November 2021.
- Environmental Research Letters, doi:10.1088/1748-9326/11/12/120207. Nach: deutschlandfunk.de, Forschung aktuell, Meldungen, 12. Dezember 2016: Klimawandel: Die Methankonzentrationen in der Atmosphäre steigen derzeit ungewöhnlich schnell (20. Juni 2017)
- S. Solomon, D. Qin, M. Manning, Z. Chen, M. Marquis, K. B. Averyt, M.Tignor and H. L. Miller (eds.): ipcc.ch: The Physical Science Basis. Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change (PDF; 3,7 MB). In: IPCC, 2007: Summary for Policymakers. In: Climate Change 2007, Cambridge University Press, Cambridge, United Kingdom and New York, NY, USA.
- Benjamin Hmiel u. a.: Preindustrial 14CH4 indicates greater anthropogenic fossil CH4 emissions. In: Nature. 578, 2020, S. 409–412, doi:10.1038/s41586-020-1991-8.
- Treibhausgas-Emissionen in Deutschland. Umweltbundesamt, 25. April 2019, abgerufen am 29. Februar 2020.
- Yuzhong Zhang u. a.: Quantifying methane emissions from the largest oil-producing basin in the United States from space. In: Science Advances. 6, 2020, S. eaaz5120, doi:10.1126/sciadv.aaz5120.
- Silke Hasselmann: USA haben den Ausstoß des Klimagases Methan zu niedrig angegeben. (Memento vom 27. Februar 2014 im Internet Archive) auf: Deutschlandfunk. 14. Februar 2014, (20. Februar 2014)
- Robert W. Howarth: Ideas and perspectives: is shale gas a major driver of recent increase in global atmospheric methane?. In: Biogeosciences. 16, 2019, S. 3033, doi:10.5194/bg-16-3033-2019.
- Stephen Leahy: Fracking boom tied to methane spike in Earth’s atmosphere. In: National Geographic. 15. August 2019, abgerufen am 20. August 2019.
- Xinrong Ren u. a.: Methane Emissions from the Marcellus Shale in Southwestern Pennsylvania and Northern West Virginia Based on Airborne Measurements. In: Journal of Geophysical Research: Atmospheres. 124, 2019, S. 1862–1878, doi:10.1029/2018JD029690.
- Scientists shocked by Arctic permafrost thawing 70 years sooner than predicted. In: The Guardian, ISSN 0261-3077, Abruf 18. Juni 2019
- Katrin Kohnert, Andrei Serafimovich, Stefan Metzger, Jörg Hartmann, Torsten Sachs: Strong geologic methane emissions from discontinuous terrestrial permafrost in the Mackenzie Delta, Canada. In: Scientific Reports. 7, 2017, S. 5828, doi:10.1038/s41598-017-05783-2.
- Volker Mrasek: Methanverluste – Lecks in der Öl- und Gasindustrie. In: Deutschlandfunk. Deutschlandradio, 6. Dezember 2017, abgerufen am 8. Dezember 2017.
- Josh Gabbatiss: Coal mines emit more methane than oil-and-gas sector, study finds. Carbon Brief, 24. März 2020, abgerufen am 29. März 2020 (englisch).
- Jillian Ambrose: Methane emissions from coalmines could stoke climate crisis – study. In: The Guardian. 15. November 2015, ISSN=0261-3077
- mbe: Satellitenbild der Woche: Riesiges Methanleck in den USA entdeckt. In: spiegel.de. 11. Oktober 2014, abgerufen am 11. Oktober 2014.
- S. Conley, G. Franco, I. Faloona, D. R. Blake, J. Peischl, T. B. Ryerson: Methane emissions from the 2015 Aliso Canyon blowout in Los Angeles, CA. In: Science. 351, 2016, S. 1317–1320, doi:10.1126/science.aaf2348.
- Sudhanshu Pandey u. a.: Satellite observations reveal extreme methane leakage from a natural gas well blowout. In: Proceedings of the National Academy of Sciences. 116, 2019, S. 26376, doi:10.1073/pnas.1908712116.
- Livestock's Long Shadow – Environmental Issues and Options (en), FAO 2006, Rom, (Kurzfassung, en)
- Pflanzen mit schlechtem Atem. Auf: wissenschaft.de vom 12. Januar 2006.
- D.N. Kamra, N. Agarwal, P.C. Sakthivel, L.C. Chaudhary: Garlic as a rumen modifier for eco-friendly and economic livestock production. In: Journal of Applied Animal Research. 40, 2012, S. 90–96, doi:10.1080/09712119.2011.607764.
- Margarida R. G. Maia, António J. M. Fonseca, Hugo M. Oliveira, Carla Mendonça, Ana R. J. Cabrita: The Potential Role of Seaweeds in the Natural Manipulation of Rumen Fermentation and Methane Production. In: Scientific Reports. 6:32321, 2016, doi:10.1038/srep32321.
- Robert D. Kinley, Rocky de Nys, Matthew J. Vucko, Lorenna Machado, Nigel W. Tomkins: The red macroalgae Asparagopsis taxiformis is a potent natural antimethanogenic that reduces methane production during in vitro fermentation with rumen fluid. In: Animal Production Science. 56, 2016, S. 282–289, doi:10.1071/AN15576.
- Breanna M. Roque, Joan K. Salwen, Rob Kinley, Ermias Kebreab: Inclusion of Asparagopsis armata in lactating dairy cows’ diet reduces enteric methane emission by over 50 percent. In: Journal of Cleaner Production. 234, 2019, S. 132, doi:10.1016/j.jclepro.2019.06.193.
- Breanna M. Roque, Marielena Venegas, Robert D. Kinley, Rocky de Nys, Toni L. Duarte, Xiang Yang, Ermias Kebreab, James E. Wells: Red seaweed (Asparagopsis taxiformis) supplementation reduces enteric methane by over 80 percent in beef steers. In: PLOS ONE. 16, 2021, S. e0247820, doi:10.1371/journal.pone.0247820.
- Victoria Baca-González, Patricia Asensio-Calavia, Sergio González-Acosta, Jose Manuel Pérez de la Lastra, Antonio Morales de la Nuez: Are Vaccines the Solution for Methane Emissions from Ruminants? A Systematic Review. In: Vaccines. 8, 2020, S. 460, doi:10.3390/vaccines8030460.
- Livestock methane and nitrogen emissions., bei Agriculture.viv.gov.au; abgerufen am 11. Juli 2021.
- Julien Mouli-Castillo, Georgina Orr, James Thomas, Nikhil Hardy, Mark Crowther, R. Stuart Haszeldine, Mark Wheeldon, Angus McIntosh: A comparative study of odorants for gas escape detection of natural gas and hydrogen. In: International Journal of Hydrogen Energy. 46, 2021, S. 14881–14893, doi:10.1016/j.ijhydene.2021.01.211.
- Michael J. Economides, Kai Sun, Gloria Subero: Compressed Natural Gas (CNG): An Alternative to Liquefied Natural Gas (LNG). In: SPE Production & Operations. 21, 2006, S. 318–324, doi:10.2118/92047-PA.
- A. Rojey, C. Jaffret u. a.: Natural Gas. Production Processing Transport. Institut Français du Pétrole Publications, Èditions Technip, Paris, 1997, ISBN 978-2-7108-0693-6, S. 319.
- Rodolfo Taccani, Gabriele Maggiore, Diego Micheli: Development of a Process Simulation Model for the Analysis of the Loading and Unloading System of a CNG Carrier Equipped with Novel Lightweight Pressure Cylinders. In: Applied Sciences. 10, 2020, S. 7555, doi:10.3390/app10217555.
- Dietrich Henschler: Toxikologie chlororganischer Verbindungen der Einfluss von Chlorsubstituenten auf die Toxizität organischer Moleküle. Verlag Chemie, Weinheim, New York, Basel, Cambridge, Tokio, 1994, ISBN 3-527-29262-4, S. 11.
- K. Kawara, B. Gregory, T. Yamamoto, H. Shibai: Infrared spectroscopic observation of methane in Comet P/Halley. In: Astronomy and Astrophysics. 207, 1, 1988, S. 174–181, bibcode:1988A&A...207..174K
- Lee Marotta, Denis Yates: Methane, Ethylene, and Ethane in Water by Headspace-Gas Chromatography (HS-GC) with Flame Ionization Detection (FID). Abgerufen am 26. Oktober 2014.


