Antoine Laurent de Lavoisier
Antoine Laurent de Lavoisier [lavwaˈzje] (* 26. August 1743 in Paris; † 8. Mai 1794 ebenda) war ein französischer Chemiker und Naturwissenschaftler, Rechtsanwalt, Hauptzollpächter, Ökonom und Leiter der französischen Pulververwaltung. Er führte quantitative Messmethoden in die Chemie ein, erkannte die Rolle des Sauerstoffs bei der Verbrennung und widerlegte damit die damals vorherrschende Phlogistontheorie. Lavoisier schuf viele Grundlagen der modernen Chemie. Er gilt als deren Begründer[1] und als Vater der ersten chemischen Revolution.[2] Trotz seines hohen wissenschaftlichen Ansehens und seines Engagements für Reformen wurde er wegen seiner Rolle im Ancien Régime ein Opfer der Terrorherrschaft während der Französischen Revolution.
.jpg.webp)

Leben und Wirken

Herkunft
Seine Vorfahren stammten aus Villers-Cotterêts, einer kleinen Stadt in einem großen Waldgebiet nördlich von Paris; sie stiegen aus dem Bauernstand auf (einer seiner Vorfahren war in der Stadt im 17. Jahrhundert Postmeister). Antoine Laurent de Lavoisier war der älteste Sohn des Arztes und Rechtsanwalts Jean Antoine Lavoisier (1715–1775) und von dessen Frau Émilie Punctis (ca. 1729 bis 1748), die die Tochter eines Advokaten war. Sein Vater erbte noch als Jurastudent in Paris 1741 von seinem Onkel Waroquier den Posten eines Anwalts am Parlement, dem obersten Gericht in Paris. Seine Eltern heirateten am 28. Mai 1742[3] und wohnten in Paris in der Straße Cul-de-sac Pecquet (quartier des Blancs-Manteaux) im alten Haus des Onkels. Seine zwei Jahre jüngere Schwester war Marie Marguerite Émilie Lavoisier (1745–1760). Nach dem frühen Tod der Mutter zog die Familie mit den Halbwaisen in das Haus der Großmutter mütterlicherseits, Madame Punctis, in der Rue de Four St. Eustache. Dort lebte Lavoisier bis zu seiner Heirat im Jahre 1771. Den Platz seiner Mutter in der Erziehung nahm seine Tante Constance Punctis ein. Der Vater von Lavoisier kaufte 1775 einen Posten, der ihm einen erblichen Adelstitel verschaffte und den Lavoisier bei seinem Tod erbte.
Studium, Geologie und erste Experimente
Bereits in jungen Jahren interessierte sich Lavoisier für die Naturwissenschaften. Er besuchte ab 1754 als Tagesschüler das Collège Mazarin (Collège des Quatre Nations), wo er neben einer gründlichen klassischen Ausbildung (er gewann Preise für griechische und lateinische Übersetzungen) auch die beste damals in Paris mögliche Ausbildung in Naturwissenschaften und Mathematik genoss. Er hörte Vorlesungen des Chemikers Guillaume-François Rouelle (1703–1770), des Experimentalphysikers Jean-Antoine Nollet (1700–1770), des Mathematikers Nicolas Louis de Lacaille (1713–1762) und des Botanikers Bernard de Jussieu (1699–1777), wobei ihn insbesondere Lacaille in den Naturwissenschaften unterrichtete und förderte. Statt des Bakkalaureat-Abschlusses begann er 1761 auf Wunsch seines Vaters mit dem Jurastudium. 1764 promovierte er zum Doktor der Rechte und wurde in die Pariser Anwaltsliste immatrikuliert.
Sein besonderes Interesse galt damals der Meteorologie (auf diesem Gebiet stellte er auch später immer wieder Beobachtungen an), Geologie, Mineralogie, und Chemie. Ein Freund der Familie, Jean-Étienne Guettard (1715–1786), regte ihn früh zur Beschäftigung mit Geologie und Mineralogie an, und da dazu auch Kenntnisse der Chemie nötig waren, auch mit dieser Wissenschaft. So hörte er weitere Vorlesungen am Jardin du roi bei Guillaume-François Rouelle und besuchte dessen Laborkurse in dessen Apotheke.[4] Er legte eine Gesteins- und Mineraliensammlung an und erforschte 1763 die Umgebung seines Heimatorts mit Guettard. Dieser plante eine geologische Kartierung Frankreichs, die ihm 1766 genehmigt wurde, und nahm in Vorbereitung dazu Lavoisier auf seine Erkundungsreisen in Nordfrankreich und die Normandie mit.
Lavoisier richtete sich ein kleines Forschungslabor ein und begann mit ersten Experimenten. Im Alter von 22 Jahren veröffentlichte er seine erste Arbeit, eine Abhandlung über den Gips, Analyse du gypse (1765) als erste einer geplanten Reihe von Untersuchungen über Mineralanalysen. Im Gegensatz zu seinen Vorgängern untersuchte er diese mit nassen chemischen Methoden (wie in der Natur durch die Wirkung des Wassers beobachtet). Gips, wie man ihn im Pflaster von Paris fand, war nach ihm ein neutrales Salz auf Basis einer schwefelhaltigen Säure und Kalk, das bei Erhitzen Wasser freigab (Kristallwasser nach Rouelle). Zu diesen Erkenntnissen war allerdings schon Marggraf gekommen, und Étienne Mignot de Montigny, der die Arbeit für die Akademie prüfte, hatte dies auch schon veröffentlicht, auch wenn er dies nicht so gründlich behandelte wie Lavoisier. Er hielt darüber einen Vortrag vor der Akademie (1765), die ihn 1768 in ihrer Mémoir-Reihe veröffentlichte, in der vor allem Nichtmitglieder veröffentlichten. Schon damals bemühte er sich um die Aufnahme in die Académie des sciences zunächst als adjoint als damals jüngster Kandidat. Zunächst zog man allerdings in der Sektion Chemie den älteren Cadet de Gassicourt vor. Lavoisier verstand sich damals und auch später in erster Linie als Experimentalphysiker, für die damals noch keine Sektion existierte (sie wurde erst 1785 auf Initiative von Lavoisier eingerichtet) und nur in analytischen Arbeiten wie der über Gips als Chemiker.[5]
1764 beteiligte er sich mit einer gründlichen, das Thema erschöpfenden Preisschrift an dem Wettbewerb, die der Generalleutnant der Pariser Polizei für eine Arbeit über die beste Straßenbeleuchtung ausgelobt hatte. Zwar gewann keiner den Preis, er erhielt aber 1766 von der Akademie im Namen des Königs eine Goldmedaille. Mit Guettard machte er im Jahr 1767 eine Studienreise in die Vogesen, Elsaß und Lothringen, als Teil der Arbeiten zu einem mineralogisch-geologischen Atlas von Frankreich. Bis 1770 arbeitete er mit Guettard zusammen an insgesamt 16 regionalen geologisch-mineralogischen Karten (mit Symbolen für Gesteins- und Mineralvorkommen) und war mit dem Projekt bis 1777 verbunden, als es Antoine Monnet übernahm. Lavoisier war dabei für barometrische Höhenmessungen, Neigungsmessungen, Wasser- und Mineralanalysen zuständig. Lavoisier begann aber auch ein Forschungsprogramm für eine Theorie der Geologie, wobei er von Rouelle, Guettard und Buffon (Théorie de la terre 1749) ausging. Guettard ging von zwei Formationen aus, einem kristallinen Grundgebirge (terre ancienne) und der Sedimentablagerung aus einer Meeresüberflutung (terre nouvelle). Lavoisier erkannte in der Terre nouvelle bald eine Abfolge mehrerer Meeresvorstöße mit wechselnder Ablagerung von feinem und grobem Material. Auch die Terre ancienne bestand nicht aus einer Schicht, sondern nach Lavoisier wahrscheinlich aus einer Abfolge älterer Küstenablagerungen. Sein Interesse an Geologie schwand auch später nicht, seine Überlegungen dazu veröffentlichte er aber erst 1788.
Er gab seine Pläne für die Aufnahme in die Akademie, dank Unterstützung durch seine Familie, nicht auf. 1768 veröffentlichte er eine Arbeit über Analyse von Wasserproben, die er auf seinen Reisen mit Guettard getätigt hatte. Außer Mineralwasser untersuchte er auch Trinkwasserproben, was er für gesellschaftlich viel bedeutender hielt. Neben der Bestimmung von Salzen nach dem Verdampfen benutzte er auch ein von ihm neu entwickeltes Hydrometer zur Bestimmung des spezifischen Gewichts der Proben. Im Jahre 1768 wurde er dann in der Académie des sciences als Assistent der Chemie (chimiste-adjoint) gewählt. Die direkte Wahl fiel zwar auf den älteren Metallurgen und Bergbauingenieur Gabriel Jars, er wurde aber mit Sondergenehmigung adjoint chimiste surnuméraire und als Jars 1769 starb rückte er auf dessen Posten.

Lavoisier und die Ferme générale
1768 trat Lavoisier der Ferme générale bei, der Organisation der Hauptzollpächter.[6] Die Zahl dieser Hauptzollpächter (fermiers) war anfangs auf 40, ab 1775 dann auf 60 Personen begrenzt. Der Auftragnehmer, also der fermier, verpflichtet sich zur Zahlung einer Pacht an die Staatskasse und erhielt im Gegenzug einen Überschuss aus den Zolleinnahmen, so beispielsweise für den Handel mit Salz und Tabak und die Einfuhr von Waren nach Paris. Zölle wurden nicht nur an den Außengrenzen, sondern auch zwischen den Provinzen im Land erhoben, wo erhebliche Preisunterschiede zum Beispiel für Salz bestanden. Der Schmuggel blühte und die Zolleinnehmer hatten eigene bewaffnete Beamte, die diesen bekämpften und das Recht hatten, Grund und Haus jeder Person zu durchsuchen. Die Strafen auf Salzschmuggel waren drakonisch (Galeere) und die Steuerpächter waren beim einfachen Volk verhasst. Für die Pacht etwa von 1768 bis 1774 hatte die Ferme 90 Millionen Livres per annum zu zahlen. Somit musste ein Pächter 2,25 Millionen Livres vorstrecken. Um solch hohe Summen vorlegen zu können, verbargen sich hinter einem Ferme häufig gleich mehrere Personen, die man als Gehilfen bezeichnete. Lavoisier war zunächst Gehilfe des Fermiers François Baudon (* 1686).[7]
Die ersten Tätigkeiten Lavoisiers in der Ferme générale bestanden in Inspektionsreisen; so hielt er sich etwa einige Monate im Jahr 1768 in der Picardie auf. Im nächsten Jahr war er mit der Kontrolle der Tabakfabriken und Zollstellen im Norden Frankreichs beschäftigt. Sein Vorgesetzter war sein späterer Schwiegervater, an ihn wurden die Berichte adressiert. 1779 wurde er vollwertiges Mitglied der Ferme. Deren Gewinne wurden ab 1780 durch Finanzminister Jacques Necker zur Hälfte dem Staat übertragen und die Zinsforderungen der Ferme für ihr vorgestrecktes Kapital beschränkt.
Lavoisier war nachdem er 1782 Leiter der Pariser Zölle geworden war Initiator des 1785 begonnenen Baus der Mauer der Generalpächter (Mur des Fermiers généraux), deren Zweck es war, den Schmuggel bei der Erhebung der Einfuhrsteuer auf Waren nach Paris zu unterbinden. Paris hatte seit dem 16. Jahrhundert keine Mauer mehr gehabt und der Bau, für den Grundstücke enteignet wurden, erzeugte viel Unwillen. Ein Pamphlet griff 1787 Lavoisiers Arbeiten über Atmung auf und sprach davon, sie würde die Stadt in ihrer eigenen schlechten Luft ersticken lassen.[8] Im Laufe der Jahre in seiner Tätigkeit als Mitglied der Korporation der Steuerpächter Ferme générale konnte Lavoisier ein großes Vermögen erwerben, aus dem er beträchtliche Summen für die Finanzierung seiner Forschungen einsetzte. Er setzte auch einige Reformen durch, wie die Abschaffung der antisemitischen Hufsteuer (Droit de pied fourchu) von 30 Silberstücken für Juden, die durch Clermontoise reisten (dieselbe Steuer wurde auf Schweine erhoben). Juden mieden deshalb den Bezirk und die Wirtschaft litt.[9]
Die Fermiers hatten auch das Tabakmonopol (Import, Produktion, Verkauf an Händler) mit bedeutenden Steuereinnahmen (30 Millionen Livres pro Jahr) und Lavoisiers Tätigkeit in der Verbesserung des Tabaks spielte später bei seinem Prozess eine Rolle, da man ihnen Verfälschung des Tabaks vorwarf. Es waren aber vor allem die Schmuggler, die den Tabak zum Beispiel mit Asche streckten. Lavoisier fand eine einfache Methode, dieses durch Zugabe von Säure festzustellen. Dabei beobachtete Lavoisier, dass kleine Mengen Asche den Geschmack verbesserten und er fand auch, dass die Produktqualität durch kleine Wassermengen verbessert wurde, sodass systematisch 6,3 Prozent Volumenanteil Wasser hinzugefügt wurden. Das berücksichtigte er aber beim Preis im Weiterverkauf. Sein dichtes System von Kontrollen machte ihn aber nicht nur bei den Schmugglern, sondern auch bei den Tabakverkäufern unpopulär.[10]

Hochzeit und Laboratorium in der Rue Neuve des Bons Enfants
Lavoisier, damals 28 Jahre alt, heiratete am 16. Dezember 1771[11] die erst 13-jährige Marie Anne Pierette Paulze, spätere Marie Lavoisier (1758–1836). Sie war die Tochter von Jacques Paulze (1723–1794)[12] und Claudine Catherine Thoynet de Rozières. Als Generalsteuereinnehmer (Hauptzollpächter) im Agrarbereich fungierte Jacques Paulze als Vorgesetzter Lavoisiers in der Ferme générale und war einer von deren einflussreichsten Mitgliedern. Außerdem war er Direktor der Französischen Ostindienkompanie Directeur de la Compagnie des Indes und sein Schwager war der Finanzminister Joseph Marie Terray.
Das junge Ehepaar bezog ein Haus in der Rue Neuve des Bons Enfants (heute Rue Radziwill),[13] das von einem Garten umgeben war. Dieses Haus war ein Hochzeitsgeschenk von Lavoisiers Vater, der sich auf ein Gut in der Nähe von Paris, in Le Bourget, zurückzog. Dort, in der Rue Neuve des Bons Enfants, und ab 1776 in ihrer Wohnung im Arsenal war es den beiden nun möglich, ein großes Laboratorium einzurichten, in dem seine Frau, die nach Anleitung durch Lavoisier ebenfalls gerne experimentierte, unter anderem das Laborbuch führte (in der Regel war sie bei den Experimenten anwesend). Sie übersetzte auch wissenschaftliche Werke aus dem Englischen (die Sprachkenntnisse von Lavoisier waren begrenzt) und war eine gute Zeichnerin (Schülerin von David) und steuerte Illustrationen zum Beispiel für Lavoisiers Hauptwerk Traité de la chimie bei. Eines von Lavoisiers größten Verdiensten war es, bei seinen Experimenten alles genau zu notieren, zu messen und zu wiegen. Er ließ Apparate und Instrumente konstruieren, mit denen vor allem Gase genauer als bisher gemessen und gewogen werden konnten. Später war er in der Lage, größere Gasmassen zu speichern und Gase bis auf eine Genauigkeit von 50 Milligramm zu wiegen.[14] Wertvoll für spätere Naturwissenschaftler war auch die methodische Dreiteilung der Darstellung von chemischen Versuchen, die sich bis heute erhalten hat. Er gliederte die Versuchsbeschreibungen in:
- Experiment (préparation de l’expérience, heute: Versuchsbeschreibung, Materialien und Methoden)
- Ergebnis (effet, heute: Versuchsergebnis, Ergebnisse)
- Betrachtungen (réflexions, heute: Schlussfolgerungen, Diskussion).[15]
Lavoisier unterhielt einen ausgedehnten Briefwechsel mit Wissenschaftlern in ganz Europa und hatte eine große Bibliothek mit den wichtigsten wissenschaftlichen Zeitschriften. Er teilte seine Zeit streng ein und bemühte sich, neben seinen sonstigen Verpflichtungen, bis zu sechs Stunden täglich experimentieren zu können, von 6 bis 9 Uhr morgens und 19 bis 22 Uhr sowie an einem Tag der Woche (Samstag) am ganzen Tag (sein Jour de bonheur, wie seine Frau in ihrer biographischen Notiz schrieb),[16] worauf er sich besonders freute und darauf hinfieberte.[17] Häufig waren Gäste anwesend bei den Experimenten und Lavoisier unterhielt sich dabei mit ihnen über die Versuche. Zu den ausländischen Gästen zählten unter anderem Benjamin Franklin, Arthur Young, Martinus van Marum und James Watt. Er arbeitete auch gern mit anderen Wissenschaftlern zusammen. Insbesondere sein Labor im Arsenal war eines der bestausgestatteten in Europa, in Frankreich war nur das von Guyton de Morveau annähernd vergleichbar.[18]
Das Ehepaar ging gerne in die Oper und hatte eine eigene Loge. Die Ehe war harmonisch und glücklich, sie hatten aber keine Kinder.
Académie des sciences und andere Gesellschaften
Lavoisier war bereits 1768 mit nur 25 Jahren in den erlesenen Kreis der Wissenschaftler der Französischen Akademie, Académie des sciences, aufgenommen worden, als jüngstes ordentliches Mitglied. 1772 wurde er assoziiertes Mitglied und 1778 pensionnaire (der höchste Rang). Er nahm regelmäßig an den zweimal wöchentlich stattfindenden Sitzungen der Akademie teil. Später fanden Sitzungen von verschiedenen Ausschüssen der Akademie häufig unter seinem Vorsitz in seinem Privathaus statt, von Experimenten und Gastmahlen begleitet, für deren guten Ruf seine Ehefrau sorgte. Ein Komitee, in dem Lavoisier Mitglied war, untersuchte den Zustand der Gefängnisse und Hospitäler, ein anderes, in dem auch Benjamin Franklin war, den tierischen Magnetismus von Franz Anton Mesmer.
Im Jahre 1782 wurde er Mitglied der Société royale de médecine, im Jahre 1783 in der Société royale d’agriculture und im Jahre 1785 in dem Comité d’agriculture, wo er auch über seine Landwirtschaftsexperimente vortrug. Ein Ziel seiner Bemühungen war die Verbesserung der Erträge in der für ihre schlechten Böden bekannten Sologne.
Lavoisier wurde als weithin berühmter Wissenschaftler 1784 zum Leiter (Direktor) der Akademie der Wissenschaften Frankreichs berufen. In dieser Funktion hatte er auch Zugang zum König, unter anderem war es seine Aufgabe, die Mitglieder dem König vorzustellen. 1788 wurde er zum Mitglied (Fellow) der Royal Society gewählt.[19]
Inspekteur über die Schießpulverfabriken und Geschäftsmann

Im Jahre 1775 wurden er und drei weitere Personen von Jacques Turgot (1727–1781) zu Inspekteuren über die Schießpulverfabriken ernannt (Comité des Poudres et Salpêtres).[20] Um einheitliche Bedingungen zu schaffen, verfasste er 1777 ein kleines Buch mit Vorschriften über die Pulverherstellung, das in den Revolutionskriegen 1794 in hoher Auflage neu aufgelegt wurde, ohne Lavoisier zu nennen. Die Qualitätssteigerung in der Pulverherstellung durch Lavoisier war ein wichtiger Faktor für die Erfolge der französischen Armeen während der Revolutionskriege. In seiner leitenden Funktion in der staatlichen Pulververwaltung war er in der Lage, die Produktion erheblich zu steigern und erreichte hohe Einsparungen bei den Produktionskosten. In dieser Zeit lernte er auch Eleuthère Irénée du Pont de Nemours (1771–1834) kennen.[21] In der alten, 1822 geschlossenen Pulvermühle in Corbeil-Essonnes arbeitete Du Pont für Lavoisier als Chemikant. Er kam auch mit Benjamin Franklin, damals Pariser Vertreter der aufständischen Amerikaner während des Unabhängigkeitskriegs, in freundschaftlichen Kontakt und stand mit ihm später in Briefkontakt; die Amerikaner bezogen Pulver aus Frankreich. Eleuthère Irénée du Pont baute später in den USA deren Pulverproduktion auf und war der Begründer der US-amerikanischen Chemiedynastie DuPont.
Im Arsenal von Paris, einem ausgedehnten Munitionsdepot und Waffenlager am rechten Seineufer, verfügte Lavoisier ab 1776 über eine Dienstwohnung mit einem gut ausgestatteten Laboratorium im sogenannten Petit Arsenal (Hôtel des Régisseurs) nicht weit von der Bastille.[22] Lavoisier erhielt als einer der Direktoren (Régisseurs) der Régie de Poudre (Pulververwaltung) im Arsenal 2.400 Livres im Jahr und einen kleinen Anteil für jedes Pfund produzierten Pulvers. Sein Vermögen nahm zu und er kaufte 1778 das Gut Fréchines bei Blois, das im Lauf der Zeit auf 200 Hektar anwuchs. Das von seinem Vater 1778 geerbte Gut verpachtete er. Lavoisier begann, sich auch wissenschaftlich mit Landwirtschaft auf seinem Gut zu befassen, versuchte, viele Ideen umzusetzen, doch seine „Experimente“ waren dort weniger erfolgreich und er machte Verluste, da er hartnäckig an ihnen festhielt,[23] auch wenn er insgesamt die Produktion auf seinem Gut steigerte. Als Gutsherr errichtete er eine Schule und nach der schlechten Ernte von 1787 unterstützte er die Bevölkerung in Blois und Romorantin, die die Kornpreise nicht mehr zahlen konnten.[24]
Lavoisier gehörte zur wohlhabendsten Schicht Frankreichs. Nach Claude Viel[25] waren die Chemikalien und Instrumente in seinem Nachlass 3,8 bis 4,3 Millionen Franc von 1993 wert, und allein seine Experimente zur Wassersynthese kosteten ihn (im Geldwert von 1993) 10 Millionen Franc.[26] Das konnte er nicht von seinem Gehalt allein finanzieren, sondern nur durch die Einnahmen als Generalpächter.[27] Als Geschäftsmann war er Anhänger des Freihandels und der Physiokraten, erkannte durchaus die Mängel im System und kritisierte die Ausbeutung der Bauern in Form von Frondiensten, hohen Pachtgebühren und Leibeigenschaft. Bei Gründung des Vorläufers der Nationalbank, der Caisse d’escompte, durch Turgot 1776 wurde er einer der Direktoren und spielte in ihr eine wichtige Rolle.
Französische Revolution, Hinrichtung und Nachwirken
Lavoisier war in der Sitzung 1787/88 Mitglied der Stände-Versammlung in der Provinz Orléans, wo sein Gut lag. In der Versammlung setzte er sich für Reformen ein, sie kam aber zu keinen bedeutenden Beschlüssen. Er kandidierte auch für die Generalstände von 1789 einberufenen Generalstände, wurde aber nur Ersatzabgeordneter.
Am Anfang der Französischen Revolution war er noch in der Leitung der Pulververwaltung und als Bankdirektor unmittelbar Teil der Ereignisse. Er geriet unter Druck, als die revolutionären Massen misstrauisch jede Pulverlieferung aus dem Arsenal verfolgten, und war auch vorübergehend im Juli 1789 verhaftet, bis Lafayette und der mit Lavoisier befreundete Bürgermeister Jean-Sylvain Bailly die Lage klärten. Andere Amtsträger waren zu dieser Zeit vom Mob bei solchen Gelegenheiten an den Laternen erhängt worden. Er meldete sich zur Bürgerwehr und wurde in den Gemeinderat von Paris gewählt, spürte aber auch unmittelbar, wie unpopulär er war (das Bild von David von ihm und seiner Frau musste aus diesem Grund aus einer Kunstausstellung entfernt werden). Die Steuerpächter wurden anfangs noch nicht abgesetzt, da man auf ihre Einnahmen angewiesen war, was diese in Sicherheit wog (keiner von ihnen verließ das Land). Auch Lavoisier sah 1790 in einem Brief an Joseph Black, dass seine Tage in öffentlichen Ämtern gezählt waren, aber noch immer keine unmittelbare Bedrohung, sondern eher Gelegenheit zu mehr Freizeit, was er zu einer Englandreise nutzen wollte. Lavoisier setzte auch seine Forschung zur Atmung fort, wobei er mit Armand-Jean-François Seguin zusammenarbeitete, und bereitete noch größere Veröffentlichungen vor. Er engagierte sich politisch im gemäßigten, aber kurzlebigen Club der Freunde der Verfassung, dem auch der Physiokrat Pierre Samuel du Pont de Nemours sowie Condorcet und Abbé Sieyes angehörten. Im September 1790 wurde er nicht mehr in den Gemeinderat gewählt. Die Akademie litt unter mangelnder Finanzierung, stieß aber 1790 ein Programm zur einheitlichen Einführung von Maßen (metrisches System) und Gewichten an, das 1791 offiziell genehmigt wurde und in deren Kommission Lavoisier als Sekretär und Schatzmeister war und der er bis zu seiner Entlassung mit Laplace und anderen im Dezember 1793 angehörte. Mit Haüy war er dort außerdem für die Bestimmung der Dichte des Wassers zuständig. Im März 1791 wurde den Steuerpächtern der Vertrag gekündigt und deren Aufgabe von der staatlichen Zollverwaltung übernommen, womit ein sich lange hinziehender Abwicklungsprozess begann. Lavoisier bemühte sich vergeblich um die Mitgliedschaft im Zollausschuss. Im Sommer 1791 verlor er auch im Rahmen einer Umstrukturierung seinen Posten als einer der Direktoren der Pulververwaltung. Die Wohnung und das Labor im Arsenal durfte er nach seinem Protest allerdings weiter bewohnen. Im Juni 1791 lieh er Pierre Samuel du Pont de Nemours 70.000 Livres, damit er eine Druckerei kaufte, die nicht nur dessen Zeitschrift, sondern auch Werke der Akademie und damit Lavoisiers eigene chemische Arbeiten drucken sollte. Das wurde bald darauf von seinem Sohn Eleuthère Irénée du Pont übernommen. Im Herbst 1791 wurde er in Zeiten finanzieller Not Schatzmeister der Akademie und unterstützte notleidende Kollegen teilweise aus eigener Tasche. In den Augen der Revolutionäre war die Akademie eine Institution des Königs und des Adels. Im selben Jahr richtete die Nationalversammlung ein Konsultationsbüro für wissenschaftliche und technische Probleme ein, dessen Chemie-Ausschuss Lavoisier angehörte und für die er als erste Aufgabe Material für Papiergeld vorschlug. Er veröffentlichte 1791 einen umfangreichen Bericht über die finanzielle Situation des Staates und eine Studie über die Situation der Landwirtschaft.
Lavoisier war ab 1791 heftigen und unflätigen Angriffen von Seiten des Arztes und revolutionären Publizisten Jean Paul Marat ausgesetzt, den er sich 1780 zum Feind gemacht hatte, als er dessen fehlerhafte Schrift über Verbrennung abkanzelte. 1792 verschärfte sich die Lage in Paris mit dem Beginn des Revolutionskriegs und nach dem Sturm auf die Tuilerien verließ auch Lavoisier seine Wohnung im Arsenal und mietete ein Haus am Boulevard de la Madeleine. Im Herbst hatte er sämtliche Ämter verloren und überlegte eine Apotheke zu eröffnen. Er war aber nach wie vor in Angelegenheiten der Akademie engagiert, die schließlich nach der Machtübernahme der Jakobiner im Sommer 1793 aufgelöst wurde. Als Mitglied des Konsultationsbüros war er an den Vorschlägen zur Reform des öffentlichen Unterrichts beteiligt, einschließlich der Gründung neuer Eliteuniversitäten wie der École Polytechnique, die Ende 1793 umgesetzt wurden. Die Revolutionäre beschlossen auch, sich genauer mit der sich verzögernden Abwicklung der Finanzverwaltung der Fermiers zu beschäftigen und diese zu beschleunigen. In diesem Zusammenhang wurde die Wohnung von Lavoisier durchsucht und versiegelt, was bald darauf teilweise wieder aufgehoben wurde, damit Lavoisier seine Kommissionsarbeit fortsetzen konnte.
Prozess und Hinrichtung

Als Mitglied der verhassten Fermiers généraux wurde er im November 1793 gemeinsam mit 28 Kollegen (ehemaligen Steuerpächtern) inhaftiert, zunächst unter dem Vorwand ihre Abrechnung zu beschleunigen, wozu sie vom Gefängnis in den ehemaligen Palast der Steuerpächter gebracht wurden, wo die Haftbedingungen aber schlechter waren. Ihr Vermögen wurde beschlagnahmt und auch Gut und Haus von Lavoisier erneut versiegelt. Ende Januar legten die Fermiers ihre Schlussabrechnung vor. Gleichzeitig hatte man aber eine Kontrollkommission gebildet, die zu dem Schluss kam, dass die Fermiers den Staat um 130 Millionen Livre betrogen hätten (gerüchteweise waren vorher noch erheblich höhere Summen im Gespräch). Über die Berichte wurde geheim im Finanzausschuss beraten. Besonders ein ehemaliger wegen Unterschlagung verfolgter Angestellter der Steuerverwaltung, Antoine Dupin, tat sich als treibende Kraft in der Verfolgung und Kontrolle der Abrechnung hervor. Am 5. Mai 1794 beschloss der Konvent, den Fall der Steuerpächter dem Revolutionstribunal zu übergeben.[28] Eigentlich war dieses nicht zuständig. Gegen Lavoisier persönlich hatte man inzwischen weitere Anklagepunkte wie Verfälschung des Tabaks (Zugabe von Wasser, was das Gewicht und damit den Preis erhöhte) hinzugenommen und im Prozess kam noch (ohne jeglichen Beweis) Geldzuweisung an Feinde der Republik im Ausland dazu, worauf die Todesstrafe stand. Öffentlicher Ankläger war nicht Antoine Quentin Fouquier-Tinville, sondern Liéndon. Die Anklageschrift erhielten sie erst am Vorabend des Prozesses spät nachts und sie konnten sich am Prozesstag nur je 15 Minuten mit den insgesamt vier Verteidigern beraten. Der öffentliche Prozess war eine Farce und ein Schauprozess, sie wurden einstimmig zum Tode verurteilt und ihr Vermögen wurde eingezogen. Am selben Donnerstag, dem 8. Mai 1794, wurden sie nachmittags auf dem Place de la Révolution (heute Place de la Concorde) mit der Guillotine hingerichtet. Die Guillotine war eine Erfindung von Joseph-Ignace Guillotin, der mit Lavoisier in einer Untersuchungskommission über Mesmerismus zusammengearbeitet hatte.[29] Lavoisier soll aufrecht die Stufen zur Guillotine hochgegangen sein, ohne dass man ihm Angst anmerkte.[30] In einem die Nacht zuvor verfassten Abschiedsbrief an einen Cousin schrieb er: Mein Leben war leidlich lang und glücklich und: Die Ereignisse, in die ich hineingeraten bin, werden mir wahrscheinlich die Unannehmlichkeiten des Alters ersparen. Ich werde gleichmütig sterben. Er war der vierte auf dem Schafott, sein Schwiegervater wurde vor ihm geköpft und insgesamt dauerte die Hinrichtung nur 35 Minuten.[31] Dem fanatischen vorsitzenden Richter des Revolutionstribunals Jean-Baptiste Coffinhal (1762–1794) wird oft der Ausspruch in den Mund gelegt: La république n’a pas besoin de savants et de chimistes, le cours de la justice ne peut être suspendu. („Die Republik braucht weder Wissenschaftler noch Chemiker. Der Lauf der Justiz darf nicht aufgehalten werden.“)[32] Die Geschichte ist aber nach Guerlac apokryph.[33] Der Biograph Grimaux[34] gibt an, dass sich die Quellen in Wortwahl, Umständen und Autor des Zitats widersprechen und keine direkten Zeugenaussagen bekannt sind. Fourcroy legte dem Richter in seiner Trauerrede auf Lavoisier 1795 einen etwas anderen Wortlaut zu: La republique n’avant plus besoin de savants, un seul homme d’esprit suffisait à la tete des affaires (Die Republik braucht keine Wissenschaftler, ein einziger Mann von Geist an der Spitze des Staates reicht). Da der Vorfall auch in dem Artikel über Lavoisier von Georges Cuvier in der Biographie Michaud aufgegriffen wurde, der auf unveröffentlichte biographische Aufzeichnungen von Madame Lavoisier zurückgeht (die im erhaltenen Manuskript aber nur bis 1793 gehen), hielt Grimaux eine derartige Äußerung des Richters dennoch für wahrscheinlich.
Wie die anderen an diesem Tag Guillotinierten liegt Lavoisier in einem Massengrab auf dem Cimetière des Errancis.
Nach der Hinrichtung
Lavoisiers Freund, der italienische Mathematiker und Astronom Joseph-Louis Lagrange (1736–1813) resümierte einen Tag nach der Hinrichtung verbittert:
« Il ne leur a fallu qu’un moment pour faire tomber cette tête, et cent années peut-être ne suffiront pas pour en reproduire une semblable. »
„Sie brauchten nur einen Moment, um diesen Kopf abzuschlagen, aber hundert Jahre genügen vielleicht nicht, einen ähnlichen hervorzubringen.“
Lagrange hatte als Vorsitzender des wissenschaftlichen und technischen Konsultationsbüros noch vorher eine Stellungnahme abgegeben, in der Lavoisier (der dies erbeten hatte) bescheinigt wurde, zu den führenden Wissenschaftlern Europas zu zählen. Jean Noël Hallé überbrachte es am Prozesstag dem Gericht. Auch der Ausschuss für Maße und Gewichte hatte sich vergeblich für ihn eingesetzt (René-Just Haüy und Jean-Charles de Borda, die selbst als Geistlicher bzw. ehemaliger Adliger gefährdet waren) mit dem Argument, Lavoisiers Untersuchungen über Wärmeausdehnung wären für ihre Arbeit unverzichtbar. Von anderen engen Mitarbeitern, die teilweise gut mit den Revolutionären vernetzt waren oder sogar den Jakobinern angehörten (Morveau, Hassenfratz, Gaspard Monge, Fourcroy),[36] wurden dagegen keine öffentlichen Stellungnahmen in der Zeit des Terrors bekannt, was Madame Lavoisier später erzürnte.[37] Fourcroy hatte sich aber anscheinend vor dem Prozess persönlich bei Robespierre für Lavoisier verwendet und war dafür in eine Sitzung des Ausschusses für öffentliche Sicherheit vorgedrungen, was Robespierre aber mit kaltem Schweigen überging, worauf auch kein anderer wagte, das Wort zu ergreifen.[38][39] Claude-Antoine Prieur eilte Fourcroy nach und warnte ihn eindringlich, weitere Vorstöße zu unternehmen, falls er seinen Kopf behalten wolle. Grimaux warf in seiner Lavoisier Biographie Fourcroy dagegen unlautere Motive vor. Nach Grimaux war er ein exzellenter Redner und Populisator, aber ein zweitklassiger Chemiker und als er anlässlich des Siegeszuges der chemischen Nomenklatur, an der er beteiligt war, vom Sieg der französischen Chemiker sprach, wies dies Lavoisier entschieden zurück und reklamierte die Erfolge für sich.[40] Morveau rechtfertigte sich später gegenüber dem Herausgeber der Annalen der Chemie Lorenz von Crell, dass er zu dieser Zeit gar nicht in Paris war, sondern eine aerostatische Maschine im Auftrag des Kriegsministeriums in Meudon testete.[41]
Die Witwe Marie Lavoisier war aufgebracht über die aus ihrer Sicht mangelnde Unterstützung ihres Mannes durch französische Wissenschaftler und andere hochgestellte Personen. Vom Juni bis August 1794 saß sie selbst im Gefängnis. Nach dem Ende der Terrorherrschaft wurde Lavoisier wie die anderen Steuerpächter rehabilitiert und die Witwe Lavoisier, die bei der Kampagne zur Rückerstattung der beschlagnahmten Vermögen der Fermiers eine führende Rolle spielte, bekam das beschlagnahmte Vermögen zurück. Es stellte sich nunmehr heraus, dass die Fermiers dem Staat überhaupt kein Geld schuldeten, sondern im Gegenteil noch Ansprüche hatten. Madame Lavoisier drängte auch 1795 bei der Anklage von Dupin wegen seiner verleumderischen und aktiven Rolle in der Verfolgung der Fermiers auf dessen Verurteilung. Sie hatte vor dem Prozess gegen die Fermiers noch durch persönliche Vorsprache versucht, Dupin dazu zu bewegen, ihren Mann bei der Anklage rauszuhalten, verlor aber dabei die Contenance. Auf einer Gedenkfeier am 2. August 1795 wurde Lavoisier feierlich im 1792 gegründeten Lycée des Arts (im Palais Royal) gewürdigt,[42] das Lavoisier mitgründete und dessen Vertreter den Mut aufgebracht hatten, ihm vor dem Prozess im Gefängnis eine Ehrung zu überreichen. Fourcroy hielt eine der Reden und erinnerte an die Zeit des Terrors, die viele seiner Freunde gelähmt und gehindert habe, sich für ihn einzusetzen. Die Witwe war nicht anwesend. In einer biographischen Notiz über ihren Mann schrieb sie: Il fut persecuté par les hommes qu’il avait le plus servi (Er wurde verfolgt von den Menschen, denen er am meisten gedient hatte).[43]
Lavoisier arbeitete ab 1791 an einem größeren auf fünf oder mehr Bände angelegten Werk, den Mémoires de physique et chimie, mit denen er seinen Plan weiter vorantreiben wollte, die Chemie so exakt wie die Physik zu machen. Der Druck des ersten Bandes hatte 1793 schon begonnen, als er durch die Schließung der Akademie unterbrochen wurde. Insgesamt existierten die ersten beiden Bände (je rund 410 Seiten) und 40 Seiten des vierten Bandes als Manuskripte. Marie Lavoisier ließ sie erst 1805 drucken und dann auch nur privat an ausgesuchte Gelehrte verteilen. Sie liefern wesentlich neue Erkenntnisse über Lavoisiers Forschung in den letzten Jahren auch mit Revisionen bereits veröffentlichter Arbeiten, wurden aber nicht in den Gesammelten Werken, die ab 1862 erschienen, berücksichtigt.[44] Teilweise sind die dort gesammelten Reporte auch von Séguin (der Marie Lavoisier anbot, das Vorwort zu schreiben, was diese ablehnte), Fourcroy und dessen Assistent Louis-Nicolas Vauquelin und Louis Charles Henri Macquart, denn Lavoisier nahm auch Chemiker auf, deren Arbeiten seinem System nahestanden. Er plante auch ein Lehrbuch der Agronomie und eine Überarbeitung seines Traité de Chimie.
Naturwissenschaftliches Wirken

Lavoisier war ein geschickter Experimentator und seine systematische Trennung von Vermutungen und Spekulationen zu einer klar strukturierten gedanklichen Beweisführung gaben der wissenschaftlichen Chemie das nötige Rüstzeug für weitere Fortschritte.
Eine Hauptphase seiner Forschung setzte 1772 ein, dem nach seinem Biographen Guerlac entscheidenden Jahr (Crucial year), in dem er seine gegen die Phlogistontheorie gerichtete Verbrennungstheorie zu entwickeln begann und mit dem von Joseph Priestley entdeckten Sauerstoff der Luft in Verbindung brachte. Er untermauerte das quantitativ mit Wägungen basierend auf dem von ihm erstmals für chemische Reaktionen explizit formulierten und herausgestellten Massenerhaltungssatz, entwickelte eine Theorie der Säuren mit dem Sauerstoff als Basis und klärte die Zusammensetzung von Kohlendioxid (fixe Luft nach Joseph Black) und anderen Luftbestandteilen. Außerdem begann er mit seiner Untersuchung der Atmung, was ihn dann in seiner letzten Schaffensphase besonders beschäftigte. Ein weiterer Höhepunkt war sein Nachweis nach der Entdeckung des Wasserstoffs durch Henry Cavendish, dass Wasser kein Element war, was große Aufmerksamkeit fand und auch seine Vorbereitung eines Generalangriffs auf die Phlogistontheorie abschloss, die ab 1785 erfolgte. Er legte seine Erkenntnisse 1789 in seinem Lehrbuch dar und veröffentlichte 1787 mit Kollegen eine neue, rationale chemische Nomenklatur, die international rasch Verbreitung fand. In der letzten Phase befasste er sich mit der Erforschung von Lebensvorgängen (Atmung, Gärung, Stoffwechsel) und der quantitativen Wärmelehre.
Sein Hauptwerk ist der zweibändige Traité élémentaire de la chimie von 1789, in dem er im ersten Band seine Systematik chemischer Stoffe, Wärmelehre, Analyse der Gase der Luft, Gärung, organische Analyse und Theorie der Säuren behandelt, im zweiten Band chemische Untersuchungsverfahren und Instrumente mit genauen Beschreibungen und Abbildungen.
Frühe Arbeiten
Die Arbeiten zur Mineralogie und zum Gips sowie seine Wasseranalysen wurden schon oben erwähnt.
1770 veröffentlichte er seine Abhandlung über die Natur des Wassers (Mémoire sur al nature de l’Eau et sur lés Expériences par les quelles on a prétendu prouver la possibilité de son changement en terre), die seine analytischen und experimentellen Fähigkeiten demonstrierte. Lavoisier wollte die Behauptung einiger Chemiker widerlegen, dass Wasser in Erde umgewandelt werden könne. Er erhitzte über mehrere Monate mehrfach destilliertes Wasser in einem abgeschlossenen, von Gasen befreitem Gefäß (Pelikan), fand keinerlei Zuwachs an Gewicht und führte die beobachteten Verunreinigungen durch genaues Wiegen auf die Glashülle zurück.

1772 veröffentlichte Lavoisier eine aufsehenerregende Arbeit (Sur la destruction du diamant par le feu) in den Mémoirs der Akademie, in der er mit einem Brennglas einen Diamanten unter einer luftdicht abgeschlossenen Glashaube verbrannte. Es entstand fixe Luft (Kohlendioxid) und Lavoisier konnte nachweisen, dass der Diamant aus reinem Kohlenstoff bestand. Er wiederholte den Versuch mit Variation der Atmosphäre unter der Glashaube, wobei bei fixer Luft und im Vakuum keine Verbrennung stattfand. Die ersten Experimente erfolgten 1771 im Labor von Rouelle, in größerem Maßstab führte er diese mit Pierre Joseph Macquer, Mathurin Brisson und Louis Claude Cadet de Gassicourt durch. Das Experiment bewies, dass chemische Elemente in ganz unterschiedlichen Formen auftreten können (Allotropie).

Das Prinzip der Oxidation, Rolle des Sauerstoffs und Theorie der Säuren
Vorgeschichte und Einflüsse auf Lavoisier
Bei Experimenten zur Verbrennung fand man bei typischen Substanzen wie Holz, Kohle, Papier heraus, dass der Rückstand der Verbrennung leichter war als das Ausgangsprodukt. Man schloss daraus, dass beim Verbrennen eine Substanz aus dem Ursprungsmaterial entweicht. Diese Substanz musste, obgleich unsichtbar, aber ein Gewicht haben. Da dieses Phänomen bei fast jeder Verbrennung zu beobachten war, ging man davon aus, dass es sich um ein und dieselbe Substanz handeln müsse. Georg Ernst Stahl (1659–1734) gab dieser Substanz den Namen Phlogiston. Diese Phlogistontheorie war dann bis weit in das 18. Jahrhundert hinein paradigmatisch. In England führte Robert Boyle (1626–1692) ebenfalls Verbrennungsexperimente durch. Er führte an, dass der Verbrennungsrückstand (Entstehen einer stein- oder salzartigen Substanz, Verkalken) in einigen Experimenten mit Metallen schwerer war als der Ausgangsstoff. Beobachtet wurde das im 17. Jahrhundert auch von Jean Rey, Ole Borch und John Mayow (Tractus de sal-nitro et spiritu nitro-aereo, Oxford 1669), wobei letzterer dafür einen Anteil der Luft verantwortlich machte, den er Salpeterluft nannte und auch für die Atmung und die Bildung von Säuren verantwortlich machte. Boyle führte die Gewichtszunahme auf Feuerteilchen zurück, die sich mit dem Metall vereinigten, und auch die Anhänger der Phlogistontheorie griffen zu diesen oder anderen ad hoc Erklärungen, für sie stellte die Verbrennung von Metallen mit Gewichtszunahme demnach eine Ausnahme gegenüber dem weitaus häufiger beobachteten Fall einer Gewichtsabnahme bei Kohle, Holz, Papier dar.[45] 1772 erschien ein Buch von Guyton de Morveau, das diese Gewichtszunahme auch bei der Verbrennung von anderen Metallen außer Blei und Zinn nachwies.
Den wichtigen Punkt, dass die Gewichtszunahme bei Verbrennung in einem abgeschlossenen Raum von der Luftmenge abhing, erkannte schon 1774 Giambatista Beccaria in Turin (was Lavoisier bekannt war). Beccaria beeinflusste Lavoisier wie auch andere Chemiker in Europa auch mit seinen Experimenten über die Wirkung elektrischer Entladungen auf Metallkalke, was eine Verbindung des Phlogiston mit Elektrizität schuf (veröffentlicht 1772).
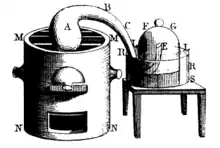

Stephen Hales empirische Forschung über die Elastizität der Luft, aber auch deren Fixierbarkeit in festen Körpern fanden in der Übersetzung seines Werkes Vegetable staticks, or an account of some statical experiments on the sap of vegetables. (1727) durch Georges-Louis Leclerc de Buffon aus dem Jahre 1735 Eingang in die französische Gelehrtenwelt und beeinflussten auch Lavoisier.[46][47] Lavoisier kannte es vermutlich auch aus den Vorlesungen von Rouelle. Eine weitere Quelle für die Idee der Fixierung von Komponenten von Luft war der anonym erschienene Enzyklopädieartikel von Turgot über die Expandierbarkeit von Gasen und Dämpfen, der auch Ideen der Phasenumwandlung von Stoffen von fest über flüssig bis gasförmig enthielt.
In den 1750er Jahren entdeckte Joseph Black beim Erhitzen von Kalkstein Kohlendioxid (fixe Luft) und fand, dass es schwerer als Luft war, die Verbrennungsflamme löschte, bei der Atmung entstand und Tiere tötete. Außerdem konnte es in Wasser gelöst durch Kalkmilch geleitet wiederum Kalkstein ausfällen. Viele Erkenntnisse von Hales und Black waren in Frankreich über die Übersetzung von Experimental Essays on Medical and Philosophical Subjects (1766) von David Macbride bekannt. Da dieser ein medizinischer Schriftsteller war, behandelte er allerdings hauptsächlich mögliche Anwendungen in der Medizin.
1774 veröffentlichte Pierre Bayen über die Freisetzung eines Gases, das er fälschlich für die fixe Luft von Joseph Black hielt, bei Erhitzung von rotem Quecksilberoxid (Quecksilberkalk). Das geschah ohne Anwesenheit einer Phlogiston-reichen Substanz wie Kohle. Bayen konnte dies mit demselben Gas auch rückgängig machen, wobei sich das Gewicht erhöhte. Er sagte sich daraufhin von der Phlogistonlehre los. Lavoisier war im Herbst 1774 Teil einer Kommission, die das untersuchen sollte. Auch Priestley berichtete über ein ähnliches Experiment 1775 und teilte die Beobachtung von 1774 schon im Oktober desselben Jahres Lavoisier und anderen französischen Wissenschaftlern bei einem Aufenthalt in Paris mit.[48] Er nannte das Gas (Sauerstoff) wenig später dephlogisierte Luft. Priestley fand, dass mit dem Gas Flammen heller leuchteten. Priestley entdeckte noch weitere Gase (er berichtet darüber in seinen ab 1774 erschienenen Experiments and Observations on Different Kinds of Air) und blieb Anhänger der Phlogistontheorie bzw. einer von ihm geschaffenen Erweiterung. Ein weiterer unabhängiger Entdecker des Sauerstoffs war Carl Wilhelm Scheele in Schweden, der aber erst 1777 darüber veröffentlichte.
Es gab in diesem Zusammenhang durchaus umstrittene Prioritätsfragen, die Lavoisier geschickt umging. Tatsache ist aber, dass er seine Erkenntnisse quantitativ untermauerte und mit vielen weiteren Experimenten überprüfte, wobei er typischerweise einer Analyse gleich die Umkehrung in einer Synthese folgen ließ.
Experimente von Lavoisier
Nach Guerlac war 1772 das entscheidende Jahr, in dem sich Lavoisier mit Verbrennung zu befassen begann, nach Beretta geschah das schon um einiges früher.[49] 1766 wurde er mit der Theorie von Johann Friedrich Meyer bekannt, der die Ätzwirkung von Löschkalk und ähnlichen alkalischen Stoffen auf ein acidum pingue zurückführte (und ebenfalls die Gewichtszunahme bei Verbrennung von Metallen zu Metallkalken). Im selben Jahr erwarb er Bücher aus der Bibliothek von Jean Hellot, darunter eine kommentierte Ausgabe des Buches von Stahl über Sulfur und seine Experimente begannen wohl schon damals.
Lavoisier beobachtete 1772 dass Phosphor und Schwefel beim Verbrennen (wobei Säuren entstanden) an Gewicht zunahmen[50] und dabei Bestandteile aus der Luft aufnahmen und er überlegte, ob die schon früher beobachtete Gewichtszunahme bei Metallen nicht auf dieselbe Weise zustande kam. Am 1. November hinterlegte er seine Beobachtungen, wie bei besonders wichtigen Entdeckungen üblich, in einem versiegelten Umschlag bei der Akademie der Wissenschaften, worin er schrieb:[51]
„Vor ungefähr acht Tagen habe ich entdeckt, dass Schwefel bei der Verbrennung keineswegs Gewicht verliert, sondern im Gegenteil Gewicht gewinnt. Das gleiche tritt beim Phosphor auf: Die Gewichtszunahme stammt aus einer beträchtlichen Menge Luft, die während der Verbrennung fixiert wird und die sich mit den Dämpfen verbindet. Diese Entdeckung hat mich zu der Annahme geführt, dass das, was man bei der Verbrennung von Schwefel und Phosphor beobachtet, auch bei allen anderen Körpern auftreten könnte, deren Gewicht bei der Verbrennung zunimmt.“
Die Experimente überzeugten ihn auch davon, dass die Luftbestandteile einen wesentlichen Anteil an der Bildung von Säuren hatten. Sie entstanden nach Lavoisier durch Verbrennen von Nichtmetallen.
Im Februar 1773 begann er ein neues Laborbuch für eine lange Reihe von Experimenten, die nach Lavoisier eine Revolution in der Physik und Chemie bewirken sollten. Untersucht werden sollten alle elastischen Fluide die bei verschiedenen chemischen Reaktionen aus Körpern entwichen und über die bei Verbrennung absorbierte Luft. Dazu unternahm er auch eine Literaturrecherche und wollte alle bekannten Experimente selbst wiederholen und seine eigenen ausdehnen. Er präsentierte seine Ergebnisse der Akademie 1773 veröffentlichte dazu im Januar 1774 ein Buch (Opuscules physiques et chimiques). Im selben Jahr erfuhr er von den Beobachtungen von Bayen und Priestley. Er untersuchte die dephlogisierte Luft von Priestley (Sauerstoff) und fand dass sie das Leben von Vögeln in abgeschlossenen Behältern verlängerte. Mit Kohlenstoff bildete es fixe Luft (Kohlendioxid), womit er deren Zusammensetzung klärte. Die Restluft nach der Verbrennung des Quecksilbers (überwiegend Stickstoff) brachte wie Blacks fixe Luft (Kohlendioxid) Flammen zum erlöschen, erzeugte aber in Kalkwasser keinen Niederschlag.
Auch das Verbrennen von Metallen (Blei, Zinn) in geschlossenen Behältern wiederholte er und fand, dass nur ein Teil der Luft (rund ein Fünftel) zur Gewichtszunahme beitrug, die abhängig vom Volumen der eingeschlossenen Luft war. Dabei fand er auch einen Fehler in den älteren Versuchen von Robert Boyle dazu. Dieser hatte behauptet, in abgeschlossenen Gefäßen eine Gewichtszunahme beobachten zu können, was er auf Feuerteilchen zurückführte, aber sich durch Lavoisier als Messfehler erwies. Er fand auch, dass der vom Metall absorbierte Anteil der Luft (Sauerstoff) schwerer war als die Luft und die nach der Kalzinierung übrig gebliebene Restluft leichter. 1774 trug er seine Ergebnisse der Akademie vor, ein erster Aufsatz (Sur la calcination des metaux dans les vaisseaux fermes et sur la cause de l’augmentation de poids qu’ils acquirent pendant cette operation) erschien 1774 in den Observations sur la physique von Rozier und der Aufsatz erschien ausführlicher 1777 in den Memoirs der Akademie. Noch wichtiger war sein Aufsatz (Memoire sur la nature du principe qui se combine avec les metaux pendant leur calcination, et qui en augmente le poids), der im April 1775 in der Zeitschrift Observations sur la physique erschien und vollständiger 1778 in den Abhandlungen der Akademie. Da die Veröffentlichungen in den Mémoirs der Akademie zu langsam mit jahrelanger Verspätung erfolgten, veröffentlichte Lavoisier zunächst in den Observations. In beiden Fällen änderte er aber, was für ihn typisch war, die Inhalte und aktualisierte sie, um inzwischen gewonnene Erkenntnisse. Priestley wurde genauso wenig wie Bayen erwähnt.
1776 erschien sein Aufsatz Sur l’existence de l’air dans l’acide nitreux (Über die Existenz von Luft in Salpetersäure), in dem er seine Theorie der Rolle von Sauerstoff bei Säuren darlegte. Für ihn war der Sauerstoff das ausschlaggebende Element, das die Natur der Säuren bestimmte, was die meisten Chemiker übernahmen (bis zur Entdeckung von Chlorwasserstoff durch Humphry Davy 1808). 1779 legte er diese Erkenntnisse in seiner Schrift Considérations générales sur la nature des acides (Allgemeine Überlegungen über die Natur der Säuren) nieder, die erst 1781 erschien. Für den Sauerstoff gebrauchte er nun statt reinstem Bestandteil der Luft (air pur), Lebensluft(air vital) oder sehr atembare Luft (air éminemment respirable) den Ausdruck Oxygen, das heißt, er sprach vom säurebildenden Prinzip als dem principe oxigine, woraus in seiner Nomenclature chimique 1787 oxygène wurde (säurebildend aus dem Griechischen). Die Stärke der Säuren wurde nach Lavoisier vom Oxidationsgrad bestimmt, was allerdings zu einigen Komplikationen führte. Das fing schon damit an, dass Wasser nach seiner Theorie eigentlich eine Säure sein sollte, woraus Lavoisier sich heraushalf, indem er dem Sauerstoff darin die niedrigste Oxidationsstufe zuwies. 1785 zeigte er, dass die Lösung von Metallen in Säuren zu ähnlichen Metallkalken wie bei der Kalzinierung an der Luft führte, was er nasse Kalzinierung nannte.
Teilweise arbeitete er in dieser Zeit mit dem Chemiker Jean-Baptiste-Michel Bucquet zusammen, der allerdings 1780 verstarb.

Kampf gegen die Phlogistonanhänger
Lavoisiers Chemie wurde bald als antiphlogistische Chemie bekannt (das Wort stammt von Richard Kirwan 1787).[52] Er propagierte sie insbesondere in seinen Reflexions sur la phlogistique von 1786, die sein Biograph Douglas McKie 1935 eine der bemerkenswertestens Schriften in der Geschichte der Chemie nannte.[53] und Henry Guerlac eine brillante dialektische Leistung. Er setzte sich darin nicht nur mit Stahl auseinander, sondern auch mit seinen moderneren Gefolgsleuten wie Pierre-Joseph Macquer, Priestley oder Antoine Baumé (ohne Priestley oder Baumé überzeugen zu können). Sein eifrigster und einflussreichster Gegner war Jean-Claude Delamétherie, der Herausgeber der Zeitschrift Observation sur la physique war und diese, in der Lavoisier vorher veröffentlicht hatte, zum Sprachrohr seiner Gegner machte. Auf seiner Seite waren die Chemiker Claude-Louis Berthollet, Antoine de Fourcroy und Guyton de Morveau, mit denen er die Nomenclature chimique (1787) verfasste, die international sehr einflussreich wurde und in die sie ihre neue Verbrennungstheorie so einbauten, sodass sich Joseph Black beklagte, dass man mit der neuen chemischen Nomenklatur auch gezwungen sei deren Theorie zu übernehmen. Außerdem veröffentlichte die Gruppe 1788 eine kritisch kommentierte Übersetzung von dem Buch von Essay on Phlogiston von Richard Kirwan (Übersetzung von Marie Lavoisier) und gründete eine neue Zeitschrift, die Annales de Chimie (1789).[54] Schließlich propagierte Lavoisier seine Theorie in seinem Lehrbuch Traité élémentaire de la chimie von 1789 und Fourcroy in seinem ebenfalls sehr einflussreichen Lehrbuch Élemens d’histoire naturelle et de chimie ab der dritten Auflage von 1788 (4. Auflage 1791, 5. Auflage 1793). Die Anhänger der alten Phlogistonlehre traten bis auf wenige Ausnahmen einer nach dem anderen in das neue Lager über, darunter auch Joseph Black, der das 1790 Lavoisier brieflich mitteilte, und Kirwan, einer deren Hauptvertreter. Er kapitulierte 1791 brieflich gegenüber Berthollet vor den französischen Chemikern, was wiederum Lavoisier ärgerte, der sich genötigt sah öffentlich darauf hinzuweisen, dass dies seine Theorie und nicht die der französischen Chemiker sei.[55] Lavoisier setzte auch, nachdem er 1784 Präsident der Akademie der Wissenschaften geworden war, sein Gewicht in der Akademie zum Beispiel bei Neuberufungen im Sinn der Antiphlogiston-Kampagne ein.
Zu Beginn seiner Kampagne in den 1780er Jahren hatte er noch kaum Anhänger. Die englischen Phlogistonanhänger sammelten sich um Richard Kirwan. Dieser erklärte die Gewichtszunahme bei Kalzination so: Phlogiston entwich bei Verbrennung, vereinigte sich mit der dephlogisierten Luft von Priestley und bildete fixe Luft, die den Metallkalk bildete. Lavoisiers Argument, dass seine Theorie unmittelbar aus Präzisionsmessungen folgen würde entgegneten die englischen Chemiker, dass Präzision in den Messungen (ein Hauptargument Lavoisiers) nicht unbedingt Präzision der gezogenen Schlussfolgerungen nach sich zöge.[56] Die Konstruktionen der Phlogistonanhänger wurden aber immer umständlicher und die Verbindung von Lavoisiers Sauerstofflehre mit der sich als äußerst nützlich erweisenden neuen Nomenklatur führten aber schließlich zum Sieg der Anhänger von Lavoisier. Jean-Antoine Chaptal übernahm die Lehre Lavoisiers 1784 und lehrte sie in seinen Kursen und Martinus van Marum war 1787 einer der ersten ausländischen Gelehrten, die seine Lehre übernahmen. Andere Chemiker wie Macquer, Priestley und Baumé wurden nie Anhänger der neuen Chemie. In Deutschland erschien der Traité 1792 in einer deutschen Übersetzung (System der antiphlogistischen Chemie) von Sigismund Friedrich Hermbstädt, der sich auch um die Verbreitung der Nomenklatur der Lavoisier-Schule im deutschsprachigen Raum verdient machte.
Um den Durchbruch seiner Oxidationstheorie zu fördern, veranstaltete Lavoisier im Juni 1789 ein Bühnenstück, das er im Arsenal aufführte. Auf der Bühne erschien das brennbare Phlogiston, es wurde von Oxygène schwerer Verbrechen beschuldigt. Der Advokat, Professor Stahl, verteidigte das Phlogiston. Schließlich wurde Phlogiston zum Feuertod verurteilt. Madame Lavoisier war dabei die Opferpriesterin. Lorenz von Crell war dabei zugegen und fand das als Deutscher, in dessen Land die Phlogistontheorie noch vorherrschend war, überraschend und schockierend.[57] Justus von Liebig dagegen schrieb im folgenden Jahrhundert: Derselbe Geist, welcher zu Ende des vorigen Jahrhunderts in einem hochcivilisierten Volk das wahnsinnige Bestreben erweckte, die Denkmale seines Ruhms und seiner Geschichte zu vernichten, der Göttin der Vernunft Altäre zu erbauen und einen neuen Kalender einzuführen, gab Veranlassung zu dem seltsamen Feste, in welchem Madame Lavoisier im Gewande einer Priesterin das phlogistische System auf einem Altar den Flammen übergab, während eine feierliche Musik ein Requiem spielte. Damals vereinigten sich die französischen Chemiker zu einer Aenderung aller bis dahin gebräuchlichen Namen und Bezeichnungsweisen von chemischen Vorgängen und chemischen Verbindungen, es wurde eine neue Nomenclatur eingeführt, welche im Gefolge eines sich vollendeten neuen Systems sich in allen Ländern die Aufnahme erzwang. Daher denn die scheinbare Kluft zwischen der gegenwärtigen und früheren Chemie.[58]
Elemente und Verbindungen
Lavoisier benutzte die Bezeichnung Substances simples für das, was teilweise dem heutigen Elementbegriff nahekommt. Sie sind nach Lavoisier nicht weiter mit chemischen Mitteln zerlegbar, jedenfalls nach vorläufigem Kenntnisstand, denn die Liste änderte sich zum Beispiel von seiner Nomenclature chimique[59] bis zum zwei Jahre später erschienenen Traité élémentaire de la chimie, weil einige Substanzen inzwischen als zusammengesetzt erkannt wurden wie Ammoniak (Berthollet). Die Liste im Traité enthielt nur noch 33 gegenüber 55 in der Nomenclature einfache Substanzen,[60] darunter Licht, Kalorik (calorique, Wärmestoff), Sauerstoff (oxygéne), Wasserstoff (hydrogène) und Stickstoff (azote), die er nochmals gesondert hervorhob als einfache Substanzen, die in allen drei Reichen[61] vorkommen und als Elemente der Körper betrachtet werden können. In der Nomenclature fehlte unter diesen Elementen noch Stickstoff. Der Grund für diese Hervorhebung der fünf Elemente lag darin, dass Lavoisier dafür noch eine weite Verbreitung in der Natur verlangte[62] und sie übernahmen eine Rolle, in der noch Reste der Lehre der Prinzipien (Mitteln der Umwandlung) der älteren Alchemie erkennbar sind. Über die Einstufung des Lichts war sich Lavoisier nie sicher, er wusste aber aus Arbeiten von Jean Senebier und Jan Ingenhousz, dass es eine wichtige Rolle in der Pflanzenphysiologie spielte.[63] Im Stickstoff sah er nach Guerlac vielleicht nach der erfolgreichen Analyse des Ammoniaks durch Berthollet ein Alkali-Prinzip. Dann folgten in der Liste die Nichtmetalle (Schwefel (soufre), Phosphor (phosphore), Kohlenstoff (carbone) und die Radikale (Säurebestandteile) von Salzsäure (Radical muriatique), Flusssäure (Radical fluorique), Borsäure (Radical borique)) sowie die Metalle (Antimon, Silber, Arsen, Bismut, Kobalt, Kupfer, Zinn, Silber, Gold, Eisen, Mangan, Quecksilber, Molybdän, Nickel, Platin, Blei, Wolfram, Zink). Beide Gruppen ordnet er als oxidierbar und säurebildend (Nichtmetalle) bzw. durch Säuren angreifbar (Metalle) ein. Es folgen noch die alkalischen Erden Kalzium (Kreide, chaux), Magnesium (magnésie), Aluminium (alumine), Baryt (baryte, Bariumsulfat) und Silizium (silice).[64] Angegeben sind dabei heutige Entsprechungen, wie Lavoisier bemerkte,[65] war die Einteilung nur vorläufig und einige der angegebenen Metalle (außer Gold, Silber) und Erden waren mit Oxiden oder anderem vermischt oder sogar selbst Oxide (zum Beispiel nach Lavoisier sehr wahrscheinlich Baryt, das sich in einigen Experimenten wie ein Metall verhielt). Im Fall des Siliziums (Quarz u. a.) und Aluminiums (Aluminiumerde) aus der Liste zeigte dies Humphry Davy 1807 mit elektrochemischen Methoden. Gegenüber der Nomenclature hatte er die alkalischen Substanzen Pottasche, Soda, Ammoniak und neunzehn organische Radikale (wie das der Essigsäure) ausgesondert.
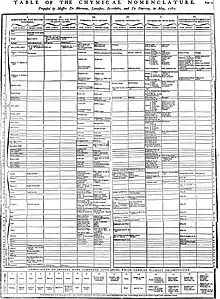
In der zweiten Ordnung der Substanzen ordnete er in seiner Nomenklatur diejenigen ein, die durch Einwirkung der Kalorik (Wärme) in den gasförmigen Zustand übergingen, und in weiteren Ordnungen (drei bis sieben) Substanzen, die durch Einwirkung von Sauerstoff entstanden, wobei er mehrere Oxidationsstufen unterschied (ein Vorläufer des Valenzbegriffs). Dem Sauerstoff kam in dem System eine zentrale Bedeutung zu. Von Lavoisier stammen auch die heute noch gebräuchlichen unterschiedlichen Endungen von Säuren und Salzen je nach Sauerstoffanteil, wie Schwefelsäure (acide sulfurique), schweflige Säure (acide sulfureux, mit weniger Sauerstoff), Sulfat (Salz der Schwefelsäure), Sulfit (Salz der schwefligen Säure).
Spekulationen, die nicht vom Experiment überprüft werden konnten, war Lavoisier grundsätzlich abgeneigt, so bezeichnete er in einer bekannten Passage im Discours préliminaire seines Traité von 1789, den er auch als seinen Beitrag zur Logik und Philosophie der Wissenschaften verstand, weitere Hypothesen über die Natur der Elemente wie die Existenz von Atomen und Molekülen als metaphysisch mit einer Vielzahl von Möglichkeiten, über die man beim augenblicklichen Stand der Wissenschaft nicht entscheiden könne:[66]
„Alles was man über die Anzahl und Natur der Elemente sagen kann, ist meiner Meinung nach rein metaphysisch: Dies sind unlösbare Probleme, für die es unendlich viele Lösungen gibt, von denen sehr wahrscheinlich keine mit der Natur übereinstimmt. Ich begnüge mich deshalb damit zu sagen, dass wenn wir mit dem Namen Elemente die einfachen und unteilbaren Moleküle meinen, die die Körper bilden, wir sie wahrscheinlich nicht kennen. Wenn wir dagegen mit dem Namen Element oder den Prinzipien der Körper die Idee des letzten Punktes verbinden, bis zu dem wir Stoffe analysieren können, so sind alle Substanzen die wir nicht weiter mit welchen Mitteln auch immer zerlegen können die Elemente. Wir können zwar nicht garantieren, dass diese Körper, die wir als einfach betrachten, nicht selbst aus zwei oder einer viel größeren Anzahl von Prinzipien zusammengesetzt sind, aber da sie bisher nicht getrennt wurden oder für die wir bisher kein Mittel haben, sie zu trennen, müssen wir sie aus unserer Sicht wie einfache Körper behandeln und erst als zusammengesetzt, wenn Erfahrung und Beobachtung uns einen Beweis liefern.“
Chemische Nomenklatur
Von besonderem Einfluss war die von Lavoisier und Morveau angestoßene Einführung einer rationalen chemischen Nomenklatur, mit der anorganische Verbindungen nun einfach und schnell bezeichnet werden konnten. Anorganische Stoffe und Säuren hatten vor 1787 recht sonderbare Namen: Alembrotsalz, Kolkothar, algarothisches Pulver, Pompholix, Zinkblumen, Vitrolsäure usw. Vielfach stammten die Bezeichnungen noch aus der Alchemie. Die ersten Ideen und Vorschläge zu einer neuen Nomenklatur stammten von Guyton de Morveau (Mémoire sur les dénominations chymiques, 1782).[67] 1787 erschien dann das rund 250 Seiten starke Buch Nomenclature chimique, in dem Lavoisier, Mourveau, Claude-Louis Berthollet und Fourcroy die neue Nomenklatur im Rahmen der Theorie von Lavoisier vorlegten. Lavoisier, Morveau und Kollegen entwickelten dabei eine binäre Notation, um die Salze aus ihren Basen und Säuren zu erklären. Ein Vorbild war dabei auch das Klassifikationssystem der Biologie von Carl von Linné. Für Lavoisier spielte auch der Einfluss von Étienne Bonnot de Condillac und seiner Verbindung von Sprache und Logik eine Rolle.
Neben der Nomenklatur wurden auch Zeichen nach Jean-Henri Hassenfratz (1755–1827) und Pierre-Auguste Adet (1763–1834) für die chemischen Elemente eingeführt.[15] Diese Symbole unterschieden sich noch ein wenig von den späteren – im Jahre 1814 von Jöns Jakob Berzelius (1779–1848) entwickelten und heute gebräuchlichen – Elementsymbolen.
Die Entdeckung des Wasserstoffs und Synthese von Wasser
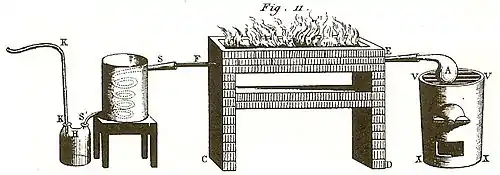
Cavendish gilt als Entdecker des Wasserstoffs (1766), den er durch Einwirken von Säuren auf Metalle gewann und brennbare Luft (inflammable air) nannte und die Anhänger der Phlogistonlehre wie Cavendish selbst identifizierten zunehmend Wasserstoff mit Phlogiston. Für Lavoisier konnte der Wasserstoff nicht wie Cavendish annahm aus dem Metall stammen, sondern musste aus der Säure kommen, seine Versuche mit Wasserstoff durch Verbrennung eine Säure zu bilden schlugen aber fehl. Bei der Verbrennung von Wasserstoff an Luft gab es anscheinend überhaupt kein Reaktionsprodukt, was ein Problem für seine Theorie war.[68] Cavendish hatte nun 1781 von Experimenten von Priestley erfahren, dass bei Verbrennung von Sauerstoff und Wasserstoff ein Tau entstand, den Cavendish in eigenen Experimenten 1783 mit Wasser identifizierte. Seine Experimente zur Wassersynthese veröffentlichte er aber erst 1784 und interpretierte sie in einer eigenen Abwandlung der Phlogistontheorie.[69] Lavoisier hatte 1783 durch Charles Blagden von Cavendishs neuen Experimenten gehört, einem engen Vertrauten von Cavendish, der 1783 in Paris weilte und Experimenten von Lavoisier und Laplace beiwohnte.
Lavoisier stellte die Versuche nach und 1783 bis 1785 eigene Untersuchungen an, gewann 1783 aus den beiden Gasen wiederum Wasser und stellte daraufhin die These auf:
„Die Verbrennung der beiden Luftarten und ihre Umwandlung zu Wasser, Gewichtsteil für Gewichtsteil, erlaubt kaum noch Zweifel daran, dass diese Substanz, die bislang als Element betrachtet wurde, ein zusammengesetzter Stoff ist.“
Damit brachte Lavoisier (der allerdings in Cavendish einen Vorläufer hatte) die noch auf Aristoteles beruhenden alten Denkgebäude, die Luft und Wasser für unzerstörbare Elemente hielten, zum Einsturz, und beseitigte gleichzeitig das letzte Hindernis für seinen Angriff auf die Phlogistontheorie. Er untermauerte seine Erkenntnis mit einem weiteren Experiment (1784 mit Meusnier): Er erhitzte Eisenspäne bis zur Rotglut, leitete Wasserdampf darüber und stellte fest, dass sich das Eisen zu Eisenoxid verwandelt und dabei an Gewicht zugenommen hatte. Er stellte weiterhin fest, dass zwar ein Teil des Wasserdampfes wieder zu Wasser kondensiert war, ein anderer Teil sich jedoch zu sogenannter brennbarer Luft zersetzt hatte. Lavoisier erkannte, dass er reinen Wasserstoff (hydrogène, wasserbildend von Lavoisier genannt) in seinem Gasbehälter gewonnen hatte. Er nannte das Gas Knallgas. Das alles stellte er 1785 in spektakulären Experimenten dem Publikum vor.
Auch hier kam es zu Unstimmigkeiten über die Priorität, da Lavoisier sich in seiner Veröffentlichung unklar darüber ausdrückte, dass er von Blagden über Cavendishs Experimente vor der Durchführung seiner eigenen informiert worden war.
Zu den Quellen für die Experimente von Lavoisier[70] zählen auch ein von dem Abbé Felice Fontana 1777 erfundenes Gerät, eine Art umgestülptes Reagenzglas in einem Quecksilberbad. In einem Experiment enthielt das Glas über dem Quecksilber Wasser und Fontana führte rotglühende Kohle ein, die in dem Reagenzglas Wasserstoff erzeugte. Das Instrument wurde von ihm viel benutzt und ist auf dem Gemälde von David von Lavoisier und seiner Frau abgebildet. 1782 demonstrierte Alessandro Volta in Paris Lavoisier sein elektrisches Eudiometer, von ihm elektrische Kanone genannt. In einem abgeschlossenen Glasgefäß löste er mit elektrischen Entladungen Verbrennungen in verschiedenen Gasen aus. Dabei hatte er auch bei der Reaktion von Sauerstoff (dephlogisierte Luft) und Wasserstoff (entflammbare Luft) die Bildung einer feuchten Substanz beobachtet, war davon aber so überrascht, dass er nicht daran dachte sie mit Wasser zu identifizieren. Er zeigte diesen Versuch aber höchstwahrscheinlich auch Lavoisier (Beccara). Geräte dieser Art waren später auch in Lavoisiers Labor, mit denen die Experimente zur Wassersynthese und -analyse einfacher durchzuführen waren. Für seine überzeugenden Demonstrationen vor Publikum benutzte Lavoisier aber ein großes speziell gefertigtes Gasometer. In seinen Experimenten wurde Lavoisier damals teilweise von dem Mathematiker Gaspard Monge, der sich seit 1777 für Chemie interessierte, Jean-Baptiste Meusnier de la Place, der über Monge Kontakt zu Lavoisier bekam, Fourcroy (1785) und von Laplace unterstützt.[71]
Gesetz der Massenerhaltung und organische Analyse
Das Gesetz der Massenerhaltung bei chemischen Umsetzungen war im 18. Jahrhundert zwar eine bei Wissenschaftlern häufig gemachte allgemeine Annahme, die aber auch mit Unsicherheiten behaftet war, da man zum Beispiel in der Wärme nach der Phlogistontheorie auch einen Stoff sah, der zu Gewichtsänderungen bei Stoffen führen konnte. Edme Mariotte formulierte das Prinzip (Essai de logique 1678) und es war grundsätzlich eine Folge atomistischer Ideen, Lavoisier formulierte es aber als Erster explizit bei chemischen Reaktionen.[72] Lavoisier konnte aus der Verkalkung von Metallen (Metalloxidation) durch sorgfältige Gewichtsmessungen der Luftabnahme, bzw. des spezifischen Gewichtes von Luft, ferner aus Gewichtsbestimmungen durch Zersetzung von 100 Gran[73] Wasser in 15 Gran entzündlichem Gas (Wasserstoff) und 85 Gran Lebensluft (Sauerstoff) nachweisen, dass eine Massenerhaltung bei chemischen Umsetzungen vorliegt. Erst diese klaren Beweise konnten die Phlogistontheorie umstürzen. 1789 stellte er in seinem Traité (Band 1, Kapitel XIII über Gärung) das Prinzip der Massenerhaltung fest:[74]
„Nichts wird bei den Operationen künstlicher oder natürlicher Art geschaffen, und es kann als Prinzip angesehen werden, dass bei jeder Operation eine gleiche Quantität Materie vor und nach der Operation existiert.“
Lavoisier benutzte systematisch in der Darstellung seiner Messergebnisse Bilanztabellen der Gewichte, ebenso wie später bei der Messung der Wärme. Für ihn entsprach der Genauigkeit der theoretischen Analyse unmittelbar die Genauigkeit der Experimente und umgekehrt, oder wie es sein Gefolgsmann Jean Baptiste Biot ausdrückte: Man fühlte die Notwendigkeit der Verbindung von Genauigkeit im Experiment mit Strenge der theoretischen Ableitung.[75] Er wurde somit der Begründer der Stöchiometrie, der chemischen Mathematik, die später von Jeremias Benjamin Richter durch das Erkennen des mathematischen Zusammenhanges bei Salzbildungen verbessert wurde.
Neben seinen Arbeiten zur Atmung war er auch ein Pionier der organischen Analyse in seiner Untersuchung der Verbrennung organischer Stoffe und der Gärung, über die er zuerst in seinem Traité berichtet. Er wusste, dass bei der Verbrennung pflanzlicher Stoffe Wasser und Kohlendioxid entstehen, wollte aber wissen, in welcher Kombination Kohlenstoff, Wasserstoff und Sauerstoff in den pflanzlichen Stoffen wie Alkohol vorkamen. Zunächst verbrannte er Öle, dann leicht flüchtigere Substanzen wie Alkohol und Äther, wobei er bei Alkohol auf ein Gewichtsverhältnis von Kohlenstoff zu Wasserstoff von 3.6 zu 1 kam (nahe dem korrekten 4:1). Bei der Gärung unterschied er wie seine Vorgänger alkoholische Gärung, säureerzeugende Gärung (zum Beispiel Essigsäure erzeugend) und Verwesung. Die heftige Bewegung bei alkoholischer Gärung sah er als Anzeichen für eine heftige chemische Reaktion bei der Umordnung der drei Grundelemente (organische Prinzipien) C, H, O. In diesem Zusammenhang stellte er am Beispiel der Gärung auch erste einfache Reaktionsgleichungen auf, in der Form: Most = Alkohol + Kohlendioxid (Mout de raisin = acide carbonique + alkool).[76][77] Sie war in seinem Traité allerdings nicht wirklich quantitativ gestützt und war nach Arthur Harden ein Beispiel dafür, wie das Genie eines Forschers über die experimentellen Daten triumphierte.[78]
Wärmetheorie, Physiologie der Atmung
Pionier auf diesem Gebiet war in den Jahren 1756 bis 1766 der Schotte Joseph Black, der die Konzepte latente Wärme, spezifische Wärmekapazität und Methoden zu deren Messung einführte, wobei die praktischen Messungen überwiegend James Watt als Erster ausführte, der deren Bedeutung für Anwendungen erkannte. Schüler von Black in Glasgow setzten dessen Arbeit fort (William Irvine (1743–1787), Adair Crawford mit Anwendungen in der Physiologie).[79] Insbesondere Crawford beeinflusste auch Lavoisier.
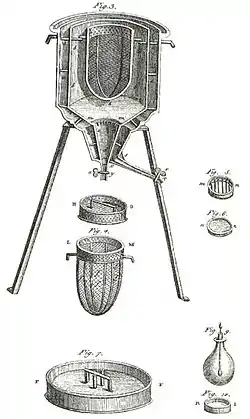
Lavoisier ging wie in seiner Nomenclature chimique von 1787 und seinem Traité élémentaire de la chimie von 1789 dargelegt von der Existenz eines „Wärmestoffs“ („Caloricum“, le calorique) aus, den er zu den grundlegenden Elementen zählte. Er nannte das Vermögen der chemischen Körper den Wärmestoff zu fassen, in seiner Traité élémentaire de chimie von 1789, auch Fähigkeit der Körper den Wärmestoff aufzunehmen (capacité des corps pour contenir la materière de la chaleur). Nach Lavoisier wurde bei der Verbrennung mit Hilfe des Oxygens (Sauerstoff) aus der Luft auch Wärmestoff freigesetzt, der somit auch Bestandteil der Luft wäre (gasförmiger Sauerstoff bestand aus Kalorik und Sauerstoff). Gelegentlich wurde eingewandt, dass der Wärmestoff nichts anderes als die Phlogistontheorie in neuem Gewand sei, allerdings konnten die Wirkungen im Gegensatz zum Phlogiston exakt gemessen werden. Einen Beweis für die Existenz eines solchen Wärmefluids konnte Lavoisier nie erbringen, wie er 1785 selbst zugeben musste (er sah das aber als geläufige Annahme, die auch seine Phlogistongegner machten).[80] In seinem Traité von 1789 erklärte er sogar, dass die Annahme der realen Existenz einer Wärmesubstanz gar nicht für seine Argumentation notwendig wäre, nur die Existenz einer wie auch immer gearteten repulsiven Kraft, die den chemischen Affinitäten entgegenwirkt, die die Körper zusammenhalten.[81]
Laplace und Lavoisier begannen ihre Experimente 1777 und setzten sie bis 1784 fort, mit dem Schwerpunkt im Winter 1782/83 sowie 1783/84. Sie stellten zunächst fest, dass es zwei vorherrschende Auffassungen von der Natur der Wärme gibt: die des Wärmestoffes, eines überall verteilten unwägbarem Fluidums, das in unterschiedlichem Ausmaße zwischen die Räume eines Körpers eindringen konnte und dessen Temperatur bestimmte. Dieser Ansicht neigte Lavoisier zu. Laplace hingegen hatte die Vorstellung, dass Wärme durch die Bewegung kleinster Teile (Moleküle) des Körpers entstünde. Sie wollten nicht zwischen beiden Theorien entscheiden, die nach ihrer Ansicht vielleicht beide zutrafen, da einige Eigenschaften für die eine, andere für die andere Theorie sprachen, sondern Eigenschaften betrachten, die aus beiden Theorien folgten, so die Erhaltung der Wärmemenge, in der Fluidtheorie gültig ebenso wie aufgrund der Energieerhaltung in der Atomtheorie.[82]
Laplace und Lavoisier benutzten das Eiskalorimeter zur Messung der Wärme. Die zum Beispiel bei der Verbrennung verschiedener Stoffe freigesetzte Wärme schmolz eine entsprechende Menge des Eises und war damit Maß für die Wärmebildung bei der Verbrennung des jeweiligen Stoffes. Das Kalorimeter bestand aus einer Reihe ineinandergeschachtelter Töpfe. In den innersten Topf kam der Probekörper. In die äußeren wurde zerstoßenes Eis gefüllt, einerseits zur Isolation, andererseits konnte über die Menge des Schmelzwassers um den inneren Behälter die vom Probekörper abgegebene Wärme gemessen werden. Laplace und Lavoisier maßen zunächst in Festkörpern, Flüssigkeiten und Lösungen, später mit einem speziellen Kalorimeter auch in Gasen (Wärmekapazitäten und Wärmemengen bei chemischen Reaktionen wie Verbrennung, Lösung, Mischung). Sie wollten auch andere zu weiteren Forschungen mit ihren Methoden anregen. Damit schufen sie die Thermochemie. In der Folge setzten sich bis Anfang des 19. Jahrhunderts statt Eiskalorimeter adiabatische Flüssigkeitskalorimeter durch; Eiskalorimeter wurden erst durch Robert Bunsen und John Herschel in abgewandelter Form wieder genutzt. Die Experimente von Lavoisier und Laplace gehören zu den wenigen von Lavoisier, die in neuerer Zeit mit nach dem Vorbild des Originals nachgebauten Apparaturen überprüft wurden, und ziemlich gute Übereinstimmung auch bezüglich der erreichten Genauigkeit lieferten.[83] In ihren Experimenten zur Wärme wurden Laplace und Lavoisier durch den Lavoisierschüler Philippe Gengembre unterstützt.

An einer Stelle[84] gibt es einen bemerkenswerten Hinweis auf die mögliche Verwendung kalorischer Messungen bei der Untersuchung von chemischen Reaktionen: Das Gleichgewicht zwischen der Wärme, welche die Moleküle der Körper voneinander zu entfernen strebt, kann ein sehr genaues Mittel sein, um diese Affinitäten miteinander zu vergleichen. Mit Affinitäten sind dabei die anziehenden Kräfte gemeint, die die Körper zusammenhalten und der abstoßenden Kraft der Wärme entgegenwirken. Wie aus der den nachgelassenen Mémoirs de physique et chimie von Lavoisier deutlich wird, übernahm auch Lavoisier spätestens 1793 diese atomistische Sichtweise. Neben einer repulsiven Kraft zwischen den Molekülen vermittelt durch die Kalorik wirken demnach anziehende Kräfte (Affinitäten).[85] Überwog die Abstoßung bildeten sich Gase, bei überwiegender Anziehung Flüssigkeiten, wobei er auch schon den Fall engen Kontakts (chemische Verbindung) ins Auge fasste. Er plante auch das Gebiet der chemischen Affinitäten der Stoffe in Angriff zu nehmen, was er bis dahin vermieden hatte, da die hergebrachte Theorie nur qualitativer Natur war.[86]
Laplace und Lavoisier gaben ihren Wärmeforschungen zusätzlich eine physiologische Richtung. So bestimmten beide die Menge Kohlendioxid, air fixe (fixe Luft), die ein Kleintier (Meerschweinchen) während einer bestimmten Zeit ausatmete. Dann setzten sie das Tier in das Eiskalorimeter und maßen, wie viel Eis während seiner Anwesenheit in den gleichen zehn Stunden schmolz. Dabei verglichen sie neben den Gasmengen auch die Wärmebildung des Tieres und verglichen sie mit der bei der Verbrennung von Kohle. Lavoisier und Laplace zogen das Fazit, dass Atmung dasselbe wäre wie Verbrennung und dazu diente, die Körperwärme der Tiere zu erhalten. Das war auch ein wichtiger Schritt zur chemischen Erklärung der Lebensvorgänge.
Die Bedeutung des Sauerstoffs bei der Atmung und dass dabei Kohlendioxid entsteht, wies Lavoisier zuerst 1776 in Experimenten mit Philibert Trudaine de Montigny nach. Den Atmungsvorgängen waren auch seine letzten Experimente 1790/91 gewidmet, in denen er von Armand-Jean-François Seguin unterstützt wurde, der sie auch nach seinem Tod fortsetzte. Als Versuchsperson diente nun ein Mensch (Seguin). Danach nahm der Verbrauch von Sauerstoff bei der Atmung mit körperlicher Leistung, Verdauung und Temperatur zu, die Aufnahme erfolgte in den Tubuli der Lunge. Schon 1785 fand er, dass nicht der ganze Sauerstoff in Kohlendioxid überging, ein Teil ging seiner Vermutung nach in Wasser über, was er ebenfalls mit Seguin weiter untersuchte.
Sonstiges und Benennungen nach Lavoisier
- Das Lycée Lavoisier in Paris ist ihm zu Ehren benannt. Dort wurden seit 1793 für die Öffentlichkeit Vorlesungen gehalten und es ist auf Initiative von Lavoisier gegründet worden. Ebenso eine Straße im 8. Arrondissement und es gibt Statuen von ihm am Rathaus und im Cours Napoléon des Louvre.
- Lavoisier ist namentlich auf dem Eiffelturm verewigt. Siehe dazu: Die 72 Namen auf dem Eiffelturm.
- Er ist der einzige nichtdeutsche Wissenschaftler, der im Deutschen Museum in München mit einer Büste geehrt wurde.[87]
- Im Deutschen Museum ist das Labor Lavoisiers rekonstruiert worden.[88] Instrumente aus dem Labor von Lavoisier sind im Conservatoire national des arts et métiers in Paris ausgestellt, das auf Initiative von Lavoisier gegründet wurde.
- Carl Djerassi und Roald Hoffmann schrieben ein Theaterstück Oxygen über die Entdeckung des Sauerstoffs, das 2001 uraufgeführt wurde.[89]
- Der Asteroid (6826) Lavoisier wurde nach ihm benannt.
- Die Lavoisier-Medaille der SCF.
- Der Mondkrater Lavoisier ist nach ihm benannt.
- Das UK Antarctic Place-Names Committee benannte im Jahr 1960 die vor der Westküste der Antarktischen Halbinsel liegende Lavoisier-Insel nach ihm.
- Die Pflanzengattung Lavoisiera DC. aus der Familie der Schwarzmundgewächse (Melastomataceae) ist nach ihm benannt.[90]
Schriften (Auswahl)
- Oeuvres de Lavoisier. 6 Bände, Paris: Imprimerie National 1862 bis 1894 (Hrsg. J. B. Dumas, Edouard Grimaux), Band 1 – Internet Archive (Traité élémentaire de chimie), Band 2 – Internet Archive (Mémoirs de chimie et de physique), Band 3 – Internet Archive (Mémoirs et rapports sur divers sujets de chimie et de la physique pure), Band 4 – Internet Archive (Mémoirs et rapports sur divers sujets de chimie et de la physique pure).
- Oeuvres de Lavoisier: Correspondance. Band 1–3 (Hrsg. René Fric), Paris: Albin Michel, Band 4 (Hrsg. Michelle Goupil), Paris: Belin 1986, Band 5,6, 7 (Hrsg. Patrice Beret), Paris: Academie des Sciences, Hermann 1993, 1997, 2012.
- Opuscules physiques et chimiques. Paris 1774 (nur der erste von mehreren geplanten Bänden erschien. archive.org).
- Englische Übersetzung: Essays physical and chemical, 1776. (archive.org).
- Deutsche Übersetzung in C. E. Weigel: Lavoisier physikalisch-chemische Schriften. Greifswald, 1783–1794.
- Réflexions sur le phlogistique, pour servir de développement à la théorie de la combustion & de la calcination, publiée en 1777. Mémoires de l’Académie royale des sciences 1786.
- Englische Übersetzung von Nicholas W. Best: Lavoisier’s „Reflections on phlogiston“ I: against phlogiston theory. Foundations of Chemistry, Band 17, 2015, S. 137–151, Teil 2, Band 18, 2016, S. 3–13.
- Méthode de nomenclature chimique, proposée par MM. de Morveau, Lavoisier, Bertholet [sic] & de Fourcroy. On y a joint un nouveau système de caractères chimiques, adaptés à cette nomenclature, par MM. Hassenfratz & Adet. Paris 1787, 2. Auflage 1789 (archive.org, archive.org Ausgabe 1789).
- Deutsche Übersetzung von Karl von Meidinger: Methode der chemischen Nomenklatur für das antiphlogistische System. Wien 1793, (archive.org), und in gekürzter Form von Christoph Girtanner: Anfangsgründe der antiphlogistischen Chemie. Berlin 1792. Digitalisat, Bayerische Staatsbibliothek.
- Traité élémentaire de chimie. 2 Bände, Paris 1789, 2. Auflage 1793, archive.org Band 1, archive.org Band 2).
- Deutsche Ausgabe von Sigismund Friedrich Hermbstädt: System der antiphlogistischen Chemie von Anton Lorenz Lavoisier. Berlin, Stettin 1792. Digitalisat der 2. Auflage 1803, Teil 1, Bayerische Staatsbibliothek.
- Mémoires de chimie. Paris, 2 Bände (von Lavoisier noch 1792 konzipiert, privat von seiner Witwe ab 1803 verbreitet, sie enthalten auch Beiträge weiterer Wissenschaftler).
- Gedruckt als Mémoires de physique et de chimie. 2 Bände, Bristol: Thoemmes Continuum, 2004.
- Mit Pierre Simon Laplace: Mémoir sur la chaleur. Mémoir Acad. Sci., 1780 (erschienen erst 1784), S. 355–480 (auch in Oeuvres Band 2 und Nachdruck Gauthier-Villars 1920).
- Englische Übersetzung: Memoir on Heat. (Übersetzer Henry Guerlac), New York: Neale Watson Academic Publications, 1982.
- Deutsche Übersetzung: Zwei Abhandlungen über die Wärme. (aus den Jahren 1780/1784), Hrsg. Isidor Rosenthal, Ostwalds Klassiker, Leipzig 1892, (archive.org). Dabei wurden auch die Ergänzungen Mémoire contenant les expériences faites sur la chaleur pendant l’hiver de 1783 à 1784, par MM. de Laplace et Lavoisier, pour servir de supplément au mémoire sur la chaleur publié en 1780, berücksichtigt (geschrieben 1793, Versuche Winter 1783/84), die erst in den Mémoires de chimie et physique, herausgegeben von Marie Lavoisier, erschienen und in den Oeuvres, Band 2.
- De la richiesse territoriale de la France. (Hrsg. Jean-Claude Perrot), Paris: Editions du C.T.H.S., 1988.
- Patrice Bret (Hrsg.): Lavoisier et l’encyclopédie méthodique: le manusrit des régisseurs des poudres et salpetres. Florenz: Olschki 1997 (Manuskripte über Pulverherstellung, Detonation und Kohle die Lavoisier 1793 für eine Enzyklopädie und ein Handbuch vorbereitete).
- Marcellin Berthelot: La revolution chimique – Lavoisier. Paris 1890 (mit Auszügen aus den Laborbüchern von Lavoisier, archive.org).
- Mémoire sur al nature de l’Eau et sur lés Expériences par les quelles on a prétendu prouver la possibilité de son changement en terre. Mémoirs Acad. Sci. 1770 (Oeuvres, Band 2).
- Deutsche Übersetzung: Das Wasser. Ostwalds Klassiker, Leipzig: Akademische Verlagsgesellschaft 1930.
- Untersuchungen über das Wasser. Herausgegeben von Peter Buck. Mit einer Einleitung und Biografie von Hermann Klie. Franzbecker – Didaktischer Dienst, Bad Salzdetfurth 1983, ISBN 3-88120-050-9. (Reihe Reprinta Historica Didactica 4).
Weitere Bilder
 Antoine Laurent de Lavoisier; Porträt
Antoine Laurent de Lavoisier; Porträt Detailausschnitt. Verbrennung durch Fokussierung des Sonnenlichts durch optische Linsen auf ein brennbares Material. Ein Experiment das Lavoisier in den 1770er Jahren durchgeführt hatte.
Detailausschnitt. Verbrennung durch Fokussierung des Sonnenlichts durch optische Linsen auf ein brennbares Material. Ein Experiment das Lavoisier in den 1770er Jahren durchgeführt hatte. Verbrennung durch Fokussierung des Sonnenlichts durch optische Linsen. Darstellung des gesamten Versuchsaufbaus.
Verbrennung durch Fokussierung des Sonnenlichts durch optische Linsen. Darstellung des gesamten Versuchsaufbaus. Reaktionsgefäß zur kontrollierten Verbrennung von Wasserstoff
Reaktionsgefäß zur kontrollierten Verbrennung von Wasserstoff Lavoisierstatue am Rathaus
Lavoisierstatue am Rathaus Lavoisierstatue von Jacques-Léonard Mallet im Louvre
Lavoisierstatue von Jacques-Léonard Mallet im Louvre Elementsymbole zur Zeit Lavoisiers, Teil 1
Elementsymbole zur Zeit Lavoisiers, Teil 1 Elementsymbole zur Zeit Lavoisiers, Teil 2
Elementsymbole zur Zeit Lavoisiers, Teil 2 Kalorimeter von Lavoisier
Kalorimeter von Lavoisier Lavoisier, Stich von J. F. Bolt
Lavoisier, Stich von J. F. Bolt Lavoisier in seinem Labor bei den Atmungsexperimenten, Diorama
Lavoisier in seinem Labor bei den Atmungsexperimenten, Diorama
Literatur
- Bernadette Bensaude-Vincent: Lavoisier: Mémoires d’une revolution. Paris: Flammarion, 1993.
- Enrico Bellone (Hrsg.): Lavoisier: Die Revolution in der Chemie. Spektrum der Wissenschaft – Biographie, 1998.
- Marco Beretta: Imaging a Career in Science. The Iconography of Antoine Laurent Lavoisier. Science History Publications, Canton, MA 2001, ISBN 0-88135-294-2.
- Marco Beretta (Hrsg.): Lavoisier in Perspective. München, Deutsches Museum 2005.
- Martin Carrier: Antoine L. Lavoisier und die Chemische Revolution. In: Pierre Leich (Hrsg.): Leitfossilien naturwissenschaftlichen Denkens. Königshausen & Neumann, Würzburg 2001, ISBN 3-8260-2121-5, online (PDF; 245 kB).
- Arthur Donovan: Antoine Lavoisier: Science, Administration, and Revolution. Cambridge University Press, 1993.
- Édouard Grimaux: Lavoisier 1743–1795, d’après sa correspondance, ses manuscrits, ses papiers de famille et d’autres documents inédits. Paris 1888, 1896, 3. Auflage 1899, (archive.org).
- Henry Guerlac: Lavoisier, Antoine-Laurent. In: Charles Coulston Gillispie (Hrsg.): Dictionary of Scientific Biography. Band 8: Jonathan Homer Lane – Pierre Joseph Macquer. Charles Scribner’s Sons, New York 1973, S. 66–91 (ergänzt in den Ergänzungsbänden (Band 4) von Marco Beretta, Scribner’s 2008).
- Henry Guerlac: Lavoisier—The Crucial Year. The Background and Origin of His First Experiments on Combustion in 1772. Ithaca, N.Y.: Cornell University Press, 1961.[91]
- Henry Guerlac: Antoine-Laurent Lavoisier: Chemist and Revolutionary. Scribner, New York 1975.
- Frederic L. Holmes Lavoisier and the Chemistry of Life: an exploration of scientific creativity. Princeton University Press, 1985, Reprint University of Wisconsin Press, 1987.
- Frederic L. Holmes Antoine Lavoisier – the next crucial year: or, the sources of his quantitative method in chemistry. Princeton University Press, 1997.
- Ursula Klein, Wolfgang Lefèvre: Materials in eighteenth-century science. MIT-Press, Cambridge 2007, ISBN 978-0-262-11306-9.
- Albert Ladenburg: Vorträge über die Entwicklungsgeschichte der Chemie, von Lavoisier bis zur Gegenwart. 4. vermehrte und verbesserte Auflage. Vieweg, Braunschweig 1907. (Unveränderter Nachdruck: Wissenschaftliche Buchgesellschaft, Darmstadt 1974, ISBN 3-534-06011-3. archive.org).
- Douglas McKie: Antoine Lavoisier. Victor Gollancz, London 1935, 1952, (archive.org).
- Jean-Pierre Poirier: Lavoisier. University of Pennsylvania Press, 1996.
- Walther Skaupy: Große Prozesse der Weltgeschichte. Die Dubarry und Antoine Laurent Lavoisier vor dem französischen Revolutionstribunal. Magnus Verlag, Essen, S. 63 ff.
- Madison Smartt Bell: Lavoisier in the Year One: The Birth of a New Science in an Age of Revolution. Atlas Books, Norton 2005.
- Max Speter: Lavoisier. In: Günther Bugge: Das Buch Der Grossen Chemiker. Band 1, Verlag Chemie, Weinheim 1984, ISBN 3-527-25021-2.
- Ferenc Szabadváry: Antoine-Laurent Lavoisier. Teubner, Leipzig 1987.
- E. Ashworth Underwood: Lavoisier and the history of respiration. In: Proceedings of the Royal Society of Medicine. Band 37, 1943, S. 247–262. PMC 2180993 (freier Volltext).
Weblinks
- Literatur von und über Antoine Laurent de Lavoisier im Katalog der Deutschen Nationalbibliothek
- Kurzbiografie und Verweise auf digitale Quellen im Volltext im Virtual Laboratory des Max-Planck-Instituts für Wissenschaftsgeschichte (englisch).
- Walter Jansen: Wissenschaftsbiographie von Lavoisier an der Universität Oldenburg (PDF; 596 kB).
- Jean-Pierre Poirier (Comité Lavoisier, Académie des Sciences de Paris): Les amis de Lavoisier.
Einzelnachweise und Anmerkungen
- Georg Korn: Joseph-Ignace Guillotin (1738–1814). Ein Beitrag zur Geschichte der Medicin und des ärztlichen Standes. 1891, S. 23.
- The Chemical Revolution of Antoine-Laurent Lavoisier. International Historic Chemical Landmark an der Académie des Sciences in Paris 1999, American Chemical Society.
- Die genealogischen Tafeln von Lavoisier sind abgedruckt in:
Grimaux: Lavoisier. 1895, S. 326. - Christian Warolin: Lavoisier a-t-il bénéficié de l’enseignement de l’apothicaire, Guillaume-François Rouelle? In: Revue d’histoire de la pharmacie. Band 83, Nr. 307, 1995, S. 361–367, doi:10.3406/pharm.1995.4257 (französisch).
- Guerlac: Dictionary of Scientific Biography. Band 8, S. 70.
- Ferenc Szabadváry: Antoine Laurent Lavoisier. Der Forscher und seine Zeit 1743–1794. Gemeinschaftsausgabe des Akadémiai Kiadó, Budapest und der Wissenschaftlichen Verlagsgesellschaft, Stuttgart 1973, S. 28 ff.
- Zu F. Baudon.
- McKie: Lavoisier. S. 43.
- W. R. Aykroyd: Three Philosophers: Lavoisier, Priestley and Cavendish. London 1935, S. 89.
- Zu Lavoisiers Reform der Tabakproduktion, der Einführung einer rigorosen Qualitätskontrolle und der Aufsicht über den Tabakhandel siehe:
Arthur Donovan: Antoine Lavoisier. Cambridge UP 1993, S. 123 ff. - Kirchliche Hochzeit. Der Ehevertrag wurde am 4. Dezember unterschrieben.
Grimaux: Lavoisier. 1895, S. 40. - Genealogie der Familie von Marie Lavoisier in:
Grimaux: Lavoisier. 1895, S. 330. - Szabadvary: Lavoisier. Teubner, 1987, S. 12.
- 50 Milligramm entsprachen in etwa der kleinsten Gewichtseinheit grains (Gran). Lavoisier gibt die Gewichte in den Maßen an: Pfund (livres), Unzen (once, ein Pfund entsprach 16 Unzen), Gros (eine Unze entsprach 8 Gros) und grains (ein Gros entsprach 8 grains).
- Max Speter: Lavoisier. In: Günther Bugge: Das Buch Der Grossen Chemiker. Band I, Verlag Chemie, Weinheim 1974, ISBN 3-527-25021-2, S. 304.
- Claude Viel: Le salon et le laboratoire de Lavoisier à l’Arsenal, cénacle où s’élabora la nouvelle chimie. In: Revue d’histoire de la pharmacie. Band 83, Nr. 306, 1995, S. 255, doi:10.3406/pharm.1995.4478 (französisch, freier Volltext).
- Szabadvary: Lavoisier. S. 14. Die Angaben folgen Madame Lavoisier.
Guerlac: Dict. Sci. Biogr. S. 84. - Claude Viel: Le salon et le laboratoire de Lavoisier à l’Arsenal, cénacle où s’élabora la nouvelle chimie. In: Revue d’histoire de la pharmacie. Band 83, Nr. 306, 1995, S. 263, doi:10.3406/pharm.1995.4478 (französisch, freier Volltext).
- Eintrag zu Lavoisier, Antoine Laurent (1743–1794) im Archiv der Royal Society, London
- Patrice Bret: Lavoisier à la régie des poudres: Le savant, le financier, l’administrateur et le pédagogue. Secrétaire général du Comité Lavoisier de l’Académie des Sciences. Text über seine administrative Bedeutung in französischer Sprache (PDF; 565 kB).
- Jaime Wisniak: The History of Saltpeter Production with a Bit of Pyrotechnics and Lavoisier. In: Chem. Educator. Band 5, Nr. 4, 2000, S. 205–209, doi:10.1007/s008970000401a.
- Claude Viel: Le salon et le laboratoire de Lavoisier à l’Arsenal, cénacle où s’élabora la nouvelle chimie. In: Revue d’histoire de la pharmacie. Band 83, Nr. 306, 1995, S. 255–266, doi:10.3406/pharm.1995.4478 (französisch, freier Volltext).
- Szabadvary: Lavoisier. 1987, S. 17.
- McKie: Lavoisier. S. 42.
- Claude Viel: Le salon et le laboratoire de Lavoisier à l’Arsenal, cénacle où s’élabora la nouvelle chimie. In: Revue d’histoire de la pharmacie. Band 83, Nr. 306, 1995, S. 263, doi:10.3406/pharm.1995.4478 (französisch, freier Volltext).
- Die Wassersynthese-Experimente kosteten ihn rund 50.000 Livres, wobei 1 Livre rund 200 Franc Wert war.
- Als Mitglied der Akademie verdiente er jährlich 2000 bis 5000 Livre, aus der Pulververwaltung erhielt er 17.000 Livre, aus der Generalpacht 145.000 Livre, also rund 29 Millionen Franc.
- Charles Coulston Gillispie: Science and Polity in France. Princeton UP, 2004, S. 322.
- Georg Korn: Joseph-Ignace Guillotin (1738–1814). Ein Beitrag zur Geschichte der Medicin und des ärztlichen Standes. 1891, S. 23.
- Szabadvary: Lavoisier. S. 66. Mit Abdruck des in der Nacht vor dem Urteil verfassten Abschiedsbriefs.
- Gillespie: Science and Polity in France. S. 323.
- Grimaux: Lavoisier. 1895, S. 376.
- Henri Guerlac: Artikel Lavoisier. In: Dictionary of Scientific Biography. Band 8, S. 85. Dort wird auf J. Guillaume Un mot légéndaire: La république n’a pas besoin de savants, Révolution francais, Band 38, 1900, S. 385–399 und Études revolutionnaires, Reihe 1, Paris 1908, S. 136–155 verwiesen.
- Grimoux: Lavoisier. 1895, Appendix VIII, S. 376 ff.
- Lagrange, zitiert von Jean Baptiste Joseph Delambre: Notices sur la vie et les ouvrages de M. Le Comte J.-L. Lagrange. In: Delambre (Hrsg.): Oeuvres de Lagrange. Band 1, Gauthier-Villars 1867, S. XL. Danach äußerte er dies am Tag nach der Hinrichtung gegenüber Delambre.
- McKee: Lavoisier. 1935, S. 299.
- Grimaux: Lavoisier. S. 334. In der Korrespondenz von Madame Lavoisier gibt es keinen Brief von Hassenfratz, Fourcroy oder Mourveau, mit denen sie den Kontakt abbrach da sie sich nicht für ihren Mann eingesetzt hatten. Da zum Beispiel Fourcroy auch auf der Trauerfeier 1795 sprach blieb sie fern.
- Madison Smartt Bell: Lavoisier in the Year One. Atlas Books, Norton, 2005, S. 182.
- Die Szene mit Robespierre wird auch in Arthur Donavan, Antoine Lavoisier: Science, Administration and Revolution, S. 295 f., erwähnt. Georges Cuvier schrieb in seinen Memoiren, dass Fourcroy zu dieser Zeit selbst in Gefahr war und seine Handlungsmöglichkeiten eingeschränkt und die Szene mit Robespierre ist einer Notiz zu Fourcroy von Cuvier enthalten (Fonds Cuvier), die sich auf das Zeugnis von dessen Cousin André Laugier beruft, nach Gillespie: Science and Polity in France: The End of the Old Regime, Princeton UP 2004, S. 324 f., Fourcroy setzte sich durchaus für bedrohte Wissenschaftler ein, so rettete er den wegen Verbindungen zum Herzog von Orléans denunzierten Jean d’Arcet (Darcet) vor dem Terror. Grimaux: Lavoisier. S. 311.
- Grimaux: Lavoisier. S. 310.
- Gillispie: Science and Polity in France. 2004, S. 324.
- P. Lemay: La pompe funèbre de Lavoisier au lycée des Arts. In: Revue d’Histoire de la Pharmacie. 1958, S. 230–236, Digitalisat.
- Charles Gillispie: Notice biographique de Lavoisier par Madame Lavoisier. Revue d’histoire des sciences, Band 9, 1956, S. 52–61, hier S. 61, Digitalisat.
- Marco Beretta: Artikel Lavoisier. In: New Dictionary of Scientific Biography. Band 4, 2008, S. 217.
- Szabadvary: Lavoisier. S. 25.
- Henry Guerlac: Lavoisier: The Crucial Year. The background and Origin of his first experiments on combustion in 1772. Ithaka, New York 1961. Guerlac: Artikel Lavoisier. In: Dictionary Scientific Biography. Band 8, S. 72.
- Marco Beretta: Lavoisier as a reader of chemical literature. In: Revue d’histoire des sciences. Band 48, Nr. 48-1-2, 1995, S. 71–94, doi:10.3406/rhs.1995.1222.
- Szabadvary: Lavoisier. S. 32.
- Marco Beretta: Artikel Lavoisier. In: New Dictionary of Scientific Biography. Band 4, 2008, S. 214.
- Auch das war schon vorher beobachtet worden, wie Lavoisier selbst anmerkte, in diesem Fall der Pariser Pharmazeut Pierre Mitouard, was Lavoisier bekannt war, und Andreas Sigismund Marggraf.
- Lavoisier: Détails historique sur la cause de augmentation de poids. Oeuvres, Band 2, Paris 1862, S. 103.
- Kirwan: Essay on Phlogiston. London 177, S. 7, (archive.org).
- McKie: Lavoisier. 1935, S. 220.
- Die Idee dazu hatte 1787 sein Mitarbeiter Adet (man war über die Rezeption der Nomenclature chimique in Frankreich enttäuscht) und um die Druckerlaubnis schnell zu erhalten gab man vor eine Übersetzung der Annalen der Chemie von Lorenz von Crell herausbringen zu wollen. Lavoisier war anfangs nicht direkt beteiligt, spielte aber bald eine führende Rolle in der Zeitschrift ebenso wie seine Kollegen Berthollet und Morveau. Die erste Ausgabe erschien 1789. Beccara: Artikel Lavoisier. In: New Dictionary of Scientific Biography. Band 4, 2008, S. 216.
- Szabadvary: Lavoisier. S. 44. Nach Grimaux: Lavoisier. S. 310 antwortete Lavoisier in diesem Sinn auf eine Äußerung von Fourcroy über den Sieg der französischen Chemiker.
- Jan V. Golinski: The nicety of experiment: Precision of measurement and precision of reasoning in late eighteenth-century chemistry. In: M. Norton Wise (Hrsg.): The Values of Precision. Princeton UP 1995, S. 75 f.
- Lorenz von Crell veröffentlichte einen Brief darüberin den Chemischen Annalen, Band 1, 1789, S. 519. Zitiert in Karl Hufbauer: The Formation of the German Chemical Community (1720–1795). University of California Press, 1982, S. 96.
- Justus von Liebig: Chemische Briefe. Band 1, Wintersche Verlagshandlung, Leipzig, Heidelberg, 4. Auflage, 1859, S. 46 f. (Dritter Brief, zuerst 1844). Vorher betonte Liebig, dass die Chemie zu den ältesten Wissenschaften gehörte entgegen dem Eindruck vieler seiner Zeitgenossen, sie wäre eine junge Wissenschaft.
- Liste der Substanzen von Lavoisier und Kollegen in der Nomenclature chimique, nach einer englischen Übersetzung herausgegeben von Lyman Spalding in Hanover, New Hampshire 1799.
- Auflistung der einfachen Substanzen im Traité 1789 in der Internet Database of Periodic Tables.
- Nach der Bezeichnung von Linné waren das die drei Reiche Mineralien, Pflanzen und Tiere.
- Henry Guerlac: Artikel Lavoisier. In: Dictionary of Scientific Biography. Band 8, S. 82. Nach einer Notiz von Lavoisier von 1792.
- Guerlac: Dict. Sci. Biogr. Band 8, S. 82.
- Die Liste der Elemente ist zum Beispiel in Lavoisier: Traité. Band 1, 1793, S. 192.
- Lavoisier: Traité. Band 1, 1793, S. 172 ff.
- Lavoisier: Traité de la chimie. Band 1, 1789, S. XVII. Original: Tout ce qu’on peut dire sur le nombre & sur la nature des élémens se borne suivant moi à des discussions purement métaphysiques : ce sont des problèmes indéterminés qu’on se propose de résoudre, qui sont susceptibles d’une infinité de solutions, mais dont il est très-probable qu’aucune en particulier n’est d’accord avec la nature. Je me contenterai donc de dire que si par le nom d’élémens, nous entendons désigner les molécules simples & indivisibles qui composent les corps, il est probable que nous ne les connoissons pas : que si au contraire nous attachons au nom d’élémens ou de principes des corps l’idée du dernier terme auquel parvient l’analyse, toutes les substances que nous n’avons encore pu décomposer par aucun moyen, sont pour nous des élémens ; non pas que nous puissions assurer que ces corps que nous regardons comme simples, ne soient pas eux-mêmes composés de deux ou même d’un plus grand nombre de principes, mais puisque ces principes ne se séparent jamais, ou plutôt puisque nous n’avons aucun moyen de les séparer, ils agissent à notre égard à la manière des corps simples, & nous ne devons les supposer composés qu’au moment où l’expérience & l’observation nous en auront fourni la preuve.
- Michaela Hörmann: Der Ausbau der Chemie-Terminologie in Frankreich im 18. Jahrhundert. Hamburg 1997 (Diplomarbeit Berlin 1995). S. 41.
- Szabadvary: Lavoisier. S. 36.
- Martin Carrier: Cavendishs Version der Phlogistonchemie oder: Über den empirischen Erfolg unzutreffender theoretischer Ansätze. In: J. Mittelstraß: Chemie und Geisteswissenschaften. Akademie Verlag, Berlin 1992, S. 35–52, Online.
- Beccara: Artikel Lavoisier. In: New Dictionary of Scientific Biography. Band 4, 2008, S. 215.
- Claude Viel: Le salon et le laboratoire de Lavoisier à l’Arsenal, cénacle où s’élabora la nouvelle chimie. In: Revue d’histoire de la pharmacie. Band 83, Nr. 306, 1995, S. 259, doi:10.3406/pharm.1995.4478 (französisch, freier Volltext).
- Guerlac: Lavoisier. In: Dict. Sci. Biogr. S. 82, Fussnote 41.
- Christoph Girtanner: Anfangsgründe der antiphlogistischen Chemie. 3. Auflage. J. F. Unger, Berlin 1801, S. 606, urn:nbn:de:bvb:12-bsb10072661-1.
- Lavoisier: Traité de la chimie. Paris 1801, S. 140 f. Car rien ne se crée, ni dans les opérations de l’art, ni dans celles de la nature, et l’on peut poser en principes que dans touts opération, il y a une égale quantité de matière avant et après l’opération.
- Biot, zitiert nach Jan Golinski: The nicety of experiment: Precision of measurement and precision of reasoning in late eighteenth-century chemistry. In: M. Norton Wise (Hrsg.): The Values of Precision. Princeton UP 1995, S. 75.
- Szabadvary: Lavoisier. Teubner, S. 22.
- Lavoisier: Traité de la chimie. Band 1, 1802, S. 141.
- Zitiert nach Guerlac: Dict. Sci. Biogr. Band 8, S. 83.
- David Fenby: Heat, its measurement from Galileo to Lavoisier. In: Pure & Applied Chemistry. Band 59, 1987, doi:10.1351/pac198759010091, S. 91–100.
- Robert Morris: Lavoisier and the Caloric Theory. In: British Journal for the History of Science. Band 6, 1972, S. 31. Er bezieht sich auf eine Stelle in Lavoisiers Sur la phlogistique von 1783.
- Lavoisier: Traité. Band 1, 1801, S. 5–6.
- Laplace, Lavoisier: Abhandlung über die Wärme. Ostwalds Klassiker, S. 6 f.
- Beretta: Lavoisier. In: New Dictionary of Scientific Biography. Band 4, 2008, S. 215 f.
- Laplace, Lavoisier: Abhandlung über die Wärme. Ostwalds Klassiker, S. 39. Die Stelle stammt wahrscheinlich von Laplace. Nach Morris, British J. History Science, Band 6, 1972, S. 31, gibt es aber viele Hinweise, dass Lavoisier zu dieser Zeit zunehmend auch mit Molekülmodellen und Kräften zwischen diesen argumentierte.
- Marco Beretta: Artikel Lavoisier. In: New Dictionary of Scientific Biography. Band 4, 2008, S. 217.
- Es gibt ein Manuskriptfragment von 1768 mit der Skizze einer atomistischen Struktur der Materie, was er aber erst wieder in den nachgelassenen Mémoires von 1793 aufgriff.
- Eva Königsmann: Antoine Lavoisier im Ehrensaal des Deutschen Museums. In: Welt.de. 13. September 2003, abgerufen am 24. Dezember 2014.
- Das Chemielabor aus dem 18. Jahrhundert genannt „Lavoisier-Labor“. Abgerufen am 24. Dezember 2014.
- Richard Zare: Oxygen – Chemie im Theater.
- Lotte Burkhardt: Verzeichnis eponymischer Pflanzennamen. Eine Sammlung eponymischer, biografischer und bibliografischer Angaben zu Ehrungen in der Pflanzenwelt. Erweiterte Edition. In: BGBM.org. Botanischer Garten und Botanisches Museum Berlin, Freie Universität Berlin, Berlin 2018.
- Für dieses Werk erhielt Guerlac 1958 den Pfizer Award von der von George Sarton und Lawrence Joseph Henderson gegründeten History of Science Society (HSS).