Methylamin
Methylamin (nach IUPAC-Nomenklatur: Methanamin, oft auch als Aminomethan bezeichnet) ist eine organisch-chemische Verbindung aus der Stoffgruppe der primären aliphatischen Amine. Es kommt als 40%ige wässrige Lösung und als druckverflüssigtes Gas in den Handel.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
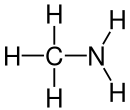 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Methylamin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | CH5N | |||||||||||||||||||||
| Kurzbeschreibung |
farbloses Gas mit ammoniakartigem Geruch[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 31,06 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
gasförmig[1] | |||||||||||||||||||||
| Dichte | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
−6,3 °C[1] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| pKS-Wert |
10,657[2] | |||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK | ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||||||||
| ΔHf0 |
−22,5 kJ·mol−1[6] | |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Geschichte
Der deutsche Chemiker Heinrich Debus synthetisierte 1863 Methylamin durch katalytische Hydrierung von Cyanwasserstoff an Platin.[7]
Vorkommen
Methylamin kommt in Bingelkräutern (Mercurialis), im ätherischen Öl der Blätter der Wasserminze, in einigen Algen sowie im Knochenöl und in Holzdestillaten vor. Es ist ein biogenes Amin und wurde beim Mensch und Tier in kleineren Mengen im Urin nachgewiesen. Außerdem geht man davon aus, dass es Bestandteil der Uratmosphäre war. Daher kann man Spuren von Methylamin auch im All finden.[3]
Gewinnung und Darstellung
Zur großtechnischen Synthese von Methylamin setzt man Methanol mit Ammoniak bei Temperaturen von 350–450 °C und Drücken von 15–25 bar in Gegenwart von Aluminiumoxid (-silicat oder -phosphat) in Rohrreaktoren um.[8][9]
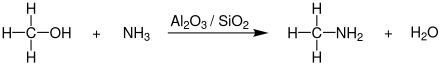
Als Nebenprodukte werden neben Wasser auch noch Dimethylamin und Trimethylamin gebildet, die durch mehrstufige Druck- sowie Extraktivdestillation abgetrennt werden müssen. Das Gewichtsverhältnis von Mono-, Di- und Trimethylamin bei dieser Reaktion beträgt durchschnittlich ca. 20:20:60.[8]
Die Produktionskapazität für Methylamine betrug 1996 weltweit ungefähr 830.000 Jahrestonnen.[9]
Im Labor kann Methylamin in kleineren Mengen durch Umsetzung von Formaldehyd mit Ammoniumchlorid gewonnen werden, wobei man zuerst Methylammoniumchlorid erhält.[10] Das farblose Salz kann hiernach durch eine starke Base, wie z. B. Natriumhydroxid, in das Methylamin überführt werden:
Eigenschaften
Physikalische Eigenschaften
Methylamin hat eine relative Gasdichte von 1,1 (Dichteverhältnis zu trockener Luft bei gleicher Temperatur und gleichem Druck) und eine Gasdichte unter Normbedingungen (0 °C und 1013 mbar) von 1,4301 kg·m−3. Die Dichte der flüssigen Phase am Siedepunkt beträgt 0,6942 kg·l−1, die Gasdichte bei 15 °C ist mit 1,3283 kg·m−3 angegeben. Des Weiteren weist Monomethylamin einen Dampfdruck von 3,00 bar bei 20 °C, 4,20 bar bei 30 °C und 7,8 bar bei 50 °C auf.[1] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend:
im Temperaturbereich von 190 K bis 267 K.[11] Die kritische Temperatur liegt bei 156,9 °C, der kritische Druck bei 74,1 bar und die kritische Dichte bei 0,216 g·cm−3.[1]
Chemische Eigenschaften
Methylamin ist ein extrem leicht entzündbares Gas aus der Stoffgruppe der primären Amine. Methylamin-Luft-Gemische sind deshalb explosiv.[1][3]
Die wässrigen Lösungen reagieren stark alkalisch. Bei 20 °C lösen sich 1080 g·l−1 in Wasser. Eine wässrige Lösung von Methylamin bei 20 °C und einer Konzentration von 100 g·l−1 weist einen pH-Wert von 14 auf. Mit Säuren reagiert es zu kristallisierenden, wasserlöslichen Methylammonium-Salzen.
Verwendung
Methylamin ist ein wichtiges Zwischenprodukt der chemischen und weiterverarbeitenden Industrie. Es wird zur Synthese von Pharmazeutika (z. B. Desoxyn, Theophyllin) und Pestiziden (z. B. Carbaryl, Metam-Natrium, Carbofuran) eingesetzt. Ein großer Teil wird auch zu N-Methyl-2-pyrrolidon (NMP), einem bedeutenden organischen Lösungsmittel weiterverarbeitet. Außerdem ist es Ausgangsstoff für Guanidine, Amide, Imine, Aminoalkohole, Diamine, modifizierte Aminosäuren und α-Aminophosphonate. Des Weiteren dient es zur Synthese von Metallkomplexen und zur Modifikation von Polymeren. Außerdem wird Methylamin auch zu N,N′-Dimethylharnstoff umgesetzt, welcher wiederum zur Synthese von Coffein, Arzneistoffen oder Herbiziden eingesetzt wird. In der organischen Synthese wird Monomethylamin auch zur Einführung einer Methylamino-Gruppe in andere Moleküle eingesetzt.[3]
Sicherheitshinweise
Gasförmiges Monomethylamin wird hauptsächlich über den Atemtrakt aufgenommen. Bei Kontakt mit wässrigen Lösungen kann es auch zu einer Hautresorption kommen. Bei Aufnahme oder Inhalation kann es zu starken Reizungen der Schleimhäute, insbesondere im Atemtrakt und den Augen, kommen. Diese können schnell zu Verätzungen führen. Durch unterkühltes, flüssiges MMA kann es ebenfalls zu Vereisungen und Verätzungen der Haut kommen. Bei längerer Exposition zeigte sich zudem eine Störung des Allgemeinbefindens. Außerdem bildet Methylamin mit Luft explosive Gemische. Bei hoher Konzentration besteht Erstickungsgefahr. Der Stoff wird zudem als gewässergefährdend eingestuft. Methylamin weist eine untere Explosionsgrenze von 4,99 Vol.-% bei 60 g·cm−3 und eine obere Explosionsgrenze von 20,7 Vol.-% bei 270 g·cm−3 auf. Die Zündtemperatur beträgt 430 °C. Der Stoff fällt somit in die Temperaturklasse T2 und in die Explosionsklasse IIA. Mit einem Flammpunkt von −30 °C gilt Methylamin als extrem leicht entflammbar. Der Flammpunkt einer 40%igen wässrigen Lösung beträgt −18 °C[1]
Einzelnachweise
- Eintrag zu Methylamin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 71. Auflage. (Internet-Version: ), CRC Press/Taylor and Francis, Boca Raton, FL, Dissociation Constants of Organic Bases in Aqueous Solutions, S. 8-33.
- Eintrag zu Methylamin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 2. Februar 2019.
- Eintrag zu Methylamine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 2. Februar 2019. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 74-89-5 bzw. Methylamin), abgerufen am 14. September 2019.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-20.
- Heinrich Debus: Ueber die Darstellung des Methylamins aus Blausäure und Wasserstoff. In: Liebigs Annalen der Chemie. Band 128, 1863, S. 200 (hathitrust.org [abgerufen am 20. März 2019]).
- Patent EP1931466B1: Formkörper enthaltend ein Alumosilikat und Aluminiumoxid und Verfahren zur kontinuierlichen Herstellung von Methylaminen. Veröffentlicht am 14. November 2012, Anmelder: BASF SE, Erfinder: Marco Bosch, Roderich Röttger, Jan Eberhardt, Thomas Krug, Theodor Weber, Karl-Heinz Ross, Manfred Julius.
- Hans-Jürgen Arpe: Industrielle Organische Chemie - Bedeutende Vor- und Zwischenprodukte. 6. Auflage. WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim 2007, ISBN 978-3-527-31540-6, S. 55.
- C. S. Marvel, R. L. Jenkins: Methylamine Hydrochloride In: Organic Syntheses. 3, 1923, S. 67, doi:10.15227/orgsyn.003.0067; Coll. Vol. 1, 1941, S. 347 (PDF).
- J. G. Aston, C. W. Stiller, G. H. Messerly: Heat capacities and entropies of organic compounds. III. Methylamine from 12K to the boiling point. Heat of vaporization and vapor pressure. The entropy from molecular data. In: Journal of the American Chemical Society. Band 59, Nr. 9, 1937, S. 1743–1751, doi:10.1021/ja01288a054 (englisch).



