Archaeen
Die Archaeen (Archaea, Singular: Archaeon; von altgriech. ἀρχαῖος archaĩos ‚uralt‘, ‚ursprünglich‘),[1] früher auch Archaebakterien, Archebakterien oder Urbakterien genannt, bilden eine der drei Domänen, in die alle zellulären Lebewesen eingeteilt werden. Die anderen beiden Domänen sind die Bakterien (Bacteria), die mit den Archaeen zu den Prokaryoten zusammengefasst werden, und die Eukaryoten (Eukaryota), die im Unterschied zu den Prokaryoten einen Zellkern besitzen.
| Archaeen | ||||
|---|---|---|---|---|
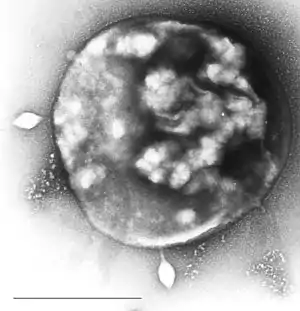
Archaeon der Spezies Sulfolobus | ||||
| Systematik | ||||
| ||||
| Wissenschaftlicher Name | ||||
| Archaea | ||||
| Otto Kandler & Mark L. Wheelis | ||||
| Überstämme | ||||
Beschreibung
Archaea sind einzellige Organismen, die nicht wie eukaryotische Zellen einen Zellkern mit Kernmembran haben, sondern – wie auch die Bacteria – in sich geschlossene DNA-Moleküle (zirkuläre Chromosomen[2]), die im Zellplasma als Kernäquivalent ohne Hülle vorliegen. Archaeen und Bakterien werden daher auch Prokaryoten genannt.
Die separate Stellung der Archaeen als eine eigenständige Domäne ist begründet durch eine Reihe genetischer, physiologischer, struktureller und biochemischer Merkmale, insbesondere deutliche Unterschiede in der Sequenz der in den Ribosomen enthaltenen RNA (der kleinen ribosomalen Untereinheit, 16S rRNA).
Ende der 1970er Jahre wurde von den US-amerikanischen Mikrobiologen Carl Woese und George Fox die Eigenständigkeit der Archaeen und ihre Zugehörigkeit zu einer eigenen systematischen Einheit neben den Bakterien (Eubakterien) und Eukaryoten erkannt und beschrieben. In der Sequenz der ribosomalen RNA entdeckten die Forscher auffällige Unterschiede zu Bakterien. Auch die Struktur der Zellen und deren Eigenheiten im Stoffwechsel ließen auf eine separate Gruppe von Prokaryoten schließen. Diese Ergebnisse wurden in den folgenden Jahren bestätigt, und weitreichende Fortschritte in der molekularen Biologie machten eine generelle Änderung der Taxonomie notwendig: Eubakterien wurden in Bacteria umbenannt und Archaebakterien in Archaea. Beide wurden 1990 im Rahmen eines Drei-Domänen-Systems als zwei eigenständige Domänen neben der Domäne der Eukarya beschrieben. Dabei stehen die Archaea den Eukarya phylogenetisch vermutlich näher als die Bacteria. Zwar lassen sich in Archaeen keine Zellorganellen finden, doch können sie zur Stabilisierung ihrer Form besondere, einem Cytoskelett vergleichbare Filamente ausbilden.[3][4]
Viele kultivierte Arten der Archaeen sind an extreme Milieubedingungen angepasst. So gibt es Arten, die bevorzugt bei Temperaturen von über 80 °C wachsen (hyper-thermophil), andere leben in hoch konzentrierten Salzlösungen (halophil) oder in stark saurem Milieu (pH-Wert zuweilen sogar unterhalb 0; acidophil) bzw. stark basischem Milieu (pH-Wert oberhalb von 10; alkaliphil). Thermoplasmatales der Gattung Picrophilus (P. oshimae und P. torridus) haben ein Wachstumsoptimum bei einem pH-Wert von 0,7 und können sogar bei einem pH-Wert von −0,6 noch überleben.
Archaeen sind in der Forschung von Interesse, da in ihnen vielleicht Merkmale des frühen Lebens auf der Erde erhalten blieben. Aber auch ihr außergewöhnlicher Stoffwechsel ist von Interesse, zum Beispiel die Fähigkeit, bei 110 °C zu wachsen. Auch im Hinblick auf Anwendungen ist der ungewöhnliche Stoffwechsel interessant; beispielsweise werden Archaeen bei der Boden- und Gewässersanierung eingesetzt oder zur Methangewinnung in Biogasanlagen.
Bislang sind keine Krankheitserreger aus der Gruppe der Archaeen bekannt.
Eigenschaften
In vielen molekularbiologischen Eigenschaften sind die Archaeen den Eukaryoten ähnlicher als den Bakterien. Dennoch besitzen sie typisch bakterielle Eigenschaften, z. B. die Zellgröße, das Fehlen eines Zellkerns, die Art der Zellteilung, sie besitzen ein in sich geschlossenes DNA-Molekül, ebenfalls verhältnismäßig einfach aufgebaute Fortbewegungsorgane (Flagellen) und - wie die Bakterien - Ribosomen mit dem Sedimentationskoeffizienten 70S (allerdings sind die archaeellen Ribosomen komplexer in ihrer Struktur). Die Gene beider Domänen sind in sogenannten Operons organisiert. Archaeen können auch Plasmide tragen, wie beispielsweise ein Archaeon (mit der vorläufigen Bezeichnung Sulfolobus NOB8H2) der Familie Sulfolobaceae [en] im Phylum Crenarchaeota.[5]
Die zentralen molekularen Prozesse, zum Beispiel Translation und Transkription, sind dagegen denjenigen der Eukaryoten recht ähnlich: Archaeen benutzen ähnliche, aus mehreren Proteinuntereinheiten zusammengesetzte RNA-Polymerasen (Rifampicin- und Streptolydigin-resistent), bei der Translation kommen sehr ähnliche Initiations- und Elongationsfaktoren vor, der Beginn der Transkription wird durch eine sogenannte TATA-Box markiert.
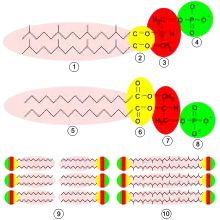
Die Archaeen besitzen jedoch auch viele einzigartige Eigenschaften, besonders der Aufbau der Zellwand zeigt deutliche Unterschiede zu den anderen Domänen: Die archaeellen Zellwände enthalten Pseudopeptidoglycan (Pseudomurein) und sind generell sehr vielfältig in ihrem Aufbau: Manchen Archaeen fehlt eine Zellwand völlig (Thermoplasma), andere besitzen hochkomplexe, aus vielen Schichten bestehende Zellwände (Methanospirillum). Aufgrund des anderen Aufbaus sind Archaeen generell gegen Zellwandantibiotika resistent. Auch die Zusammensetzung der archaeellen Plasmamembran unterscheidet sich: In Bakterien und Eukaryoten sind Fettsäuren über eine Esterbindung an die Glycerolmoleküle gebunden, bei Archaeen findet man Glyceroldiether oder sogar Bis-Glycerol-Tetraether (einschichtige Membran, Monolayer) und verzweigte Isopreneinheiten statt einfacher Fettsäuren. Hyperthermophile Archaeen besitzen häufig derart stabilisierte Zellmembranen (Glycerol-Tetraether),[6] die nicht nur thermostabiler sind, sondern auch Anpassungen an saure Umgebungen darstellen können.[7]
Einige Archaeenarten können sich in Relation zu ihrer Größe sehr schnell fortbewegen. Mit 400 bis 500 „Körperlängen pro Sekunde“ (englisch „bodies per second“, abgekürzt „bps“) sind Methanocaldococcus jannaschii und Methanocaldococcus villosus die schnellsten bislang vermessenen Lebewesen.[8] Zum Vergleich: Ein Sportwagen mit 400 bps käme auf eine Geschwindigkeit von über 6000 km/h. Das Bakterium Escherichia coli bewegt sich dagegen mit rund 20 bps fort, ähnlich schnell wie ein Gepard. Darüber hinaus kommunizieren Archaeen miteinander und koordinieren so ihr Verhalten.[9]
Habitate

Die meisten der bisher bekannten Archaeen sind Extremophile, d. h. den extremen Bedingungen ihrer Biotope angepasst. Viele Vertreter besitzen die Fähigkeit, bei sehr hohen Temperaturen (Hyperthermophile über 80 °C), sehr niedrigen oder sehr hohen pH-Werten (Acidophile bzw. Alkaliphile), hohen Salzkonzentrationen (Halophile) oder hohen Drücken (Barophilie) zu leben.
Hyperthermophile Archaeen findet man häufig in vulkanischen Gebieten, marinen (Schwarzer Raucher) und terrestrischen (Geysire, Solfatarenfelder), so z. B. vulkanisch geprägten Habitaten des Yellowstone-Nationalparks. Halophile gedeihen gut in Umgebungen mit hohem Salzgehalt, so z. B. im Toten Meer oder auch in natürlich vorkommenden marinen Solen.
Auch methanogene Archaeen sind in gewisser Weise „extrem“: Sie wachsen ausschließlich unter anoxischen Bedingungen und benötigen häufig molekularen Wasserstoff für ihren Stoffwechsel. Diese Archaeenarten sind relativ weit verbreitet und kommen in Süßwasser, Meer und Boden vor, aber auch als Symbionten im Darmtrakt von Tieren und Menschen. Archaeen konnten sogar in den Falten des menschlichen Bauchnabels nachgewiesen werden, wobei dies selten ist.[10]
Wegen dieser „Extremophilie“ hat man die ökologische Bedeutung der Archaeen zunächst als relativ gering eingeschätzt. Erst in den letzten Jahren wurde durch Einsatz feinerer molekularbiologischer Nachweismethoden deutlich, dass Archaeen zu großen Anteilen in verhältnismäßig kaltem Meerwasser, aber auch in Böden und Süßwasser-Biotopen vorkommen. In bestimmten ozeanischen Bereichen machen z. B. Crenarchaeota bis zu 90 % der vorhandenen Lebewesen aus. Insgesamt schätzt man, dass in den Ozeanen etwa 1,3 × 1028 Archaeen und 3,1 × 1028 Bakterien vorkommen.
Die Mehrzahl der isolierten und als Reinkultur im Labor verfügbaren Archaeenarten ist allerdings nach wie vor „extremophil“; in einigen Fällen ist eine Kultivierung auch unter weniger extremen Bedingungen gelungen. Aus den bisherigen Untersuchungen geht hervor, dass die Archaeen eine bedeutende Rolle für den Stickstoff-, Kohlenstoff- und Schwefelkreislauf im Ökosystem der Erde spielen.
Stoffwechsel
Die meisten der bisher bekannten Archaeenarten sind autotroph, d. h. sie benötigen zum Wachstum keine organischen Stoffe, sie gewinnen den Kohlenstoff zum Aufbau ihrer Körperbestandteile ausschließlich durch Assimilation von Kohlenstoffdioxid. Aber auch Heterotrophie, die Gewinnung des Kohlenstoffs aus organischen Verbindungen, ist weit verbreitet.
Die Mehrzahl der bisher kultivierten Archaeen zeichnet sich durch einen anaeroben Stoffwechsel aus; für viele anaerobe Archaeen ist Sauerstoff (O2) toxisch.
Eine Besonderheit archaeellen Stoffwechsels ist die Methanogenese, die ausschließlich von Methan produzierenden Archaeen, den sogenannten Methanogenen, vollbracht werden kann. Sie besitzen eine Reihe einzigartiger Cofaktoren, beispielsweise Coenzym F420 oder Methanofuran.
Die meisten hyperthermophilen Archaeen sind Anaerobier; der energiegewinnende Stoffwechsel ist entweder chemoorganotroph oder chemolithotroph (die Energie wird aus chemischen Umsetzungen organischer bzw. anorganischer Verbindungen gewonnen). Schwefelverbindungen spielen hierbei oft eine große Rolle: Während des Stoffwechsels wird der Schwefel reduziert und dabei Energie freigesetzt.
Bekannt ist aber der Schwefelstoffwechsel der extrem thermo- und acidophilen Art Acidianus ambivalens (früher: Desulfurolobus ambivalens), aus der Ordnung Sulfolobales, welche aerob Schwefel oxidieren kann.[11]
Halophile Archaeen sind meist aerob-chemoorganotroph, sie gewinnen ihre Energie aus chemischen Umsetzungen von organischen Verbindungen. Unter anoxischen Bedingungen oder bei Nährstoffmangel sind viele extrem Halophile sogar zur Nutzung von Lichtenergie fähig: Sie besitzen das Protein Bacteriorhodopsin, das Licht absorbiert und den Protonentransfer durch die Cytoplasmamembran katalysiert; der dadurch erzeugte elektrochemische Gradient treibt die ATPase und damit die ATP-Synthese an.
Morphologie
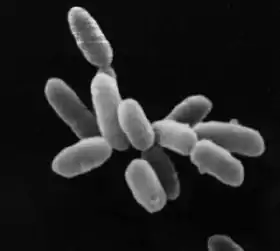
Wie die Bakterien sind auch die Archaeen in ihrer Form äußerst divers. Die Größen bzw. Längen der archaeellen Zellen variieren von etwa 0,4 (Nanoarchaeum equitans) bis zu 100 µm (Methanospirillum hungatei), durchschnittlich sind die Zellen etwa 1 µm groß. Die Zellen zeigen verschiedene Formen, z. B.: Kokken (z. B. Methanococcus jannaschii), Stäbchen (Thermoproteus neutrophilus), Spirillen-förmig (Methanospirillum hungatei), gelappte Kokken (Archaeoglobus fulgidus), Scheiben (Thermodiscus maritimus), lange Filamente (Thermofilum pendens) oder sogar quadratisch (Haloquadratum walsbyi).
Sie besitzen oft Geißeln (Flagellen) zur Fortbewegung, oder auch fadenartige Anhängsel (Pili) zur Anheftung an Oberflächen.
Systematik
Die Platzierung der Archaeen im System der Taxonomie ist nicht ganz unumstritten. Anfangs nur durch Aussehen und Physiologie klassifiziert, wird heute aufgrund neuer Möglichkeiten allgemein die Einteilung mittels phylogenetischer Analyse akzeptiert, wie es Carl Woese (1977, 1990) vorgeschlagen hat.[12][13]
Für die Beschreibung von Genus und Art gibt es eine festgelegte Prozedur.[14] Durch Publikation oder Validierung im International Journal of Systematic and Evolutionary Microbiology (IJSEM)[15] sind Gattung und Art festgelegt. Höhere Taxa können hier auch beschrieben werden. Der aktuelle Stand kann in der List of Prokaryotic names with Standing in Nomenclature (LPSN),[16] gepflegt durch Jean Euzéby, eingesehen werden. Dies entspricht dem internationalen Code der Nomenklatur von Bakterien (ICNB).[17] Taxa, die diesem Standard nicht entsprechen, werden in Anführungszeichen dargestellt.
Darüber hinaus wurde die globale Einteilung innerhalb der Archaeen und Bakterien mittels phylogenetischer Analyse des 16S-rRNS-Gens reformiert.[18] Eine aktuelle Zusammenstellung der Taxa aus dieser und zahlreichen weiterführenden Publikationen erscheint in Bergey's Manual,[19] und in Taxonomic Outline of the Bacteria and Archaea,[20] wobei mittlerweile zusätzlich zum 16S-rRNS-Gen teilweise weitere phylogenetische Markergene hinzugezogen werden. Einige dieser Taxa haben ihre Berechtigung, sind aber bis heute nicht valide publiziert oder werden generell nicht vom ICNB erfasst. Solche Taxa werden in Anführungszeichen dargestellt.
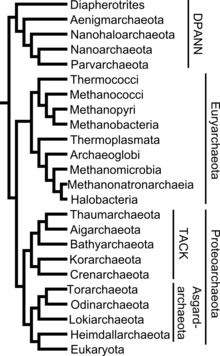
Die hier wiedergegebene Systematik enthält die Taxa von Phylum bis Familie. Bei manchen Taxa gibt es widersprüchliche Einträge. Diese wurden anhand von Originalliteratur und einer phylogenetischen Analyse auf Stichhaltigkeit geprüft.[22][23][24]
Vor einigen Jahren wurde die Beschreibung der zusätzlichen Phyla „Korarchaeota“ und „Nanoarchaeota“ veröffentlicht. Ein Vertreter des vorgeschlagenen Phylums „Nanoarchaeota“ konnte erfolgreich co-kultiviert[25] und sein Genom sequenziert werden,[26] das sogenannte Nanoarchaeum equitans. Vom vorgeschlagenen Phylum „Korarchaeota“, zunächst anhand seiner 16S rRNA-Gen-Basensequenzen in Proben heißer Quellen nachgewiesen,[27] gibt es Anreicherungskulturen. Daraus konnte nun die komplette Basensequenz des Genoms veröffentlicht werden,[28] mit dem informellen Namen „Candidatus Korarchaeum cryptofilum“ versehen. Ohne isolierte Stämme haben die Vertreter dieser Phyla nach den derzeitigen Regeln des ICSB keinen validierten Platz in der Taxonomie,[29] stellen jedoch zwei von vier bekannten Phyla der Archaeen dar.
- Superphylum „Euryarchaeota“ Woese et al. 1990
- Klasse Archaeoglobi
- Klasse Halobacteria
- Klasse Methanobacteria
- Klasse „Methanococci“ Boone 2002
- Klasse „Methanomicrobia“
- Klasse „Methanopyri“ Garrity & Holt 2002
- Klasse Thermococci
- Klasse Thermoplasmata
- Klasse „Eurythermea“ Cavalier-Smith 2002[30]
- Klasse „Neobacteria“ Cavalier-Smith 2002[30]
- Superphylum „DPANN“
- Superphylum „Proteoarchaeota“ Petitjean et al. 2014
- Supergruppe „TACK“ („Filarchaeota“ Cavalier-Smith, T. 2014[31])
- Supergruppe „Asgardarchaeota“ Violette Da Cunha et al. 2017 (Asgard-Gruppe)[32]
Archaeen im Menschen
Archaeen wurden beim Menschen im Darm (Colon), im Mund (Zahnflora), im Bauchnabel[33] und in der Vagina nachgewiesen.[34] Im Darm treten vor allem Archaeen auf, die der Gattung Methanobrevibacter zugehören, im Speziellen Methanobrevibacter smithii. Diese zählen zu den methanogenen Archaea. Nicht bei allen Menschen kommt M. smithii im Darm vor, und bei Säuglingen unter zwei Jahren wurden bisher noch nie Archaeen identifiziert. In einer Studie wurden Archaeen auch auf der Haut nachgewiesen, die zum Phylum Thaumarchaeota gehören.[35] Möglicherweise korreliert die Anzahl jener Archaeen mit der Häufigkeit des Schwitzens.
Methanogene der Arten M. smithii und Methanosphaera stadtmanae leben vergesellschaftet mit syntrophen Bakterien im menschlichen Verdauungstrakt, sodass sie einen Einfluss auf die Verdauung ausüben.[36] Diese nutzen die beiden Produkte bakterieller Gärungen, Wasserstoff und Formiat, für die Methanogenese. Eine hohe Konzentration an Wasserstoff hemmt die ATP-Erzeugung anderer Bakterien. M. smithii baut unter Methanbildung auch Methanol ab, das für den Menschen toxisch ist. Daher haben die Methanogenen einen positiven Einfluss auf die menschliche Darmflora. Ob diese auch beeinflussen, wie viel Energie der Mensch aus der Nahrung aufnehmen kann, ist noch Gegenstand der Forschung.
Obwohl Archaeen in engem Kontakt zum Menschen stehen, gibt es keinen Hinweis auf humanpathogene Arten.[37] Es wurde aber eine Korrelation zwischen Erkrankung und Anzahl von methanogenen Archaeen nachgewiesen: Je mehr Archaeen beispielsweise im (entzündeten) Zahnfleisch vorhanden waren, desto stärker war eine entsprechende Parodontitis ausgeprägt. Hierbei treten insbesondere Archaeen der Art Methanobrevibacter oralis auf. Auch bei Patienten mit Darmkrebs bzw. Divertikulose war die Menge methanogener Archaeen in jenen Bereichen erhöht. Dennoch tragen diese Archaeen nur indirekt zur Erkrankung bei, indem sie das Wachstum echt pathogener Bakterien fördern – die Archaeen selbst sind es nicht. Wenn man Archaeen als „Kopathogene“ oder „Pathobionten“[38] (Symbionten, die unter bestimmten Bedingungen pathologisch werden) betrachtet, dann könnte die Erkrankung mit Medikationen therapiert werden, die diese Archaeen zum Ziel haben. So inhibieren beispielsweise Statine das Wachstum der bei einer Parodontitis vergesellschafteten Methanobrevibacter oralis.[35]
Warum die bekannten Archaeen nicht humanpathogen sind, ist noch nicht eindeutig geklärt. Die Einzigartigkeit vieler Kofaktoren und Vitamine, die im Menschen nicht vorkommen, ist nicht notwendigerweise die Ursache.[39][40] Selbst dass die durch pathogene Prozesse erzeugten Mikrohabitate besetzt werden, ist kein Alleinstellungsmerkmal der Archaeen – prinzipiell könnten auch Organismen mit ähnlichem (anaeroben, hydrogenotrophen) Stoffwechsel diese Habitate nutzen.[38]
Biotechnologisches Potential
Archaeelle Stoffwechselleistungen, Zellbestandteile oder Enzyme werden industriell angewendet. Vor allem die Extremophilen besitzen viele Eigenschaften, die sich biotechnologisch nutzen lassen. Einige Beispiele, die sich bereits in der Entwicklungsphase oder Anwendung befinden:
- Biotechnologie
- Biogas-Gewinnung
- Mikrobielle Erzlaugung („microbial ore leaching“ oder „bioleaching“): Bei diesem Prozess werden niederwertige, sulfidische Erze ausgelaugt (die Sulfidanteile werden mikrobiell zu Sulfat oxidiert und dadurch die Schwermetalle in einen löslichen Zustand überführt); dies wird zum Beispiel zur Gewinnung von Kupfer, Zink und Nickel angewendet.
- Medizin: Verwendung von Zellwandbestandteilen (sogenannte S-Layer) als Träger für Impfstoffe
- Nanotechnologie
- Verwendung der S-Layer für die Ultrafiltration
- Bacteriorhodopsin/ Purpurmembran phototropher halophiler Archaeen als Biosensoren
- Biologie
- Gewinnung hitzeresistenter Enzyme, z. B. α-Amylasen, proteolytische Enzyme, DNA-Polymerasen
- Gewinnung neuer Restriktionsenzyme
Literatur
Archaeen in Standardwerken
- Georg Fuchs (Hrsg.): Allgemeine Mikrobiologie. (begr. von Hans G. Schlegel). 8. Auflage. Georg Thieme Verlag, Stuttgart/ New York 2007, ISBN 978-3-13-444608-1.
- Martin Dworkin, Stanley Falkow, Eugene Rosenberg, Karl-Heinz Schleifer, Erko Stackebrandt (Hrsg.) The Prokaryotes, A Handbook of the Biology of Bacteria. 7 Bände, 3. Auflage. Springer-Verlag, New York u. a., 2006, ISBN 0-387-30740-0.
- Joseph W. Lengeler, Gerhart Drews, Hans G. Schlegel (Hrsg.) Biology of the Prokaryotes. Georg Thieme Verlag, Stuttgart 1999, ISBN 3-13-108411-1.
- H. König: Archaea. In: Encyclopedia of Life Sciences. John Wiley & Sons, 2003, (doi:10.1038/npg.els.0000443)
- Michael T. Madigan, John M. Martinko, Thomas Lazar (Übersetzer) und Freya Thomm-Reitz (Übersetzer): Brock Mikrobiologie. 11., aktualisierte Auflage. Pearson Studium, 2009, ISBN 978-3-8273-7358-8;
Beschreibungen in der wissenschaftlichen Literatur
- C. R. Woese, O. Kandler, M. L. Wheelis: Towards a natural system of organisms: Proposal of the domains Archaea, Bacteria and Eucarya. In: Proc. Natl. Acad. Sci. U.S.A. Band 87(12), 1990, S. 4576–4579. PMID 2112744; PDF (freier Volltextzugriff, engl.)
- B. M. Karner, E. F. DeLong, D. M. Karl: Archaeal dominance in the mesopelagic zone of the Pacific ocean. In: Nature. Band 409(6819), 2001, S. 507–510. PMID 11206545; doi:10.1038/35054051
- R. Cavicchioli: Cold-adapted archaea. In: Nat Rev Microbiol. 4(5), 2006, S. 331–343. PMID 16715049; doi:10.1038/nrmicro1390
- H. Huber, M. J. Hohn, R. Rachel, T. Fuchs, V. C. Wimmer, K. O. Stetter. A new phylum of Archaea represented by a nanosized hyperthermophilic symbiont. In: Nature. Band 417(6884), 2002, S. 63–67. PMID 11986665; doi:10.1038/417063a
- E. Conway de Macario, Alberto J. L. Macario: Methanogenic archaea in health and disease: a novel paradigm of microbial pathogenesis. In: Int J Med Microbiol. 299 (2), 2009, S. 99–108. PMID 18757236; doi:10.1016/j.ijmm.2008.06.011
- R. Cavicchioli: Archaea - timeline of the third domain. In: Nat Rev Microbiol. 9(1), 2011, S. 51–61. PMID 21132019; doi:10.1038/nrmicro2482
- R. E. Valas, P. E. Bourne: The origin of a derived superkingdom: how a gram-positive bacterium crossed the desert to become an archaeon. In: Biology direct. Band 6, 2011, S. 16, ISSN 1745-6150. doi:10.1186/1745-6150-6-16. PMID 21356104. PMC 3056875 (freier Volltext).
- Hans-Peter Horz: Archaeal Lineages within the Human Microbiome: Absent, Rare or Elusive? In: Life (Basel). 5(2), 2015, S. 1333–1345. doi:10.3390/life5021333
Weblinks
- Archaeen wandeln in sauren Böden Ammonium um, Auf Pflanzenforschung.de vom 20. Dezember 2011: Archaeen oxidieren in sauren Böden Ammoniak zu Nitrat
- Nadja Podbregar: Unser Ur-Urahn war ein Archaeon. Auf wissenschaft.de vom 6. Mai 2015
- Josephine Franke: Mikrobiom des Darms ist diverser als gedacht – Archaeen machen 1,2 Prozent der mikrobiellen Darmbesiedelung aus. Auf scinexx.de vom 18. Januar 2022
- Chris Rinke: Behind the Paper: Standardising archaeal taxonomy, Nature Microbiology Community, 21. Juni 2021
Einzelnachweise
- Merriam-Webster Online Dictionary
- A. L. Hartman et al.: The Complete Genome Sequence of Haloferax volcanii DS2, a Model Archaeon In: PLOS ONE. Band 5, Nr. 3, 2010, S. e9605 PMC 2841640 (freier Volltext)
- J. D. Trent et al.: Chaperonin filaments: the archaeal cytoskeleton? In: PNAS. Band 94, Nr. 10, 1997, S. 5383–5388. PMID 9144246; PDF (freier Volltextzugriff, engl.)
- F. Hara et al.: An actin homolog of the archaeon Thermoplasma acidophilum that retains the ancient characteristics of eukaryotic actin. In: J. Bacteriol. Band 189, Nr. 5, 2007, S. 2039–2045. PMID 17189356; PDF (freier Volltextzugriff, engl.)
- C. Schleper et al.: A multicopy plasmid of the extremely thermophilic archaeon „Sulfolobus“ effects its transfer to recipients by mating. In: J. Bacteriol. Band 177, 1995, S. 4417–4426. PMID 7635827.
- A. Pearson et al.: Factors Controlling the Distribution of Archaeal Tetraethers in Terrestrial Hot Springs. In: Appl. Environ. Microbiol. Band 74, 2008, S. 3523–3532, als (PDF)
- E. Boyd et al.: The role of tetraether lipid composition in the adaptation of thermophilic archaea to acidity. In: Front Microbiol. Band 4 (62), April 2013, doi:10.3389/fmicb.2013.00062, PMC 3615187 (freier Volltext).
- Bastian Herzog, Reinhard Wirth: Swimming Behavior of Selected Species of Archaea. In: Applied and Environmental Microbiology. Band 78, Nr. 6, 2012, S. 1670–1674, doi:10.1128/AEM.06723-11
idw-online.de vom 28. Februar 2012: Archaeen sind die schnellsten Lebewesen der Welt – Mikroorganismen glänzen mit Weltrekord. - Guenther Witzany (Hrsg.): Biocommunication of Archaea. Springer, Switzerland 2017, ISBN 978-3-319-65535-2, S. 325.
- Hulcr J, Latimer AM, Henley JB, Rountree NR, Fierer N, et al. (2012) A Jungle in There: Bacteria in Belly Buttons are Highly Diverse, but Predictable. PLoS ONE 7(11): e47712. doi:10.1371/journal.pone.0047712
- T. Urich et al.: The sulphur oxygenase reductase from Acidianus ambivalens is a multimeric protein containing a low-potential mononuclear non-haem iron centre. In: Biochem J. Band 381, Teil 1, 2004, S. 137–146. doi:10.1042/BJ20040003
- C. R. Woese, G. E. Fox: Phylogenetic structure of the prokaryotic domain: the primary kingdoms. In: Proc. Natl. Acad. Sci. U.S.A. Band 74, Heft 11, 1977, S. 5088–5090. PMID 270744
- C. R. Woese et al.: Towards a natural system of organisms: proposal for the domains Archaea, Bacteria, and Eucarya. In: Proc. Natl. Acad. Sci. U.S.A. Band 87, Heft 12, 1990, S. 4576–4579. PMID 2112744
- B. J. Tindall et al.: Valid publication of names of prokaryotes according to the rules of nomenclature: past history and current practice. In: Int J Syst Evol Microbiol. Band 56, Heft 11, 2006, S. 2715–2720. PMID 17082418. doi:10.1099/ijs.0.64780-0.
- International Journal of Systematic and Evolutionary Microbiology. (IJSEM)
- J. P. Euzéby: List of bacterial names with standing in nomenclature: a folder available on the Internet. In: Int. J. Syst. Bacteriol. Band 47, 1997, S. 590–592. PMID 9103655 - List of Prokaryotic names with Standing in Nomenclature (Memento vom 30. Dezember 2010 im Internet Archive) (LPSN)
- S. P. Lapage et al.: International Code of Nomenclature of Bacteria, 1990 Revision. (Bacteriological Code). ASM Press, Washington, D.C. 1992, ISBN 1-55581-039-X.
- C. R. Woese et al.: A phylogenetic definition of the major eubacterial taxa. In: Syst. Appl. Microbiol. Band 6, 1985, S. 143–151. PMID 11542017.
- Bergey's Manual Trust, Department of Microbiology, 527 Biological, Sciences Building, University of Georgia, Athens, GA 30602-2605, USA - Bergey's Manual
- George M. Garrity et al.: Taxonomic Outline of the Bacteria and Archaea. Release 7.7, 6. März 2007, Michigan State University Board of Trustees, www.taxonomicoutline.org
- C. Schleper, G. Jurgens, M. Jonuscheit: Genomic studies of uncultivated archaea. In: Nat Rev Microbiol. 3, Nr. 6, 2005, S. 479–488. doi:10.1038/nrmicro1159. PMID 15931166.
- W. Ludwig et al.: ARB: a software environment for sequence data. In: Nucleic Acids Res. Band 32, 2004, S. 1363–1371.
- E. Pruesse et al.: SILVA: a comprehensive online resource for quality checked and aligned ribosomal RNA sequence data compatible with ARB. In: Nuc. Acids Res. Band 35, Nr. 21, 2007, S. 7188–7196.
- P. Yarza et al.: The All-Species Living Tree Project: a 16S rRNA-based phylogenetic tree of all sequenced type strains. In: Syst. Appl. Microbiol. 2008, doi:10.1016/j.syapm.2008.07.001.
- H. Huber et al.: A new phylum of Archaea represented by a nanosized hyperthermophilic symbiont. In: Nature. 417, 2002, S. 63–67. PMID 11986665.
- E. Waters et al.: The genome of Nanoarchaeum equitans: insights into early archaeal evolution and derived parasitism. In: Proc Natl Acad Sci U.S.A. 100, 2003, S. 12984–12988. PMID 14566062.
- S. M. Barns et al.: Perspectives on archaeal diversity, thermophily and monophyly from environmental rRNA sequences. In: Proc Natl Acad Sci U.S.A. 93, 1996, S. 9188–9193. PMID 8799176.
- J. G. Elkins et al.: A korarchaeal genome reveals insights into the evolution of the Archaea. In: Proc Natl Acad Sci U.S.A. 105, 2008, S. 8102–8107. PMID 18535141.
- P. De Vos, H. G. Trüper: Judicial Commission of the International Committee on Systematic Bacteriology. IXth International (IUMS) Congress of Bacteriology and Applied Microbiology. Minutes of the meetings, 14, 15 and 18 August 1999, Sydney, Australia. In: Int. J. Syst. Evol. Microbiol. Band 50, 2000, S. 2239–2244.
- Taxa above the rank of class. In: List of Prokaryotic names with Standing in Nomenclature. Abgerufen am 8. August 2017 (englisch).
- T. Cavalier-Smith: The neomuran revolution and phagotrophic origin of eukaryotes and cilia in the light of intracellular coevolution and a revised tree of life. In: Cold Spring Harb. Perspect. Biol.. 6, Nr. 9, 2014, S. a016006. doi:10.1101/cshperspect.a016006. PMID 25183828. PMC 4142966 (freier Volltext).
- Paul-Adrian Bulzu, Adrian-Stefan Andrei, Michaela M. Salcher, Maliheh Mehrshad, Keiichi Inoue, Hideki Kandori, Oded Beja, Rohit Ghai, Horia L. Banciu: Casting light on Asgardarchaeota metabolism in a sunlit microoxic niche, in: Nat Microbiol, Band 4, S. 1129–1137, doi:10.1038/s41564-019-0404-y
- Souri Somphanith: Plunging into the Unknown: Belly Button Bacteria and You. In: PLOS Blogs.
- E. Conway de Macario, Alberto J. L Macario: Methanogenic archaea in health and disease: a novel paradigm of microbial pathogenesis. In: Int J Med Microbiol. 299 (2), 2009, S. 99–108. PMID 18757236
- Mor N. Lurie-Weinberger und Uri Gophna: Archaea in and on the Human Body: Health Implications and Future Directions. In: PLOS Pathogens. Band 11, Nr. 6, 11. Juni 2015, S. e1004833, doi:10.1371/journal.ppat.1004833, PMID 26066650 (plos.org [abgerufen am 13. März 2017]).
- Joan L. Slonczewski, John W. Foster: Mikrobiologie: Eine Wissenschaft mit Zukunft. 2. Auflage. Spektrum Akademischer Verlag, Berlin/ Heidelberg 2012, ISBN 978-3-8274-2909-4, S. 854.
- R. Cavicchioli et al.: Pathogenic archaea: do they exist? In: Bioessays. 25(11), 2003, S. 1119–1128. PMID 14579252; doi:10.1002/bies.10354
- Rustam I. Aminov: Role of archaea in human disease. In: Frontiers in Cellular and Infection Microbiology. Band 3, 1. Januar 2013, doi:10.3389/fcimb.2013.00042, PMID 23964350 (frontiersin.org [abgerufen am 13. März 2017]).
- W. Martin: Pathogenic archaebacteria: do they not exist because archaebacteria use different vitamins? In: Bioessays. 26(5), 2004, S. 592–593. PMID 15112239; doi:10.1002/bies.20044.
- R. Cavicchioli, P. Curmi: Response to William Martin's letter. In: Bioessays. 26(5), 2004, S. 593. doi:10.1002/bies.20043.