Summenformel
Eine Summenformel (auch Bruttoformel genannt[1]) dient in der Chemie dazu, die Art und Anzahl der Atome einer chemischen Verbindung anzugeben. Besteht die Verbindung aus diskreten Molekülen, ist die Summenformel eine Molekülformel.[2][3] Für ein Salz wird eine Formeleinheit angegeben, die ihrer stöchiometrischen Zusammensetzung gerecht wird. Eine Summenformel ist oft nicht gleich der Verhältnisformel, die die kleinstmöglichen Zahlenverhältnisse der Atome der beteiligten chemischen Elemente in einer chemischen Verbindung angibt.
| Strukturformeln | andere Darstellungsweisen | ||||||
|---|---|---|---|---|---|---|---|
| Elektronen- formel |
Valenzstrich- formel |
Keilstrich- formel |
Skelett- formel |
Konstitutions- formel |
Summen- formel |
Verhältnis- formel | |
| Wasser | existiert nicht | existiert nicht | H2O | H2O | |||
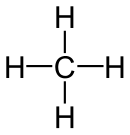
| Methan | 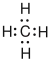 |
 |
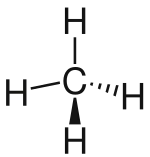 |
existiert nicht | CH4 | CH4 | CH4 |
| Propan | 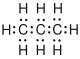 |
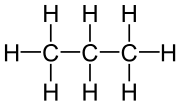 |
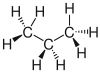 |
CH3–CH2–CH3 | C3H8 | C3H8 | |
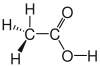
| Essigsäure | 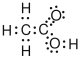 |
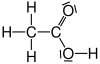 |
 |
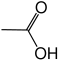 |
CH3–COOH | C2H4O2 | CH2O |
Aufbau
Die Summenformel einer chemischen Verbindung besteht aus den Elementsymbolen der enthaltenen chemischen Elemente und kleinen, tiefgestellten arabischen Ziffern für deren jeweilige Anzahl in dieser Verbindung. Diese Anzahl der Atome steht als Index immer rechts tiefgestellt neben den Elementsymbolen, wobei die Ziffer „1“ nicht ausgeschrieben wird.[4] Statt „H2O1“ für Wasser wird daher „H2O“ geschrieben.
Besteht eine Verbindung aus diskreten Molekülen, gibt eine Summenformel die Zusammensetzung des Moleküls an. Die Summenformel für Dischwefeldichlorid lautet S2Cl2, und für Ethan C2H6. Die Verhältnisformeln lauten SCl bzw. CH3.
Für die Reihenfolge der Elemente in Summenformeln gibt es unterschiedliche Strategien. In Tabellenwerken und Datenbanken wird – insbesondere bei organischen Verbindungen – zumeist das Hill-System bevorzugt. Dieses gibt zuerst alle Kohlenstoffatome, dann die Wasserstoffatome an und sortiert alle anderen Atomsymbole streng alphabetisch. Dieses System erleichtert das Auffinden von Verbindungen bei Unkenntnis über den Namen der Verbindung.
Für anorganische Verbindungen wird häufig ein anderer Weg gewählt, der den stöchiometrischen Zusammensetzungen der Verbindungen gerecht wird: Das Element höherer Elektronegativität (im Periodensystem in der Regel weiter rechts oder oben) steht in der Summenformel wie auch im Namen des Stoffes üblicherweise rechts von einem Element niedrigerer Elektronegativität. Beispielsweise wird Natriumchlorid als „NaCl“ und nicht als „ClNa“ geschrieben. Bei komplexen Salzen wird erst das Kation mit Zentralatom und seinen Liganden und dann das Anion mit Zentralatom und seinen Liganden angegeben, wie (NH4)2SO4 für Ammoniumsulfat. Anorganische Säuren werden analog zu den verwandten Salzen angegeben. Die Wasserstoffatome stehen anstelle der Kationen vorne, wie beim H3PO4, der Summenformel der Phosphorsäure. Diese Formeln stellen die Formeleinheiten für stöchiometrische Berechnungen dar und nicht die Struktur der Verbindungen.
Beispiele und Unterscheidung
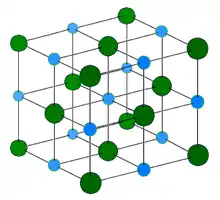
- In Natriumchlorid NaCl ist das Stoffmengenverhältnis von Natrium zu Chlor n(Na) :n(Cl) = 1 : 1. Als Größengleichung geschrieben: n(Na) = n(Cl). Die Summenformel von Natriumchlorid sagt nichts über die Struktur der Verbindung aus (vgl. Abbildung).
- im Aluminiumoxid Al2O3 ist das Stoffmengenverhältnis n(Al) : n(O) = 2 : 3. Als Größengleichung: 3 × n(Al) = 2 × n(O)
- H2O, ein Wasser-Molekül besteht aus zwei Wasserstoff-Atomen (H) und einem Sauerstoff-Atom (O), (Atomzahlenverhältnis 2:1);
- H2SO4, ein Schwefelsäure-Molekül, besteht aus zwei Wasserstoff-Atomen, einem Schwefel-Atom (S) und 4 Sauerstoff-Atomen (Atomzahlenverhältnis 2:1:4).
- im Hexan C6H14 ist das Stoffmengenverhältnis n(C) : n(H) = 6 : 14 = 3 : 7 Die Verhältnisformel des Moleküls wäre daher C3H7. Diese repräsentiert jedoch nicht das Molekül, da sie nicht die realen Atomzahlen angibt und somit teilweise nicht eindeutig ist.
Bei einfachen Verbindungen ist die Molekül-/Summenformel oft gleich der Verhältnisformel, die das kleinstmögliche Zahlenverhältnis angibt.
Zur Bedeutung von Summenformeln
Summenformeln werden auch bei der Formulierung von chemischen Reaktionsgleichungen benutzt. Dabei werden die Ausgangs- und Endstoffe der Reaktion (Edukte und Produkte) im Reaktionsschema in der anorganischen Chemie in der Regel in Form von Summenformeln angegeben. Diese bilden damit die Grundlage für stöchiometrische Berechnungen. In der organischen Chemie werden nur selten Summenformeln verwendet, da sie kaum Informationen enthalten, die für den Ablauf der Reaktionen in der organischen Chemie wichtig sind.
Siehe auch
Einzelnachweise
- Eintrag zu Summenformel. In: Römpp Online. Georg Thieme Verlag, abgerufen am 20. Juni 2014.
- Eintrag zu molecular formula. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.M03987 – Version: 2.3.1.
- Hans-Dieter Jakubke, Ruth Karcher (Hrsg.): Lexikon der Chemie. Spektrum Akademischer Verlag, Heidelberg, 2001.
- Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 433.