Thorium(IV)-oxid
Thorium(IV)-oxid (Thoriumdioxid, ThO2) ist das einzige stabile Oxid des radioaktiven Elements und Actinoids Thorium. In der Natur kommt die Verbindung als Mineral Thorianit vor.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
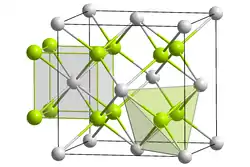 | ||||||||||||||||
| _ Th4+ _ O2− | ||||||||||||||||
| Kristallsystem |
kubisch | |||||||||||||||
| Raumgruppe |
Fm3m (Nr. 225) | |||||||||||||||
| Koordinationszahlen |
Th[8], O[4] | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Thorium(IV)-oxid | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Verhältnisformel | ThO2 | |||||||||||||||
| Kurzbeschreibung |
weißer, kristalliner Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 264,04 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
10 g·cm−3[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
4400 °C[3] | |||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser und Säuren[2] | |||||||||||||||
| Gefahren- und Sicherheitshinweise | ||||||||||||||||

Radioaktiv | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Herstellung
Thorium(IV)-oxid kann durch Oxidation von Thorium und nachfolgende Reinigung (Befreiung von Thoriumresten) hergestellt werden.
Es kann auch durch thermische Zersetzung von Thorium(IV)-hydroxid, Thorium(IV)-oxalat, Thorium(IV)-carbonat oder Thorium(IV)-nitrat hergestellt werden. Thorium(IV)-sulfat ist als Ausgangsmaterial weniger gut geeignet, da die letzten Spuren Sulfat nur sehr schwer abgespalten werden.[7]
Eigenschaften
Thorium(IV)-oxid ist ein geruchloses weißes Pulver. Das Mineral Thorianit kristallisiert kubisch im Fluoritgitter. Es hat den höchsten Schmelzpunkt aller Oxide, weist eine hohe Lichtbrechung und eine hohe Dichte von 9,86 g·cm−3 auf. Die Wasserlöslichkeit von Thoriumdioxid ist sehr gering. Erst im stark sauren pH-Bereich unter pH = 4 steigt die Löslichkeit leicht an. Das enthaltene Thorium ist ein Alphastrahler. Die Aktivität von einem Gramm Thorium(IV)-oxid beträgt 7100 Becquerel.
Anwendungen
Thorium(IV)-oxid dient als Zusatz in optischen Gläsern, um die Lichtbrechung zu erhöhen. Früher war es Bestandteil von Glühstrümpfen. Weiterhin gibt es Wolframelektroden, die zwischen 0,35 % und 4,20 % Thoriumdioxid enthalten, um beim Wolframinertgasschweißen (WIG) den elektrischen Funken zu stabilisieren. Aufgrund der Radioaktivität des Thoriums wird die zivile Anwendung eingeschränkt. Thoriumdioxid wird auch als Brutmaterial in Brutreaktoren genutzt.
Thorium(IV)-oxid kann als Katalysator bei der Decarboxylierung von Carbonsäuren eingesetzt werden.[8]
Gefahren
Thorium(IV)-oxid wirkt reizend auf Haut und Augen. Bei Verletzungen kann es in den Körper gelangen und toxisch wirken, beim Einatmen kann es sich in der Lunge ablagern und diese bestrahlen. Auch beim Verschlucken ist es giftig. Der extrem langlebige Stoff erhöht das Krebsrisiko.[6] Das Röntgenkontrastmittel Thorotrast, das zum Hervorheben von Details in Röntgenbildern bis Ende der 1940er-Jahre diente, wurde aufgrund des Krebsrisikos nach dem Zweiten Weltkrieg nicht mehr eingesetzt.
Einzelnachweise
- Eintrag zu THORIUM DIOXIDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 13. November 2021.
- Eintrag zu Thoriumdioxid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 30. November 2014.
- Thoriumdioxid bei webelements.com.
- Datenblatt Thorium(IV)-oxid bei Sigma-Aldrich, abgerufen am 5. November 2012 (PDF).
- Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung.
- BOC Edwards Sicherheitsdatenblatt (Memento vom 28. September 2007 im Internet Archive).
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 1145.
- J. F. Thorpe and G. A. R. Kon: Cyclopentanone In: Organic Syntheses. 5, 1925, S. 37, doi:10.15227/orgsyn.005.0037; Coll. Vol. 1, 1941, S. 192 (PDF).
Literatur
- Mathias S. Wickleder, Blandine Fourest, Peter K. Dorhout: Thorium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 52–160; doi:10.1007/1-4020-3598-5_3.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1972.

