Uran(III)-chlorid
Uran(III)-chlorid ist eine chemische Verbindung bestehend aus den Elementen Uran und Chlor. Es besitzt die Formel UCl3 und gehört zur Stoffklasse der Chloride. Es ist ein Zwischenprodukt in der Wiederaufarbeitung abgebrannter Kernbrennstoffe.
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
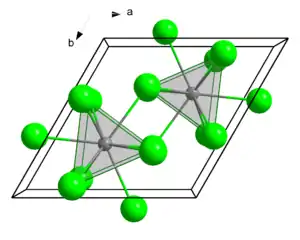 | ||||||||||
| _ U3+ _ Cl− | ||||||||||
| Kristallsystem | ||||||||||
| Raumgruppe |
P63/m (Nr. 176) | |||||||||
| Gitterparameter |
a = 745,2 pm | |||||||||
| Koordinationszahlen |
U[9], Cl[3] | |||||||||
| Allgemeines | ||||||||||
| Name | Uran(III)-chlorid | |||||||||
| Andere Namen |
Urantrichlorid | |||||||||
| Verhältnisformel | UCl3 | |||||||||
| Kurzbeschreibung |
rote Kristalle[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 344,39 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
5,50 g·cm−3[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
1657 °C[3] | |||||||||
| Gefahren- und Sicherheitshinweise | ||||||||||

Radioaktiv | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Darstellung
Es gibt zwei Wege zur Synthese von Uran(III)-chlorid. Zum einen kann es durch die Umsetzung von metallischem Uran in einer Salzschmelze aus Natriumchlorid und Kaliumchlorid bei 670–710 °C erhalten werden.[7]
Eine weitere Möglichkeit durch Erhitzen von Uran(IV)-chlorid unter Wasserstoffatmosphäre.[8]
Eigenschaften
Bei Raumtemperatur ist Uran(III)-chlorid ein roter, sehr hygroskopischer, kristalliner Feststoff, der sehr gut in Wasser löslich ist. UCl3 besitzt eine geringere Stabilität als Uran(IV)-chlorid (UCl4), da die Oxidationsstufe +3 in saurer Lösung stabilisiert wird. In salzsaurer Lösung besitzt UCl3 eine höhere Stabilität als in Wasser.[9] Uran(III)-chlorid schmilzt bei 837 °C und siedet bei 1657 °C, es hat eine Dichte von 5,50 g/cm3.
Drei Hydrate des Uran(III)-chlorids sind bekannt:
- UCl3 · 2 H2O · 2 CH3CN
- UCl3 · 6 H2O
- UCl3 · 7 H2O
Sie werden durch Reduktion von Uran(IV)-chlorid in Acetonitril in Gegenwart von Wasser und Propionsäure hergestellt.[10]
Kristallstruktur
Die Struktur des Uran(III)-chlorids ist die Leitstruktur für eine Reihe weiterer Verbindungen. In dieser werden die Uranatome von je neun Chloratomen umgeben. Als Koordinationspolyeder ergibt sich dabei ein dreifach überkapptes, trigonales Prisma, wie sie auch bei den späteren Actinoiden und den Lanthanoiden häufig anzutreffen ist. Es kristallisiert im hexagonalen Kristallsystem in der Raumgruppe P63/m (Raumgruppen-Nr. 176) mit den Gitterparametern a = 745 pm und c = 433 pm und zwei Formeleinheiten pro Elementarzelle.[11] Weitere Verbindungen, die in einer Uran(III)-chloridstruktur kristallisieren, sind unter anderem Neptunium(III)-chlorid, Plutonium(III)-chlorid, Americium(III)-chlorid, Curium(III)-chlorid und Antimon(III)-chlorid.
Verwendung
Uran(III)-chlorid wird zur Darstellung verschiedener Uranmetallocene verwendet, zum Beispiel in Reaktionen mit Tetrahydrofuran (THF) und Methylcyclopentadienylnatrium.[12] Es kann auch als Katalysator Verwendung finden beispielsweise bei Reaktionen zwischen Lithiumaluminiumhydrid (LiAlH4) und Alkenen, zur Synthese von Alkylaluminiumverbindungen.[13]
Uran(III)-chlorid wird in Salzschmelzen eingesetzt und spielt eine Rolle bei der Wiederaufarbeitung abgebrannter Kernbrennstoffe.[14][15]
Sicherheitshinweise
Ähnlich wie andere lösliche Uranverbindungen wird UCl3 leicht resorbiert.[16] Es ist hochtoxisch beim Einatmen und Verschlucken. Außerdem besteht die Gefahr der Anreicherung im menschlichen Körper, was vor allem die Leber und die Nieren betrifft. Für Wasserorganismen ist es ebenfalls giftig und kann Langzeitschäden in der Wasserwelt verursachen. Wie alle Uranverbindungen ist es radioaktiv. Die Aktivität ist von der Isotopenzusammensetzung des Urans abhängig.
Einzelnachweise
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1969.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Properties of the Elements and Inorganic Compounds, S. 4-97.
- Uran(III)-chlorid bei www.webelements.com.
- Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag uranium compounds with the exception of those specified elsewhere in this Annex im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Uranverbindungen in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung.
- K. Serrano, P. Taxil, O. Dugne, S. Bouvet, E. Puech: „Preparation of Uranium by Electrolysis in Chloride Melt“, in: J. Nucl. Mater., 2000, 282 (2–3), S. 137–145 (doi:10.1016/S0022-3115(00)00423-2).
- Ira Remsen: Inorganic Chemistry, New York: Henry Holt and Company, 1890.
- Arthur Messinger Comey, Dorothy A. Hahn: A Dictionary of Chemical Solubilities: Inorganic. New York: The MacMillan Company, 1921.
- A. Mech, M. Karbowick, T. Lis: „Monomeric, Dimeric and Polymeric Structure of the Uranium Trichloride Hydrates“, in: Polyhedron, 2006, 25 (10), S. 2083–2092 (doi:10.1016/j.poly.2006.01.004).
- Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements: Bd. 3, 2006, Springer, ISBN 1-4020-3555-1.
- J. G. Brenna, R. A. Anderson, A. Zalkin: „Chemistry of Trivalent Uranium Metallocenes: Electron-Transfer Reactions with Carbon Disulfide. Formation of [(RC5H4)3U]2[μ-η1,η2-CS2]“, in: Inorg. Chem., 1986, 25 (11), S. 1756–1760 (doi:10.1021/ic00231a007).
- J. F. Le Marechal, M. Ephritikhine, G. J. Folcher: „Hydroalumination of Olefins by the LiAlH4/UCl4 System“, in: Organomet. Chem., 1986, 309 (1–2), C1–C3 (doi:10.1016/S0022-328X(00)99589-5).
- Y. Okamoto, P. Madden, K. Minato,: „X-Ray Diffraction and Molecular Dynamics Simulation Studies of Molten Uranium Chloride“, in: J. Nucl. Mater., 2005, 344 (1–3), S. 109–114; doi:10.1016/j.jnucmat.2005.04.026.
- Y. Okamoto, F. Kobayashi, T. Ogawa: „Structure and Dynamic Properties of Molten Uranium Trichloride“, in: J. Alloys Compd., 1998, 271–273, S. 355–358 (doi:10.1016/S0925-8388(98)00087-5).
- Rosalie Bertell: „Gulf War Veterans and Depleted Uranium“, May 1999.
Literatur
- Ingmar Grenthe, Janusz Drożdżynński, Takeo Fujino, Edgar C. Buck, Thomas E. Albrecht-Schmitt, Stephen F. Wolf: Uranium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 253–698 (doi:10.1007/1-4020-3598-5_5).


