Hydroxygruppe
Die Hydroxygruppe (ältere, immer noch verwendete Bezeichnung Hydroxylgruppe[1]) –OH ist die funktionelle Gruppe der Alkohole und Phenole und kommt auch in Kohlenhydraten oder bei Hydroxycarbonsäuren als Strukturelement eines Alkohols vor. Die Hydroxygruppe ist aber auch ein Teilelement der Carboxygruppe in Carbonsäuren, dort aber gebunden an das C-Atom einer Carbonylgruppe, das einen höheren Oxidationszustand hat. Die Hydroxygruppe ist deshalb in Carbonsäuren kein Strukturelement eines Alkohols, sondern hat die sauren Eigenschaften einer Carbonsäure.

Die Hydroxygruppe ist weder identisch mit dem negativ geladenen OH-Ion (−OH, siehe Hydroxid-Ion) noch mit dem neutralen OH-Radikal (·OH, kurz Hydroxyl genannt, siehe Hydroxyl-Radikal).
Alkohole
Eine alkoholische Hydroxygruppe verleiht dem Molekül polare Eigenschaften. So können sich zum Beispiel zwischen Ethanolmolekülen Wasserstoffbrücken ausbilden. Dadurch kommt es zu einer Anziehung und Vernetzung benachbarter Alkoholmoleküle, was beispielsweise den flüssigen Aggregatzustand des Ethanols bedingt. Allerdings kann eine Hydroxygruppe auch zur Senkung des Siede- und Schmelzpunktes beitragen, wenn die Hydroxygruppe mit anderen polaren Gruppen innerhalb eines Moleküls (intramolekular) eine Wasserstoffbrückenbindung eingehen kann. Damit wird die Polarität des Moleküls nach außen (intermolekular) geschwächt. So liegt beispielsweise der Siedepunkt von Rizinolsäure deutlich unterhalb des Siedepunktes der Ölsäure.
Phenole
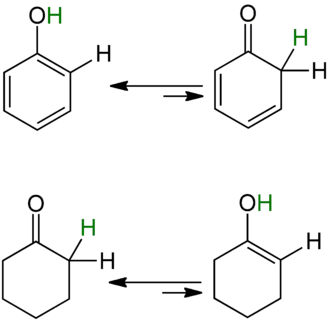
Phenolische Hydroxygruppen haben im Vergleich zu alkoholischen stärker saure Eigenschaften, da das bei der Deprotonierung entstehende Phenolat-Anion mesomeriestabilisiert ist. Der +M-Effekt überwiegt den −I-Effekt. Das gilt zwar auch für aliphatische Enole, doch bei diesen liegt bei der Keto-Enol-Tautomerie im Gegensatz zu den Phenolen fast ausschließlich das Keton vor, weil es energetisch begünstigt ist. Bei den Phenolen ist es aber wegen der Ausbildung des aromatischen Systems genau umgekehrt (vgl. Hückel-Regel).
Literatur
- Phillip Fresenius, Klaus Görlitzer: Organisch-Chemische Nomenklatur, 3. Auflage Wissenschaftliche Verlagsgesellschaft Stuttgart 1991, ISBN 3-8047-1167-7.
- Peter Sykes: Reaktionsmechanismen – eine Einführung, 8. Auflage VCH Weinheim 1982 ISBN 3-527-21090-3.
- Organikum, 16. Auflage, VEB Deutscher Verlag der Wissenschaften Berlin 1985, ISBN 3-326-00076-6.
Weblinks
Einzelnachweise
- Eintrag zu Hydroxy-Gruppe. In: Römpp Online. Georg Thieme Verlag, abgerufen am 28. August 2019.