Sekundär (Chemie)
Das Adjektiv sekundär (abgekürzt sek.; von lat. secundarius) bedeutet „an zweiter Stelle“ und wird in der Chemie auch als Wortbildungselement benutzt, z. B. in Sekundärprodukt und Sekundärmetabolit. Die Kurzform sec- wird als Deskriptor in halbsystematischen Substanznamen verwendet, beispielsweise bei sec-Butanol.
Organische Chemie
| Rot markierte Zentralatome in verschiedenen Stoffgruppen. Vergleich von sekundären mit primären, tertiären und quartären Zentralatomen. | ||||
| primär | sekundär | tertiär | quartär | |
| Kohlenstoffatom einer organischen Verbindung |
 |
 |
 |
 |
| Alkohol |  |
 |
 |
existiert nicht |
| Amin |  |
 |
 |
 (siehe QAV) |
| Carbonsäureamid[1] |  |
 |
 |
existiert nicht |
| Phosphin |  |
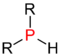 |
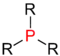 |
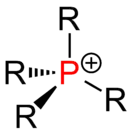 (siehe QPV) |
In der organischen Chemie ist das Wort „sekundär“ eine Bezeichnung für den Substitutionsgrad zweier von mehreren an ein Zentralatom[2] (Kohlenstoff, Stickstoff, Phosphor) gebundenen Wasserstoffatomen durch organische Reste (Organyl-Rest, wie Alkyl-Rest, Alkenyl-Rest, Aryl-Rest, Alkylaryl-Rest etc.), z. B. enthalten sekundäre Alkohole ein sekundäres Kohlenstoffatom (Zentralatom = Kohlenstoff), sekundäre Amine ein sekundäres Stickstoffatom (Zentralatom = Stickstoff), sekundäre Phosphine ein sekundäres Phosphoratom (Zentralatom = Phosphor).
Beispiele für sekundäre Zentralatome
- ein Kohlenstoffatom in einem Alkan oder einem Alkohol, das neben zwei Substituenten noch ein oder zwei Wasserstoffatome trägt, oder
- ein Stickstoffatom in einem Amin, das mit zwei Kohlenstoffatom verbunden ist.
Dies führt bei sekundären Verbindungen meist zu einer leichten sterischen Hinderung der funktionellen Gruppe und dazu, dass typische Reaktionen schwerer ablaufen als bei primären Verbindungen der gleichen Stoffklasse. Beispiele für solche Verbindungen sind sekundäre Alkohole,[3] sekundäre Amine und sekundäre Phosphine.
Ein typisches Beispiel für ein sekundäres Kohlenstoffatom ist das mittlere Kohlenstoffatom in Propan oder sind alle sechs Kohlenstoffatome im Cyclohexan.
Anorganische Chemie
In der anorganischen Chemie ist das Wort „sekundär“ eine Bezeichnung für Salze, die durch Neutralisation von zwei Hydroxygruppen einer mehrbasigen Säure entstanden sind, z. B. Calciumhydrogenphosphat, CaHPO4.[2]
Einzelnachweise
- Laut IUPAC-Nomenklatur sind sekundäre, bzw. tertiäre Amide mit zwei, bzw. drei Acylgruppen am Stickstoff substituiert. Da jedoch im allgemeinen Gebrauch primäre Amide mit einer Acylgruppe und zwei Kohlenwasserstoffsubstituenten am Stickstoff „tertiäre Amide“ genannt werden, wird die Klassifizierung in primäre, sekundäre und tertiäre Amide nicht empfohlen. Eintrag zu Amide. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. Mai 2019.
- Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 1274.
- Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 5: Pl–S. 8. neubearbeitete und erweiterte Auflage. Franckh'sche Verlagshandlung, Stuttgart 1987, ISBN 3-440-04515-3, S. 3791.