Calcit
Calcit, Kalzit, Kalkspat oder Doppelspat, ist ein sehr häufig vorkommendes Mineral aus der Mineralklasse der „Carbonate und Nitrate“ mit der chemischen Zusammensetzung Ca[CO3] und damit chemisch gesehen Calciumcarbonat.
| Calcit | |
|---|---|
 | |
| Allgemeines und Klassifikation | |
| Andere Namen |
|
| Chemische Formel | Ca[CO3] |
| Mineralklasse (und ggf. Abteilung) |
Carbonate und Nitrate – wasserfreie Carbonate ohne fremde Anionen |
| System-Nr. nach Strunz und nach Dana |
5.AB.05 (8. Auflage: Vb/A.02) 14.01.01.01 |
| Ähnliche Minerale | Aragonit, Dolomit |
| Kristallographische Daten | |
| Kristallsystem | trigonal |
| Kristallklasse; Symbol | ditrigonal-skalenoedrisch; 3 2/m |
| Raumgruppe | R3c (Nr. 167)[1] |
| Gitterparameter | a = 4,99 Å; c = 17,06 Å[1] |
| Formeleinheiten | Z = 6[1] |
| Häufige Kristallflächen | {1010}, {0001}, {0112}, {0221} |
| Zwillingsbildung | (0001), sehr häufig Gleitzwillinge (polysynthetische Translationslamellen) nach (0112) |
| Physikalische Eigenschaften | |
| Mohshärte | 3 |
| Dichte (g/cm3) | 2,6 bis 2,8; rein 2,715[2] |
| Spaltbarkeit | sehr vollkommen nach (1011) Spaltwinkel 75° |
| Bruch; Tenazität | muschelig, spröde |
| Farbe | meist farblos, milchig weiß, grau, gelb, rosa, rot, blau, grün, braun bis schwarz |
| Strichfarbe | weiß |
| Transparenz | durchsichtig bis undurchsichtig |
| Glanz | Glasglanz, auch Perlmuttglanz |
| Kristalloptik | |
| Brechungsindizes | nω bei ~590 nm: 1,640 bis 1,660; rein 1,658 (Im Bereich von 190 bis 1700 nm fällt nω von etwa 1,6 auf etwa 1,4.) nε bei ~590 nm: 1,486 Im Bereich von 190 bis 1700 nm fällt nε von etwa 1,9 auf etwa 1,5.[3] |
| Doppelbrechung | δ = 0,154 bis 0,174; rein 0,172 |
| Optischer Charakter | einachsig negativ |
| Achsenwinkel | 2V = kann anomal zweiachsig auftreten 2Vx dann 4–14° (bis 25°) |
| Pleochroismus | nicht vorhanden |
| Weitere Eigenschaften | |
| Chemisches Verhalten | in kalten, verdünnten Säuren unter heftigem Brausen löslich |
| Besondere Merkmale | sehr starke Doppelbrechung; gelegentlich Fluoreszenz in rot oder orange; häufige Zwillingslamellen |
Calcit kristallisiert im trigonalen Kristallsystem und entwickelt verschiedene Kristall- beziehungsweise Aggregatformen (Habitus). In reiner Form ist Calcit farblos und durchsichtig. Durch vielfache Lichtbrechung aufgrund von Gitterbaufehlern oder polykristalliner Ausbildung kann er aber auch weiß erscheinen, wobei die Transparenz entsprechend abnimmt, und durch Fremdbeimengungen eine gelbe, rosa, rote, blaue, grüne, braune oder schwarze Farbe annehmen.
Mit einer Mohshärte von 3 gehört Calcit zu den mittelharten Mineralen, das heißt, er ist mit einer Kupfermünze ritzbar. Er dient als Bezugsgröße auf der bis 10 (Diamant) reichenden Skala nach Friedrich Mohs.
Etymologie und Geschichte
Calcit in Form von Kalkstein war bereits in der Antike bekannt und wurde im Alten Griechenland als χάλιξ chálix bezeichnet mit der Bedeutung „kleiner Stein“ oder „Kies“, aber auch Kalk beziehungsweise Kalkstein. Die im Römischen Reich verwendete Bezeichnung calx wird als Lehnwort aus dem Griechischen angesehen, steht jedoch in der Bedeutung nur für rohen und gelöschten Kalk, der als Mörtel diente. Der als Baustoff verwendete Kalkstein wurde den Marmoren zugeordnet.[4]
Den bis heute gültigen Namen Calcit (ursprünglich Kalzit) für das Mineral prägte 1845 Wilhelm von Haidinger, der den bis dahin fehlenden, übergeordneten Namen für alle dessen Ausbildungsformen (Kalkstein, Kalkspat, Doppelspat, Mondmilch usw.) beanstandete. Er orientierte sich dabei an der übergeordneten Bezeichnung Calcaire von Delamétherie und Beudant, die allerdings auf die französische Sprache beschränkt blieb.[5][4]
Die Eigenschaft von Calcit, in allen Formen und Kombinationen des rhomboedrischen Systems kristallisieren zu können, hatte für die Herleitung der Gesetze der Kristallographie eine nicht zu unterschätzende Bedeutung. So hatte der englische Arzt William Pryce bereits 1778 die Grundlagen der Kristallographie vorgeahnt, als er in der Mineralogia Cornubiensis feststellte, dass sich alle Formen des Calcits durch einfache Spaltung aus der Grundform des Rhomboeders ergeben. Der französische Mineraloge René-Just Haüy (1743–1822) entwickelte auf dieser Grundlage die erste, auch praktisch nutzbare Kristallographie. Wie so oft rankt sich auch um Haüys Entdeckung eine Legende. Haüy stürzte ein großer Calcitkristall vom Tisch zu Boden und zersprang in viele Einzelteile. Beim Aufheben der Bruchstücke bemerkte Haüy, dass zwar alle eine andere Form hatten, aber alle dem rhomboedrischen Islandspat glichen. Haüy wiederholte den Vorgang mit den unterschiedlichen Kristallformen des Calcits und jedes Mal erhielt er einen Rhomboeder. Aus dieser Beobachtung schloss er, dass die Kristalle aus der Wiederholung des Elementargitters beziehungsweise der Elementarzelle in den drei räumlichen Richtungen entstehen. Seine Beobachtungen hielt er in den Jahren 1781 und 1782 in seinem Buch Memoire sur la structure des crystaux fest. Darin waren erstmals die Grundgesetze der Kristallographie formuliert und am Beispiel des Calcits erläutert.[2]
Klassifikation
In der veralteten 8. Auflage der Mineralsystematik nach Strunz gehörte der Calcit zur gemeinsamen Mineralklasse der „Carbonate, Nitrate und Borate“ und dort zur Abteilung der „Wasserfreien Carbonate ohne fremde Anionen“, wo er als namensgebendes Mineral die „Calcitgruppe“ mit der System-Nr. Vb/A.02 und den weiteren Mitgliedern Gaspéit, Magnesit, Otavit, Rhodochrosit, Siderit, Smithsonit und Sphärocobaltit bildete.
Im zuletzt 2018 überarbeiteten und aktualisierten Lapis-Mineralienverzeichnis nach Stefan Weiß, das sich aus Rücksicht auf private Sammler und institutionelle Sammlungen noch nach dieser klassischen Systematik von Karl Hugo Strunz richtet, erhielt das Mineral die System- und Mineral-Nr. V/B.02-20. Auch in der „Lapis-Systematik“ entspricht dies der Abteilung „Wasserfreie Carbonate [CO3]2-, ohne fremde Anionen“, wo Calcit ebenfalls namensgebend die „Calcitgruppe“ mit den weiteren Mitgliedern Gaspéit, Magnesit, Otavit, Rhodochrosit, Siderit, Smithsonit, Sphärocobaltit und Vaterit bildet.[6]
Die seit 2001 gültige und von der International Mineralogical Association (IMA) bis 2009 aktualisierte[7] 9. Auflage der Strunz'schen Mineralsystematik ordnet den Calcit in die neu definierte Klasse der „Carbonate und Nitrate“ (die Borate bilden jetzt eine eigene Klasse), dort aber ebenfalls in die Abteilung der „Carbonate ohne zusätzliche Anionen; ohne H2O“ ein. Diese ist allerdings weiter unterteilt nach der Gruppenzugehörigkeit der beteiligten Kationen, so dass das Mineral entsprechend seiner Zusammensetzung in der Unterabteilung „Erdalkali- (und andere M2+) Carbonate“ zu finden ist, wo es die nach wie vor existierende „Calcitgruppe“ mit der System-Nr. 5.AB.05 bildet. Vaterit bildet jetzt eine eigene Gruppe.
Die vorwiegend im englischen Sprachraum gebräuchliche Systematik der Minerale nach Dana ordnet den Calcit wie die veraltete Strunz-Systematik in die gemeinsame Klasse der „Carbonate, Nitrate und Borate“ und dort in die Abteilung der „Wasserfreien Carbonate“ ein. Auch hier ist als er als Namensgeber der „Calcitgruppe (Trigonal: R3c)“ mit der System-Nr. 14.01.01 innerhalb der Unterabteilung 14.01 Wasserfreie Carbonate mit einfacher Formel A+CO3 zu finden.
Kristallstruktur
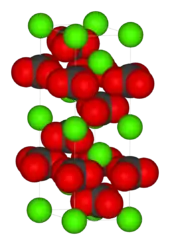
Calcit kristallisiert trigonal in der Raumgruppe R3c (Raumgruppen-Nr. 167) mit den Gitterparametern a = 4,99 Å und c = 17,06 Å sowie 6 Formeleinheiten pro Elementarzelle.[1]
Die Kristallstruktur besteht aus einer entlang der c-Achse [0001] aufgebauten, schichtartigen Anordnung von ebenen CO3-Gruppen und eckenverknüpften Calcium-Oktaedern. Jedes Sauerstoffion der CO3-Gruppe ist dabei mit je einem Calciumion der darunter und der darüber liegenden Schicht verbunden und bildet dadurch ein 3-dimensionales Netzwerk.[1]
Eigenschaften
Physikalische Eigenschaften
Charakteristisch für Calcitkristalle ist eine besonders hohe Doppelbrechung. Licht, das nicht entlang der optischen Achse des Kristalls einfällt, wird in zwei Lichtbündel aufgespalten, einen ordentlichen und einen außerordentlichen Strahl. Für diese beiden Strahlen gelten aufgrund unterschiedlicher Polarisationsrichtungen andere Brechungsindizes. Dies zeigt sich darin, dass bei einem bestimmten Blickwinkel jedes durch einen klaren Kristall beobachtete Objekt doppelt erscheint, eine zur Identifikation von Calcit sehr hilfreiche Eigenschaft, daher auch der häufige Name Doppelspat. In Island, dem bekanntesten Vorkommen für Doppelspat, wird er als silfurberg (Silberfels) bezeichnet.
Die theoretische Dichte des Calcits beträgt 2,71 g/cm³. Die effektive Dichte schwankt jedoch zwischen 2,6 und 2,8 g/cm³, je nachdem, wie viel Calcium-Ionen im Kristallgitter durch andere Metall-Ionen wie Eisen, Mangan oder Zink ersetzt sind.[2]
Je nach Fundort kann Calcit durch Einlagerung von Seltenen Erden[8] unter UV-Licht rot, blau oder gelb, aber auch andersfarbig fluoreszieren. Weiterhin kommen auch phosphoreszierende, kathodo-, thermo- und selten auch tribolumineszierende Calcite vor.[9]
 Illustration der hohen Doppelbrechung eines großen Calcit-Einkristalls („Doppelspat“) durch Verdopplung der darunterliegenden Schrift…
Illustration der hohen Doppelbrechung eines großen Calcit-Einkristalls („Doppelspat“) durch Verdopplung der darunterliegenden Schrift… …und mithilfe eines Laserstrahls.
…und mithilfe eines Laserstrahls..JPG.webp) Calcit (pink) und Quarz (violett) aus Mexiko unter UV-Licht
Calcit (pink) und Quarz (violett) aus Mexiko unter UV-Licht
Chemische Eigenschaften
Verglichen mit anderen Mineralen ist Calcit kaum resistent gegenüber der Verwitterung. Er ist viel weicher als Quarz oder Feldspat und bereits in saurem Wasser löslich. In kalten, verdünnten Säuren löst sich Calcit unter heftiger Gasentwicklung auf.
Farbe

Reiner Calcit ist durchsichtig und farblos. In der Natur ist er jedoch nur selten zu finden. Sieht man einmal ab vom Islandspat, so ist natürlicher Calcit meistens honiggelb bis gelbbraun gefärbt, massive Varietäten sind milchig weiß. Die verschiedenen Färbungen des Calcits entstehen, wenn Ionen anderer Metalle wie Eisen, Zink, Cobalt oder Mangan die Calcium-Ionen im Kristallgitter ersetzen. So ergibt Eisen einen gelbbraunen Farbton, Zink führt zu einem gräulich-weißen Farbton, Cobalt gibt rosa Farbtöne und Mangan schließlich verleiht malven- oder veilchenfarbige Töne. Zudem sind manganhaltige Varietäten oft karminrot fluoreszierend. Ist dem Calcit eine geringe Menge des Malachits beigemischt, so kann er sogar eine grüne Farbe annehmen, wie es in den Sekundärcalcit-Adern des Kalkmassivs von Vizarron in Zentralmexiko zu beobachten ist. Diese, wie auch alle anderen oben genannten Färbungen heben oft einzelne Wachstumszonen der Calcit-Kristalle hervor und sind recht häufig zu beobachten. Außergewöhnlich ist himmel- bis lavendelblauer Calcit, dessen Färbung auf Fehlstellen im Kristallgitter zurückzuführen sind, die durch Strahlung radioaktiver Minerale entstanden sind. Der blaue Farbton schwächt sich mit der Zeit ab und verschwindet nach einigen Monaten vollständig, wenn die Kristalle der Sonne ausgesetzt sind.[2]
Modifikationen und Varietäten


Calciumcarbonat ist trimorph und kommt in der Natur neben dem trigonal kristallisierenden Calcit noch als orthorhombisch kristallisierender Aragonit und als hexagonal kristallisierender Vaterit vor.
Anthrakolith oder auch Anthrakonit ist die Bezeichnung für eine schwarze, kohlenstoffreiche bis bituminöse Varietät von Calcit.[10][6]
Die Varietät Atlasspat (auch Seidenspat bzw. englisch Satin Spar[11][12]) besteht aus feinfaserigem Calcit[13] mit seidenähnlichem Glanz auf den Oberflächen. Die Verwendung des Namens Atlasspat ist allerdings uneinheitlich und wird auch für feinfaserigen Gips mit Seidenglanz verwendet.[14]
Als Blätterspat oder auch Papierspat werden Calcitvarietäten mit dünnen, blätterartigen Kristallen bezeichnet.
Durch Einlagerung von Eisenionen gelbbraun bis orange gefärbte Calcite werden als Honigcalcit oder Orangencalcit bezeichnet.[14]
Kanonenspat ist eine Calcitvarietät mit langsäulig gestrecktem, pseudohexagonalem Habitus.[15]
Als Kobaltocalcit (auch Cobaltocalcit) werden durch die Beimengung von Cobalt rosa bis pink gefärbte Varietäten bezeichnet. Ebenso kennt man durch Beimengungen von Mangan zartrosa gefärbte Calcite.[16]
Eine Pseudomorphose von Calcit nach Ikait wird als Glendonit bezeichnet.
Bildung und Fundorte
.jpg.webp)
_.jpg.webp)

Gebildet wird Calcit nach dem chemischen Gleichgewicht:
Das Gleichgewicht der obigen Reaktion verlagert sich mit steigender Temperatur zunehmend auf die rechte Seite. In warmen Gewässern können Lebewesen also mit geringerem Energieaufwand Kalkgehäuse bilden. In Dampfkesseln und anderen Gefäßen, in welchen kalkhaltiges Wasser erhitzt wird, entsteht auf diese Weise Kesselstein.
Calcit kann sowohl massiv als auch körnig, faserig oder in Kristallen auftreten und zeigt in letzterem Falle den höchsten Formenreichtum aller Minerale. Es ist als Gesteinsbildendes Mineral eines der häufigsten Minerale der Erdkruste und kommt sowohl in magmatischen, zum Beispiel in Karbonatiten, in metamorphen (Marmor) oder Sedimentgesteinen wie Kalkstein vor. Es tritt allein oder vergesellschaftet mit anderen Mineralen in Gängen auf, entsteht aber auch an der Erdoberfläche. Häufig entstand/entsteht Calcit durch Biomineralisation, sei es in Gesteinsformationen, im Boden, als in Teilen unerwünschter Zahnbelag (neben bevorzugt Calcium-Hydroxylapatit) usw.; hier aber immer in ganz bestimmten Mikro-Umweltbedingungen.[17]
Calcit löst sich gut in saurem Wasser und wird dadurch leicht aus Kalkstein ausgelaugt, wodurch Höhlensysteme entstehen. Der gelöste Calcit lagert sich an anderer Stelle wieder ab. Dabei entstehen die typischen Tropfsteine, die Stalagmiten und Stalaktiten.
Die weitaus größten Calcitvorkommen gehen auf Meeresablagerungen zurück. Dabei setzen sich die calcithaltigen Skelette und Schalen unzähliger kleiner Meerestiere wie etwa Muscheln, Korallen und diverser Protisten, wie die Coccolithophoriden, am Meeresgrund ab. Diese Kalkalgen sind kleiner als 30 Mikrometer und werden zum Nanoplankton gezählt. Sie bilden winzige Kalkschilde, die sogenannten Coccolithen, die nach dem Absterben der Algen auf den Ozeanboden sinken. Die Kreidefelsen von Dover bestehen aus solchen Coccolithen. Auch Korallenriffe spielen bei der Calcitbildung eine herausragende Rolle.
Anorganische, abiogene Bildungsbereiche von Calcit sind flache, im Intertidalbereich gelegene, tropische Meeresplattformen. Dort wird Calcit in Form von millimeterkleinen Kügelchen (Kalkooiden) ausgefällt. Calcit im Marmor geht auf thermische Metamorphose von Calcitsedimenten zurück.
Ab einer Meerestiefe von 3500 Metern, der so genannten Calcit-Kompensationstiefe, löst sich Calcit vollständig in Wasser. Daher bleiben in dieser Tiefe weder calcithaltige Sedimente noch Muschelschalen oder Skelette erhalten.
Calcit kommt als Einlagerung in die Statolithenmembran der Makulaorgane des Innenohres vor. Es spielt dort eine große Rolle bei der Wahrnehmung von Beschleunigungen und der Lotrichtung.
Bekannt aufgrund außergewöhnlicher Calcitfunde ist vor allem Island, wo neben dem wasserklaren Doppelspat auch die bisher größten Kristalle gefunden wurden. Am Helgustadir nahe Reyðarfjörður hatte der größte Kristall eine Abmessungen von 7 m × 7 m × 2 m und der schwerste ein Gewicht von 280 t.[18] In der „Sterling Bush“-Höhle im Lewis County (New York) wurde ein Calcit-Rhomboeder von 109 cm × 95 cm × 46 cm und einem Gewicht von rund 500 kg gefunden.[19]
Einer der größten in Museen ausgestellten Calcite mit einem Gewicht von 230 kg befindet sich im Natural History Museum in London.[20]
Verwendung
Baumaterial und Rohstoff
Die calcithaltigen Gesteine Marmor, Kalkstein und Onyxmarmor sind ein hochwertiges Dekorations- und Baumaterial, daneben wird Calcit in Kalkstein zur Produktion von Zement und Kunstdünger und als Zuschlagstoff bei der Verhüttung von Erzen eingesetzt. Außerdem wird es in sauren, rutilumhüllten und basischen Elektroden als Schutzgasbildner beim Lichtbogenhandschweißen eingesetzt.
Optisches Bauelement
Besonders reine Kristalle werden wegen ihrer optischen Eigenschaften (stark doppelbrechend) in der optischen Industrie, insbesondere in der Polarisationsoptik, beispielsweise Polarisationsprismen in Form von Glan-Taylor-Prismen oder als Verzögerungsplatte verwendet.
Schmuckstein

Calcit ist für eine kommerzielle Schmucksteinherstellung eigentlich zu weich und aufgrund seiner vollkommenen Spaltbarkeit auch zu empfindlich. Gelegentlich wird er aber dennoch im Glattschliff als Cabochon oder Trommelstein angeboten. Versierten Sammlern gelingt es darüber hinaus auch, Calcit in Facettenform zu bringen.[21][22]
Terrariensubstrat
Gemahlener Calcit bzw. Kalkstein wird als „Kalziumsand“ in unterschiedlich feiner Körnung unter diversen Markennamen als Substrat für Terrarien im Handel angeboten. Die Grundidee dabei ist, dass „Kalziumsand“ wegen seiner Säurelöslichkeit nach Aufnahme durch Terrarientiere, im Gegensatz zu herkömmlichem säureunlöslichem Quarzsand, nicht zu Verstopfung führt. Allerdings soll auch „Kalziumsand“ zu Verklumpungen im Magen-Darm-Trakt und somit zu schwerer Obstipation führen, die nur chirurgisch behandelt werden kann. Auch Augenlider und Lippen können schnell verkleben. Die vermutete Hauptursache der Aufnahme von Terrariumsubstraten ist eine Unterversorgung der Tiere mit Kalzium. Aufgrund der generell negativen Folgen der Substrataufnahme sollte dem nicht durch den Einsatz von „Kalziumsand“, sondern durch Anbieten von Sepiaschulp und Anreicherung des Futters mit kalziumhaltigen Nahrungsergänzungsmitteln entgegengewirkt werden.
Navigationshilfe
Doppelspat wurde möglicherweise von den Wikingern bei ihren Fahrten als Navigationshilfe benutzt. Aufgrund seiner doppelbrechenden Eigenschaften entstehen bei der Betrachtung der Sonne durch einen solchen Kristall zwei Lichtbündel, deren Intensität vom Einfallswinkel des Sonnenlichts abhängig ist. Sind beide Lichtbündel in ihrer Intensität identisch, so ist der Kristall zur Sonne ausgerichtet. Forscher stellten in einem Experiment fest, dass dies selbst bei Bewölkung und sogar bis zu 40 Minuten nach Sonnenuntergang zuverlässig funktioniert.[23][24][25]
Siehe auch
Literatur
- Johann Carl Freiesleben: Calcit. In: Magazin für die Oryktographie von Sachsen. Band 7, 1836, S. 118–121 (rruff.info [PDF; 338 kB; abgerufen am 18. November 2019]).
- Helmut Schröcke, Karl-Ludwig Weiner: Mineralogie. Ein Lehrbuch auf systematischer Grundlage. de Gruyter, Berlin; New York 1981, ISBN 3-11-006823-0, S. 503–515.
Weblinks
- Calcit. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 7. Dezember 2020. und Mineralienportrait/Calcit. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 7. Dezember 2020.
- Calcite. In: mindat.org. Hudson Institute of Mineralogy, abgerufen am 18. November 2019 (englisch).
- David Barthelmy: Calcite Mineral Data. In: webmineral.com. Abgerufen am 18. November 2019 (englisch).
- Calcite search results. In: rruff.info. Database of Raman spectroscopy, X-ray diffraction and chemistry of minerals (RRUFF), abgerufen am 18. November 2019 (englisch).
Einzelnachweise
- Hugo Strunz, Ernest H. Nickel: Strunz Mineralogical Tables. Chemical-structural Mineral Classification System. 9. Auflage. E. Schweizerbart’sche Verlagsbuchhandlung (Nägele u. Obermiller), Stuttgart 2001, ISBN 3-510-65188-X, S. 286 (englisch).
- Wolfgang F. Tegethoff: Calciumcarbonat. Von der Kreidezeit ins 21. Jahrhundert. Springer-Verlag, 2013, ISBN 978-3-0348-8259-0, S. 10 (eingeschränkte Vorschau in der Google-Buchsuche).
- Daniel W.Thompson, Michael J. De Vries, Thomas E. Tiwald, John A. Woollam: Determination of optical anisotropy in calcite from ultraviolet to mid-infrared by generalized ellipsometry. In: Thin Solid Films. Band 313–314, 1998, S. 341–346, doi:10.1016/S0040-6090(97)00843-2 (englisch).
- Hans Lüschen: Die Namen der Steine. Das Mineralreich im Spiegel der Sprache. 2. Auflage. Ott Verlag, Thun 1979, ISBN 3-7225-6265-1, S. 246.
- Wilhelm von Haidinger: Handbuch der bestimmenden Mineralogie : enthaltend die Terminologie, Systematik, Nomenklatur und Charakteristik der Naturgeschichte des Mineralreiches. Braumüller & Seidel, Wien 1845, S. 464–465 (reader.digitale-sammlungen.de [abgerufen am 18. November 2019]).
- Stefan Weiß: Das große Lapis Mineralienverzeichnis. Alle Mineralien von A – Z und ihre Eigenschaften. Stand 03/2018. 7., vollkommen neu bearbeitete und ergänzte Auflage. Weise, München 2018, ISBN 978-3-921656-83-9.
- Ernest H. Nickel, Monte C. Nichols: IMA/CNMNC List of Minerals 2009. (PDF 1703 kB) In: cnmnc.main.jp. IMA/CNMNC, Januar 2009, abgerufen am 18. November 2019 (englisch).
- Hans Jürgen Rösler: Lehrbuch der Mineralogie. 4. durchgesehene und erweiterte Auflage. Deutscher Verlag für Grundstoffindustrie (VEB), Leipzig 1987, ISBN 3-342-00288-3, S. 695.
- Calcite. In: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Hrsg.): Handbook of Mineralogy, Mineralogical Society of America. 2001 (englisch, handbookofmineralogy.org [PDF; 68 kB; abgerufen am 18. November 2019]).
- Anthrakolith. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 18. November 2019.
- Richard V. Gaines, H. Catherine W. Skinner, Eugene E. Foord, Brian Mason, Abraham Rosenzweig: Dana’s New Mineralogy. 8. Auflage. John Wiley & Sons, New York u. a. 1997, ISBN 0-471-19310-0, S. 428.
- Calcite Satin Spar (kurz Satin Spar). In: mindat.org. Hudson Institute of Mineralogy, abgerufen am 18. November 2019 (englisch, deutsche Synonyme Atlasspat bzw. Atlasspath).
- Ulrich Henn: Edelsteinkundliches Wörterbuch. Hrsg.: Deutsche Gemmologische Gesellschaft. Eigenverlag, Idar-Oberstein 2001, ISBN 3-932515-24-2, S. 10.
- Namensuche, Handelsnamen und was sie bedeuten. EPI – Institut für Edelsteinprüfung, abgerufen am 18. November 2019 (Eingabe des entsprechenden Varietäten- bzw. Handelsnamen nötig).
- Kanonenspat. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 18. November 2019.
- Kobaltocalcit. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 18. November 2019. und Manganocalcit. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 18. November 2019.
- Karl-Erich Schmittner, Pierre Giresse: Micro-environmental controls on biomineralization: superficial processes of apatite and calcite precipitation in Quaternary soils, Roussillon, France. In: Sedimentology. Band 46, Nr. 3, 1999, S. 463–476, doi:10.1046/j.1365-3091.1999.00224.x (englisch).
- Mineralrekorde. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 18. November 2019.
- Charles Palache: The largest crystal. In: minsocam.org. American Mineralogist, abgerufen am 18. November 2019 (ursprünglich publiziert in: American Mineralogist. Band 17, 1932, S. 362–363).
- Krassmann: Giant Iceland Spar from Helgustadir, Iceland. In: mineral-exploration.de. 28. Februar 2018, abgerufen am 3. April 2018.
- Walter Schumann: Edelsteine und Schmucksteine. Alle Arten und Varietäten. 1900 Einzelstücke. 16., überarbeitete Auflage. BLV Verlag, München 2014, ISBN 978-3-8354-1171-5, S. 224.
- Michael R. W. Peters: Calcit (mit Bildbeispielen geschliffener Calcite). In: realgems.org. 24. Juli 2011, abgerufen am 18. November 2019.
- Wikinger nutzten transparentes Mineral als Sonnenkompass. scinexx das wissensmagazin, 2. November 2011, abgerufen am 18. November 2019.
- Guy Ropars, Gabriel Gorre1, Albert Le Floch, Jay Enoch, Vasudevan Lakshminarayanan: A depolarizer as a possible precise sunstone for Viking navigation by polarized skylight. In: Proceedings of the Royal Society A. 2011, doi:10.1098/rspa.2011.0369.
- Albert Le Floch, Guy Ropars, Jacques Lucas, Steve Wright, Trevor Davenport, Michael Corfield, Michael Harrisson: The sixteenth century Alderney crystal: a calcite as an efficient reference optical compass? In: Proceedings of the Royal Society A. Band 469, Nr. 2153, 2013, doi:10.1098/rspa.2012.0651.