Natriumnitrat
Natriumnitrat (auch Natronsalpeter oder Chilesalpeter), NaNO3, ist das Natriumsalz der Salpetersäure. Die chemische Verbindung liegt im reinen Zustand in Form einer hygroskopischen, das heißt wasseranziehenden, weißen Substanz oder farblosen Kristallen vor.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
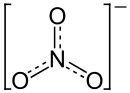 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Natriumnitrat | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | NaNO3 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser, hygroskopischer Feststoff[3] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 84,99 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,26 g·cm−3 (20 °C)[4] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
Zersetzung ab 380 °C[4] | ||||||||||||||||||
| Löslichkeit |
leicht in Wasser (874 g·l−1 bei 20 °C)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Natriumnitrat findet vielfältige Anwendung als Stickstoffdünger und in der Lebensmittelkonservierung sowie in geringerem Maße für die Herstellung von Glas oder Emaille. Ferner wird es auch für pyrotechnische Erzeugnisse oder Festtreibstoff für Raketenantriebe verwendet – allerdings nur eingeschränkt, denn obwohl Natriumnitrat in seiner Molekülstruktur dem auch heute noch häufig verwendeten Kaliumnitrat ähnelt, schränkt die hygroskopische Eigenschaft den Einsatz für die Pyrotechnik deutlich ein, primär der verminderten Lagerbarkeit und Stabilität wegen.
Geschichte
Im Jahr 1736 stellte Duhamel Natriumnitrat erstmals synthetisch dar. Die ersten Ladungen von Chilesalpeter erreichten England in den 1820er Jahren. Im Laufe der Zeit stieg der Verbrauch und 1859 importierte England bereits 47.000 Tonnen. Schon 1870 wurden von Iquique, einer Hafenstadt im Norden Chiles, bereits 147.000 Tonnen Chilesalpeter nach Liverpool und Hamburg verschifft.[6]
Die zunehmende Profitabilität der Salpeterexporte führte zwischen 1879 und 1884 schließlich zum Salpeterkrieg, auch Pazifischer Krieg genannt, zwischen Chile einerseits und Peru und Bolivien andererseits um die Gebiete Región de Arica y Parinacota, Región de Tarapacá und Región de Atacama, im heutigen Norden Chiles, wo die ergiebigsten Vorkommen von Chilesalpeter zu finden waren. Mit der Erfindung des Haber-Bosch-Verfahrens und der damit verbundenen Erzeugung von synthetischem Natriumnitrat verlor die Gewinnung von Chilesalpeter aus den chilenischen Vorkommen ständig an Bedeutung.
Vorkommen
Natriumnitrat ist das wichtigste natürlich vorkommende Nitrat. Als Mineral kommt es als Nitronatrit vor. Hauptfundort ist Chile, daher auch der Trivialname Chilesalpeter.[7] Die Lagerstätten in der Atacama-Wüste sind die Reste von abgelagertem Vogelkot (Guano), dessen organische Anteile verwittert sind. Weitere natürliche Vorkommen gibt es in Ägypten, Kleinasien, Kolumbien und Kalifornien.
Gewinnung

Natürliche Vorkommen werden durch Auslaugung mit heißen Solen gewonnen und durch Filtration von Fremdstoffen gereinigt. Das in der Kälte auskristallisierte Natriumnitrat hat eine Reinheit von etwa 98 %. Das in den Mutterlaugen enthaltene Iodat geht in die Iodgewinnung.
Natriumnitrat kann auch durch Umsatz von Natriumcarbonat mit Salpetersäure gewonnen werden:
Hier bietet sich die Absorption von Restgasen der Ammoniakoxidation in konzentrierter Natriumcarbonat-Lösung an:
Zur Oxidation des Nitrits wird dieses mit Salpetersäure angesäuert, an der Luft zu Nitrat oxidiert und mit Natriumcarbonat neutralisiert. In Vakuumverdampfern wird es bis zum Feststoff eingeengt.
Natriumnitrat kann auch durch Umsetzung von Natriumhydroxid mit Salpetersäure gewonnen werden:
Eigenschaften
.jpg.webp)
Physikalische Eigenschaften
- wichtige thermodynamische Eigenschaften
Chemische Eigenschaften
In heißer Schwefelsäure wird es unter Bildung von Salpetersäure zu Natriumhydrogensulfat umgesetzt:
Bei Temperaturen oberhalb von 380 °C zersetzt es sich zu Natriumnitrit:
Bei Temperaturen oberhalb von 800 °C zu Natriumoxid:
Verwendung

Natriumnitrat wird als Düngemittel, in der Baustoffindustrie als Zementzusatz, als Hilfsstoff in chemischen Abflussreinigern, als Latentwärmespeicher und als Konservierungsmittel zum Pökeln von Fleisch- und Wurstwaren verwendet (siehe Pökelsalz). Außerdem dient es als Grundstoff zur Herstellung von Kaliumnitrat.
Pökelsalz
Pökelsalz besteht aus Kochsalz, dem geringe Mengen Natriumnitrat E 251, Natriumnitrit E 250, Kaliumnitrit E 249 und/oder Kaliumnitrat E 252 zugesetzt sind. Die Nitrate selbst wirken nicht antibakteriell. Sie werden jedoch im Pökelprozess enzymatisch in Nitrite umgewandelt, die gegen Bakterien, vor allem gegen den Botulismus-Erreger Clostridium botulinum, wirken. Bei diesem Prozess wird der chemisch wenig beständige Muskelfarbstoff Myoglobin in eine stabilere Variante umgewandelt (Umrötung). Als Folge davon behält das Fleisch seine rote Farbe. Ungepökelte Fleisch- und Wurstwaren nehmen bald nach der Schlachtung eine graue Farbe an, durch das Pökeln sieht auch alte Fleischware frisch aus. Zudem wird beim Pökeln ein typisches Aroma ausgebildet.
Natriumnitrat wird für Wurstwaren, Hartkäse, Schnittkäse, eingelegte Heringe und Sprotten verwendet.
Nitrate selbst sind ungefährlich. Problematisch ist ihr Einsatz, weil sie in Nitrite umgewandelt werden. Diese Umwandlung ist im Lebensmittel, aber auch im menschlichen Körper möglich. Nitrite wiederum wirken gefäßerweiternd und blutdrucksenkend. In höheren Dosierungen können sie zu akuten Vergiftungserscheinungen (Methämoglobin-Bildung) führen. Nitrit kann bei gleichzeitiger Aufnahme von Fleisch- oder Milcheiweiß im menschlichen Körper zu stark krebserregenden Nitrosaminen umgewandelt werden.
Nachweis
- Nachweisreaktionen
- Natrium: als hell leuchtend gelb in der blauen Bunsenbrennerflamme
- Nitrat: Spatelspitze Substanz mit verdünnter Schwefelsäure lösen und mit einer kalt gesättigten Eisen(II)-sulfatlösung versetzen. Mit etwas konzentrierter Schwefelsäure unterschichten. An der Grenzschicht entsteht ein brauner Ring, der als Nachweis für Nitrat gilt (Ringprobe).
Quellen
- Eintrag zu E 251: Sodium nitrate in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 23. August 2020.
- Eintrag zu SODIUM NITRATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 26. Februar 2020.
- Eintrag zu Natriumnitrat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 27. November 2021.
- Eintrag zu Natriumnitrat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- Datenblatt Natriumnitrat (PDF) bei Merck, abgerufen am 19. Januar 2011.
- Adolf Beer: Allgemeine Geschichte des Welthandels, Verlag Wilhelm Braumüller, Wien, 1884, S. 201.
- Rainer Kündig, Christoph Bühler, Heinz Surbeck: Angewandte Mineralogie und nichtmetallische Rohstoffe – Nutzung und Umweltaspekte I (PDF; 1,3 MB)


