Prostatakrebs
Der Prostatakrebs (medizinisch Prostatakarzinom; PCa) ist eine bösartige Tumorerkrankung und geht vom Drüsengewebe der Vorsteherdrüse (Prostata) aus. In Deutschland sterben knapp drei von hundert Männern an Prostatakrebs.[1][2] Der Prostatakrebs gehört zu den häufigsten Krebserkrankungen des Mannes: Innerhalb der Gruppe der an Krebs verstorbenen Männer ist er für etwa zehn Prozent der Todesfälle verantwortlich und stellt damit die dritthäufigste tödliche Krebserkrankung nach Lungen- und Darmkrebs dar.[2]
| Klassifikation nach ICD-10 | |
|---|---|
| C61 | Bösartige Neubildung der Prostata |
| ICD-10 online (WHO-Version 2019) | |
Die Erkrankung ist im Frühstadium symptomlos. Im fortgeschrittenen Stadium können Beschwerden wie Blasenentleerungsstörungen, Knochenschmerzen und später Gewichtsverlust und Blutarmut auftreten. Wird die Diagnose erst gestellt, wenn bereits Symptome aufgetreten sind, hat häufig schon eine Metastasierung stattgefunden, vorrangig in die lokalen Lymphknoten oder in das Skelett (Knochenmetastasen).
Eine Behandlung mit Aussicht auf Heilung ist nur möglich, wenn das entartete Gewebe die Organgrenzen noch nicht überschritten hat und keine Metastasen vorliegen. Da es in der Regel erst bei fortgeschrittener Erkrankung zu Beschwerden kommt, wird in Deutschland eine regelmäßige Früherkennungsuntersuchung für Männer über 45 Jahren (ab dem 41. Lebensjahr für Männer mit positiver Familienanamnese) angeboten, um die Krebsdiagnose möglichst früh in einem noch heilbaren Stadium zu stellen.
Das Prostatakarzinom tritt überwiegend bei älteren Männern auf, die eine Symptomatik vielfach nicht mehr erleben würden. So hat sich seit zirka Anfang dieses Jahrtausends das »aktive Beobachten« (siehe unten) als brauchbares Konzept für Männer entwickelt, die sich (zumindest zunächst) keiner invasiven Therapie unterziehen möchten. Die Entscheidung zur Behandlung ist schwierig und vom Einzelfall abhängig. Therapeutische Optionen sind die Operation mit kompletter Entfernung der Prostata (Prostatektomie), die Strahlentherapie, die Hormontherapie und in manchen Fällen die Chemotherapie. In der Erprobungsphase befindet sich noch die therapeutische Hyperthermie („Nanotherapie“).
Prostatakrebs ist auch bei Tieren beschrieben; unter den Haustieren ist er beim Hund am häufigsten.
Die Prostata
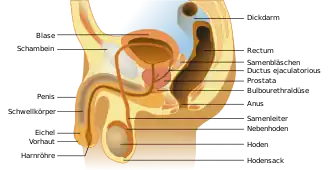
Die Prostata oder Vorsteherdrüse ist eine akzessorische Geschlechtsdrüse aller männlichen Säugetiere einschließlich des Menschen. Sie liegt beim Menschen unterhalb der Harnblase und umkleidet die Harnröhre bis zum Beckenboden. Sie ähnelt beim Mann in Größe und Form einer Kastanie. An die Rückseite der Prostata grenzt der Mastdarm (Rectum). Deswegen kann sie vom Enddarm aus mit den Fingern ertastet und beurteilt werden. Aufgabe der Prostata ist die Abgabe eines Sekrets, das zusammen mit dem der Bläschendrüse, der Bulbourethraldrüse und den aus dem Hoden stammenden Samenzellen das Sperma bildet. Wachstum und Funktion der Vorsteherdrüse werden vorwiegend von dem Geschlechtshormon Testosteron gesteuert.
Epidemiologie
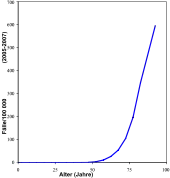
Das Prostatakarzinom ist in Deutschland die häufigste diagnostizierte Krebserkrankung des Mannes und steht nach dem Bronchialkarzinom und dem kolorektalen Karzinom an dritter Stelle bei den krebsbedingten Todesursachen der Männer. Rund 26 Prozent aller bei Männern jährlich neu auftretenden Krebserkrankungen betreffen die Prostata. Das entspricht einer altersstandardisierten Inzidenzrate von etwa 99,1 auf 100.000 männliche Personen.[3] Nach einer aktuellen Statistik erkranken in Deutschland 2018 jährlich ca. 65.000 Männer neu an Prostatakrebs.[3] Die beobachtbare, vermeintlich starke Zunahme in den letzten Jahrzehnten ist eher auf verbesserte diagnostische Methoden und eine allgemein höhere Lebenserwartung zurückzuführen als auf eine tatsächliche Zunahme der Fallzahlen.
| Jahr | 1980 | 1985 | 1990 | 1995 | 2000 | 2016 | 2018 |
|---|---|---|---|---|---|---|---|
| Jährliche Neuerkrankungen in Deutschland[3] |
16.800 | 21.600 | 27.500 | 35.400 | 44.800 | 58.780 | 65.200 |
Die jährliche Mortalität (Gesamtzahl der Todesfälle) liegt um 15.000.[3] Nach einer Übersichtsstudie von 2015 stieg die Rate von „schlafendem“ (latentem) Prostatakrebs bei der Autopsie von Personen, die durch andere Ursachen gestorben waren, von 5 % in der Altersgruppe bis 30 Jahre auf 59 % in der Altersgruppe ab 80 Jahre.[4] Eine ähnliche Übersichtsstudie, ebenfalls von 2015, zeigte auf einer etwas abweichenden Datengrundlage denselben Trend.[5]
Es gibt starke geographische und ethnische Unterschiede in der Häufigkeit: Männer schwarzafrikanischen Ursprungs haben die höchste Inzidenzrate, am niedrigsten ist sie bei Asiaten.[6]
Die Daten für die weltweiten Erkrankungsraten sind nicht zuverlässig, da sie zum Teil auf Schätzungen beruhen und die diagnostischen Möglichkeiten in den einzelnen Regionen sehr differieren. Die auf Daten der Internationalen Agentur für Krebsforschung (IARC) beruhende Erhebung GLOBOCAN gibt für das Jahr 2002 insgesamt knapp 680.000 Neuerkrankungen und etwa 220.000 Todesfälle an. Hiernach ist die jährliche Inzidenzrate in Zentralasien mit weniger als 3/100.000 Einwohner am niedrigsten, die höchste ist auf dem nordamerikanischen Kontinent mit über 160/100.000 Einwohner zu verzeichnen.[7]
Risikofaktoren und protektive Faktoren
Genetik
Die Ursache der Erkrankung ist bisher weitgehend unbekannt. Die genetische Disposition spielt bei der Entstehung der Erkrankung eine Rolle (familiäre Häufung). Daher gelten Männer, deren Väter oder Brüder Prostatakrebs hatten, als Risikopatienten mit etwa doppeltem Erkrankungsrisiko.[8] Diese Männer sollten die üblicherweise erst ab dem fünfzigsten Lebensjahr erforderliche Krebsfrüherkennung durch Kontrolle des prostataspezifischen Antigens bereits ab dem 45. Lebensjahr wahrnehmen. Nun konnte auch in einer Studie gezeigt werden, dass dem beim jungen Mann auftretenden Adenokarzinom der Prostata eine andere Pathophysiologie zugrunde liegt. Es zeigte sich, dass der testosteronbindende Androgenrezeptor eine erhöhte Aktivität aufweist, wodurch eine ganze Reihe von Genen verändert und die Entstehung eines Karzinoms erleichtert wird.[9]
Lebensweise
Die großen Unterschiede in der Krankheitshäufigkeit bei verschiedenen Ethnien werden auch auf deren Lebensgewohnheiten zurückgeführt, zumal die Nachkommen von Emigranten nicht das Erkrankungsrisiko ihrer Vorfahren tragen, sondern das des neuen Heimatlandes annehmen. Eine gewisse Rolle wird hierbei der Ernährung zugeschrieben.
Wie wichtig dabei die Lebensweise ist, zeigt folgender Zusammenhang: Obgleich weltweit die in Autopsien entdeckten Prostatakarzinome ungefähr gleich häufig auftreten, ist das tatsächliche Auftreten (Inzidenz) von Prostatakrebs von großen geographischen Unterschieden geprägt: Während in den USA jährlich etwa 120 (Weiße) beziehungsweise 200 (Farbige) und in Deutschland 100 von 100.000 Einwohnern an Prostatakrebs erkranken, sind es in Japan nur etwa zwölf von 100.000 Einwohnern.[10][11] Wenn jedoch Japaner von Japan nach Kalifornien ziehen und „amerikanisiert“ werden, steigt ihr Prostatakrebsrisiko deutlich und nähert sich US-amerikanischem Niveau.[12] Für die deutlich niedrigere Inzidenz werden vor allem die asiatische Ernährung und Lebensweise verantwortlich gemacht. Die aktuelle Studienlage weist auf die Bedeutung einer pflanzenreichen Kost und bestimmter Pflanzenstoffe in Bezug auf die Prävention, das Fortschreiten und das Überleben bei Prostatakrebs hin.[13]
Es konnten keine Hinweise darauf gefunden werden, dass die Sterilisation (Vasektomie) das Erkrankungsrisiko erhöht.[14] Doch ein sicherer Einflussfaktor ist der Testosteronspiegel, da die Tumorzellen auf die Stimulation durch Androgene angewiesen sind: Eunuchen entwickeln kein Prostatakarzinom. Im Gegensatz dazu stellen die im fortgeschrittenen Lebensalter häufige gutartige Vergrößerung der Prostata (benigne Prostatahyperplasie) und die Prostataentzündung, ob chronisch oder akut, keine unabhängigen Risikofaktoren dar. Noch widersprüchlich ist die aktuelle Datenlage zur eventuellen Krebsförderung durch erhöhte Spiegel des Gewebshormons IGF-1 (insulinähnlicher Wachstumsfaktor).[15]
Nach einer 2003 veröffentlichten Studie soll häufiges Ejakulieren in jüngeren Jahren das Erkrankungsrisiko senken.[16] Australische Wissenschaftler verglichen Daten zu Sexualpraktiken von 1079 Prostatakrebs-Patienten mit denen von 1259 gesunden Männern im Alter zwischen 20 und 50 Jahren. Ihr Ergebnis: Zwanzigjährige, die öfter als viermal pro Woche ejakulieren, senken ihr Risiko für den Prostatakrebs um ein Drittel. Methodisch ist hierbei das Ursache-Wirkungs-Verhältnis nicht geklärt; es könnte sein, dass Männer mit einem gesunden, leistungsfähigen Genitaltrakt öfter ejakulieren und die Gesundheit der Genitalien die eigentliche Ursache ist, weshalb sie später auch nicht so häufig erkranken. Im Gegensatz dazu hatten frühere Studien häufige Sexualkontakte mit einem deutlich erhöhten Risiko für Prostatakrebs in Zusammenhang gebracht. Dies könnte jedoch, nach Ansicht der australischen Forscher, durch die höhere Infektionsgefahr bedingt sein. Betrachtet man die Zahl der Ejakulationen insgesamt, so hätten diese einen schützenden Effekt, weil durch die häufige Bildung von Samenflüssigkeit krebserregende Substanzen aus der Prostata herausgeschwemmt werden. Auch würden die Prostatazellen auf diese Art zum Ausreifen angeregt, was sie für Karzinogene weniger anfällig machen könnte. Eine 2016 veröffentlichte Studie (Datenbasis über 30.000 Männer) zieht ebenfalls den Schluss, dass das Erkrankungsrisiko mit steigender Ejakulationsfrequenz sinkt.[17] Die Autoren räumen aber auch ein, dass sexuell aktive Männer möglicherweise seltener zu Vorsorgeuntersuchungen gehen, so dass potentielle Erkrankungen in dieser Untersuchungsgruppe häufiger unentdeckt bleiben. Für ein gesenktes Erkrankungsrisiko werden verschiedene physiologische Gründe vorgeschlagen. So kann häufiges Ejakulieren die Funktion und Teilungsgeschwindigkeit der randständigen Epithelzellen beeinflussen, so dass eine frühe Tumorgenese behindert wird.
Ein weiterer möglicher Risikofaktor ist Sonnenmangel. In Nordamerika und Europa besteht ein auffälliges Nord-Süd-Gefälle bei der Häufigkeit von Prostatakrebs, das sich derzeit nur durch die unterschiedliche Besonnung der männlichen Bevölkerung erklären lässt.[18] Hierfür ist vermutlich Cholecalciferol (Vitamin D3) verantwortlich, das eine chemopräventive Wirkung hat. Der größte Teil des im Körper verfügbaren Cholecalciferols wird durch UV-B-Bestrahlung in der Haut gebildet.[19] Ein Mangel an Vitamin D erhöht signifikant das Risiko für Prostatakrebs.[20] Welche Blutspiegel von Calcidiol, bzw. welche UV-Dosis, optimal sind, ist allerdings noch unklar.[21] Die „Sonnenmangel-Theorie“ ist mit Vorbehalt zu sehen, denn auf der anderen Seite ist wissenschaftlich bewiesen, dass zu viel Besonnung ein Risikofaktor für das Auftreten von Hautkrebs ist.[22] Möglicherweise überwiegen aber die Vorteile der Besonnung.[21]
Ernährung
Der 2014 vom WCRF/CUP herausgegebene Bericht zeigte, dass im Gegensatz zur Ernährung die Körpermaße (Körpergröße, sowie Umfang an Körperfett) einen „überzeugenden Einfluss“ auf das Risiko haben, an Prostatakrebs zu erkranken. Die vom WCRF-CUP verwendeten Studien wurden 2016 in einer Metaanalyse untersucht.[23] Hier kamen die Autoren aber zu dem Ergebnis, dass es für einen Zusammenhang zwischen Ernährung, Körpermaßen und körperlicher Aktivität auf das Prostatakrebsrisiko keinen überzeugenden Beweis gebe. Möglicherweise können diese Faktoren das Risiko zwar beeinflussen, große Effekte können aber nicht geschlussfolgert werden.
Ob die Ernährung einen Einfluss auf das Auftreten des Prostatakrebs hat, wird kontrovers diskutiert. Nach Auffassung des DKFZ-Krebsinformationsdienstes gibt es bislang keine „Diät gegen Prostakrebs“. Vitamintabletten oder Mineralstoffe würden unter Umständen sogar schaden. Neuere Studien ließen allerdings erkennen, dass Übergewicht möglicherweise das Krankheitsrisiko steigert, zumindest das für eine fortgeschrittene, schwere Erkrankung. Übergewicht werde aber nicht nur durch das bestimmt, was man isst, sondern auch davon, wie viel Energie man verbraucht.[24]
2021 kam eine Studie mit rund 47.000 beteiligten Männern zu dem Schluss, dass eine gesunde pflanzenbasierte Ernährung bei jungen Männern das Gesamtrisiko und das Risiko für schweren Prostatakrebs reduzieren kann.[25]
Fleisch
Gegenstand vieler Kontroversen ist, ob sich das Risiko für das Prostatakarzinom mit dem Genuss von Fleisch, insbesondere rotem Fleisch, erhöht. Es liegen Daten von verschiedenen Fall-Kontroll- und Kohortenstudien Ende der 90er-Jahre vor, die man so schlussfolgern könnte, dass der Verzehr von rotem Fleisch zu einem um mindestens 30 % erhöhten Risiko führt, an Prostatakrebs zu erkranken.[26] In einem ähnlichen Zeitraum wurde außerdem in einer prospektiven Studie an 51.529 Männern in Heilberufen gezeigt, dass sich das Risiko für das metastasierende Prostatakarzinom mit dem Verzehr von rotem Fleisch um 60 % erhöhe (relatives Risiko = 1,6 für das höchste Quintil, verglichen mit dem niedrigsten, 95 %-Konfidenzintervall = 1,0–2,5).[27] Tierische Fette führten zu einem 1,63-fachen Risiko. Offenbar spielen hierbei auch die klassischen Karzinogene wie heterozyklische Amine (HMA) und polyzyklische aromatische Kohlenwasserstoffe (PAH), die beim Braten, Schmoren oder Grillen des Fleisches entstehen, eine Rolle.[28] Hoher Fleischkonsum soll aber nicht nur das Risiko von Prostatakrebs erhöhen, sondern nachweislich auch von Brust- und Darmkrebs. Epidemiologische Zusammenhänge sind auch mit Nieren-, Lungen- und Bauchspeicheldrüsenkrebs nachgewiesen.[29] In einer Kohortenstudie mit etwa 1000 Patienten wurde gezeigt, dass die Wahrscheinlichkeit eines Rezidivs bei bereits operierten Patienten sinkt, wenn sie ihre Ernährung von rotem Fleisch und Eiern auf Geflügel und Fisch umstellen.[30]
In späteren Analysen zeichnete sich ein nicht mehr so einheitliches Bild ab. Das World Cancer Research Fund (WCRF) gab 2007 einen Bericht zum Thema „Ernährung, körperliche Aktivität und Krebsprävention: Eine globale Perspektive“ heraus, die Datenlage für Prostatakrebs wurde hierbei zuletzt 2014 aktualisiert (im sogenannten Continuous Update Project, CUP).[31] Hierbei kamen die Autoren über die damals verfügbare Datenlage zu dem Schluss, dass Aussagen über Erkrankungsrisiko und Verzehr an rotem und verarbeitetem Fleisch nur bestenfalls begrenzt zutreffen. Eine 2015 durchgeführte Metaanalyse hat dies bestätigt: Der Verzehr von (rotem) Fleisch führt nicht zu einem erhöhten Risiko, an Prostatakrebs zu erkranken.[32] Auch die Hypothese, dass HMAs und die Art, das Fleisch bei hohen Temperaturen zu erhitzen, Risikofaktoren für Prostatakrebs darstellen, konnte in der Metaanalyse nicht gezeigt werden. Eine 2016 veröffentlichte Metaanalyse zeigte darüber hinaus, dass der erhöhte Verzehr von Geflügelfleisch das Erkrankungsrisiko für letalen Prostatakrebs geringfügig senkt, während ein erhöhter Konsum von Eiern dieses geringfügig erhöht.[33] Außerdem konnte man nach Verzehr von Fisch keinen wesentlichen Effekt beobachten – unabhängig vom Grad oder von Stadium der Erkrankung.
Milch
Der World Cancer Research Fund sieht nur eine beschränkte Evidenz dafür, das Milchprodukte Prostatakrebs verursachen. Die Evidenz reicht mit Stand 2018 nicht dafür aus, sich gegen einen Verzehr auszusprechen.[34][35]
Eine im Februar 2020 veröffentlichte Übersichtsarbeit von Walter C. Willett et al. sieht auf der Basis ausgewählter Beobachtungsstudien einen statistischen Zusammenhang von Milchkonsum und dem Auftreten von Prostatakrebs.[36][37]
Eine im Juli 2020 veröffentlichte systematische Übersichtsarbeit schätzt die bisherigen Forschungsergebnisse hingegen als „nicht schlüssig“ ein. Während die Mehrheit der ausgewerteten Studien den statistischen Zusammenhang nahelegen, zeige eine große schwedische Studie aus dem Jahr 2020 keinen Zusammenhang zwischen Milchkonsum und einem erhöhten Risiko für die Entwicklung von Prostatakrebs. Während einige der ausgewerteten Studien eine Korrelation zwischen einem erhöhten Risiko für Prostatakrebs und einem hohen Fettgehalt in der Milch fanden, deuteten andere darauf hin, dass die fettfreien Bestandteile der Milch mit dem höheren Risiko für Prostatakrebs verbunden sein könnten. Die Autoren verweisen darauf, dass Milch und Milchprodukte Bestandteile der westlichen Ernährung sind. Es sei daher möglich, dass das erhöhte Risiko für die Entwicklung von Prostatakrebs nicht insbesondere mit Milch und Milchprodukten zusammenhänge, sondern mit den insgesamt krebserzeugenden Wirkungen der westlichen Ernährung. Derzeit gäbe es keine formellen klinischen Empfehlungen zum Konsum von Milchprodukten für Patienten, bei denen das Risiko einer Prostatakrebsentwicklung besteht oder bei denen in der Vergangenheit Prostatakrebs aufgetreten ist. Ärzte könnten Patienten mit einem höheren Risiko für die Entwicklung von Prostatakrebs trotz der widersprüchlichen Forschungsergebnisse empfehlen, den Konsum von Milch oder Milchprodukten, insbesondere solchen mit hohem Fettgehalt, zu vermeiden oder zu reduzieren. Risiken, Nutzen und Grenzen eines solchen Ernährungsansatzes sollten mit dem Patienten besprochen werden. Wenn beschlossen wird, den Verzehr von Milchprodukten zu unterbinden oder zu begrenzen, sollte der Patient über geeignete Kalzium- und Vitamin D-Supplementierung informiert werden.[38]
Eine große epidemiologische Studie aus Japan aus dem Jahr 2021 untersuchte 26.464 Männer und den Zusammenhang von Milchprodukten und Prostatakrebs. Milchkonsum zeigte einen dosisabhängigen Effekt auf die Entstehung von Prostatakrebs, wobei das Risiko um 37 % erhöht war. Die Autoren kommen zu dem Schluss, dass ein hoher Konsum von Milchprodukten das Risiko für Prostatakrebs bei japanischen Männern erhöht.[39]
Soja
Mehrere Meta-Studien konnten bislang zeigen, dass der regelmäßige Konsum von Soja das Risiko, an Prostatakrebs zu erkranken, verringert.[40]
Eine Meta-Studie aus dem Jahr 2018, welche 30 Studien auswertete, stützt dieses Ergebnis. Für allgemeinen Soja-Konsum ergab sich eine Risikoreduktion um 29 %. Der Effekt scheint jedoch bei nicht-fermentierte Sojaprodukte (bspw. Sojamilch, Tofu, Sojabohnen) größer zu sein als bei fermentierten (bspw. Nattō oder Miso). So lag die berechnete Risikoreduktion für nicht-fermentierte Sojaprodukte bei 35 % und bei fermentierten bei 14 %.[41]
Calcium
Im Zusammenhang mit der chemopräventiven Wirkung von Vitamin D3 wurden auch mögliche negative Effekte hoher Calciumzufuhr betrachtet. Eine hohe Calciumzufuhr vermindert die körpereigene Cholecalciferol-Produktion. Bei vielen Studien wird ein Effekt von in Nahrungsmitteln enthaltenes Calcium (wie z. B. Milch oder Käse) auf die das Erkrankungsrisiko oder die Mortalität untersucht. Manche Studien weisen darauf hin, dass das Risiko an Prostatakrebs zu erkranken, erhöht ist.[42][43]
Phytotherapie
Ein Nutzen sogenannter Phytohormone aus Soja lässt sich nicht belegen, auch isoliert gegebene sekundäre Pflanzenstoffe zeigen keine Wirksamkeit. Fachgesellschaften warnen auch vor Beispielen in der Werbung, deren Wirksamkeit nicht belegt ist (z. B. Lycopin aus Tomaten).[44]
Gegenstand zahlreicher Studien ist Granatapfelsaft, dieser ist der am besten untersuchte Pflanzenstoff bei Prostatakrebs.[45] So sollen die darin enthaltenen phytochemischen Pflanzenstoffe wirksam bei der Senkung des oxidativen Stresses und bei der Modulierung von Entzündungswegen sein.[46] Zudem üben die enthaltenen Substanzen in Zellkultur einen inhibitorischen Effekt auf das Tumorwachstum aus.[43] Im Mittelpunkt steht die Auswertung des PSA-Wertes (prostataspezifisches Antigen), das als zentraler Marker für einen möglichen Therapieerfolg gewertet wird. Die Ergebnisse zahlreicher Studien sind uneinheitlich, es fehlen verlässliche Überlebensdaten.[45] Außerdem ist nicht bekannt, ob sich ein möglicher positiver Einfluss auf den PSA-Wert auf den Tumor auswirkt. Die Datenlage ist zu begrenzt, um Aussagen über eine mögliche Therapieform (als Ergänzung oder als Ersatz für die die klassische Therapieform) zu treffen.[44] Ein pauschaler Gebrauch von Granatapfelprodukten bei Patienten mit Prostatakarzinom wird nicht empfohlen. Jedoch ist die Einnahme von Granatapfelsaft nebenwirkungsarm.[43]
Molekularbiologische Aspekte des Prostatakarzinoms
Wie allen Neoplasien liegt auch dem Prostatakarzinom letztlich die irreversible Veränderung des Erbgutes einer einzigen Zelle zugrunde. Alle Krebszellen sind Abkömmlinge (Klone) dieser Zelle. Verkomplizierend kommt hinzu, dass sich deren Erbgut weiter verändert, da die physiologischen Vorgänge, die DNA-Schäden reparieren oder mutierte normale Körperzellen absterben lassen würden (Apoptose), in Krebszellen nicht zum Tragen kommen. Mit der Zeit entwickelt sich daher ein Mosaik aus Zellen mit unterschiedlich stark verändertem Genom. Klinisch entspricht dem ein inhomogenes Erscheinungsbild des Tumors und ein zunehmendes „Bösartigerwerden“ über die Jahre.
Anders als viele andere epitheliale Malignome hat das Prostatakarzinom keine typische Adenom-Karzinom-Sequenz und auch kein spezifisches Mutationsmuster. Stattdessen kommen sehr heterogene genomische Veränderungen in Form von Punktmutationen an verschiedenen Stellen, Verlusten von Allelen oder ganzen Chromosomen und bisweilen zusätzlich Polyploidie vor. Häufig sind jedoch in einem späteren (metastasierten) Stadium zumindest auch klassische Tumorsuppressorgene wie TP53 von Deletionen oder Mutationen betroffen. Eine wichtige Rolle scheinen Veränderungen des den Androgenrezeptor codierenden Gens zu spielen. Derzeit sind mindestens 17 genetisch verschiedene Zelllinien des Prostatakarzinoms bekannt.[47]
Symptomatik
In frühen Stadien ist Prostatakrebs nahezu immer symptomlos. Hauptbeschwerden ergeben sich beim fortgeschrittenen Karzinom aus der Blockade des Harnabflusses und bestehen somit in Störungen der Miktion (Urinieren). Möglich sind ein verzögerter Beginn, eine verlängerte Miktion mit schwachem Strahl, Nachtropfen oder die Unterbrechung des Harnstrahls während des Wasserlassens. Oft bleibt Restharn in der Blase zurück. Irritative Beschwerden sind vermehrter oder überwiegend nächtlich auftretender Harndrang (Nykturie), häufiges Lassen geringer Urinmengen (Pollakisurie), erschwertes Wasserlassen (Dysurie) oder Schmerzen beim Wasserlassen (Algurie). Durch Druckschädigung von Nerven des Kreuzbeinbereichs kann es zu Erektionsstörungen kommen. Sichtbares Blut im Urin (Hämaturie) oder Ejakulat (Hämatospermie) ist hingegen selten.
Beschwerden können im fortgeschrittenen Stadium mit Metastasierung auch primär durch die Metastasen entstehen, während das Prostatakarzinom klinisch stumm bleibt (okkultes Karzinom). Am häufigsten sind hier Schmerzen der Wirbelsäule und des Beckens. Bei starker metastatischer Durchsetzung kann es zu spontanen Knochenbrüchen ohne Trauma, sogenannten pathologischen Frakturen, kommen. Da häufig die Wirbelsäule die erste Aussaatstrecke bildet, sind komplexe neurologische Ausfälle durch Rückenmarksverletzung wie Querschnittsyndrome oder das Cauda-equina-Syndrom nicht selten. Lymphknotenmetastasen können zu Lymphödemen der Beine oder des Hodensacks führen. Insgesamt stellen jedoch Knochenmetastasen für die meisten Patienten die vorherrschende Manifestation der Erkrankung dar und sind auch die hauptsächliche Ursache für die Morbidität und Mortalität des Prostatakarzinoms.[48]
Fortgeschritten metastasierte Tumoren führen in der Regel auch zu Allgemeinsymptomen wie Anämie und ungewolltem Gewichtsverlust.
Diagnostik
Körperliche Untersuchung
Mit der digital-rektalen Untersuchung kann ein erfahrener Untersucher bereits die Verdachtsdiagnose stellen, da der Tastbefund typisch ist. Allerdings werden so die selteneren Tumoren der vorderen Organregionen unter Umständen übersehen und allgemein erst recht fortgeschrittene Stadien erkannt.[49]
Ultraschall
Genauere Lokalisation und Größenbestimmung erlaubt die Ultraschalluntersuchung (transrektale Sonografie). Tumoren ab zehn Millimeter Durchmesser können damit zuverlässig gefunden werden, kleinere jedoch nur zu etwa 20 %.[50]
HistoScanning ist eine ultraschallbasierte, noch nicht abschließend evaluierte Methode, die jedoch auch wesentlich höhere Sensitivität und Spezifität als gewöhnlicher Ultraschall oder digital-rektale Untersuchungen verspricht.[51]
Magnetresonanztomographie
Die Magnetresonanztomographie hat sich dem transrektalen Ultraschall als etwa gleichwertig erwiesen, ist jedoch wesentlich aufwändiger und kostenintensiver in der Durchführung. Der Primärtumor stellt sich in T2-Gewichtung in der MRT als umschriebene dunkle Region mit relativ heller Umgebungszone dar.[50]
Moderne multi-parametrische MRT-Untersuchungen mit Endorektalspule, Diffusion (ADC) oder DTI, Perfusion (DCE) und 1H-Spektroskopie haben eine Sensitivität von gemittelt 86 % und einer Spezifität von 94 %. Negativer Vorhersagewert ist 95 %.[52] Durch die schnell vorangehende Entwicklung der MRT-Technologie sind die Zahlen je nach eingesetzter Technik und Wissensstand des Radiologen potentiell noch deutlich höher. Das multi-parametrische MRT ist somit sehr mächtig und gesundheitlich unbedenklich, jedoch recht aufwändig.[53][54][55]
Positronen-Emissions-Tomographie
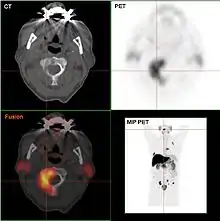
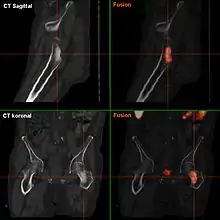
Außerdem etabliert sich immer mehr die Positronen-Emissions-Tomographie (PET) mit 18F-Cholin (radioaktiv markierter Tracer). Vor allem mittels 18F-Cholin-PET/CT kann zuverlässig Prostatakrebs-Gewebe von benigner Hyperplasie, chronischer Prostatitis und gesundem Prostatagewebe differenziert werden.[56][57]
Etablierte Verfahren
Ein oft genutzter Laborparameter in der Prostatakrebsdiagnostik ist das prostataspezifische Antigen (PSA). Es ist spezifisch für die Prostata, allerdings nicht für ein Tumorleiden, sondern kann auch bei Entzündungen zum Beispiel bei einem Harnwegsinfekt, gutartiger Prostatavergrößerung, einem Harnverhalt oder aber auch, teils für mehrere Tage, nach jeder mechanischen Beanspruchung im Beckenbereich, etwa durch Sport, v. a. Fahrradfahren, Sex oder medizinische Maßnahmen, wie digitale-rektale Untersuchung (DRU), transrektale Prostatasonographie, oder Blasenkatheter, erhöht sein. Ein Wert über 4 ng/ml gilt als abklärungsbedürftig. Eine Differenzierung, wenn eine infektiöse Ursache (Prostatitis, Harnwegsinfekt) ausgeschlossen wurde, erlaubt die Bestimmung des komplexierten und freien Anteils des PSA. Liegt der Anteil des freien PSA unter 10 %, ist ein Prostatakarzinom wahrscheinlich, ein Anteil von 10–20 % gilt als Graubereich, bei mehr als 20 % kann man von einer gutartigen Veränderung ausgehen.[58] In der Tumornachsorge nach operativer oder Strahlentherapie ist das PSA der entscheidende Parameter. Dieselbe Bedeutung kommt ihm in der Verlaufskontrolle einer antiandrogenen Behandlung (Hormontherapie) zu.
Die prostataspezifische saure Phosphatase (PAP) hat heute nur noch untergeordnete Bedeutung.
Nicht etablierte Verfahren
Des Weiteren stehen eine Protein-Muster-Diagnostik und der PCA3-Test zur Verfügung, als Material wird Urin verwendet. Beide Verfahren sind nicht etabliert, die Kosten werden in Deutschland üblicherweise von den gesetzlichen Krankenkassen nicht übernommen.[59]
Histologie
Beweisend für ein Prostatakarzinom ist ausschließlich der Nachweis von Krebszellen in einer bioptisch entnommenen Gewebeprobe. Die Biopsie wird transrektal unter Ultraschallkontrolle durchgeführt. Es werden mit einer Hohlnadel mindestens je drei Gewebeproben aus beiden Seiten des Organs entnommen. Bei einer großen Prostata sollte naturgemäß die Zahl der Biopsien höher liegen. Ein Pathologe begutachtet das Prostatagewebe und stellt seine Diagnose.
Der Aussagewert dieser sogenannten Systematischen Biopsie ist jedoch sehr gering. Selbst bei einer Probenanzahl von 12 werden nur etwa 25-50 % der tatsächlichen Krebsfälle entdeckt. Auch eine Erhöhung der Probenanzahl auf 24 erhöht die Rate nur unwesentlich.[60] Zusätzlich ist das Risiko einer falschen Klassifizierung der Gefährlichkeit eines festgestellten Krebsbefalls mit ca. 20-50 % beträchtlich.[61][62]
Diagnostik zur Stadienbestimmung bei nachgewiesener Erkrankung
Falls sich die Diagnose „Prostatakrebs“ bestätigt, ist eine Stadienbestimmung, das sogenannte Staging, erforderlich. Hier wird festgestellt, ob der Tumor bereits ausgestreut hat oder ob es sich um ein auf die Prostata begrenztes Karzinom handelt.
Zu den erforderlichen Untersuchungen gehört eine Ultraschalluntersuchung der Organe des Bauchraumes, insbesondere der Leber, der Nieren und Lymphknoten, sowie eine Röntgenuntersuchung der Lunge. Eine Skelettszintigrafie wird zum Ausschluss von Knochenmetastasen in Abhängigkeit vom PSA-Wert durchgeführt. Zusätzlich können noch eine Computertomographie von Bauch und Lunge sowie eine Ausscheidungsurografie der Nieren mit Kontrastmittel zur Beurteilung des Harnleiterverlaufes und eine Blasenspiegelung erfolgen.
Zur exakten Beurteilung eines organüberschreitenden Wachstums (Stadium T3) bei stanzbioptisch gesichertem Prostatakarzinom hat sich bisher kein bildgebendes Verfahren (CT, MRT mit Endorektalspule, transrektale Ultraschalluntersuchung) etablieren können.
Pathologie und Histopathologie
Stanzbiopsien und Operationspräparate werden von einem Pathologen untersucht.
Makroskopische Pathologie
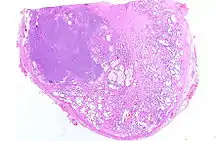
Makroskopisch (mit bloßem Auge) erscheint das Karzinom meist gelb oder weißlich, relativ homogen und unscharf begrenzt. Mehrheitlich geht es von den Epithelien der peripheren Drüsenanteile aus, zu etwa 85 % in den hinteren (rektalen) Anteilen der Vorsteherdrüse und breitet sich in den äußeren Zonen des Organs aus. Zur Verlegung der Harnröhre mit Beschwerden des Harnlassens kommt es daher erst spät, meist nachdem die Organkapsel schon durchbrochen wurde.
Ausgedehnte Karzinome der Stadien T3/T4 können die Samenblasen, die Harnblase, den Beckenboden oder das Rektum infiltrieren. Die Metastasierung ist zunächst lymphogen (über die Lymphbahnen) in die ortständigen Lymphknoten. Häufig erfolgt später eine hämatogene Aussaat (über die Blutbahn). Typisch sind Knochenmetastasen in Becken, Kreuzbein und Lendenwirbelsäule, Oberschenkelknochen, Brustwirbelsäule und Rippen. So ist bei 80 % bis 90 % der Patienten mit einem metastasierenden Prostatakarzinom das Achsenskelett (Wirbelsäule, Becken und Strukturen, die am Rumpf oder nahe am Rumpf gelegen sind) betroffen.[48] Diese sind fast immer osteoblastisch (knochenbildend). Fernmetastasen in Lunge und Leber durch hämatogene Aussaat (über den Blutkreislauf) sind seltener.[63]
Mikroskopische Pathologie
97 % aller Prostatatumoren sind Adenokarzinome, das heißt, sie entstehen aus entarteten Drüsenzellen. Ein Übergangsstadium zum manifesten Krebs wird als prostatische intraepitheliale Neoplasie (PIN) bezeichnet und entspricht einem Carcinoma in situ. Beim eigentlichen Karzinom kommen verschiedene histopathologische Wachstumsmuster vor, auch gleichzeitig nebeneinander: glandulär beziehungsweise azinär (drüsenartig), kribriform (siebartig) und solide. Das Ausmaß der Entdifferenzierung ist Grundlage des Gradings. 40–50 % der Tumoren liegen bei Diagnosestellung multifokal vor.[50]
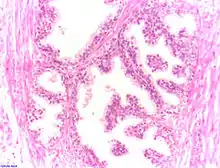 Normales Prostatagewebe
Normales Prostatagewebe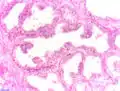 Prostatische intraepitheliale Neoplasie (PIN)
Prostatische intraepitheliale Neoplasie (PIN).jpg.webp) Karzinom vom azinären Typ
Karzinom vom azinären Typ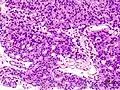 Entdifferenziertes Karzinom
Entdifferenziertes Karzinom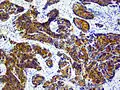 Knochen- und Weichteilmetastase eines Prostatakarzinoms mit immunhistochemischem Nachweis einer PSA-Expression (braun)
Knochen- und Weichteilmetastase eines Prostatakarzinoms mit immunhistochemischem Nachweis einer PSA-Expression (braun)
Die Nicht-Adenokarzinome (weniger als drei Prozent) sind meist urothelialer Herkunft, leiten sich also aus dem Übergangsgewebe der Harnröhre oder -blase ab (siehe Blasenkrebs). Äußerst selten sind Sarkome (Leiomyosarkom, Fibrosarkom, Rhabdomyosarkom) des Stromas beim Erwachsenen. Bei Kindern sind Rhabdomyosarkome die häufigste Form des Prostatakrebses, werden aber nicht wie bei erwachsenen Patienten als Prostatakarzinom aufgefasst, sondern als Weichteilsarkom.[64][65]
Tumorgrad und Gleason-Score
Bei der mikroskopischen Untersuchung des entnommenen Gewebes werden die biologischen Eigenschaften des Tumors genauer bestimmt und seine Bösartigkeit ermittelt. So beschreibt ein besonderes Einordnungsschema (G: Histopathologisches Grading), wie stark sich die Tumorzellen mikroskopisch von normalen, „ausgereiften“ Zellen unterscheiden.
Zum Grading des Prostatakarzinoms wird entsprechend der S3-Leitlinien zur Früherkennung, Diagnose und Therapie des Prostatakarzinoms der Gleason-Score verwendet.[66] Dabei wird nach dem histologischen Bild in der Stanzbiopsie das am schlechtesten differenzierte und das am häufigsten vorkommende Tumorgewebe mit Punktwerten zwischen 1 und 5 (zusammen also zwischen 2 und 10) bewertet und addiert. Bei einer bereits erfolgten Operation wird der häufigste und der am zweithäufigsten vorkommende Gleason-Grad in der gesamten Prostata addiert. Die beiden addierten Gleason-Grade müssen in der richtigen Reihenfolge und in der Stanzbiopsie in Prozent (des Gesamttumors und des gesamten gewonnenen Gewebes) angegeben werden. Ein Gleason-Score 3+4 stellt einen besser differenzierten Grad dar, als Gleason-Score 4+3, obwohl die Summe gleich ist. Ihre Summe wird in der Stanzbiopsie demnach anders interpretiert als im Operationspräparat. Eine Besonderheit ist, dass die Gleason-Grade 1 und 2 in der Stanzbiopsie nicht diagnostiziert werden können.[67]
Der Gleason-Score ist neben der Tumorgröße, dem Vorliegen von Lymphknoten- und Fernmetastasen (TNM-Klassifikation) ein wichtiger Prognosefaktor. Manchmal können zusätzliche Informationen zum Grading (z. B. DNA-Zytometrie) hilfreich sein. Ein Gleason-Score kann nur bei Vorliegen eines nicht vorbehandelten Adenokarzinoms der Prostata erstellt werden, für Urothelkarzinome und neuroendokrine Tumoren wird ein anderes Grading-System benutzt.[66]
DNA-Zytometrie
Bei niedrigem Gleason-Grad kann die als Biopsie entnommene Probe zusätzlich auf den so genannten Ploidiegrad untersucht werden. Dieses Verfahren wird DNA-Zytometrie genannt und von einzelnen urologischen Chefärzten an Kliniken wie auch Pathologen eingesetzt.[68][69] Sie kann im Falle eines niedrigen Malignitätsgrades des Karzinoms weitere Hinweise auf die Aggressivität der Tumorzellen geben und so als Hilfe zur Therapieentscheidung Anwendung finden.[70]
Tumorstadien
Manifestationsstadien
Man unterscheidet nach Mostofi[71] folgende Manifestationsstadien:
| Manifestationsstadium | Beschreibung |
|---|---|
| Manifestes Karzinom | Der Primärtumor verursacht Symptome oder ist klinisch diagnostizierbar (palpabel). |
| Okkultes Karzinom | Die Metastasen werden symptomatisch oder klinisch diagnostizierbar, nicht aber der Primärtumor. |
| Inzidentielles Karzinom | Zufallsbefund bei der Untersuchung oder Operation unter anderer Fragestellung. |
| Latentes Karzinom | Zufälliger Obduktionsbefund bei einem aus anderer Ursache Verstorbenen. |
Staging (TNM-System)
Bei der Beurteilung des Tumorstadiums nach dem TNM-System werden Größe und örtliche Ausdehnung des Prostatatumors (T), Lymphknotenbefall (N, von engl. node ‚Knoten‘) und Metastasen (M) berücksichtigt. Die Ziffern hinter den Buchstaben stehen für Größe und Ausdehnung des Primärtumors (T1-T4), das Vorliegen von befallenen Lymphknoten (N0-N1) sowie das Vorhandensein und die Verteilung von Fernmetastasen (M0-M1c). Ein recht guter Prädiktor für die Entdifferenzierung, die lokale Invasion der Nachbarorgane und die Wahrscheinlichkeit der Fernmetastasierung ist auch die Tumorgröße. Die „Schwelle der Kurabilität“, also die Größe des Tumors, bis zu welcher man eine Behandlung mit der Zielsetzung der Heilung (kurative Behandlung) als möglich erachtet, wird bei 4 cm³ angesetzt. Ist diese Schwelle überschritten, so ist eine Heilung in der Regel nicht mehr möglich. Jedoch können durchaus auch kleinere Tumoren bereits metastasiert sein und sich somit einer kurativen Behandlung entziehen.[50]
| Stadium | Beschreibung |
|---|---|
| Tx | Es kann keine Aussage zur Ausdehnung des Primärtumors getroffen werden. |
| T1 | Der Tumor ist klein und nicht tastbar. Er wird zufällig im Rahmen einer Prostataoperation wegen BPH oder erhöhter PSA-Werte gefunden (Inzidentaltumor). |
| T1a | Der Tumor befällt weniger als 5 % des Gewebes. |
| T1b | Der Tumor befällt mehr als 5 % des Gewebes. |
| T1c | Der Tumor wurde durch eine Nadelbiopsie diagnostiziert. |
| T2 | Der Tumor liegt noch innerhalb der Prostatakapsel. |
| T2a | Der Tumor befällt weniger als 50 % eines Seitenlappens. |
| T2b | Der Tumor befällt mehr als 50 % eines Seitenlappens. |
| T2c | Der Tumor befällt beide Seitenlappen. |
| T3 | Der Tumor hat sich über die Prostatakapsel hinaus ausgebreitet. |
| T3a | Der Tumor hat sich über die Prostatakapsel ausgebreitet, ohne die Samenblasen zu befallen. |
| T3b | Der Tumor hat sich über die Prostatakapsel ausgebreitet und befällt die Samenblasen. |
| T4 | Der Tumor hat Nachbarstrukturen befallen (infiltriert) oder ist fixiert (unverschieblich). |
| Nx | Es kann keine Aussage zu regionären Lymphknotenmetastasen getroffen werden. |
| N0 | Keine Metastasen in den regionären Lymphknoten. |
| N1 | Metastasen in den regionären Lymphknoten. |
| M0 | Keine Fernmetastasen nachweisbar. |
| M1 | Der Tumor hat Fernmetastasen gebildet. |
| M1a | Metastasen in anderen Lymphknoten (nicht regionäre Lymphknoten). |
| M1b | Metastasen in den Knochen. |
| M1c | Metastasen in anderen Organen und/oder Strukturen. |
An der Einordnung in das TNM-Schema orientiert sich die Behandlung. Auch die Prognose kann unter Hinzuziehung weiterer Parameter abgeschätzt werden.
Ein anderes Schema der Stadieneinteilung ist das nach Whitmore-Jewett (modifiziert nach Hopkins). Hier werden die Grade A (mikroskopisches Karzinom, praktisch immer inzidentiell – entspricht T1), B (makroskopisch, auf die Prostata begrenzt – entspricht T2); C (organüberschreitend, auf das kleine Becken begrenzt – entspricht T3/4M0) und D (mit Fernmetastasen – entspricht T1-4M1) unterschieden. Dieses Schema wird im angloamerikanischen Raum bevorzugt, ist aber in Deutschland nicht üblich.
Prognosefaktoren
Wichtigste Faktoren für die Einschätzung der Prognose sind das Tumorstadium nach TNM, der PSA-Blutwert und die Differenzierung des Tumors, der Gleason-Score.
Therapie
Aktive Überwachung, Strahlentherapie oder Operation: Ergebnisse der britischen ProtecT-Studie
Bis vor Kurzem war nicht eindeutig geklärt, ob Operation oder Strahlentherapie als gleichwertig anzusehen sind; es gab keinen direkten Vergleich beider Therapieverfahren. Ferner war unklar, ob eine Behandlung (egal welche) einen Vorteil gegenüber der aktiven Überwachung erbringt. Die in Deutschland zu dieser Frage durchgeführte PREFERE-Studie wurde im Herbst 2016 geschlossen. Fast zeitgleich wurde aber eine britische Studie veröffentlicht (sog. ProtecT-Studie), in der drei Methoden miteinander verglichen wurden, nämlich aktive Überwachung, Operation und Strahlentherapie (Bestrahlung von außen mit Linearbeschleuniger, kombiniert mit sechsmonatiger antihormoneller Therapie).
Wichtige Ergebnisse der ProtecT-Studie sind:
- Aktive Überwachung ist möglich. Es gibt in den ersten zehn Jahren nach Diagnose keine erhöhte Todesrate.
- Allerdings traten bei Patienten, die zunächst nur überwacht und nicht sofort behandelt wurden, vermehrt Metastasen auf. Da dies längerfristig nachteilig ist, sollte man eine Therapie bei jüngeren Patienten und/oder bei Tumoren mit Risikokonstellation prüfen.
- In der Patientengruppe, die zunächst nur aktiv überwacht wurde, musste man innerhalb von zehn Jahren dann doch die Hälfte der Patienten mit Bestrahlung oder Operation behandeln, weil die Krebserkrankung messbar vorangeschritten war. Bei aktiver Überwachung gilt also bezüglich einer weiteren Behandlung: aufgeschoben, aber nicht endgültig aufgehoben.
- Ein wichtiges Ergebnis betrifft den Vergleich von Operation und Strahlentherapie. Beide Verfahren waren hinsichtlich der Beherrschung der Tumorerkrankung gleich gut (im Trend war die Bestrahlung sogar etwas besser). Beide Therapieverfahren wurden gut vertragen; die Nebenwirkungen waren bei Strahlentherapie aber deutlich geringer als bei Operation, obwohl die Bestrahlung noch nicht mit heute üblichen präziseren Bestrahlungstechniken durchgeführt wurde.
Die beiden Originalpublikationen der Studie,[75] eine Zusammenfassung der österreichischen Cochrane,[76] ein Kommentar aus dem New England Journal of Medicine[77] sowie eine Pressemitteilung der Deutschen Gesellschaft für Radioonkologie[78] sind frei verfügbar. Die Aussagen gelten nur für Patienten mit den entsprechenden Kriterien, insbesondere einem Tumor mit weniger aggressiver Einstufung.
Weitere Ergebnisse zur Frage, welche Behandlungsmethode die besten Erfolgsaussichten bietet, stammen aus der 2012 publizierten sogenannten „Grimm-Studie“. In dieser Metaanalyse wurden anhand der Daten von ca. 52.000 Patienten mit lokalisiertem Prostatakarzinom 11 Methoden (operative Verfahren, Bestrahlungsmethoden, HiFu usw.) untersucht und verglichen. Die besten Ergebnisse bei allen drei Risikogruppen lieferte stets ein Bestrahlungsverfahren. Den ausgeprägtesten Vorteil in Bezug auf die langjährige Tumorkontrolle zeigte die Bestrahlung im Vergleich zur Operation bei Patienten mit Hochrisiko-Prostatakrebs.[79]
Operation
Bei lokal begrenztem Prostatakarzinom (T1/2) und guter Konstitution ist die radikale (vollständige) Operation der Prostata, bei der Prostata, Samenbläschen und die regionalen Lymphknoten entfernt werden, die klassische Methode. Diese so genannte „radikale Prostatektomie“ (RPE) kann auf vier unterschiedliche Arten durchgeführt werden:
- als retropubische radikale Prostatektomie (RRP)
- als radikale perineale Prostatektomie (RPP) durch Schnitt am Damm (zwischen After und Hodensack)
- minimalinvasiv – laparoskopisch
- roboterassistiert (RARP)
RRP wird vom Bauch aus durchgeführt, RPP wird extraperitoneal, also ohne Eröffnung der Bauchhöhle, ausgeführt. Die RPP ist weniger zeitaufwändig und mit geringeren Blutungen verbunden als die RRP, aber der Zugang ist relativ schmal. Ein Nachteil ist die fehlende Entfernung der Beckenlymphknoten bei der RPP, so dass ein zweiter Eingriff mittels laparoskopischer pelviner (auf das Becken bezogener) Lymphadenektomie manchmal notwendig ist. Einzelne Zentren haben Techniken publiziert, welche die Lymphknotenentfernung ermöglichen.[80]
Bei der minimalinvasiven Methode wird mittels Bauchspiegelungstechnik über einige kleine Schnitte die Prostata operiert. Vorteil im Vergleich zur „offenen“ Operation ist hier vor allem der zumeist geringere Blutverlust und die kleinen Wunden.
Eine Weiterentwicklung der „minimalinvasiven“ Technik ist die roboterassistierte Prostatektomie. Hier wird mit Hilfe eines Operationsroboters die laparoskopische Technik durchgeführt. Der Roboter wird dabei vom Operateur mittels einer speziellen Konsole fernbedient und führt keine eigenständigen Bewegungen aus. Vorteil für den Operateur gegenüber der Standard-Laparoskopie ist hierbei die nahezu uneingeschränkte Beweglichkeit der Instrumente, die hervorragende Sicht (dreidimensional über ein Doppel-Optik-System) und die Feinheit der Bewegung, da der Roboter etwa das natürliche Zittern der Hand ausgleicht. Nachteil der Robotertechnik gegenüber der „Standard-Laparoskopie“ sind die vergleichsweise hohen Anschaffungs- und Unterhaltskosten für das Krankenhaus, so dass in Deutschland bisher nur wenige Zentren auf diese Technik zurückgreifen können, bei einigen Abteilungen wird eine private Zuzahlung zur Deckung der Materialkosten verlangt, da die Krankenkassen diese derzeit nicht übernehmen. Eine Verbesserung der Operationsergebnisse durch die Robotertechnik konnte bisher wissenschaftlich nicht belegt werden.
Gelingt es bei der Operation, den Tumor vollständig zu entfernen, ist eine Heilung möglich, und die Prognose für ein Langzeitüberleben (fünf Jahre oder mehr) liegt zwischen 80 und 90 Prozent. Gemäß der weltweit größten urologischen Studie (52.000 Patienten) zur Behandlung des lokalisierten Prostatakrebses ist die Operation bei Patienten mit geringem oder mittlerem Risiko der Bestrahlung nach fünf Jahren im Ergebnis geringgradig unterlegen. Den größten Vorteil zeigte die Bestrahlung im Vergleich zur Operation insbesondere bei Patienten, die ein hohes Risiko haben, Metastasen zu entwickeln.[79]
Das Risiko, an der Operation oder ihren Folgen zu versterben, beträgt etwa 1,5 Prozent.[81] Ein relevantes Risiko der Operation ist in erster Linie die Gefahr der langfristigen Harninkontinenz und beträgt je nach Studie zwischen 2 und 40 Prozent.[82] So benötigten etwa in einer britischen Studie aus dem Jahr 2006 27,8 % der Patienten täglich bis zu eine Einlage.[83] Zum Verlust der Erektionsfähigkeit (erektile Dysfunktion) in Folge einer Verletzung der Nervi cavernosi (Äste der parasympathischen Beckeninnervation) kommt es in etwa 80 % der Fälle.[84] Ein trockener Orgasmus ist meist weiterhin möglich[85], eine Studie zeigt, dass 71 % der operierten Männer orgasmusfähig waren.[86] Verletzungen des Nervus obturatorius, die im Rahmen der Lymphknotenentfernung auftreten können, oder des Rektums sind selten. In fünf bis 20 Prozent der Fälle kommt es, bedingt durch die Lymphknotenentfernung, zu einer Lymphozele. Als Spätfolge tritt in etwa 32 % der Fälle eine Verengung der Verbindungsstelle zwischen Harnröhre und Blase (Anastomose) auf, die so genannte Anastomosenstriktur.[81]
Etliche Zentren bieten eine „nerverhaltende“ Operationsmethode (nach Patrick Craig Walsh) an, bei der die kavernösen Nerven, die in unmittelbarer Lagebeziehung zur Prostata verlaufen, geschont werden. Das Risiko der postoperativen erektilen Dysfunktion kann damit auf zehn Prozent (bei jungen Patienten), bis 50 % (bei älteren Patienten) gesenkt werden, der Erfolg ist aber signifikant von der Erfahrung des Operateurs abhängig. Zudem birgt die Technik das Risiko einer zu wenig radikalen Ausräumung des Tumors. Es erhöht sich damit das langfristige Risiko eines Lokalrezidives.
Die Art der angewandten Operationsmethode scheint keinen signifikanten Einfluss auf die onkologischen Ergebnisse (Überlebensrate, rezidivfreies Überleben etc.) des Eingriffs zu haben, vielmehr scheint die jeweilige Erfahrung des einzelnen Operateurs ausschlaggebend zu sein.
Strahlentherapie (Radiatio)
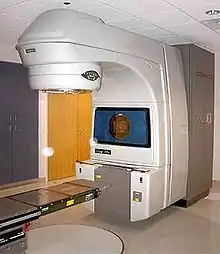
Eine gleichwertige und nebenwirkungsärmere Alternative zur Operation ist bei lokal begrenztem Prostatakarzinom mit niedrigen und mittleren Risikofaktoren (siehe Prognosefaktoren) die alleinige Strahlentherapie. In einer Vergleichsstudie[87] wurden über 1600 Patienten entweder mit radikaler Operation, perkutaner Strahlentherapie oder einer abwartenden Strategie behandelt. Nach einer Nachbeobachtungszeit von zehn Jahren ergab sich kein Vorteil einer Methode bezüglich des krebsspezifischen Überlebens, also der Wahrscheinlichkeit, am Prostatakrebs zu versterben. In der Behandlungsgruppe mit abwartender Strategie zeigte sich eine Verdopplung der Wahrscheinlichkeit des Auftretens von Fernabsiedlungen (Metastasen). Hinsichtlich der für Patienten wichtigsten Nebenwirkungen Inkontinenz und sexueller Funktion (Potenz) resultierte die Prostataoperation häufiger in einer signifikanten Verschlechterung beider Funktionen. Die Strahlentherapie zeigte signifikant häufiger Darmnebenwirkungen. Bezüglich der Lebensqualität ergaben sich keine Unterschiede zwischen den Gruppen.[88]
Die Strahlentherapie ist für verschiedene Gruppen von Patienten anwendbar, etwa nach Wiederauftreten eines operierten Tumors, bei metastasierten Tumoren oder auch als Konkurrenzmethode zur Operation. Sie erfolgt entweder von außen (perkutane Strahlentherapie) oder durch „Spickung“ (Brachytherapie) (von griechisch brachýs = nah) der Prostata mit radioaktivem Material. Die perkutane Bestrahlung wird mittels Linearbeschleuniger durchgeführt. Bei der Brachytherapie unterscheidet man zwischen der Implantation von „Seeds“ (radioaktiven Partikeln kurzer Halbwertszeit, auch „Low-Dose-Rate Brachytherapy“, LDR-Brachytherapie genannt) und dem „Afterloading“ („High-Dose-Rate Brachytherapy“, HDR-Brachytherapie), wobei für eine (mit einem speziellen Planungsprogramm über PC) vorausberechnete Zeit eine radioaktive Quelle in Hohlnadeln, die in dem zu bestrahlenden kranken Gewebe stecken, eingeführt und anschließend wieder entfernt werden. Die HDR-Brachytherapie kann sowohl mit der perkutanen Bestrahlung kombiniert als auch als alleinige Monotherapie angewandt werden. Die LDR-Brachytherapie („Seeds“) kann nicht mit anderen Formen der Bestrahlung kombiniert werden; diese Therapie stellt eine direkte Alternative zur Operation dar. Vorteile der Bestrahlung sind der Wegfall des OP-Risikos und die Möglichkeit einer ambulanten Behandlung. Nachteile sind Nebenwirkungen wie zeitweiliger Durchfall und Verdauungsstörungen.[89][90] Im Rahmen einer Metaanalyse wurde der Einfluss der Brachytherapie alleine oder in Kombination mit perkutaner Bestrahlung in Bezug auf das tumorfreie Überleben als allen anderen damit verglichenen Methoden als überlegen bewertet. Ziel dieser sogenannten „Grimm-Studie“, die 2012 publiziert wurde, war der Vergleich aller damals gängigen Behandlungsmethoden des nicht metastasierten Prostatakarzinomes. Die besten Ergebnisse bei allen drei Risikogruppen wurden jeweils durch die Brachytherapie alleine oder in Kombination erbracht. Den ausgeprägtesten Vorteil in Bezug auf die langjährige Tumorkontrolle zeigte die kombinierte Brachytherapie im Vergleich zur Operation bei Patienten mit Hochrisiko-Prostatakrebs.[79] Kritisiert wurde die Studie dafür, dass neue Verfahren wie z. B. die dosiseskalierte perkutane Bestrahlung[91] oder hypofraktionierte Protonentherapie,[92] die mittlerweile zumindest äquivalente Ergebnisse erbrachten, nicht in die Metaanalyse aufgenommen wurde. Um den Stellenwert der Operation im direkten Vergleich mit Bestrahlungsverfahren erneut zu ermitteln, wurde 2013 die sogenannte „PREFERE“-Studie aufgelegt,[93] die 2016 jedoch abgebrochen werden musste.
Bei einer geringen Zahl von Patienten treten nach Strahlentherapie eines Prostatakarzinoms bleibende Schädigungen von Darm (Radioproktitis, Radiocolitis) und Harnblase (Radiocystitis) auf. Auch ein Verlust der Gliedsteife (erektile Dysfunktion) sowie eine Störung der Schließmuskelfunktion des Afters oder der Harnblase ist bei wenigen Patienten nach Bestrahlung eines Prostatakarzinoms beobachtet worden.[94][95] Die Strahlenbelastung angrenzender Organe kann durch den Einsatz sogenannter Goldmarker gesenkt werden, so dass auch das Risiko von Nebenwirkungen reduziert wird. Diese vor Beginn der Strahlentherapie in der Prostata abgelegten drei „Seeds“ erlauben es, die Prostata bei jeder Bestrahlungssitzung indirekt zu lokalisieren (sogenannte Image Guided Radio Therapie, IGRT), so dass eine gezieltere Bestrahlung mit einem geringeren „Sicherheitssaum“ möglich ist. Hierbei handelt es sich bisher jedoch um eine individuelle Gesundheitsleistung.
Ein neues Therapieverfahren ist die Hochpräzisionsbestrahlung der Prostata. Dabei wird die gesamte Strahlendosis in nur fünf Behandlungssitzungen über einen Zeitraum von etwa anderthalb Wochen verabreicht. Die US-Fachgesellschaft für Strahlentherapie (ASTRO) sieht diese Methode bereits als eine Alternative zu den Standardverfahren an.[96] In Deutschland wird diese Therapie aktuell in einer vom Bundesamt für Strahlenschutz genehmigten klinischen Studie an den Universitätskliniken Kiel, Lübeck, Rostock und Frankfurt angeboten und mit dem Bestrahlungsroboter Cyberknife (in Kooperation mit Saphir Radiochirurgie) durchgeführt.[97][98]
Wenn zum Zeitpunkt der Diagnose bereits eine Absiedelung in andere Organe stattgefunden hat, ist die Erkrankung meist nicht mehr heilbar. Durch Strahlentherapie kann hier jedoch zumindest die Ausbreitung des Krebses verzögert werden. Hier findet vor allem die Bestrahlung von Knochenmetastasen ihre Anwendung, die gefährdete Knochenbezirke stabilisiert und somit erheblich zur Mobilität und Schmerzfreiheit bei Patienten mit metastasierten Tumoren beiträgt.
Protonentherapie
Eine neue Form der Strahlentherapie ist die Behandlung mit Protonen. Hierbei nützt man das physikalische Phänomen des bragg peak, bei der die Strahlenenergie nur an einer vorbestimmten Stelle im Körper abgegeben wird. Der Vorteil der Protonentherapie liegt in der Genauigkeit wirksam den Krebsherd zu behandeln und dennoch dicht angrenzendes gesundes Gewebe zu schonen. Im März 2014 wurden erstmals 5-Jahres-Langzeitergebnisse der Protonenbestrahlung bei Prostatakrebs publiziert. Insgesamt wurden in den drei hier zusammengefassten Studien 211 Patienten mit nicht-metastasierten Prostatakrebs mit Protonen behandelt und über einen Zeitraum von durchschnittlich über 5 Jahren (5,2 Jahre) nachbeobachtet. Die Tumorkontroll-Rate nach fünf Jahren (cPFS) betrug bei Prostatakarzinom mit niedrigem Risiko und mit mittlerem Risiko jeweils 99 %, bei Prostatakarzinom mit hohem Risiko 76 %. Die Rate an schweren Nebenwirkungen gemäß internationaler Einteilungsrichtlinie CTCAE Version 3.0 (bzw. aktueller Version 4.0) lag am Darm (z. B. Blutung des Enddarmes) bei 1 % (0,5 %), am Harntrakt (z. B. Inkontinenz) bei 5,4 % (1 %).[92]
Prostata-Rektum-Hydrogel-Abstandshalter
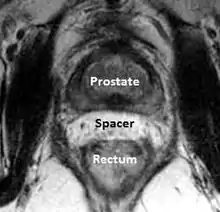
Bei Prostatakrebs ist eine Strahlentherapie, die entweder in Form einer Brachytherapie oder externen Strahlentherapie durchgeführt wird, eine der am häufigsten gewählten Behandlungsmethoden.
Obwohl die Strahlentherapie bei Prostatakrebserkrankungen im Vergleich zu anderen Behandlungsmethoden bessere Erfolge zeigt, birgt die Verletzung des Rektums durch die Bestrahlung (strahleninduzierte Proktitis) eine Gefahr, da sich das Rektum unmittelbar hinter der Prostata befindet. Die durch Strahlen ausgelöste Schädigung des Rektums kann zu Diarrhoe, rektalem Druck, zur Schleimhautproduktion und zu Blutungen führen. Bis zum Auftreten dieser Symptome kann es sechs bis zwölf Monate dauern. Die Symptome können jedoch zu jedem Zeitpunkt bis zu 30 Jahren nach der Bestrahlungstherapie auftreten.[99][100]
Eine aufkommende Strategie zur Minderung dieser rektalen Schädigung ist die Platzierung eines Abstandshalters zwischen diesen beiden Strukturen, wodurch das Rektum auf wirkungsvolle Art und Weise vom hochdosierten Strahlenfeld weggedrückt wird. Forschern war es möglich, diese Abstandshalter herzustellen, indem sie verschiedene Materialien in dem potenziellen Raum zwischen der Prostata und dem Rektum platzierten.
Die Injektion von Hyaluronsäure in den Raum zwischen Prostata und Rektum führte zu einem zusätzlichen Raum von mehr als einem Zentimeter ohne Beschwerden durch Tenesmen oder das Gefühl einer rektalen Füllung. Bei Patienten, die mit Hyaluronsäure behandelt wurden, traten im Vergleich zu Patienten, die keinen Abstandshalter aus Hyaluronsäure erhalten hatten, bei proktoskopischen Untersuchungen deutlich seltener rektale Schleimhautbeschädigungen (5 % vs. 36 %, p = 0,002) und keine makroskopischen rektalen Blutungen (0 % vs. 12 %, p = 0,047) auf.[101] Eine ähnliche Studie wurde mittels Collageninjektionen in den gleichen Raum durchgeführt. Mit dieser Methode schuf man einen Raum von durchschnittlich 1,1 cm zwischen der Prostata und dem anterioren Rektum, was zu einer mehr als 50-prozentigen Minderung der rektalen Strahlungsdosis während der Strahlentherapie an der Prostata führte.[102]
Forscher bewerteten einen absorbierbaren Ballon, der in den Raum zwischen Prostata und Rektum eingesetzt wurde, und ermittelten einen beinahe zwei Zentimeter großen Raum mit einer errechneten Reduktion der rektalen Bestrahlung.[103] Untersuchungen von in gleichem Raum injiziertem, absorbierbarem Hydrogel (das sich derzeit in den USA in der Phase der klinischen Erprobung befindet), resultierten in einem zusätzlichen Raum von einem Zentimeter mit einer Minderung der rektalen Strahlung (V70) von 60 %.[104][105]
Obwohl sich die Prostata-Rektum-Abstandshalter noch in der Phase der klinischen Erprobung befinden, besteht ein vielversprechendes Potenzial dahingehend, dass sie nicht nur zur Minderung unbeabsichtigter rektaler Strahlenaussetzung und der daraus resultierenden Komplikationen beitragen, sondern außerdem höhere Dosierungen bei der Strahlentherapie von Krebspatienten ermöglichen. Somit kann die Überlebensrate der Patienten verbessert werden.[106] Zusätzlich kann durch eine höhere Dosierung pro Behandlung eine vollständige Behandlung mit weniger Arztbesuchen realisiert werden, was zum einen angenehmer für den Patienten ist und zum anderen zu erheblichen Einsparungen der medizinischen Kosten führt.[107]
Im Gegensatz zu den USA, in denen sich das Hydrogel noch in der klinischen Erprobung befindet, ist das Hydrogel in Europa bereits CE-zertifiziert und in einigen Ländern auf dem Markt erhältlich.
Hochintensiver fokussierter Ultraschall
Ein seit 1996 in Deutschland angewandtes Verfahren ist der hochintensive fokussierte Ultraschall (HIFU). Die Methode beruht darauf, dass die gesamte Prostata vom Enddarm aus mit gerichteten Ultraschallwellen erhitzt und das Karzinom damit zerstört wird. Dazu wird der Schallkopf in das Rektum eingeführt. Die Behandlung erfolgt in einer Sitzung, der Krankenhausaufenthalt beträgt nur drei bis fünf Tage. In mehreren Studien mit Nachbeobachtungszeiten von mittlerweile bis zu zehn Jahren wurden die Effektivität und die Sicherheit des Verfahrens nachgewiesen. Die HIFU-Therapie wird von mehr als 30 Zentren in Deutschland angewandt, die Behandlungskosten werden von den gesetzlichen Krankenkassen im Rahmen des DRG-Systems übernommen. Das Verfahren ist sowohl kurativ als auch palliativ einsetzbar. Im Gegensatz zu strahlentherapeutischen Verfahren ist es im Rezidivfall wiederholbar, es stellt also keine „therapeutische Sackgasse“ dar. Aufgrund der geringen Belastung für den Patienten eignet sich HIFU besonders auch für ältere Patienten sowie für die Patienten, die neben dem Krebs noch an weiteren schweren Erkrankungen leiden. Nach der aktuellen S3-Leitlinie zum Prostatakarzinom (Version 2.0, 1. Aktualisierung 09.2011) ist allerdings die „… HIFU-Therapie beim lokal begrenzten Prostatakarzinom ein experimentelles Verfahren. Die HIFU-Therapie soll nur im Rahmen von prospektiven Studien angewendet werden.“
Therapie mit HIFU wird seit August 2017 erstmals auch in Österreich, am Klinikum Wels, angeboten.[108]
Hormontherapie
Die Hormontherapie, die auch als Androgen-Deprivations-Therapie bezeichnet wird, basiert auf der meist vorhandenen Abhängigkeit des Prostatakarzinoms vom Testosteron. Sie wird eingesetzt als palliative Therapie bei metastasierten Tumoren oder ergänzend zu anderen Therapiemaßnahmen wie z. B. einer Strahlentherapie. Eine Hormontherapie in Form eines Hormonentzuges kann als (meist reversible) chemische Kastration durch Gabe von GnRH-Agonisten oder -Antagonisten durchgeführt werden. Ziel ist es, den Testosteronspiegel auf unter 50 ng/dl abzusenken. Da das Prostatakarzinom meist stark testosteronabhängig ist, kommt es bei beiden Verfahren meist zu einem deutlichen Rückgang bzw. Stillstand der Krankheit, so dass der Patient oft über Jahre keine karzinombedingten Beschwerden hat. Bei der chemischen Kastration mittels GnRH-Agonisten kann ein sogenanntes Flare-up-Phänomen entstehen, ein kurzzeitig stark beschleunigter Krankheitsverlauf, bedingt durch einen kurzzeitigen Anstieg des Testosterons. Dieser kann durch die kurzzeitige Gabe von Antiandrogenen wie Cyproteronacetat unterbunden werden, was insbesondere bei ausgeprägter Metastasierung zu empfehlen ist. Aktuelle Studiendaten liefern Hinweise darauf, dass die Therapieoptionen bei Patienten mit kardiovaskulären Erkrankungen sorgfältig abgewogen werden sollten. Darüber hinaus gibt es Studien, die gezeigt haben, dass GnRH-Antagonisten gegenüber den GnRH-Agonisten mit einem deutlich geringeren Risiko für kardiovaskuläre Erkrankungen einhergehen.[109][110]
Als Nebenwirkungen bei beiden Kastrationsverfahren kommt es meist zu Testosteronmangelsymptomen, unter anderem kann es zu Hitzewallungen, zu depressiven Zuständen, zu Anämie, Muskelabbau und als Langzeitwirkung zu Osteoporose kommen, wobei bei Orchiektomie sowohl die psychischen Belastungen durch die irreversible chirurgische Kastration als auch die Osteoporose durch das nicht gleichzeitig supprimierte Hormon LH stärker in Erscheinung treten. Außerdem kommt es zur erektilen Dysfunktion, die meist als nicht allzu schlimm empfunden wird, da auch die Libido nachlässt. Um diese therapiebedingten Nebenwirkungen zu minimieren, kann bei einigen Patienten die intermittierende Hormonblockade (intermittierende Androgendeprivation) zur Anwendung kommen, das heißt, therapiefreie Intervalle werden bewusst eingeplant.[111][112] Eine weitere Alternative für ausgesuchte Patienten ist die alleinige Gabe eines Antiandrogens. Im Laufe der Therapie kann eine Kastrationsresistenz des Prostatakarzinomes eintreten, das heißt, trotz eines auf unter 50 ng/dl unterdrückten Testosterons kommt es zu einem Fortschreiten der Erkrankung.
Der unkritische Einsatz der Hormontherapie als alleinige Therapie des lokalisierten, also nicht metastasierten Prostatakarzinoms führt nicht zu einer Lebensverlängerung.[113]
Chemotherapie
Die Chemotherapie galt beim Prostatakrebs lange als wenig wirksam. Einige Patienten (responder) mit metastasiertem Prostatakarzinom können jedoch von einer Chemotherapie profitieren. Die Ansprechrate liegt bei etwa 20 %. Zumeist hat die Chemotherapie ihren Platz bei der Behandlung des Tumorrezidivs und versagender Hormontherapie (sogenanntes kastrationsresistentes Prostatakarzinom). Auch sie ist bisher rein palliativ. Angewendete Therapeutika sind Cyclophosphamid, Doxorubicin (Adriamycin), 5-Fluoruracil, Suramin und andere; für diese konnte jedoch bisher kein Überlebensvorteil gezeigt werden. In einer 2004 in der renommierten Zeitschrift The New England Journal of Medicine publizierten Arbeit konnte erstmals ein statistisch signifikanter Überlebensvorteil von median 2,5 Monaten für diejenigen Patienten nachgewiesen werden, welche alle drei Wochen das Medikament Docetaxel erhielten.[114] Eine erstmals 2014 auf der Jahrestagung der American Society of Clinical Oncology. (ASCO) in Chicago vorgestellte, 2015 ebenfalls im New England Journal of Medicine. publizierte Studie zeigte auch bei Patienten mit einem metastasierten, hormonsensitiven Prostatakrebs einen Überlebensvorteil durch eine frühzeitige Docetaxel-Chemotherapie.[115]
Im Jahr 2011 wurden in Deutschland neue Medikamente zugelassen, die in Phase-III-Studien gute Erfolge für Patienten mit fortgeschrittenem kastrationsrefraktären Prostatakarzinomen auch nach Gabe einer Docetaxel-basierten Chemotherapie zeigten: Cabazitaxel (Handelsname Jevtana), zugelassen am 17. März 2011 sowie Abirateron (Zytiga), zugelassen am 5. September 2011. Weitere Medikamente sind aktuell in Entwicklung. Enzalutamid wurde im Juni 2013 unter dem Handelsnamen Xtandi in Europa zugelassen.[116][117] Sowohl Enzalutamid als auch Abirateron sind inzwischen auch zur Anwendung vor einer Chemotherapie im kastrationsresistenten Stadium zugelassen.
Streng genommen handelt es sich bei diesen beiden Medikamenten nicht um Chemotherapeutika, sondern um Präparate mit einer antiandrogenen Wirkung, also eine Form der Hormontherapie.
Palliativtherapie
Im fortgeschrittenen Stadium, das keine kurative (heilende) Behandlung mehr erlaubt, können dennoch medizinische Maßnahmen die Beschwerden lindern und die Lebensqualität auf einem passablen Niveau halten. Bisphosphonate, wie beispielsweise Zoledronat, haben sich als wirksam erwiesen, um osteoporotische Veränderungen im Zuge der antiandrogenen Therapie ebenso wie durch Skelettmetastasen hervorgerufene Frakturen zu reduzieren.[118] Zur Linderung der Knochenschmerzen werden Opioide wie Morphin oder Oxycodon eingesetzt. Durch die äußere Bestrahlung von Knochenmetastasen können ebenfalls für einige Zeit die Schmerzen reduziert werden. Die Injektion bestimmter Radioisotope, wie Strontium-89, Phosphor-32, Samarium-153 oder Radium-223 (Alpharadin, Xofigo),[119] die sich in stoffwechselaktiven Knochenmetastasen anreichern, hat einen ähnlichen Effekt (siehe Radionuklidtherapie von Knochenmetastasen).
Aktives Beobachten
Unter bestimmten Umständen kann eine Strategie des „aktiven Beobachtens“ (engl. active surveillance) in Betracht kommen.[120] Daneben kommt watchful waiting, „Beobachten und Abwarten“, zur Anwendung. Definitionsgemäß hat Active Surveillance bei ansonsten gesunden und für eine kurative Therapie geeigneten Patienten das Ziel, unter genauer Überwachung einschließlich regelmäßiger Kontrollbiopsien die rechtzeitige kurative Behandlung bis zu einem Zeitpunkt aufzuschieben, an dem sich möglicherweise die Tumorbiologie oder der Wunsch des Patienten ändern. Als sekundäre Behandlung wird dann in den meisten Fällen die radikale Prostatektomie gewählt (48 %). Demgegenüber werden Patienten unter Watchful Waiting erst bei einer symptomatischen Progression palliativ behandelt.
Faktoren, die aktives Beobachten sinnvoll erscheinen lassen, sind beispielsweise das Alter des Patienten, der sonstige Gesundheitszustand und der mit Methoden der DNA-Zytometrie gemessene so genannte Ploidiegrad, ein Kennwert für die chromosomale Veränderung der Krebszellen, der auch gut als Verlaufskontrolle geeignet ist. Die DNA-Zytometrie ist eine sehr preiswerte Methode, die von den Krankenkassen bezahlt wird, und aus allen Arten von Biopsien (Stanzbiopsie und nebenwirkungsarmer Feinnadel-Aspirationsbiopsie, kurz FNAB) gemacht werden kann. Die einfachste Methode der Verlaufskontrolle ist die regelmäßige Ermittlung der PSA-Verdopplungszeit.
Patienten, die eine Perspektive des aktiven Beobachtens verfolgen, versuchen, das Fortschreiten eines Karzinoms aktiv, beispielsweise durch die Einnahme von Nahrungsergänzungsmitteln, zu verlangsamen. Von ärztlicher Seite werden diese Bestrebungen teils sehr kritisch beobachtet und als „Vabanquespiel“ bezeichnet, andererseits aber auch unterstützt, um eine so genannte Übertherapie zu vermeiden.
Die Patienten, die sich für die Methode des active surveillance entscheiden, wägen Nebenwirkungen und Nutzen einer frühzeitigen, invasiven Therapie (OP, Bestrahlung) ab. Durch aktives Beobachten unter Aufsicht eines Arztes können immer noch rechtzeitig kurative Schritte unternommen werden, wenn diese aufgrund eines Fortschreitens der Krankheit nötig werden sollten. Ein aktuelles Review von Weißbach und Altwein kommt zu folgender Schlussfolgerung: 88 gesichtete Studien zum active surveillance belegen konsistent hohe tumorspezifische Überlebensraten (99–100 %) bei Behandlung durch aktives Beobachten.[121] Alle sieben recherchierten Leitlinien zur Behandlung des Prostatakarzinoms seit 2006 erwähnen in ihren Empfehlungen das aktive Beobachten als Therapieoption für PCa mit geringem Progressionsrisiko. Das National Institute for Health and Clinical Excellence (in Großbritannien) empfiehlt in diesem Fall sogar ausschließlich „active surveillance“ als Behandlungsstrategie.[122]
Die Prognose beim aktiven Beobachten kann unter geeigneten Umständen derjenigen unter den üblichen Therapien entsprechen, ohne dass die Nebenwirkungen der anderen Prostatakrebsbehandlungen in Kauf genommen werden müssen. Wenn diese Strategie erfolgreich ist, verstirbt der Patient mit und nicht an seinem Karzinom.
Irreversible Elektroporation
Mit der Technologie der irreversiblen Elektroporation (IRE) ist eine nicht-thermische, gewebeselektive Ablation bei Prostatakarzinomen möglich. IRE kann dabei sowohl fokal als auch großflächig eingesetzt werden. Potentiell sind aufgrund der intrinsischen Gewebeselektivität der Technik Potenzerhalt und Kontinenzerhalt sehr wahrscheinlich. Auch kann IRE potentiell bei komplizierten Rezidiven – selbst nach radikalen Prostatektomien und Strahlentherapien – eingesetzt werden. Nekrose tritt physikalisch bedingt nicht auf, wodurch auch keine Schmerzen oder intraprostatäre Vernarbungen oder Entzündungen zu erwarten sind.[123] Die erste Studie bezüglich des Einsatzes von IRE für die Prostata stammt aus dem Jahr 2007.[124] Somit ist das Verfahren noch sehr neu. Es existieren dafür noch keine Langzeitdaten. Auch die Anzahl verfügbarer Studien diesbezüglich ist bisher dünn. Prostatakrebsbehandlungen mit IRE werden in Deutschland von Universitätskliniken und einem Privatinstitut durchgeführt und weiterentwickelt.[125] Gesetzliche Krankenkassen übernehmen die Behandlungskosten bisher nicht (Stand März 2013).
Photodynamische Therapie
Photodynamische Therapie (PDT) ist eine sich gerade in der Erprobung befindende Therapie. Der Grundgedanke ist, den Photoeffekt zwischen dem von Lasern erzeugten Licht und einem lichtempfindlichen, sich nur an Krebs anreichernden Chemotherapeutikum (Photosensibilisator) zu nutzen, um einen lokalen zytotoxischen Effekt hervorzurufen. Freigesetzt wird ein 1O2, das direkt Tumorzellen durch Nekrose und/oder Apoptose töten kann. WST-11 und 5-ALA sind zwei sich im Versuchsstadion befindliche Photosensibilisatoren.
Vorteile dieser Methode sind: Wiederholbarkeit, vermutlich geringe Kosten, echte Zellselektivität, minimaler lokaler Schaden. Nachteile sind: Bisher unbekannte Nebenwirkungen der Chemotherapeutika, unbekannter Einfluss der möglichen Tumorhypoxytät.[126]
Immuntherapie
Ein neuer therapeutischer Ansatz ist die „Impfung“ mit antigenpräsentierenden Zellen, die mit einem rekombinanten Fusionsprotein (PA2024) beladen werden und die körpereigene Immunantwort stimulieren. Versuche finden derzeit mit einigem Erfolg bei Patienten mit androgen-unabhängigem Prostatakarzinom statt. Diese Patienten konnten bisher nur schwer behandelt werden, da sie auf eine Hormontherapie nicht ansprechen. Die meist gut verträgliche immuntherapeutische Behandlung (Krebsimmuntherapie) führte im Rahmen der Studien zu signifikanten Remissionen und zur Verlängerung der Überlebenszeit.[127] Diese Behandlung ist in Deutschland noch nicht zugelassen.
Nachsorge
Nach den „Patientenleitlinien“ sind Nachuntersuchungen wie folgt vorzunehmen: Im ersten und zweiten Jahr alle drei Monate; im dritten und vierten Jahr alle sechs Monate und ab dem fünften Jahr jährlich. Dies umfasst vor allem regelmäßige Kontrollen des PSA-Wertes. Bildgebende Verfahren werden nur bei entsprechendem klinischem Verdacht auf ein Tumorrezidiv oder eine Krankheitsprogression eingesetzt.
Prognose und Auswirkungen auf die Lebenserwartung
Die Prognose des Prostatakarzinoms ist für eine bösartige Geschwulst beziehungsweise eine Krebserkrankung relativ günstig. Zumindest im lokalisierten Stadium (es wird hier auch illustrierend vom „Haustierkrebs“ gesprochen) ist die Lebenserwartung kaum verkürzt. Man nimmt an, dass letztlich weniger als ein Fünftel der an Prostatakrebs Erkrankten auch an ihm versterben, also die Letalität weniger als 20 % beträgt. Grund hierfür ist die späte Manifestation und die zu diesem Zeitpunkt meist bestehende Komorbidität. In einer Studie konnte gezeigt werden, dass im lokalisierten Stadium die Prognose beim Zuwarten (siehe dazu den Abschnitt „Aktives Beobachten“) nicht schlechter ist als bei sofortiger Therapie.[128] Die hohe Mortalität ist somit vor allem auf die auffallend hohe Prävalenz im höheren Lebensalter zurückzuführen.
Das diagnosespezifische Fünfjahresüberleben nach Diagnosestellung liegt bei Tumoren, die auf die Drüse begrenzt sind, bei 80 bis 99 %.[129] Bei gestreuten Tumoren liegt dieser Wert jedoch mit etwa 30 % deutlich niedriger.[130] Die Aussicht auf Heilung (also darauf, alle Krebszellen zu zerstören) ist nur bei nicht metastasierten Karzinomen gegeben und dort unter aggressiver Therapie recht gut: Auf die Prostata begrenzte Karzinome können zu fast 90 %, die Organkapsel überschreitende zu etwa 50 % definitiv geheilt werden. Bei einem lokal begrenzten Prostatakarzinom liegt die Heilungschance bei etwa 70 %.[131] Zur genaueren Abschätzung der Prognose dienen die so genannten Partin-Tabellen,[132] bei denen eine Kombination aus PSA-Wert, Gleason-Score und T-Stadium zur Prognoseeinschätzung herangezogen wird.
Die hier gemachten Aussagen gelten für das Adenokarzinom der Prostata. Die seltenen neuroendokrinen und kleinzelligen Prostatakarzinome haben eine deutliche schlechtere Prognose mit einer Überlebenszeit von durchschnittlich einem Jahr.
Früherkennung
Zur Früherkennung werden vor allem Abtasten, PSA-Test und Ultraschall angeboten. Das Abtasten ist eine Kassenleistung. PSA-Test und Ultraschall übernehmen die gesetzlichen Krankenkassen nur bei einem Krebsverdacht oder bei Beschwerden, die auf Prostatakrebs hindeuten.
PSA-Tests und Ultraschall-Untersuchungen zur Früherkennung von Prostatakrebs sind keine Leistung der gesetzlichen Krankenkassen. Viele Arztpraxen bieten sie jedoch als individuelle Gesundheitsleistung (IGeL) an. Wegen der unsicheren Ergebnisse, unnötiger Verunsicherung der Patienten und dem Risiko der Überdiagnostik und Überbehandlung empfehlen die maßgeblichen medizinischen Fachgesellschaften Untersuchungen zur Früherkennung ausdrücklich nicht, sondern nur die Information der Patienten – mit Vor- und Nachteilen – dass solche Untersuchungen möglich sind. Für die Hausarztpraxis wird sogar empfohlen, dass die Ärzte diese Möglichkeit nicht von sich aus ansprechen, sondern nur dann, wenn ein Patient einen entsprechenden Wunsch äußert.[133]
Im Dezember 2019 veröffentlichte das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) einen Vorbericht unter der Überschrift: Prostatakrebsscreening mittels PSA-Test. Darin wurden folgende Schlussfolgerungen gezogen:
„Das Prostatakarzinomscreening mittels PSA-Test schadet deutlich mehr Männern durch Überdiagnosen, als es Männern nutzt. Daher wird zusammenfassend festgestellt, dass der Nutzen des Prostatakarzinomscreenings mittels PSA-Test den Schaden nicht aufwiegt.“[134]
Auch der transrektale Ultraschall zur Früherkennung von Prostatakrebs ist in Deutschland eine sogenannte Individuelle Gesundheitsleistung und muss von den gesetzlichen Krankenkassen nicht bezahlt werden. Der IGeL-Monitor des Vereins Medizinischer Dienst des Spitzenverbandes Bund der Krankenkassen hat diese Leistung mit „tendenziell negativ“ bewertet. Der Grund: Man habe in der systematischen Literaturanalyse keine Studien gefunden, die Nutzen und Schaden des Ultraschalls zur Prostatakrebs-Früherkennung untersucht hätten.[135]
In einem Interview mit dem Deutschlandfunk (Ausstrahlung am 4. Januar 2006) wies Robert Allan Weinberg, Krebsforscher am Whitehead-Institut für biomedizinische Forschung in Cambridge bei Boston, darauf hin, dass in den Vereinigten Staaten sechsmal häufiger Prostatakrebs diagnostiziert werde als in Dänemark. Die Sterblichkeit sei in beiden Ländern jedoch gleich hoch.[136]
Das National Cancer Institute der USA hat folgende Statistik für Prostata-Screening vorgelegt (Stand: Dezember 2015):[137] Wenn 1000 Männer im Alter zwischen 55 und 69 Jahren zehn Jahre lang im Abstand von ein bis vier Jahren einen PSA-Test vornehmen lassen, dann
- werden 100–120 Männer einen falsch positiven Befund erhalten, der möglicherweise Ängste und weitere diagnostische Maßnahmen zur Folge hat;
- werden 110 Männer einen positiven Befund (eine korrekte Diagnose) für Prostatakrebs erhalten;
- werden 4–5 der Männer mit korrekt diagnostiziertem Prostatakrebs trotz des Screenings innerhalb der Zehn-Jahres-Frist an den Folgen des Prostatakrebs’ sterben;
- wird im besten Fall ein Todesfall aufgrund des Screenings verhindert;
- werden mindestens 50 der gescreenten Männer Komplikationen aufgrund der Behandlungen entwickeln, darunter erektile Dysfunktion, Inkontinenz und – seltener – Herz-Kreislauf-Erkrankungen
Geschichte
Der älteste bisher nachgewiesene Fall eines metastasierten Prostatakarzinoms wurde anhand von typischen Knochenveränderungen bei einem 2700 Jahre alten Skelett eines Skythen-Fürsten in Sibirien diagnostiziert. Entdecker waren Forscher der Universität Göttingen um Michael Schultz.[138]
Die Vorsteherdrüse wurde zuerst von dem venezianischen Anatom Niccolò Massa im Jahr 1536 beschrieben. Die erste Illustration veröffentlichte Andreas Vesalius zwei Jahre später. Trotzdem war das Prostatakarzinom bis 1853 unbekannt.[139] Aufgrund der schlechten diagnostischen Optionen und der geringeren allgemeinen Lebenserwartung galt es im 19. Jahrhundert als seltene Krankheit. Die ersten Orchiektomien waren schon um 1890 versucht worden, allerdings mit bescheidenem Erfolg. Die ersten operativen Eingriffe an der Drüse selbst zielten auf Verbesserung des Wasserlassens bei Harnröhrenobstruktion. So wurde die erste radikale Prostatektomie 1904 von Hugh Young im Johns Hopkins Hospital durchgeführt.[140] Mitte des 20. Jahrhunderts wurde die palliative transurethrale Resektion (via Harnröhre) zur Behebung der Harnröhrenobstruktion eingeführt. Die radikale retropubische Prostatektomie wurde 1983 von Patrick Craig Walsh entwickelt.
1941 veröffentlichte Charles Brenton Huggins seine Studienergebnisse, in denen er (chemisch gekoppelte) Östrogene einsetzte, um bei Patienten mit inoperablem Karzinom die Testosteron-Produktion zu hemmen.[141] Die Entdeckung dieser „chemischen Kastration“ brachte ihm 1966 den Nobelpreis für Physiologie oder Medizin ein.
Die Strahlentherapie wurde im frühen 20. Jahrhundert entwickelt und bestand zunächst aus der Einpflanzung von Radium-Implantaten. Die perkutane Bestrahlung wurde seit Mitte des Jahrhunderts durchgeführt. Die erste Beschreibung der Brachytherapie stammt aus dem Jahr 1983.
Veterinärmedizin
Bei Haustieren sind Prostatatumoren wesentlich seltener zu finden als beim Menschen. Bei Katzen sind bisher nur fünf Fälle dieser Erkrankung beschrieben worden. Am relativ häufigsten erkranken Hunde. Hier sind etwa 0,2–0,6 % aller Neubildungen Tumoren der Prostata. Unter den Neoplasien der männlichen Harn- und Geschlechtsorgane beim Hund liegt der Anteil bei sechs Prozent. Bevorzugt erkranken Hunde mittelgroßer bis großer Rassen mit einem Altersdurchschnitt von acht bis zehn Jahren. Eine Kastration bewirkt keinen Rückgang der Erkrankungshäufigkeit; es gibt vielmehr Hinweise, dass die Erkrankung bei kastrierten Rüden häufiger auftritt.[142] Die Erkrankung ist differentialdiagnostisch vor allem von der wesentlich häufiger auftretenden gutartigen Prostatavergrößerung des Hundes abzugrenzen. Ein Tumor der Prostata ist beim Hund fast immer eine bösartige Neubildung, in den meisten Fällen handelt es sich wie beim Menschen um Adenokarzinome. Kastrierte Rüden weisen dagegen bei etwa 50 % der Fälle undifferenzierte Karzinome auf. Als weitere bösartige Neoplasien sind Plattenepithelkarzinome, Übergangsepithelkarzinome und Leiomyosarkome sporadisch beschrieben worden. Lediglich Einzelfälle stellen gutartige Fibrome, Adenome oder Leiomyome dar. Entsprechend ihrem aggressiven Charakter liegen zum Zeitpunkt der Diagnosestellung in 70 bis 80 % der Fälle bereits Metastasen vor. Die Verschleppung der Tumorzellen erfolgt über die Lymphbahn und betrifft in 66 % der Fälle die Lunge. Dieser Verlauf scheint bei kastrierten Rüden häufiger zu sein als bei intakten. Außerdem sind von Metastasen die Lymphknoten im Beckenbereich sowie Leber, Milz, Herz, Nieren, entferntere Lymphknoten, Knochen und die Nebennieren betroffen.
Symptome
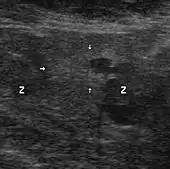
Das klinische Erscheinungsbild der Erkrankung ist variabel. Kotabsatzstörungen wie Tenesmus oder Obstipation treten wesentlich häufiger als Beschwerden bei der Miktion auf. Die Neubildung kann Schmerzsymptome im Bereich der Hinterhand hervorrufen, die bei Metastasierung in die Wirbelsäule hinein sogar als Lähmungen imponieren können. Auf rektale Palpation treten in einigen Fällen Schmerzhaftigkeiten auf. Eine Vergrößerung des Organs ist jedoch nicht in allen Fällen nachweisbar. Im Urin lassen sich in zwei Dritteln der Fälle Anzeichen für eine Entzündung oder eine Einblutung nachweisen. Tumorzellen selbst werden hier allerdings nur selten gefunden. Eine Verwendung der humanmedizinischen Marker Saure Phosphatase und Prostataspezifisches Antigen ist umstritten, zumal die humanmedizinischen Tests beim Hund nicht angewendet werden können.
Diagnostik
Im Röntgenbild können bei Metastasierung in den betroffenen Organen häufig Veränderungen nachgewiesen werden. Die Prostata selbst ist häufig vergrößert und weist Verkalkungsherde auf. Im Ultraschall ist neben einer Vergrößerung des Organs häufig eine erhöhte Echogenität und in einigen Fällen das Vorhandensein von Zysten nachweisbar. Die definitive Diagnose erfolgt mittels einer transabdominalen oder transrektalen Prostatabiopsie und anschließender pathohistologischer Untersuchung. Eine weitere Möglichkeit besteht in der Durchführung einer Kathetersaugbiopsie, bei welcher mittels eines Harnröhrenkatheters aus dem Bereich der Prostata Zellen angesaugt werden.
Therapie
Da die meisten Hunde mit einem Tumor der Prostata erst beim Vorliegen von Metastasen vorgestellt werden, ist die Prognose in den meisten Fällen von vornherein ungünstig. Früherkennungsmaßnahmen wie z. B. PSA-Tests werden gegenwärtig noch nicht angeboten. Die mittlere Überlebenszeit nach Diagnosestellung liegt bei drei Monaten. Eine chirurgische Entfernung der Prostata ist durch die meist große Ausdehnung des Tumors oft nicht möglich. Bei intakten Rüden wird die Überlebenszeit auch durch eine Kastration oder die Gabe von Antiandrogenen nicht verbessert. Auch verschiedentlich getestete Chemotherapieprotokolle oder Strahlentherapien verbesserten die Prognose nicht nachweislich.
Siehe auch
Literatur
Leitlinien
- Patientenratgeber Prostatakrebs (PDF; 1 MB), Patientenleitlinie Lokal begrenztes Prostatakarzinom (PDF; 1,5 MB), Patientenleitlinie Lokal fortgeschrittenes und metastasiertes Prostatakarzinom (PDF; 1,5 MB) (Deutsche Krebsgesellschaft)
- S3-Leitlinie Prostatakarzinom der Deutschen Gesellschaft für Urologie (DGU). In: AWMF online (Stand 2021)
Fachbücher
- Emil A. Tanagho, Jack W. McAninch: Smith’s General Urology. 17. Auflage. Mcgraw-Hill Professional, 2008, ISBN 978-0-07-145737-8.
- Hans Ulrich Schmelz, Christoph Sparwasser, Wolfgang Weidner: Facharztwissen Urologie. Springer, Heidelberg 2006, ISBN 3-540-20009-6.
- M. Kessler: Kleintieronkologie. Parey-Verlag, München 2005, ISBN 3-8304-4103-7.
Zeitschriftenbeiträge
- Lothar Weißbach, Jens Altwein: Aktive Überwachung oder aktive Therapie beim lokalen Prostatakarzinom? In: Dtsch. Ärztebl. Int. Nr. 106 (22), 2009, S. 371–376 (Artikel).
- D. G. Bostwick et al.: Human prostate cancer risk factors. In: Cancer. Band 101, Nummer 10 Suppl, November 2004, S. 2371–2490, doi:10.1002/cncr.20408. PMID 15495199. (Review).
Weblinks
- PathoPic – Bilddatenbank der Universität Basel: Adenokarzinom der Prostata (Bild eines Präparates)
- PathoPic – Bilddatenbank der Universität Basel: Tumorinfiltration der Harnblase (Bild eines Präparates)
- Prostatakrebs. In: Zentrum für Krebsregisterdaten. Robert-Koch-Institut, 29. November 2021, abgerufen am 22. Dezember 2021.
- Prostate cancer. National Cancer Institute (englisch)
- Prostatakarzinom. Online-Lehrbuch der Urologie für Ärzte und medizinisches Fachpersonal
- Prostatakrebs Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen
- Patienteninformation Früherkennung von Prostatakrebs Ärztliches Zentrum für Qualität in der Medizin
Einzelnachweise
- Statistisches Bundesamt Deutschland: Eheschließungen, Geborene und Gestorbene 1946–2011. (Memento vom 13. November 2012 im Internet Archive) (MS Excel; 242 kB) – Im Jahr 2005 starben insgesamt 388.554 Männer.
- Heft 36 Prostataerkrankungen – Gesundheitsberichterstattung des Bundes. (Memento vom 18. Dezember 2013 im Internet Archive) (PDF; 0,6 MB) Robert Koch-Institut. – Etwa 11.000 Männer sterben in Deutschland pro Jahr an Prostatakrebs (2005), das sind 22,4 % der Erkrankten.
- Prostatakrebs (Prostatakarzinom). In: Zentrum für Krebsregisterdaten. 29. November 2021, abgerufen am 22. Dezember 2021.
- K. J. Bell, C. Del Mar, G. Wright, J. Dickinson, P. Glasziou: Prevalence of incidental prostate cancer: A systematic review of autopsy studies. In: International Journal of Cancer. Band 137, Nummer 7, Oktober 2015, S. 1749–1757, doi:10.1002/ijc.29538. PMID 25821151, PMC 4682465 (freier Volltext) (Review).
- J. L. Jahn, E. L. Giovannucci, M. J. Stampfer: The high prevalence of undiagnosed prostate cancer at autopsy: implications for epidemiology and treatment of prostate cancer in the Prostate-specific Antigen-era. In: International Journal of Cancer. Band 137, Nummer 12, Dezember 2015, S. 2795–2802, doi:10.1002/ijc.29408. PMID 25557753, PMC 4485977 (freier Volltext) (Review).
- Prostata. (PDF) Krebs in Deutschland für 2017/2018. In: Zentrum für Krebsregisterdaten. RKI, 2021, S. 106-109, abgerufen am 22. Dezember 2021.
- International Agency for Research on Cancer: GLOBOCAN – Estimated cancer Incidence, Mortality, Prevalence and Disability-adjusted life years (DALYs). Datenbankabfragen.
- G. D. Steinberg et al.: Family history and the risk of prostate cancer. In: The Prostate. Band 17, Nummer 4, 1990, S. 337–347. PMID 2251225.
- A. F. Olumi: Commentary on „integrative genomic analyses reveal an androgen-driven somatic alteration landscape in early-onset prostate cancer.“; Genome Biology Unit, European Molecular Biology Laboratory (EMBL), Heidelberg, Germany.: Cancer Cell 23(2), 2013, S. 159–70. In: Urologic oncology. Band 32, Nummer 2, Februar 2014, S. 212, doi:10.1016/j.urolonc.2013.08.018. PMID 24445294.
- N. Breslow et al.: Latent carcinoma of prostate at autopsy in seven areas. The International Agency for Research on Cancer, Lyons, France. In: International Journal of Cancer. Band 20, Nummer 5, November 1977, S. 680–688. PMID 924691.
- T. Matsuda, K. Saika: Comparison of time trends in prostate cancer incidence (1973–1997) in East Asia, Europe and USA, from Cancer Incidence in Five Continents Vols IV VIII. In: Japanese journal of clinical oncology. Band 37, Nummer 7, Juli 2007, S. 556–557, doi:10.1093/jjco/hym100. PMID 17720742.
- Kalifornisches Krebsregister 2002
- S. E. Berkow et al.: Diet and survival after prostate cancer diagnosis. In: Nutrition reviews. Band 65, Nummer 9, September 2007, S. 391–403. PMID 17958206. (Review).
- M. A. Khan, A. W. Partin: Vasectomy and prostate cancer. In: Reviews in urology. Band 6, Nummer 1, 2004, S. 46–47. PMID 16985574. PMC 1472683 (freier Volltext).
- Overview: Prostate Cancer – What Causes Prostate Cancer? American Cancer Society, 8. August 2009; abgerufen am 19. Oktober 2012.
- G. G. Giles et al.: Sexual factors and prostate cancer. In: BJU International. 92, 2003, S. 211–216. PMID 12887469. doi:10.1046/j.1464-410X.2003.04319.x
- Jennifer R. Rider et al.: Ejaculation Frequency and Risk of Prostate Cancer: Updated Results with an Additional Decade of Follow-up. In: European Urology. Band 70, Nr. 6, 1. Dezember 2016, S. 974–982, doi:10.1016/j.eururo.2016.03.027, PMID 27033442.
- G. G. Schwartz, C. L. Hanchette: UV, latitude, and spatial trends in prostate cancer mortality: all sunlight is not the same (United States). In: Cancer causes & control. Band 17, Nummer 8, Oktober 2006, S. 1091–1101, doi:10.1007/s10552-006-0050-6. PMID 16933060.
- M. M. Ali, V. Vaidya: Vitamin D and cancer. In: Journal of cancer research and therapeutics. Band 3, Nummer 4, Oct-Dec 2007, S. 225–230. PMID 18270398. (Review).
- Y. R. Lou et al.: The role of Vitamin D3 metabolism in prostate cancer. In: The Journal of steroid biochemistry and molecular biology. Band 92, Nummer 4, November 2004, S. 317–325, doi:10.1016/j.jsbmb.2004.10.007. PMID 15663995. (Review).
- R. Krause et al.: UV radiation and cancer prevention: what is the evidence? In: Anticancer Research. Band 26, Nummer 4 A, Juli–August 2006, S. 2723–2727. PMID 16886683. (Review).
- H. Glossmann: Vitamin D, UV, and skin cancer in the elderly: to expose or not to expose? In: Gerontology. Band 57, Nummer 4, 2011, S. 350–353, doi:10.1159/000322521. PMID 21196703. (Review).
- G. Markozannes et al.: Diet, body size, physical activity and risk of prostate cancer: An umbrella review of the evidence. In: Eur J Cancer. Band 69, 2016, S. 61–69, doi:10.1016/j.ejca.2016.09.026, PMID 27816833 (sciencedirect.com [PDF]).
- DKFZ-Krebsinformationsdienst: Prostatakrebs: Risikofaktoren und Vorbeugung, abgerufen am 21. Februar 2021.
- Stacy Loeb, Benjamin C. Fu, Scott R. Bauer, Claire H. Pernar, June M. Chan: Mp32-06 association of plant-based dietary patterns with prostate cancer risk. In: Journal of Urology. Band 206, Supplement 3, 1. September 2021, S. e566–e567, doi:10.1097/JU.0000000000002036.06 (auajournals.org [abgerufen am 25. September 2021]).
- L. N. Kolonel: Fat, meat, and prostate cancer. In: Epidemiologic reviews. Band 23, Nummer 1, 2001, S. 72–81. PMID 11588857. (Review).
- D. S. Michaud et al.: A prospective study on intake of animal products and risk of prostate cancer. In: Cancer Causes & Control. Band 12, Nummer 6, August 2001, S. 557–567. PMID 11519764.
- E. Giovannucci et al.: A prospective study of dietary fat and risk of prostate cancer. In: Journal of the National Cancer Institute. Band 85, Nummer 19, Oktober 1993, S. 1571–1579. PMID 8105097.
- Health Education Authority: Nutritional Aspects of the Development of Cancer (Memento vom 9. Dezember 2008 im Internet Archive) (PDF; 4 MB), London 1999.
- Kathryn M. Wilson et al.: Meat, Fish, Poultry, and Egg Intake at Diagnosis and Risk of Prostate Cancer Progression. In: Eur J Cancer. Band 9, Nr. 12, 2016, S. 933–941, doi:10.1158/1940-6207.CAPR-16-0070, PMID 27651069 (aacrjournals.org [PDF]).
- Verena Katzke, Rudolf Kaaks: Krebs und Ernährung. (PDF; 1,6 MB). In: Bundesverband Prostatakrebs Selbsthilfe e. V., 1/2016, S. 17–19.
- L. C. Bylsma, D. D. Alexander: A review and meta-analysis of prospective studies of red and processed meat, meat cooking methods, heme iron, heterocyclic amines and prostate cancer. In: Nutr J. 2015, 21, 14, S. 933–941, doi:10.1186/s12937-015-0111-3. PMID 26689289, PMC 4687294 (freier Volltext)
- K. Wu et al.: Associations between unprocessed red and processed meat, poultry, seafood and egg intake and the risk of prostate cancer: A pooled analysis of 15 prospective cohort studies. In: Int J Cancer. Band 138, Nr. 10, 2016, S. 2368–2382, doi:10.1002/ijc.29973, PMID 26685908, PMC 4837898 (freier Volltext).
- Meat, fish & dairy. 24. April 2018, abgerufen am 5. März 2021 (englisch).
- WCRF: Meat, fish and dairy products and the risk of cancer. (PDF) S. 10, abgerufen am 5. März 2021.
- Milk and Health. Abgerufen am 17. Februar 2020.
- Walter C. Willett, David S. Ludwig: Milk and Health. In: New England Journal of Medicine. Band 382, Nr. 7, 13. Februar 2020, ISSN 0028-4793, S. 644–654, doi:10.1056/NEJMra1903547, PMID 32053300.
- A. Sargsyan, H. B. Dubasi: Milk Consumption and Prostate Cancer: A Systematic Review. In: World J Mens Health. 2020 Jul 27. doi:10.5534/wjmh.200051. PMID 32777868.
- Kazuya Mikami, Kotaro Ozasa, Tsuneharu Miki, Yoshiyuki Watanabe, Mitsuru Mori: Dairy products and the risk of developing prostate cancer: A large-scale cohort study (JACC Study) in Japan. In: Cancer Medicine. 4. Oktober 2021, ISSN 2045-7634, doi:10.1002/cam4.4233, PMID 34606688 (nih.gov [abgerufen am 19. Oktober 2021]).
- Catherine C. Applegate, Joe L. Rowles, Katherine M. Ranard, Sookyoung Jeon, John W. Erdman: Soy Consumption and the Risk of Prostate Cancer: An Updated Systematic Review and Meta-Analysis. In: Nutrients. Band 10, Nr. 1, 4. Januar 2018, ISSN 2072-6643, doi:10.3390/nu10010040, PMID 29300347, PMC 5793268 (freier Volltext): „This hypothesis has further been supported by four previous meta-analyses of epidemiological studies, all of which showed a protective association between soy consumption and PCa …“
- Catherine C. Applegate, Joe L. Rowles, Katherine M. Ranard, Sookyoung Jeon, John W. Erdman: Soy Consumption and the Risk of Prostate Cancer: An Updated Systematic Review and Meta-Analysis. In: Nutrients. Band 10, Nr. 1, 4. Januar 2018, ISSN 2072-6643, doi:10.3390/nu10010040, PMID 29300347, PMC 5793268 (freier Volltext).
- Thierry Capiod et al.: Do dietary calcium and vitamin D matter in men with prostate cancer? In: Nature Reviews Urology. Band 15, Nr. 7, Juli 2018, S. 453–461, doi:10.1038/s41585-018-0015-z.
- Prostate Cancer, Nutrition, and Dietary Supplements (PDQ®). In: National Cancer Institute. 12. Juli 2021, abgerufen am 22. Dezember 2021 (englisch).
- S3 Leitlinie Komplementärmedizin in der Behandlung von onkologischen PatientInnen. (PDF) In: Leitlinienprogramm Onkologie. AWMF, September 2021, abgerufen am 22. Dezember 2021.
- Jutta Hübner et al.: Komplementärmedizin in der Uroonkologie. In: Der Urologe. Band 60, Nr. 7, 1. Juli 2021, S. 953–962, doi:10.1007/s00120-021-01584-8.
- A. J. Pantuck et al. A randomized, double-blind, placebo-controlled study of the effects of pomegranate extract on rising PSA levels in men following primary therapy for prostate cancer. In: Prostate Cancer and Prostatic Disease. 18, 2015, S. 242, doi:10.1038/pcan.2015.32.
- A. van Bokhoven et al.: Molecular characterization of human prostate carcinoma cell lines. In: The Prostate. Band 57, Nummer 3, November 2003, S. 205–225, doi:10.1002/pros.10290. PMID 14518029.
- A. B. Apolo, N. Pandit-Taskar, M. J. Morris: Novel tracers and their development for the imaging of metastatic prostate cancer. In: Journal of nuclear medicine. Band 49, Nummer 12, Dezember 2008, S. 2031–2041, doi:10.2967/jnumed.108.050658. PMID 18997047. (Review).
- M. D. Krahn et al.: Screening for prostate cancer. A decision analytic view. In: JAMA. 272(10), 1994, S. 773–780. PMID 7521400.
- Ronald J. Zagoria, Glenn A. Tung: Genitourinary Radiology. Mosby, St. Louis 1997.
- L. A. M. Simmons, P. Autier, F. Zát’ura, J. Braeckman, A. Peltier, I. Romic, A. Stenzl, K. Treurnicht, T. Walker, D. Nir, C. M. Moore, M. Emberton: Detection, localisation and characterisation of prostate cancer by Prostate HistoScanning. In: BJU Int. Epub 2011 Nov. 17
- MRI in addition to or as a substitute for prostate biopsy: The clinician’s point of view. In: Diagnostic and Interventional Imaging. Band 93, 2012, S. 262–267.
- N. B. Delongchamps et al.: Multiparametric magnetic resonance imaging for the detection and localization of prostate cancer: Combination of T2-weighted, dynamic contrast-enhanced and diffusion-weighted imaging. In: BJU Int. Band 107, Nr. 9, 2011, S. 1411–1418.
- How Good is MRI at Detecting and Characterising Cancer within the Prostate? In: European Urology. Band 50, 2006, S. 1163–1175.
- Combined prostate diffusion tensor imaging and dynamic contrast enhanced MRI at 3T – quantitative correlation with biopsy. In: Magnetic Resonance Imaging. Band 28, 2010, S. 621–628.
- Bernhard Scher et al.: Value of 11C-choline PET and PET/CT in patients with suspected prostate cancer. In: European Journal of Nuclear Medicine and Molecular Imaging. Band 34, Nr. 1, Januar 2007, S. 45–53, doi:10.1007/s00259-006-0190-7, PMID 16932935.
- Sven N. Reske et al.: Imaging prostate cancer with 11C-choline PET/CT. In: Journal of Nuclear Medicine: Official Publication, Society of Nuclear Medicine. Band 47, Nr. 8, August 2006, S. 1249–1254, PMID 16883001.
- Analysenverzeichnis | Labor Krone. Abgerufen am 12. Oktober 2017 (deutsch).
- LADR: Prostata-Karzinom – Vorsorge und Früherkennung mittels prostatakrebsspezifischem PCA3-Test (PDF; 798 kB)
- M. A. Bjurlin, S. S. Taneja: Standards for prostate biopsy. In: Current opinion in urology. Band 24, Nummer 2, März 2014, S. 155–161, doi:10.1097/MOU.0000000000000031. PMID 24451092, PMC 4142196 (freier Volltext) (Review).
- M. Brock, C. von Bodman, J. Palisaar, W. Becker, P. Martin-Seidel, J. Noldus: Detecting Prostate Cancer. In: Deutsches Ärzteblatt international. Band 112, Nummer 37, September 2015, S. 605–611, doi:10.3238/arztebl.2015.0605. PMID 26396046, PMC 4581108 (freier Volltext), deutsche Version: Detektion des Prostatakarzinoms, PDF.
- A. M. Hoogland, C. F. Kweldam, G. J. van Leenders: Prognostic histopathological and molecular markers on prostate cancer needle-biopsies: a review. In: BioMed research international. Band 2014, S. 341324, doi:10.1155/2014/341324. PMID 25243131, PMC 4163394 (freier Volltext) (Review).
- Ursus-Nikolaus Riede, Hans-Eckart Schaefer: Allgemeine und spezielle Pathologie. Thieme, Stuttgart 1999, ISBN 3-13-683304-X.
- H. Y. Wu, H. M. Snyder: Pediatric urologic oncology: bladder, prostate, testis. In: Urol Clin North Am. 31(3), 2004, S. 619–627, xi. PMID 15313070.
- D. B. Groff: Pelvic neoplasms in children. In: J Surg Oncol. 77(1), 2001, S. 65–71. PMID 11344486.
- Leitlinie „Prostatakarzinom“ der Deutschen Krebsgesellschaft und der Deutschen Krebshilfe, Linkliste, aufgerufen am 12. November 2018.
- Vgl. dazu auch die Internetseite prostapath.org (Memento vom 28. März 2010 im Internet Archive) Gleason Schule – Intraduktale Prostatakarzinome; PCa-Varianten; Gleason Grading in Stanzbiopsien; Reproduzierbarkeit und Korrelation. Abgerufen am 9. Februar 2012.
- So Strohmaier, Klinikum Coburg, in dem GPK-Sonderheft vom Juni 2007 „Krebsfrüherkennung ohne Mythos“.
- Alfred Böcking: Mit Zellen statt Skalpellen. Lehmanns Fachbuchhandlung, 2006, ISBN 3-86541-177-0.
- Schriftwechsel zur DNA-Zytometrie. Eingesehen am 13. Mai 2009.
- F. K. Mostofi, C. J. Davis, I. A. Sesterhenn: Pathology of carcinoma of the prostate. In: Cancer. Band 70, Nummer 1 Suppl, Juli 1992, S. 235–253. PMID 1376194. (Review).
- Prostatakrebs-Kodierhilfe. Tumorzentrum Freiburg 2007 (Seite nicht mehr abrufbar, Suche in Webarchiven) (PDF)
- UICC: What are the changes between the 6th and 7th editions? (PDF; 2,1 MB) (Seite nicht mehr abrufbar, Suche in Webarchiven) (PDF)
- Christian Wittekind, Hans-Joachim Meyer (Hrsg.): TNM: Klassifikation maligner Tumoren. 7. Auflage. Wiley-VCH Verlag, 2010, ISBN 978-3-527-32759-1.
- F. C. Hamdy et al.: 10-Year Outcomes after Monitoring, Surgery, or Radiotherapy for Localized Prostate Cancer. In: The New England Journal of Medicine. Band 375, Nummer 15, 10 2016, S. 1415–1424, doi:10.1056/NEJMoa1606220. PMID 27626136.
- Prostatakrebs: Abwarten statt eingreifen. Medizin Transparent, 15. Januar 2018; abgerufen am 16. März 2018.
- Jenny L. Donovan, Freddie C. Hamdy, J. Athene Lane, Malcolm Mason, Chris Metcalfe: Patient-Reported Outcomes after Monitoring, Surgery, or Radiotherapy for Prostate Cancer. In: The New England Journal of Medicine. Band 375, Nr. 15, 13. Oktober 2016, S. 1425–1437, doi:10.1056/NEJMoa1606221, PMID 27626365, PMC 5134995 (freier Volltext).
- Langzeitstudie zum Prostatakrebs zeigt: Patienten profitieren von früher Behandlung – Bestrahlung ebenso effektiv wie Operation, aber schonender – Degro. Abgerufen am 12. April 2017.
- P. Grimm et al.: Comparative analysis of prostate-specific antigen free survival outcomes for patients with low, intermediate and high risk prostate cancer treatment by radical therapy. Results from the Prostate Cancer Results Study Group. In: BJU international. Band 109 Suppl 1, Februar 2012, S. 22–29, doi:10.1111/j.1464-410X.2011.10827.x. PMID 22239226. (Review). praxis-margareten.at (PDF, Volltext)
- H. Keller, J. Lehmann, J. Beier: Radical perineal prostatectomy and simultaneous extended pelvic lymph node dissection via the same incision. In: European urology. Band 52, Nummer 2, August 2007, S. 384–388, doi:10.1016/j.eururo.2006.09.045. PMID 17084507.
- P. J. Davidson, D. van den Ouden, F. H. Schroeder: Radical prostatectomy: prospective assessment of mortality and morbidity. In: European urology. Band 29, Nummer 2, 1996, S. 168–173. PMID 8647142.
- Brian McGlynn et al.: Management of urinary incontinence following radical prostatectomy. In: Urologic Nursing. Band 24, Nr. 6, Dezember 2004, S. 475–482, 515, PMID 15658733.
- E. Sacco, T. Prayer-Galetti, F. Pinto, S. Fracalanza, G. Betto, F. Pagano, W. Artibani: Urinary incontinence after radical prostatectomy: incidence by definition, risk factors and temporal trend in a large series with a long-term follow-up. In: BJU international. Band 97, Nummer 6, Juni 2006, S. 1234–1241, doi:10.1111/j.1464-410X.2006.06185.x. PMID 16686718.
- Mechanismus der Erektion auf www.urologielehrbuch.de
- Das Leben ohne Prostata. In: Helios Magazin. 4. März 2021, abgerufen am 28. Juni 2021.
- Ist Harnverlust beim Orgasmus häufig? In: Ärzte Zeitung. Springer Medizin Verlag, 31. Dezember 2013, abgerufen am 28. Juni 2021.
- Freddie C. Hamdy, Jenny L. Donovan, J. Athene Lane, Malcolm Mason, Chris Metcalfe: 10-Year Outcomes after Monitoring, Surgery, or Radiotherapy for Localized Prostate Cancer. In: The New England Journal of Medicine. Band 375, Nr. 15, 13. Oktober 2016, ISSN 1533-4406, S. 1415–1424, doi:10.1056/NEJMoa1606220, PMID 27626136.
- J. L. Donovan, F. C. Hamdy, J. A. Lane, M. Mason, C. Metcalfe: Patient-Reported Outcomes after Monitoring, Surgery, or Radiotherapy for Prostate Cancer. In: The New England journal of medicine. Band 375, Nr. 15, 13. Oktober 2016, ISSN 0028-4793, S. 1425–1437, doi:10.1056/NEJMoa1606221, PMID 27626365, PMC 5134995 (freier Volltext).
- C. M. Yablon et al.: Complications of prostate cancer treatment: spectrum of imaging findings. In: Radiographics. Band 24 Suppl 1, Oktober 2004, S. S181–S194, doi:10.1148/rg.24si045502. PMID 15486240. (Review).
- R. S. Kushwaha et al.: Physiologic changes of the anorectum after pelvic radiotherapy for the treatment of prostate and bladder cancer. In: Diseases of the Colon and Rectum. Band 46, Nummer 9, September 2003, S. 1182–1188, doi:10.1007/s10350-004-6712-0. PMID 12972961.
- D. E. Spratt et al.: Long-term survival and toxicity in patients treated with high-dose intensity modulated radiation therapy for localized prostate cancer. In: Int J Radiat Oncol Biol Phys. 85(3), 1. März 2013, S. 686–692. doi:10.1016/j.ijrobp.2012.05.023. Epub 2012 Jul 12.
- N. P. Mendenhall et al.: Five-year outcomes from 3 prospective trials of image-guided proton therapy for prostate cancer. In: International journal of radiation oncology, biology, physics. Band 88, Nummer 3, März 2014, S. 596–602, doi:10.1016/j.ijrobp.2013.11.007. PMID 24521677.
- Großstudie PREFERE bewertet Therapien. In: Aktuel Urol. 44(02), 2013, S. 105 doi:10.1055/s-0033-1343926
- G. S. Merrick, W. M. Butler: Rectal function following permanent prostate brachytherapy. In: The West Virginia medical journal. Band 100, Nummer 1, Januar–Februar 2004, S. 18–20. PMID 15119492.
- G. M. Duchesne et al.: Outcome, morbidity, and prognostic factors in post-prostatectomy radiotherapy: an Australian multicenter study. In: Urology. Band 61, Nummer 1, Januar 2003, S. 179–183. PMID 12559292.
- Pressemitteilung der ASTRO von Oktober 2012.
- Informationen zur Studie (Memento vom 6. März 2016 im Internet Archive)
- Pressemitteilung der Universität zu Lübeck
- T. E. Schultheiss, W. R. Lee, M. A. Hunt, A. L. Hanlon, R. S. Peter, G. E. Hanks: Late GI and GU complications in the treatment of prostate cancer. In: Int. J. Radiat. Oncol. Biol. Phys. Band 37, Nr. 1, Jan 1997, S. 3–11. PMID 9054871.
- N. H. Gilinsky, D. G. Burns, G. O. Barbezat, W. Levin, H. S. Myers, I. N. Marks: The natural history of radiation-induced proctosigmoiditis: an analysis of 88 patients. In: Q. J. Med. Band 52, Nr. 205, 1983, S. 40–53. PMID 6603628.
- P. J. Prada et al.: Transperineal injection of hyaluronic acid in the anterior perirectal fat to decrease rectal toxicity from radiation delivered with low-dose-rate brachytherapy for prostate cancer patients. In: Brachytherapy. Band 8, Nr. 2, 2009, S. 210–217. doi:10.1016/j.brachy.2008.11.010. PMID 19213607.
- W. R. Noyes, C. C. Hosford, S. E. Schultz: Human collagen injections to reduce rectal dose during radiotherapy. In: Int. J. Radiat. Oncol. Biol. Phys. Band 82, Nr. 5, April 2012, S. 1918–1922. doi:10.1016/j.ijrobp.2011.02.034. PMID 21514738
- G. Kovacs et al.: Significant Rectal Dose Reduction During Prostate Cancer Radiotherapy Using Novel Biodegradable Inflatable Balloon System: Interim Results of a Prospective Multi-Center Study. Abstract, ASTRO 2011.
- D. Y. Song et al.: A multi-institutional clinical trial of rectal dose reduction via injected polyethylene-glycol hydrogel during intensity modulated radiation therapy for prostate cancer: analysis of dosimetric outcomes. In: International journal of radiation oncology, biology, physics. Band 87, Nummer 1, September 2013, S. 81–87, doi:10.1016/j.ijrobp.2012.12.019. PMID 23414766. PMC 3737267 (freier Volltext).
- M. Pinkawa et al.: Application of a spacer gel to optimize three-dimensional conformal and intensity modulated radiotherapy for prostate cancer. In: Radiother Oncol. Band 100, Nr. 3, September 2011, S. 436–441. doi:10.1016/j.radonc.2011.09.005. PMID 21963289.
- M. J. Zelefsky et al.: Long-term results of conformal radiotherapy for prostate cancer: impact of dose escalation on biochemical tumor control and distant metastases-free survival outcomes. In: Int. J. Radiat. Oncol. Biol. Phys. Band 71, Nr. 4, July 2008, S. 1028–1033. doi:10.1016/j.ijrobp.2007.11.066. PMID 18280056.
- M. Ritter, J. Forman, P. Kupelian, C. Lawton, D. Petereit: Hypofractionation for prostate cancer. In: Cancer J. Band 15, Nr. 1, 2009, S. 1–6. doi:10.1097/PPO.0b013e3181976614. PMC 3039916 (freier Volltext). PMID 19197165.
- Schonende Form der Prostata-Operation orf.at, 27. August 2017, abgerufen am 27. August 2017.
- D. Margel et al.: Cardiovascular morbidity in a randomized trial comparing GnRH-agonist and GnRH-antagonist among patients with advanced prostate-cancer and pre-existing cardiovascular disease. In: American Urological Association (Hrsg.): The Journal of Urology. Elsevier-Verlag, 2019, doi:10.1097/JU.0000000000000384.
- P. C. Albertsen et al.: Cardiovascular morbidity associated with gonadotropin releasing hormone agonists and an antagonist. In: European Association of Urology (Hrsg.): European Urology. Band 65, Nr. 3. Elsevier-Verlag, 2014, S. 565–573, doi:10.1016/j.eururo.2013.10.032.
- U. W. Tunn, N. Bruchovsky, H. Renneberg, J. M. Wolff, R. Kurek: Intermittierende Androgendeprivation. In: Der Urologe A. Band 39, Nr. 1, Januar 2000.
- S. Madersbacher, U. W. Tunn: Update zur intermittierenden Hormontherapie beim Prostatakarzinom. (PDF; 721 kB). In: Journal für Urologie und Urogynäkologie. 14, 2007, (Sonderheft 3)
- Grace L. Lu-Yao et al.: Survival following primary androgen deprivation therapy among men with localized prostate cancer. In: JAMA. Band 300, Nr. 2, 9. Juli 2008, S. 173–181, doi:10.1001/jama.300.2.173, PMID 18612114, PMC 2645653 (freier Volltext).
- Ian F. Tannock et al.: Docetaxel plus prednisone or mitoxantrone plus prednisone for advanced prostate cancer. In: The New England Journal of Medicine. Band 351, Nr. 15, 7. Oktober 2004, S. 1502–1512, doi:10.1056/NEJMoa040720, PMID 15470213.
- C. J. Sweeney et al.: Chemohormonal Therapy in Metastatic Hormone-Sensitive Prostate Cancer. In: N Engl J Med. Band 373, 2015, S. 737–746. doi:10.1056/NEJMoa1503747
- Neue Arzneimittel: Xtandi (Enzalutamid). (PDF) In: akdae.de Arzneimittelkommission der deutschen Ärzteschaft. 29. November 2013, abgerufen am 29. November 2013.
- D. Mukherji, C. J. Pezaro, J. S. De-Bono: MDV3100 for the treatment of prostate cancer. In: Expert Opinion on Investigational Drugs. Band 21, Nummer 2, Februar 2012, S. 227–233, doi:10.1517/13543784.2012.651125. PMID 22229405.
- F. Saad et al.: A randomized, placebo-controlled trial of zoledronic acid in patients with hormone-refractory metastatic prostate carcinoma. In: Journal of the National Cancer Institute. Band 94, Nummer 19, Oktober 2002, S. 1458–1468. PMID 12359855.
- Europäische Arzneimittel-Agentur: Xofigo. Radium-223-Dichlorid (PDF; 75 kB). (PDF) EMA/579264/2013, EMEA/H/C/002653, 13. November 2013.
- Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms, federführende Fachgesellschaft: Deutsche Gesellschaft für Urologie e. V. (Hrsg.), Version 5.0, 2018.
- L. Weissbach, J. Altwein: Aktive Überwachung oder aktive Therapie beim lokalen Prostatakarzinom? In: Deutsches Ärzteblatt international. Band 106, Nummer 22, Mai 2009, S. 371–376, doi:10.3238/arztebl.2009.0371. PMID 19623304. PMC 2704359 (freier Volltext). (Review).
- Health and Clinical Excellence Guidance: Localised Prostate Cancer (Memento vom 15. März 2013 im Internet Archive), Großbritannien, abgerufen am 18. Oktober 2012.
- Edward W. Lee, Susan Thai, Stephen T. Kee: Irreversible electroporation: a novel image-guided cancer therapy. In: Gut and Liver. 4. Suppl 1, 2010, S. 99–104.
- Boris Rubinsky: Irreversible electroporation: implications for prostate ablation. In: Technology in cancer research & treatment. 6.4, 2007.
- KLINIKEN in Deutschland, die Irreversible Elektroporation – IRE («NanoKnife») anbieten (Stand: Juni 2015). (PDF) betrifft: Prostatakrebs – Hoffnung durch schonende Therapie. SWR, 22. Juli 2015, abgerufen am 24. Juli 2015.
- G. Bozzini et al.: Focal therapy of prostate cancer: energies and procedures. In: Urologic oncology. Band 31, Nummer 2, Februar 2013, S. 155–167, doi:10.1016/j.urolonc.2012.05.011. PMID 22795500. (Review).
- P. A. Burch et al.: Immunotherapy (APC8015, Provenge) targeting prostatic acid phosphatase can induce durable remission of metastatic androgen-independent prostate cancer: a Phase 2 trial. In: Prostate. 60, 2004, S. 197–204. PMID 15176049.
- J. E. Johansson et al.: Fifteen-year survival in prostate cancer. A prospective, population-based study in Sweden. In: JAMA: the journal of the American Medical Association. Band 277, Nummer 6, Februar 1997, S. 467–471. PMID 9020270. Abstract (deutsch) (Memento vom 18. Oktober 2004 im Internet Archive)
- C. R. Porter et al.: 25-year prostate cancer control and survival outcomes: a 40-year radical prostatectomy single institution series. In: The Journal of urology. Band 176, Nummer 2, August 2006, S. 569–574, doi:10.1016/j.juro.2006.03.094. PMID 16813891.
- Survival Rates for Prostate Cancer. In: American Cancer Society. 2. Februar 2021, abgerufen am 22. Dezember 2021 (englisch).
- P. Enders u. a.: Prostatakrebs I – Lokal begrenztes Prostatakarzinom (PDF; 1125 kB) Ein evidenzbasierter Patientenratgeber zur S3-Leitlinie Früherkennung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms, Deutsche Krebsgesellschaft, 2015.
- A. W. Partin et al.: Contemporary update of prostate cancer staging nomograms (Partin Tables) for the new millennium. In: Urology. Band 58, Nummer 6, Dezember 2001, S. 843–848. PMID 11744442.
- S3-Leitlinie Prostatakarzinom: Früherkennung, Diagnose und Therapie der verschiedenen Stadien der Deutschen Gesellschaft für Urologie (DGU). In: AWMF online (Stand 2018)
- Prostatakrebsscreening mittels PSA-Test, IQWiG, 20. Dezember 2019.
- IGeL Monitor – Ultraschall zur Früherkennung von Prostatakrebs. Abgerufen am 7. Januar 2021.
- DLF-Interview mit Krebsforscher Robert Weinberg. In: Forschung Aktuell. 4. Januar 2006.
- Emily Sohn: Screening: Diagnostic dilemma. In: Nature. Band 528, Nr. 7582, 2015, S. S120–S122 (hier: S. S121), doi:10.1038/528S120a
- Metastasen beim Skythen-Fürst. In: bild der wissenschaft. 3/2008. Konradin Medien GmbH, Leinfelden-Echterdingen.
- J. Adams: The case of scirrhous of the prostate gland with corresponding affliction of the lymphatic glands in the lumbar region and in the pelvis. In: Lancet. (1853) 1, S. 393.
- H. H. Young: Four cases of radical prostatectomy. In: Johns Hopkins Bull. 16, 1905, S. 315.
- C. Huggins, C. V. Hodges: Studies on Prostatic Cancer – 1. The effect of estrogen and of androgen injection on serum phosphatases in metastatic carcinoma of the prostate. In: Cancer Res. 1, 1941, S. 203–297.
- R. W. Nelson, C. G. Couto: Innere Medizin der Kleintiere. Urban & Fischer, München/Jena 2006, S. 1004.