Krebsprävention
Unter Krebsprävention, auch Krebsvorbeugung, Krebsprophylaxe oder Krebsvermeidung genannt, versteht man Maßnahmen oder Verhaltensregeln, die die Entstehung von Krebserkrankungen verhindern oder zumindest die Wahrscheinlichkeit für eine solche Erkrankung herabsetzen sollen.
Einige der praktizierten Maßnahmen und Verhaltensregeln sind wissenschaftlich durch eine Vielzahl von epidemiologischen und retrospektiven Studien in ihrer Wirksamkeit bewiesen. Andere krebspräventive Maßnahmen sind zwar wissenschaftlich weitgehend unstrittig, jedoch unbewiesen. Dazu kommen einige in Fachkreisen kontrovers diskutierte sowie von der evidenzbasierten Medizin eindeutig abgelehnte Maßnahmen zur Krebsprävention („Quacksalberei“).
Krebsprävention als gesamtgesellschaftliche Aufgabe
Nach Expertenschätzungen sind in der Bundesrepublik immer noch rund die Hälfte aller Krebserkrankungen auf Lebensstilfaktoren zurückzuführen. Dazu gehörten, wie Rauchen, falsche Ernährung, wenig Bewegung, zuviel Alkohol und UV-Strahlung.
Nach früheren Erhebungen ließen sich 42 % aller Krebserkrankungen und beinahe die Hälfte aller krebsbedingten Todesfälle Schätzungen zufolge alleine durch die Art und Weise der Lebensführung (Lifestyle) vermeiden[1][2]. Krebs ist keine einheitliche Erkrankung, sondern vielmehr ein Sammelbegriff für eine Vielzahl verwandter Krankheiten, die sich erheblich in ihrer Pathologie unterscheiden können. Entsprechende Unterschiede bestehen deshalb auch für den Erfolg vorbeugender Maßnahmen. Die Wirkung präventiver Maßnahmen lässt sich am Individuum allein nicht bestimmen. Dazu sind immer möglichst große, statistisch erfasste Populationen notwendig.
Von der Krebsvorbeugung ist die Krebsvorsorge (auch: Krebsfrüherkennung) abzugrenzen. Deren Ziel ist die möglichst frühzeitige Erkennung von Krebserkrankungen, um die Erfolgswahrscheinlichkeit der Behandlung der Erkrankung (Krebstherapie) zu erhöhen.
Möglichkeiten der Krebsvorbeugung

Die Vermeidung der Exposition mit Karzinogenen ist einer der Hauptansatzpunkte zur Krebsprävention. Ein anderer ist die Aufnahme von kanzeroprotektiven (krebsschützenden) Nahrungsmitteln beziehungsweise Nahrungsergänzungsmitteln. Durch Impfungen gegen bestimmte Viren (Hepatitis B und Humane Papillomviren) lässt sich das Risiko für einige Krebserkrankungen nachweislich deutlich herabsetzen.
Der Europäische Kodex gegen den Krebs führt in seiner dritten Fassung von 2003 folgende sieben Punkte aus dem Bereich der Lebensführung auf.[3]
- Verzicht auf Tabakkonsum und, wenn der Verzicht nicht möglich ist, Verzicht auf das Rauchen in Gegenwart von Nichtrauchern
- Vermeidung der Fettleibigkeit
- tägliche körperliche Bewegung
- der verstärkte Verzehr von Obst und Gemüse mindestens fünfmal am Tag und die Reduzierung der Aufnahme tierischer Fette
- die Begrenzung des Alkoholkonsums auf zwei Getränke pro Tag für Männer und eines für Frauen.
- Vermeidung exzessiver Sonnenexposition, speziell bei Kindern und Jugendlichen
- strikte Einhaltung der Vorschriften für den Umgang mit krebserregenden beziehungsweise potenziell krebserregenden Substanzen
- Vermeidung bzw. Reduzierung des Kontakts mit endokrinen Disruptoren.
Der Harvard Report on Cancer Prevention von 1996 enthält eine noch heute weitgehend gültige[4] Abschätzung der Krebsrisikofaktoren.[5] Die wesentlichen Risikofaktoren liegen dabei im Bereich der individuellen Lebensführung.
| Risikofaktor | Anteil an der Krebsentstehung | gefährdete Organe |
| Rauchen | 25 bis 30 % | Mundhöhle, Speiseröhre, Kehlkopf, Lunge, Bauchspeicheldrüse, Harnblase, Gebärmutterhals, Niere und Blut |
| Ernährung und Übergewicht | 20 bis 40 % | Mundhöhle, Speiseröhre, Kehlkopf, Bauchspeicheldrüse, Magen, Darm, Brust und Prostata |
| Alkohol | 3 % | Mundhöhle, Rachen, Speiseröhre, Kehlkopf und Leber |
| berufliche Faktoren | 4 bis 8 % | Lunge und Harnblase |
| genetische Faktoren | 5 % | Auge, Darm, Brust, Eierstöcke und Schilddrüse |
| Infektionen | 5 % | Leber, Gebärmutterhals, lymphatisches System, blutbildendes System und Magen |
| Luftschadstoffe | 2 % | Lunge |
Vermeidung der Exposition mit krebserregenden Stoffen und Strahlungen
Eine Reihe von Substanzen ist in der Lage Krebs auszulösen. Zu diesen Karzinogenen (Krebserregern) gehören unter anderem eine Vielzahl von chemischen Verbindungen im Tabakrauch, Feinstäube wie beispielsweise Asbest oder Dieselruß, Benzol und Aflatoxine (bestimmte Schimmelpilzgifte). Im weiteren Sinn werden dazu auch ionisierende Strahlen und Onkoviren gerechnet.
Verzicht auf Tabakkonsum
Statistisch gesehen sind 25 bis 30 % aller durch Krebs hervorgerufenen Todesfälle in entwickelten Ländern auf langjähriges Tabakrauchen zurückzuführen.[2] Zwischen 87 und 91 % aller Lungenkrebserkrankungen bei Männern und zwischen 57 und 86 % bei Frauen werden durch das Rauchen von Zigaretten verursacht.[6][7] Die Zusammenhänge zwischen Rauchen und Lungenkrebs sind – nicht zuletzt durch entsprechende Warnhinweise auf den Verpackungen für Tabakprodukte – inzwischen allgemein bekannt. Für eine Reihe anderer Krebserkrankungen, wie beispielsweise die Gruppe der Kopf-Hals-Karzinome (Mundhöhlenkarzinom, Nasenrachenkrebs, Mundrachenkrebs, Schlundrachenkrebs, Kehlkopfkrebs und Luftröhrenkrebs), ist der Zusammenhang zwischen Rauchen und entsprechender Krebserkrankung ebenfalls zweifelsfrei belegt.[8] Bei Brustkrebs zeigen epidemiologische Daten, dass das Risiko einer Erkrankung durch Rauchen um etwa 30 % gesteigert wird.[9][10] Auch beim kolorektalen Karzinom („Darmkrebs“) erhöht langjähriger Tabakkonsum das Erkrankungsrisiko signifikant.[11][12][13]

Vermeidung von Alkohol
Über die Wechselwirkung von regelmäßigem Alkoholkonsum und der Erhöhung des Risikos einer Krebserkrankung liegen viele Studien vor, die einen eindeutigen Zusammenhang aufzeigen. Bei Brustkrebs liegt die Schwelle, ab der der Alkoholkonsum ein signifikant höheres Erkrankungsrisiko bewirkt, unterhalb von ein bis zwei alkoholischen Getränken pro Tag. Das Risiko erhöht sich vor allem für estrogenrezeptorpositive (ER+) Tumoren. Die Art des Getränkes, ob Bier, Wein oder Spirituose, spielt dabei, wie auch die Farbe des Weines, keine Rolle. Das Risiko steigt in einer dosisabhängigen Weise. Die tägliche Zufuhr von 15 bis 30 g Alkohol, was etwa ein bis zwei alkoholischen Getränken entspricht, erhöht das Risiko um den Faktor 1,33 (=33 %, das Konfidenzintervall für 95 % Wahrscheinlichkeit liegt bei 1,01 bis 1,71).[14][15] Einmaliger wöchentlicher Konsum erhöht das Risiko um 2 % pro Drink und Wochenendkonsum um 4 %. Exzessives Trinken mit vier bis fünf Drinks pro Tag steigert das Risiko um 55 %.[16]

Vermeidung übermäßiger ultravioletter Strahlung
Der Zusammenhang zwischen Hautkrebs und jahrelanger Exposition der Haut mit Sonnenlicht (Sonnenbad zur Bräunung der Haut) ist wissenschaftlich bewiesen. Insbesondere Sonnenbrände in der Jugend erhöhen signifikant das Risiko für Hautkrebs, wie beispielsweise für das maligne Melanom.[17] Auch Solarien und Sonnenbänke erhöhen das Risiko für Hautkrebs.[6] Der Schutz der Haut vor zu intensiver Bestrahlung, beispielsweise durch zweckmäßige Kleidung, kann die Wahrscheinlichkeit einer Hautkrebserkrankung deutlich reduzieren.
Ernährung

Übersicht
Der World Cancer Research Fund (WCRF) betont, dass nicht ein einzelnes Lebensmittel vor Krebs schütze, sondern vielmehr gesunde Ernährungsmuster.[18][19] Hierzu zählen:[20]
- Lebensmittel mit hoher Energiedichte nur begrenzt verzehren
- Zuckerhaltige Getränke vermeiden
- überwiegend pflanzliche Lebensmittel konsumieren:
- täglich 5 Portionen Obst und Gemüse
- Hülsenfrüchte
- Vollkornprodukte
- verarbeitetes Fleisch vermeiden
- Verzehr von rotem Fleisch auf 350–500 g pro Woche begrenzen
- Alkoholkonsum vermeiden
- Salzkonsum begrenzen
- Nährstoffbedarf über Lebensmittel, nicht Nahrungsergänzungsmittel decken
Ein wichtiger Faktor ist Übergewicht, welches das Risiko an Krebs zu erkranken erhöht. Vermutet wird, dass ein dauerhaft erhöhter Insulinspiegel als auch Wachstums- und Angiogenesefaktoren dabei eine Rolle spielen. Letztere werden teilweise von den Fettzellen selbst gebildet, was die Entstehung und das Wachstum von Tumorzellen begünstigt. Insgesamt können 13 Krebsentitäten auf Adipositas als eigenständiger Risikofaktor zurückgeführt werden. Der WCRF empfiehlt daher einen Body-Mass-Index von nicht über 25.[21]
Der Zuckerkonsum sollte laut WCRF begrenzt werden. Hintergrund ist, dass Krebszellen einen erhöhten Zuckerbedarf haben. Es ist allerdings ein Trugschluss, dass Krebszellen durch das Vermeiden von Zucker "ausgehungert" werden könnten.[22]
Mögliche Wirkungsmechanismen von sekundären Pflanzenstoffen
Einige sekundäre Pflanzenstoffe greifen nach ihrem Verzehr unmittelbar auf positive Weise in die Karzinogenese (Tumorentwicklung) ein. Vermutet werden folgende Mechanismen:[23]
- Antioxidantien sind Radikalfänger und eliminieren freie Radikale.
- Carotinoide, Polyphenole und Flavonoide lagern sich an die DNA im Zellkern an, so dass dort keine Karzinogene anbinden können.
- Phenolsäuren, Glucosinolate und Sulfide inhibieren bestimmte Enzyme, die die Umwandlung von Prokarzinogenen, wie beispielsweise Aflatoxine oder Nitrosamine, in Karzinogene katalysieren.
- Dagegen regen Glucosinolate, Monoterpene, Sulfide und Polyphenole karzinogenentgiftende Enzyme an.
- Phenolsäuren, Ellagsäure, Ferulasäure und Kaffeesäure binden an kanzerogene polycyclische aromatische Kohlenwasserstoffe und entgiften diese so.
- Phytosterine und Saponine hemmen die Proliferation von Tumorzellen im Dickdarm.
Während der WCRF eine pflanzenbetonte Ernährung als tumorprotektiv einstuft, ist jedoch noch unklar, welchen Anteil sekundäre Pflanzenstoffe hieran haben.[24]
Nahrungsergänzungsmittel (NEM)
Lange Zeit dachte man, dass insbesondere Nahrungsergänzungsmittel mit Antioxidantien tumorprotektiv wirken müssten.[25]
Jedoch lieferten die für Selen durchgeführten Studien keinen Hinweis auf einen positiven Nutzen einer zusätzlichen Gabe von Selen. Einige Krebsarten werden zwar offensichtlich positiv, andere aber eher negativ beeinflusst. Eine Studie (SELECT) musste 2008 abgebrochen werden, da keine Schutzwirkung im Vergleich zum Placebo festgestellt werden konnte. Weder bei Selen-Gabe noch bei Vitamin-E-Gabe gab es statistisch signifikante Unterschiede.[26]
Eine Reihe epidemiologischer Studien zeigte einen positiven Effekt bei einem erhöhten Plasmaspiegel von β-Carotin (durch entsprechende pflanzliche Lebensmittel) und einem reduzierten Risiko ein Bronchialkarzinom (Lungenkrebs) zu entwickeln. In intervenierenden Studien (ATBC, CARET und E3N), bei denen Rauchern über einen längeren Zeitraum β-Carotin hingegen nicht über die Nahrung, sondern als Nahrungsergänzung verabreicht wurde, um das Krebsrisiko zu senken, entwickelten diese völlig unerwartet häufiger ein Bronchialkarzinom als die Vergleichsgruppe ohne β-Carotin.[27] Bei Trinkern erhöht β-Carotin das Risiko eines Kolorektalkarzinoms. In der „normalen“ Population führt die Einnahme von β-Carotin dagegen offensichtlich nicht zu einem erhöhten Krebsrisiko, sondern zeigt im Gegenteil die erwartete krebspräventive Wirkung.[28] Das Darmkrebsrisiko sank in einer Studie beispielsweise um 44 %.[29]
Seit 2006 müssen alle β-Carotin enthaltenden Medikamente einen Warnhinweis aufweisen, dass für Raucher ein erhöhtes Risiko besteht, an Lungenkrebs zu erkranken.
Auch für die Gabe von Vitamin D konnte in der 2018 erschienenen VITAL-Studie kein Nutzen für die Krebsprävention nachgewiesen werden.[30]
Nahrungsergänzungsmittel werden vom World Cancer Research Fund für die Krebsprävention nicht empfohlen.[31]
Übergewicht oder Fettleibigkeit
Die Zusammenhänge zwischen Übergewicht beziehungsweise Adipositas (Fettleibigkeit) und einem erhöhten Risiko für bestimmte Krebserkrankungen sind in einer Vielzahl von Studien dokumentiert.
Brustkrebs
Das Risiko einer Brustkrebserkrankung übergewichtiger beziehungsweise adipöser Patientinnen nach der Menopause ist um 30 bis 50 % höher als bei normalgewichtigen Patientinnen. Für Erkrankungen vor der Menopause ist das Risiko dagegen nicht erhöht. Eine Gewichtsabnahme, insbesondere im späteren Leben, reduziert das Risiko deutlich,[32][33] während eine Zunahme des Körpergewichts als Erwachsener das Risiko für Brustkrebs verdoppelt.[1]
Als Erklärungsmodell für das erhöhte Brustkrebsrisiko bei Übergewicht werden verschiedene Mechanismen diskutiert. Übergewichtige Patientinnen haben häufig einen erhöhten Spiegel an Sexualhormonen, die einen starken Einfluss auf das Tumorwachstum haben (siehe Hauptartikel Brustkrebs#Hormonelle Faktoren). Gleiches gilt für insulinähnliche Wachstumsfaktoren, insbesondere IGF-2. Die erhöhte Masse an Fettspeicherzellen bei übergewichtigen Patientinnen erleichtert aber auch die Einlagerung von kanzerogenen Substanzen im Fettgewebe.[32][1]
Darmkrebs
Zwischen dem Body-Mass-Index (BMI) und dem Risiko an Darmkrebs zu erkranken besteht eine eindeutige Korrelation. Dies ist insbesondere für Tumoren im distalen Colon der Fall. Die Anzahl von fakultativ präkanzerösen Dickdarmpolypen korreliert ebenfalls mit dem BMI.[34][35][36][37][38][39][40][41][42] Auch hohe Werte für das Taille-Hüft-Verhältnis steigern das Risiko für Kolorektralkarzinome.[43] Zu den gleichen Ergebnissen kommen die beiden groß angelegten Framingham- und EPIC-Studien.[44][45][46]
Prostatakrebs
Auch beim Prostatakarzinom besteht ein erhöhtes Erkrankungsrisiko bei Fettleibigkeit. Es ist mit durchschnittlich etwa 5 % allerdings relativ gering.[47][48] Eine mögliche Ursache sind erhöhte Insulin-Spiegel bei adipösen Patienten.[49][50][1]
Andere Krebserkrankungen
Starkes Übergewicht erhöht auch das Risiko für ein Nierenzellkarzinom bei Frauen.[51]
Körperliche Betätigung
Für die häufigsten Krebsarten kann das Risiko einer Erkrankung durch regelmäßige körperliche Betätigung (Sport) gesenkt werden.[15] Die biochemischen Mechanismen, die zu diesem Effekt führen, sind noch weitgehend unklar. Verschiedene Ursachen werden diskutiert. Sport reduziert das Krebsrisiko, indem Übergewicht reduziert, der Hormonhaushalt günstig beeinflusst und Entzündungen entgegengewirkt wird.[52]
Brustkrebs
Frauen können das Risiko einer Brustkrebserkrankung durch eine regelmäßige körperliche Betätigung um bis zu 50 % senken.[53][54] Die Ursache für diesen Effekt ist noch weitgehend unklar. Es werden unter anderem Veränderungen am Hormonspiegel zirkulierender Hormone vermutet. Erhöhte körperliche Aktivität senkt bei Frauen den Östrogenspiegel im Blut; dies sowohl vor[55] als auch nach der Menopause.[56][57][58][59][1] Neben den hormonellen Aspekten werden auch andere Mechanismen, beziehungsweise Confounder-Effekte, wie Reduzierung des Körpergewichtes und eine erhöhte immunologische Aktivität diskutiert.[60][61][62] Möglicherweise spielt die nach anaerober körperlicher Belastung zu beobachtende Azidose eine positive Rolle.[53]
Kolorektales Karzinom
Das Kolorektalkarzinom ist bezüglich des Einflusses von körperlicher Betätigung und Erkrankungswahrscheinlichkeit eine der am besten untersuchten Krebserkrankungen. Verschiedene Fall-Kontroll- und Kohortenstudien haben gezeigt, dass mit zunehmender körperlicher Betätigung das Risiko für diese Krebsform abnimmt.[33][63][64][65][66][67] Bei Krebserkrankungen des Rektums besteht offensichtlich keine Korrelation zur körperlichen Aktivität der Patienten.[68] Über die Ursachen der Reduzierung der Erkrankungswahrscheinlichkeit beim Kolonkarzinom durch erhöhte körperliche Aktivität herrscht noch weitgehend Unklarheit. Möglicherweise sind die durch körperliche Aktivität reduzierten Insulin- und IGF-1-Spiegel im Blut der Grund für diesen Effekt.[69][70][1]
Bronchialkarzinom
Die Mehrzahl der auf diesem Gebiet durchgeführten klinischen Studien kommt zu dem Ergebnis, dass durch körperliche Aktivität das Risiko für ein Bronchialkarzinom gesenkt werden kann. Bei moderatem Freizeitsport sinkt das Risiko um 13 %, bei Leistungssport um 30 %. Dies gilt für beide Geschlechter, mit einem geringfügig höheren positiven Einfluss bei Frauen.[71][72][73][74]
Die biologischen Mechanismen, die zu einer Abnahme des Risikos für ein Bronchialkarzinom durch körperliche Aktivität führen, sind weitgehend unklar. Verschiedene mögliche Mechanismen werden diskutiert, unter anderem die durch die körperliche Aktivität reduzierten Insulin-, IGF-, Glucose- und Triglycerid-Spiegel sowie die erhöhten Spiegel an High Density Lipoprotein.[75] Auch das ‚Training‘ des Immunsystems, das durch sportliche Betätigung die Anzahl und Aktivität von Makrophagen, NK-Zellen und zytotoxischen T-Zellen steigert, wird als Erklärungsmodell diskutiert.[76][77][78][79][80][81]
Präventive Impfung
- → siehe Hauptartikel: HPV-Impfstoff und Hepatitis B
Die präventive Impfung gegen bestimmte onkogene Viren, also Viren mit tumorauslösenden Eigenschaften, ist eine der wirksamsten Maßnahmen zur Vermeidung bestimmter Krebserkrankungen. Infektiöse Erreger und dabei im Wesentlichen onkogene Viren werden in Deutschland und den Vereinigten Staaten für etwa 5 % aller Krebserkrankungen verantwortlich gemacht.[82] Dazu gehören humane Papillomviren (HPV), Hepatitis B und C, das Epstein-Barr-Virus (EBV), das humane Herpesvirus 8 (HHV-8), das humane T-lymphotropes Virus 1 (HTLV-1) und das Merkelzell-Polyoma-Virus.
Durch die Impfung gegen Hepatitis-B-Virus kann die Wahrscheinlichkeit für ein Leberzellkarzinom (hepatozelluläres Karzinom, HCC für hepatocellular carcinoma) erheblich gesenkt werden. In Asien und Afrika ist das durch Hepatitis B verursachte Leberzellkarzinom einer der häufigsten bösartigen Tumoren. Die Weltgesundheitsorganisation hat 1992 alle Mitgliedstaaten aufgefordert, die Hepatitis-B-Impfung in die nationalen Impfprogramme aufzunehmen.[83] In Taiwan konnte so die HCC-Inzidenz erheblich gesenkt werden.[84][85][86] 2006 wurde der erste Impfstoff gegen humane Papillomviren (HPV) zugelassen. Infektionen mit diesen Viren können Tumoren speziell im Anogenitalbereich (Anus und Genitalien) hervorrufen. Zu den durch HPV induzierten Krebserkrankungen gehören unter anderem das Zervixkarzinom (Gebärmutterhalskrebs), Vulvakrebs, Peniskarzinom und Analkarzinom. Die Hochrisiko-HPV-Typen 16 und 18 werden weltweit für ca. 70 % aller Zervixkarzinome verantwortlich gemacht.[87]
Die therapeutische Impfung (Krebsimmuntherapie), beispielsweise mit Sipuleucel-T gegen das Prostatakarzinom, ist keine Krebsprävention.
Eradikation von Helicobacter pylori
→ siehe Hauptartikel: Helicobacter pylori
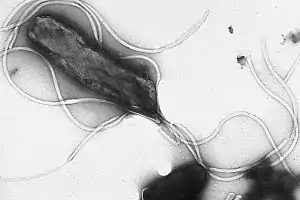
Die chronische Infektion mit dem im Magen befindlichen Stäbchenbakterium Helicobacter pylori ist ein Risikofaktor für die Entstehung eines Magenkarzinoms und eines MALT-Lymphoms. Weltweit ist etwa die Hälfte der Bevölkerung mit H. pylori infiziert.[88] Davon erkrankt nur ein kleiner Bruchteil an einer chronischen Gastritis, die der Ausgangspunkt für die Entwicklung eines Magenkarzinoms sein kann. In der Summe sterben weltweit jährlich etwa 500.000 Menschen an einem von H. pylori verursachten Magenkarzinom.[89] Die Infektionsrate ist in Entwicklungsländern erheblich höher als in Industrienationen. In Deutschland sind dennoch etwa 33 Millionen Menschen mit H. pylori infiziert. Die Mortalität von H. pylori wird von der Allgemeinheit völlig falsch eingeschätzt. Magenkrebs ist weltweit die zweithäufigste Krebstodesursache und man geht davon aus, dass der weitaus größte Teil dieser Todesfälle durch H. pylori verursacht wird.[90]
Die Eradikation von Helicobacter pylori, also die vollständige Vernichtung dieses Krankheitserregers, ist nach den Maastricht-Leitlinien der European Helicobacter pylori Study Group (EHPSG) nach bestimmten Kriterien indiziert.[91][92] Die Therapie erfolgt in der Regel durch die orale Gabe von zwei Antibiotika und einem Protonenpumpenhemmer. Ein zugelassener Impfstoff ist derzeit (2010) noch nicht verfügbar. Bei Magenbeschwerden raten die meisten Ärzte zu einer Therapie gegen die Infektion. Die molekularbiologischen Zusammenhänge zwischen Infektion und Karzinogenese sind noch weitgehend unklar. Einige Studien zeigen einen Zusammenhang zwischen dem Verzehr von viel Fleisch und der bakteriellen Erkrankung. Speziell rotes Fleisch fördert durch seinen hohen Eisengehalt offensichtlich das Wachstum des Bakteriums.[93]
Chemoprävention – Arzneimittel zur Krebsvorbeugung
Die Entwicklung von einer normalen Zelle bis zu einem Tumor geht über verschiedene präkanzeröse Stufen, bei denen genetische Veränderungen in den Zellen akkumulieren. Diesen Veränderungen (Entartungen) entgegenzuwirken ist das Ziel der Chemoprävention. Dazu können synthetische Substanzen und Naturstoffe verwendet werden. Sie sollen die präkanzerösen Prozesse im normalen Gewebe oder in den gutartigen Krebsvorstufen verlangsamen, hemmen oder gar rückgängig machen.[94]
Derzeit (Stand 2010) ist nur der Arzneistoff Tamoxifen von der Food and Drug Administration für die Prävention von Brustkrebs bei Frauen mit einem erhöhten Erkrankungsrisiko[95] zugelassen. Eine Reihe von anderen Substanzen befindet sich in der klinischen Erprobung. Dazu gehören unter anderem nichtsteroidale Antiphlogistika (non steroidal anti inflammatory drugs, NSAID) wie beispielsweise COX-2-Hemmer[96] oder Acetylsalicylsäure („Aspirin“).[97][98][99] Diese Arzneistoffe sind für andere Indikationen, aber nicht zur Chemoprävention, zugelassen. In Studien mit Patienten, die über einen längeren Zeitraum NSAIDs – beispielsweise zur Behandlung rheumatischer Erkrankungen – erhielten, konnte eine signifikante Reduzierung des Krebsrisikos festgestellt werden. Für Brustkrebs sank das Risiko um 25 %, für kolorektales Karzinom um 43 %, Bronchialkarzinom um 28 % und Prostatakrebs um 27 %.[100] Die dauerhafte Einnahme dieser Arzneistoffe ist unter Umständen mit erheblichen Nebenwirkungen verbunden. Ein Off-Label-Use wird nur bei Hochrisikopatienten, beispielsweise mit familiärer adenomatöse Polyposis (FAP) nach einer ileorektalen Anastomose, als sinnvoll angesehen.[101]
Operative Krebspräventionen
Die prophylaktische Mastektomie, also die vorbeugende Entfernung (Amputation) beider Brüste einer Frau, die ein hohes genetisch bedingtes Risiko (Prädisposition) trägt, an Brustkrebs zu erkranken, ist die sicherste Methode Brustkrebs zu verhindern.[102][103] Die Morbidität dieser Maßnahme ist sehr hoch. Während sich beispielsweise in den Vereinigten Staaten oder den Niederlanden sehr viele Hochrisikopatientinnen für diese Form der Krebsprävention entscheiden, sind deutsche Frauen der gleichen Risikogruppe wesentlich zurückhaltender.[104] In Österreich entscheiden sich 11 Prozent der Risikopatientinnen für die vorbeugende Entfernung der beiden Brüste.[105]
Eine weitere operative Krebsprävention, die bei Hochrisikopatientinnen – beispielsweise mit BRCA1-Mutation – durchgeführt werden kann, ist die prophylaktische Ovariektomie, die vorbeugende Entfernung beider Eierstöcke (Ovarien).[106][107][108]
Die beidseitige Orchiektomie (Kastration) ist die älteste Therapieform des Prostatakarzinoms.[109] Prinzipiell kann dieser Eingriff auch präventiv erfolgen. Kastraten können aufgrund des Testosteronmangels nicht an einem Prostatakarzinom erkranken. Bedingt durch die hohe Morbidität, verbunden mit psychologischen Barrieren und fehlenden Prädispositionen (keine Hochrisikopatienten), wird die beidseitige Orchiektomie nicht präventiv angewandt.
Krebsprävention – Krebsvorsorge
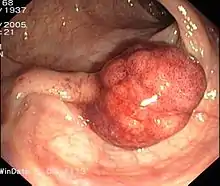
Im Grenzbereich zwischen Krebsprävention und Krebsvorsorge befindet sich die Behandlung von präkanzerösen Gewebeveränderungen. So ist beispielsweise die Entfernung von gutartigen Dickdarmpolypen bei einer Koloskopie (Darmspiegelung) eine Krebsprävention im Rahmen einer Vorsorgeuntersuchung. Aus den fakultativ präkanzerösen Dickdarmpolypen können über die Adenom-Karzinom-Sequenz im Laufe der Jahre kolorektale Karzinome entstehen. Erste Studien aus dem Rhein-Neckar-Raum zeigen, dass durch Koloskopie das Darmkrebsrisiko um bis zu 64 Prozent reduziert werden kann.[52]
Weiterführende Literatur
Fachbücher
- Harald zur Hausen und Katja Reuter: Gegen Krebs. Die Geschichte einer provokativen Idee, Rowohlt Verlag, Reinbek bei Hamburg 2010, ISBN 978-3-498-03001-8
- D. S. Alberts und L. M. Hess: Fundamentals of Cancer Prevention. Verlag Springer, 2009, ISBN 3-540-68985-0 eingeschränkte Vorschau in der Google-Buchsuche
- H. J. Senn u. a.: Cancer prevention. Band 2, Verlag Springer, 2008, ISBN 3-540-69296-7 eingeschränkte Vorschau in der Google-Buchsuche
- J. H. Bessiel: Progress in Cancer Prevention. Nova Publishers, 2008, ISBN 1-60456-327-3 eingeschränkte Vorschau in der Google-Buchsuche
- H. J. Senn u. a.: Tumor prevention and genetics. Band 3, Verlag Springer, 2005, ISBN 3-540-22228-6 eingeschränkte Vorschau in der Google-Buchsuche
- G. A. Colditz und C. J. Stein: Handbook of cancer risk assessment and prevention. Jones & Bartlett Learning, 2004, ISBN 0-7637-1883-1 eingeschränkte Vorschau in der Google-Buchsuche
- H. Vainio u. a.: Mechanisms in carcinogenesis and cancer prevention. Verlag Springer, 2003, ISBN 3-540-43837-8 eingeschränkte Vorschau in der Google-Buchsuche
- G. A. Colditz und D. J. Hunter: Cancer prevention: the causes and prevention of cancer. Verlag Springer, 2000, ISBN 0-7923-6603-4 eingeschränkte Vorschau in der Google-Buchsuche
- H. Theml: Krebs und Krebsvermeidung. Verlag C.H. Beck, 2005, ISBN 3-406-50880-4 eingeschränkte Vorschau in der Google-Buchsuche
- H. Theml: Krebszellen mögen keine Himbeeren Nahrungsmittel gegen Krebs. Das Immunsystem stärken und gezielt vorbeugen. Kösel-Verlag, 2017. ISBN 978-3-466-34663-9
Regelmäßig erscheinende Journals zum Thema Krebsprävention
- Cancer Prevention Research: monatlich erscheinendes Peer-Review-Journal der American Association for Cancer Research[110]
- Cancer Detection and Prevention: zweimonatlich erscheinendes peer-refereed Journal der International Society for Preventive Oncology[111]
Weblinks
- Krebsvorbeugung und Krebsfrüherkennung, Krebsinformationsdienst des Deutschen Krebsforschungszentrums (DKFZ), Heidelberg. Vom 3. Februar 2012, zuletzt abgerufen am 4. September 2014.
- Cancer Prevention American Cancer Society (ACS) (englisch)
- Cancer Prevention Weltgesundheitsorganisation (WHO) (englisch)
- Cancer Prevention National Cancer Institute (NCI) (englisch)
- Food, Nutrition, Physical Activity and the Prevention of Cancer: a Global Perspective. World Cancer Research Fund / American Institute for Cancer Research Expert Report, 2007.
Einzelnachweise
- Y. M. Coyle: Lifestyle, genes, and cancer. In: Methods Mol Biol 472, 2009, S. 25–56. PMID 19107428
- Islami F et al. Proportion and number of cancer cases and deaths attributable to potentially modifiable risk factors in the United States. CA Cancer J Clin. (online) 21. November 2017
- European Code Against Cancer and scientific justification. (Memento des Originals vom 25. März 2010 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. Vom 2. Juli 2003, abgerufen am 10. Juni 2010
- Grundlagen – Krebsentstehung und Metastasenbildung: Was ist Krebs?, Krebsinformationsdienst des Deutschen Krebsforschungszentrums (DKFZ), Heidelberg. Vom 19. April 2011, zuletzt abgerufen am 4. September 2014
- Harvard Report on Cancer Prevention. Volume 1: Causes of human cancer. In: Cancer Causes & Control 7, 1996, S. S3–59. PMID 9091058
- Universitätsklinikum Heidelberg: Krebsvorbeugung (Memento vom 21. Februar 2010 im Internet Archive) Abgerufen am 10. Juni 2010
- cancercode.org: Do not smoke; if you smoke, stop doing so. If you fail to stop, do not smoke in the presence of non-smokers. (Memento des Originals vom 12. April 2010 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. Vom 2. Juli 2003, abgerufen am 10. Juni 2010
- M. Spitz: Epidemiology and risk factors for head and neck cancer. In: Semin Oncol 21, 1994, S. 281–288. PMID 8209260
- P. Reynolds u. a.: Active smoking, household passive smoking, and breast cancer: evidence from the California Teachers Study. In: Journal of the National Cancer Institute 96, 2004, S. 29–37. PMID 14709736
- C. Nagata u. a.: Tobacco smoking and breast cancer risk: an evaluation based on a systematic review of epidemiological evidence among the Japanese population. In: Jpn J Clin Oncol 36, 2006, S. 387–394. PMID 16766567
- E. Botteri u. a.: Smoking and colorectal cancer: a meta-analysis. In: JAMA 300, 2008, S. 276–2778. PMID 19088354
- P. S. Liang u. a.: Cigarette smoking and colorectal cancer incidence and mortality: systematic review and meta-analysis. In: Int J Cancer 124, 2009, S. 2406–2415. PMID 19142968 (Review)
- H. Nisa u. a.:Cigarette smoking, genetic polymorphisms and colorectal cancer risk: the Fukuoka Colorectal Cancer Study. (PDF; 852 kB) In: BMC Cancer 10, 2010, 274. doi:10.1186/1471-2407-10-274 (Open Access)
- Y. Li u. a.: Wine, liquor, beer and risk of breast cancer in a large population. In: Eur J Cancer 45, 2009, S. 843–850. PMID 19095438
- N. Khan u. a.: Lifestyle as risk factor for cancer: Evidence from human studies. In: Cancer Lett 293, 2010, S. 133–143. PMID 20080335 (Review)
- L. S. Morch u. a.: Alcohol drinking, consumption patterns and breast cancer among Danish nurses: a cohort study. In: Eur J Public Health 17, 2007, S. 624–629. PMID 17442702
- S. A. Oliveria u. a.: Sun exposure and risk of melanoma. In: Arch Dis Child 91, 2006, S. 131–138. PMID 16326797, PMC 2082713 (freier Volltext) (Review)
- Pflanzenbetonte Ernährung und viel Bewegung sind beste Krebsprävention. Abgerufen am 11. März 2021.
- WCRF (Hrsg.): Der Dritte Expertenbericht. 2020 (wcrf.org [PDF]).
- Ernährungsumschau 3/2021, Seite M151
- Ernährungsumschau 3/2021, Seite M151
- Ernährungsumschau 3/2021, Seite M154
- C. Müller: Wie die Nahrung schützen kann. (Memento vom 5. Juli 2004 im Internet Archive) In: UGB-Forum 1, 1999, S. 14–17.
- Ernährungsumschau 3/2021, Seite M155
- Ernährungsumschau 3/2021, Seite M154
- S. M. Lippman u. a.: Effect of Selenium and Vitamin E on Risk of Prostate Cancer and Other Cancers. The Selenium and Vitamin E Cancer Prevention Trial (SELECT). In: JAMA 301, 2009, S. 39–51. PMID 19066370
- The Effect of Vitamin E and Beta Carotene on the Incidence of Lung Cancer and Other Cancers in Male Smokers, in: NEJM 330, 1994, S. 330–335. PMID 8127329
- R. Goralczyk: Beta-carotene and lung cancer in smokers: review of hypotheses and status of research. In: Nutr Cancer 61, 2009, S. 767–774. PMID 20155614 (Review)
- S. Offermann:β-Carotin erhöht bei Rauchern und Trinkern das Darmkrebsrisiko. In: Bild der Wissenschaft. 21. Mai 2003, abgerufen am 8. September 2019.
- Ernährungsumschau 3/2021, S. 154
- Ernährungsumschau 3/2021, Seite M151
- C. M. Friedenreich: Review of anthropometric factors and breast cancer risk. In: Eur J Cancer Prev 10, 2001, S. 15–32. PMID 11263588 (Review)
- Weight control and physical activity. In: IARC Working Group on the Evaluation of Cancer-Preventive Agents. World Health Organization und IARC (Herausgeber), Band 6, IARC Handbooks of Cancer Prevention, 2002, ISBN 92-832-3006-X
- M. C. Boutron-Rualt u. a.: Energy intake, body mass index, physical activity and the colorectal adenoma-carcinoma sequence. In: Nutr Cancer 39, 2001, S. 50–57. PMID 11588902
- A. I. Neugut u. a.: Obesity and colorectal adenomatous polyps. In: J Natl Cancer Inst 83, 1991, S. 359–361. PMID 1995919
- K. Shinchi u. a.: Obesity and adenomatous polyps of the sigmoid colon. In: Jpn J Cancer Res 85, 1994, S. 479–484. PMID 8014105
- A. L. Davidow u. a.: Recurrent adenomatous polyps and body mass index. In: Cancer Epidemiol Biomarkers Prev 5, 1996, S. 313–315. PMID 8722224
- E. Giovannucci u. a.: Physical activity, obesity and risk of colorectal adenoma in women (United States). In: Cancer Causes Control 7, 1996, S. 253–263. PMID 8740738
- C. L. Bird u. a.: Obesity, weight gain, large weight changes and adenomatous polyps of the left colon and rectum. In: Am J Epidemiol 147, 1998, S. 670–680. PMID 9554606
- S. Kono u. a.: Obesity, weight gain and risk of colon adenomas in Japanese men. In: Jpn J cancer Res 90, 1999, S. 801–811. PMID 10543250
- A. Lukanova u. a.: Body mass index and cancer. Results from the northern Sweden health and disease cohort. In: Int J Cancer 118, 2006, S. 458–466. PMID 16049963
- R. J. MacInnis u. a.: Body size and composition and colon cancer risk in men. In: Cancer Epidemiol Biomarkers Prev 13, 2004, S. 553–559. PMID 15066919
- R. J. MacInnis u. a.: Body size and composition and colon cancer risk in men. In: Cancer Epidemiol Biomarkers Prev 13, 2004, S. 553–559. PMID 15066919
- L. L. Moore u. a.: BMI and waist circumference as predictors of lifetime colon cancer risk in Framingham Study adults. In: Int J Obes Relat Metab Disord 28, 2004, S. 559–567. PMID 14770200
- T. Pischon u. a.: Body size and risk of colon and rectal cancer in the European prospective investigation into cancer and nutrition (EPIC). In: J Natl Cancer Inst 98, 2006, S. 920–931.
- Körpermaße und Dickdarmkrebs-Risiko – Neue Ergebnisse der EPIC-Studie. (Memento des Originals vom 28. September 2013 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. DIfE-Pressemitteilung 11/2006, vom 5. Juli 2006
- R. J. MacInnis und D. R. English: Body size and composition and prostate cancer risk, systematic review and meta-regression analysis. In: Cancer Causes Control 17, 2006, S. 989–1003. PMID 16933050
- M. E. Wright u. a.: Prospective study of adiposity and weight change in relation to prostate cancer incidence and mortality. In: Cancer 109, 2007, S. 675–684. PMID 17211863
- A. W. Hsing u. a.: Prostate cancer risk and serum levels of insulin and leptin, a population based study. In: J Natl Cancer Inst 93, 2001, S. 783–789. PMID 11353789
- C. S. Mantzoros u. a.: Insulin-like growth factor 1 in relation to prostate cancer and benign prostatic hyperplasia. In: Br J Cancer 76, 1997, S. 1115–1118. PMID 9365156, PMC 2228109 (freier Volltext)
- Neue Ergebnisse der EPIC-Studie: Starkes Übergewicht erhöht Nierenkrebsrisiko bei Frauen. (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis. DIfE-Pressemitteilung 12/2005, vom 14. August 2005
- F. Schubert: Viele Krebsfälle sind vermeidbar: Wie man sich schützen kann. (PDF; 3,7 MB) In: einblick Deutsches Krebsforschungszentrum (Hrsg.), 1, 2010, S. 21–24.
- K. Smallbne u. a.: Episodic, transient systemic acidosis delays evolution of the malignant phenotype: Possible mechanism for cancer prevention by increased physical activity. In: Biology Direct 5, 2010, 22. doi:10.1186/1745-6150-5-22 PMID 20406440 (Open Access)
- J. Kruk: Lifetime physical activity and the risk of breast cancer: a case-control study. In: Cancer Detect Prev 31, 2007, S. 18–28. PMID 17296272
- G. Jasienska u. a.: Habitual physical activity and estradiol levels in women of reproductive age. In: Eur J Cancer Prev 15, 2006, S. 439–445. PMID 16912573
- A. McTiernan u. a.: Effect of exercise on serum estrogens in postmenopausal women, a 12-month randomized trial. In: Cancer Res 64, 2004, S. 2923–2928. PMID 15087413
- S. R. Cummings u. a.: Prevention of breast cancer in postmenopausal women: approaches to estimating and reducing risk. In: J Natl Cancer Inst 101, 2009, S. 384–398. PMID 19276457 PMC 2720698 (freier Volltext)
- J. A. Cauley u. a.: The epidemiology of serum sex hormones in postmenopausal women. In: Am J Epidemiol 129, 1989, S. 1120–1131. PMID 2729251
- M. E. Nelson u. a.: Hormone and bone mineral status in endurancetrained and sedentary postmenopausal women. In: J Clin Endocrinol Metab 66, 1988, S. 927–933. PMID 3360900
- C. M. Friedenreich und M. R. Orenstein: Physical activity and cancer prevention: etiologic evidence and biological mechanisms. In: J Nutr 132, 2002, S. 3456S–3464S. PMID 12421870
- S. Suzuki u. a.: Effect of physical activity on breast cancer risk: findings of the Japan collaborative cohort study. In: Cancer Epidemiol Biomarkers Prev 17, 2008, S. 3396–3401. PMID 19029398
- L. Bernstein u. a.: Physical exercise and reduced risk of breast cancer in young women. In: J Natl Cancer Inst 86, 1994, S. 1403–1408. PMID 8072034
- M. Slattery: Physical activity and colorectal cancer. In: Sports Med 34, 2004, S. 239–252. PMID 15049716
- M. Slattery: Physical activity and colorectal cancer. In: Am J Epidemiol 158, 2003, S. 214–224. PMID 12882943
- B. A. Calton u. a.: Physical activity and the risk of colon cancer among women, a prospective cohort study (United States). In: Int J Cancer 119, 2006, S. 385–291. PMID 16489545
- S. C. Larsson u. a.: Physical activity, obesity and risk of colon and rectal cancer in a cohort of Swedish men. In: Eur J Cancer 42, 2006, S. 2590–2597. PMID 16914307
- C. Friedenreich u. a.: Physical activity and risk of colon and rectal cancers, the European prospective investigation into cancer and nutrition. In: Cancer Epidemiol Biomarkers Prev 15, 2006, S. 2398–2407. PMID 17164362
- K. J. Lee u. a.: Physical activity and risk of colorectal cancer in Japanese men and women, the Japan Public Health Center-based prospective study. In: Cancer Causes Control 18, 2007, S. 199–209. PMID 17206529
- R. Kaaks u. a.: Serum C-peptide, insulin-like growth factor (IGF)-I, IGF-binding proteins, and colorectal cancer risk in women. In: J Natl Cancer Inst 92, 2000, S. 1592–1600. PMID 11018095
- J. Ma u. a.: Prospective study of colorectal cancer risk in men and plasma levels of insulin-like growth factor (IGF)-I and IGF-binding proteins-3. In: J Natl Cancer Inst 91, 1999, S. 620–625. PMID 10203281
- P. Sinner u. a.: The association of physical activity with lung cancer incidence in a cohort of older women. The Iowa women’s health study. In: Cancer Epidemiol Biomarkers Prev 15, 2006, S. 2359–2363. PMID 17164357
- C. M. Alfano u. a.: Physical activity in relation to all-site and lung cancer incidence and mortality in current and former smokers. In: Cancer Epidemiol Biomarkers Prev 13, 2004, S. 2233–2241. PMID 15598785
- H. Bak u. a.: Physical activity and risk for lung cancer in a Danish cohort. In: Int J Cancer 116, 2005, S. 439–445. PMID 15800940
- K. Steindorf u. a.: Physical activity and lung cancer risk in the European prospective investigation into cancer and nutrition cohort. In: Int J Cancer 119, 2006, S. 2389–2397. PMID 16894558
- C. M. Friedenreich: Physical activity and cancer prevention: from observacional to intervention research. In: Cancer Epidemiol Biomarkers Prev 10, 2001, S. 287–301. PMID 11319168
- R. Ballard-Barbash u. a.: Physical activity across the cancer continuum: review of existing knowledge and innovative designs for future research. In: Cancer 95, 2002, S. 1134–1143. PMID 12209701
- J. A. Woods u. a.: Effects of the exercise on the immune response to cancer. In: Med Sci Sports Exerc. 26, 1994, S. 1109–1115. PMID 7808244
- J. A. Woods u. a.: Exercise and cellular innate immune function. In: Med Sci Sports Exerc 31, 1999, S. 57–66. PMID 9927011
- B. K. Pedersen u. a.: NK cell response to physical activity: possible mechanism of action. In: Med Sci Sports Exerc 26, 1994, S. 140–146. PMID 8164530
- A. Nomura u. a.: Prospective study of pulmonary function and lung cancer. In: Am Rev Respir Dis 144, 1991, S. 307–311. PMID 1859052
- A. Tardon u. a.: Leisure-time physical activity and lung cancer, a meta-analysis. In: Cancer Causes Control 16, 2005, S. 389–397. PMID 15953981, PMC 1255936 (freier Volltext)
- krebsatlas.de: Infektiöse Erreger. (Memento des Originals vom 31. Juli 2010 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. Vom 6. November 2007, abgerufen am 27. Februar 2010
- who.int: New and Under-utilized Vaccines Implementation (NUVI): Hepatitis B. Abgerufen am 11. Juni 2010 (englisch)
- M. G. Chang u. a.: Decreased Incidence of Hepatocellular Carcinoma in Hepatitis B Vaccinees: A 20-Year Follow-up Study. In: J Natl Cancer Inst 101, 2009, S. 1348–1355. PMID 19759364
- M. H. Chang: Cancer prevention by vaccination against hepatitis B. In: Recent Results Cancer Res 181, 2009, S. 85–94. PMID 19213561
- Y. H. und D. S. Chen: Hepatitis B vaccination in children: The Taiwan experience. In: Pathol Biol (Paris) 2010 [Epub ahead of print] PMID 20116181
- M. L. Gillison u. a.: HPV prophylactic vaccines and the potential prevention of noncervical cancers in both men and women. In: Cancer 113, 2008, S. 3036–3046. doi:10.1002/cncr.23764 PMID 18980286 (Review)
- J. Torrs u. a.: A comprehensive review of the natural history of Helicobacter pylori infection in children. In: Arch Med Res 31, 2000, S. 431–469. PMID 11179581 (Review)
- Helicobacter pylori. In: ZCT 1, 2008
- C. Pfaff: Magenkeim Helicobacter pylori für Entstehung von Magenkrebs bedeutender als angenommen. In: Bild der Wissenschaft (Online) Vom 13. September 2003
- P. Malfertheiner u. a.: Current concepts in the management of Helicobacter pylori infection – The Maastricht 2-2000 Consensus Report. (Memento des Originals vom 6. August 2010 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 322 kB) In: Aliment Pharmacol Ther 16, 2002, S. 167–180. PMID 11860399
- P. Malfertheiner u. a.: Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report. In: Gut 56, 2007, S. 772–781. PMID 17170018, PMC 1954853 (freier Volltext)
- Risikofaktoren und Auslöser: Wie entsteht Magenkrebs? Vom 30. März 2006, abgerufen am 11. Juni 2010
- C. Gerhäuser: Chemoprävention von Krebs. (Memento des Originals vom 23. September 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 1,0 MB) In: Forum DKG 4, 2007, S. 5–9.
- J. Cuzick u. a.: Overview of the main outcomes in breast cancer prevention trials. In: The Lancet 361, 2003, S. 296–300. PMID 12559863
- G. A. Doherty und F. E. Murray: Cyclooxygenase as a target for chemoprevention in colorectal cancer: lost cause or a concept coming of age? In: Expert Opin Ther Targets 13, 2009, S. 209–218. PMID 19236238 (Review)
- D. A. Corley u. a.: Protective association of aspirin/NSAIDs and esophageal cancer: a systematic review and meta-analysis. In: Gastroenterology 124, 2003, S. 47–56. PMID 12512029 (Review)
- J. A. Baron: Epidemiology of non-steroidal anti-inflammatory drugs and cancer. In: Prog Exp Tumor Res 37, 2003, S. 1–24. PMID 12795046 (Review)
- W. H. Wang u. a.: Non-steroidal anti-inflammatory drug use and the risk of gastric cancer: a systematic review and meta-analysis. In: J Natl Cancer Inst 95, 2003, S. 1784–1791. PMID 14652240 (Review)
- R. E. Harris: Inflammopharmacology. 17, 2009, S. 55–67. PMID 19340409 (Review)
- T. Gottstein und H. Koop: Prävention gastrointestinaler Tumoren. (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 1,4 MB) In: Forum DKG 2/2004 S. 40–45.
- H. Meijers-Heiboer u. a.: Breast cancer after prophylactic bilateral mastectomy in women with a BRCA1 oder BRCA2 mutation. In: N Engl J Med 345, 2001, S. 159–164. PMID 11463009
- L. C. Hartmann u. a.: Efficacy of Bilateral Prophylactic Mastectomy in Women with a Family History of Breast Cancer. In: N Engl J Med 340, 1999, S. 77–84. PMID 9887158
- K. Kast u. a.: Klinisches Management des familiären Mammakarzinoms – Eine Versorgungsstudie der Krankenkassen. In: Ärzteblatt Sachsen 2, 2006, S. 73–76.
- Prophylaktische Mastektomie. (Memento des Originals vom 27. Oktober 2007 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. In: Ärztewoche Online 18, 2004
- K. A. Metcalfe: Oophorectomy for breast cancer prevention in women with BRCA1 or BRCA2 mutations. In: Womens Health (Lond Engl) 5, 2009, S. 63–68. PMID 19102642 (Review)
- A. Russo u. a.: Hereditary ovarian cancer. In: Crit Rev Oncol Hematol 69, 2009, S. 28–44. PMID 18656380 (Review)
- R. B. Dann u. a.: Strategies for ovarian cancer prevention. In: Obstet Gynecol Clin North Am 34, 2007, S. 667–686. PMID 18061863 (Review)
- Krebsinformationsdienst des DKFZ: Prostatakrebs, Therapieverfahren: Hormonelle Therapie. vom 31. Juli 2008, abgerufen am 13. Juni 2010
- About Cancer Prevention Research. Abgerufen am 10. Juni 2010
- International Society for Preventive Oncology. Abgerufen am 10. Juni 2010