Cyproteron
Cyproteron ist ein synthetisches Progesteron-Derivat. Es wirkt als kompetitiver Antagonist am Androgenrezeptor, hat eine gestagene und eine antiandrogene Wirkkomponente. Die antiandrogene Wirkung wird durch einen cis-verknüpften Cyclopropanring im Ring A des Steroid-Grundgerüstes vermittelt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
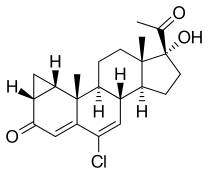 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Cyproteron | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C22H27ClO3 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
G03HA01 | ||||||||||||||||||
| Wirkstoffklasse | |||||||||||||||||||
| Wirkmechanismus |
kompetitiver Androgenrezeptor-Antagonist | ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 374,91 g·mol−1 | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Verwendung findet gewöhnlich der Essigsäureester des Cyproterons, das Cyproteronacetat.[2] Die Anwendung des Präparates ist beschränkt, da der Wirkstoff dosisabhängig mit dem Auftreten von Meningeomen in Verbindung gebracht wird.[3]
Wirkung
Therapeutische Anwendung findet der Wirkstoff bei Hypersexualität, schweren Formen von Akne, Hirsutismus (vermehrte Behaarung) und weiblicher Alopezie (androgenbedingter Haarausfall).
Bei transidenten Frauen wird er in Kombination mit Estrogenen zur Unterstützung der Feminisierung eingesetzt. Es reichen in der Regel weit weniger als 50 mg pro Tag (etwa 5 bis 10 mg), um die gewünschten verweiblichenden Effekte, wie etwa Verminderung von Körperbehaarung, Körpergeruch und Muskulatur, Verlangsamen bis Stoppen von Alopezie (androgenetischer Haarausfall) sowie Brustwachstum zu erreichen. Bei Transfrauen, bei welchen eine geschlechtsangleichende Genitaloperation nicht erfolgt ist, unterdrückt das Cyproteron, wie bei Männern, die Spermiogenese.
Bei metastasierten und nicht operablen Prostatakarzinomen ist Cyproteron eine Alternative zur Behandlung mit GnRH-Analoga. Eine weitere Indikation ist die hormonelle Kastration.
Nebenwirkungen
Bei Männern sind die am häufigsten berichteten Nebenwirkungen ein verringerter Geschlechtstrieb (Libido), erektile Dysfunktion und die reversible Hemmung der Spermatogenese, bei Frauen Zwischenblutungen, Gewichtszunahme und depressive Verstimmungen. Veränderungen an der Brustdrüse (Gynäkomastie) und Müdigkeit tritt bei Männern häufig auf, bei Frauen (Schmerzen und Spannungsgefühl in der Brust, Müdigkeit) ist die Häufigkeit nicht bekannt. Bei beiden Geschlechtern betreffen die schwerwiegendsten Nebenwirkungen gutartige und bösartige Lebertumore und thromboembolische Ereignisse, die jedoch sehr selten auftreten.[4]
Frauen, die Cyproteronacetat in Kombination mit Ethinylestradiol einnehmen, haben ein erhöhtes Risiko für Thromboembolien wie etwa Lungenembolie, venöse Thrombose, Schlaganfall oder Herzinfarkt. Nachdem es in Frankreich zu Todesfällen kam, forderte die französische Arzneimittelbehörde die Marktrücknahme der fixen Kombination 2 mg Cyproteronacetat und 35 µg Ethinylestradiol in Frankreich; die europäische Arzneimittelagentur leitete daraufhin im Februar 2013 ein Risikobewertungsverfahren für solche Präparate ein.[5]
Im Juni 2013 informierten die Hersteller und Vertreiber von Präparaten mit der Wirkstoffkombination Cyproteronacetat/Ethinylestradiol in Rote-Hand-Briefen über diese Nutzen-Risiko-Bewertung durch die EMA zusammen mit einem Warnhinweis über ein erhöhtes Risiko für venöse und arterielle Thromboembolien (VTE und ATE).[6]
Im Februar 2020 hat der Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz (PRAC) der Europäischen Arzneimittel-Agentur (EMA) zusätzliche Sicherheitsmaßnahmen bei der Verordnung von Cyproteron empfohlen. Damit soll das Risiko von Meningeomen, also gutartigen Hirntumoren, minimiert werden. Es wird geraten, Cyproteron in Dosen von täglich 10 mg oder mehr nur bei Hirsutismus, Alopezie, Akne und Seborrhö einzusetzen, falls andere Behandlungsoptionen, einschließlich der Therapie mit geringeren Mengen des Pharmakons, versagt haben. Sobald höhere Dosen zu wirken beginnen, sollte die Gabe wieder verringert werden. Die Empfehlungen sind noch umfangreicher und lassen sich im Original der Meldung (englisch) nachlesen.[7]
Medikamententests
Der Journalist Charly Kowalczyk berichtet in einem Feature auf Deutschlandfunk über Medikamententests des Präparats Androcur an Männern mit geistiger Behinderung.[8][9] Auf SWR2 versucht er, mögliche Langzeitfolgen der versuchsweisen Verabreichung von Cyproteronacetat an Jugendliche in einem deutschen Heim Anfang der siebziger Jahre anhand eines Einzelschicksals zu ergründen.[10][11]
Handelsnamen
- Monopräparate
- Androbas (CH), Androcur (D, A, CH), Andro-Diane (A), MaskuPel (A), Virilit (D), Generika (D, CH), Cyprostat (AU)
- Kombinationspräparate
- Attempta (D), Bella HEXAL (D), Bellgyn (A), Clevia (D), Climen (D, A, CH), Cyproderm (D), Cypestra (CH), Dialuna (A), Diane (D, A, CH), Elleacnelle (CH), Ergalea (D), Feminac (CH), Femogyn (A), Holgyeme (CH), Midane (A), Minerva (A, CH), Morea Sanol (D), Xylia (A), Generika (A)
Einzelnachweise
- Datenblatt Cyproterone acetate bei Sigma-Aldrich, abgerufen am 30. Juni 2019 (PDF).
- Externe Identifikatoren von bzw. Datenbank-Links zu Cyproteron-Acetat: CAS-Nummer: 427-51-0, EG-Nummer: 207-048-3, ECHA-InfoCard: 100.006.409, PubChem: 9880, ChemSpider: 9496, DrugBank: DB04839, Wikidata: Q426185.
- A. Weill et al.: Exposition prolongée à de fortes doses d’acétate de cyprotérone et risque de méningiome chez la femme. In: Revue d’Épidémiologie et de Santé Publique, Volume 68, Supplement 1, März 2020, S. S3-S4, ansm.sante.fr (PDF) abgerufen am 29. April 2020
- Fachinformation Androcur 50 mg Tabletten, Stand Juni 2011.
- European Medicines Agency starts safety review of Diane 35 and its generics, Pressemitteilung der Europäischen Arzneimittelagentur (EMA) vom 8. Februar 2013.
- Rote Hand Brief Juni 2013. (PDF; 291 kB) Abgerufen am 23. Februar 2016.
- Meeting highlights from the Pharmacovigilance Risk Assessment Committee (PRAC) 10-13 February 2020, PM EMA vom 14. Februar 2020, abgerufen am 17. Februar 2020
- Charly Kowalczyk: Geistig behinderte Menschen als Versuchskaninchen pdf (PDF) 13. Dezember 2016.
- sueddeutsche.de
- Auf der Suche nach Schorsch. Medikamentenversuche an Jugendlichen und ihre Folgen, SWR2, Fünfteilige Feature-Serie von Charly Kowalczyk (jede Folge etwa 27:00 min), 19. September 2018. Abgerufen am 23. Oktober 2018
- Auf den Spuren von Schorsch. Medikamentenversuche an Jugendlichen und ihre Folgen, SWR2, Audiofeature von Charly Kowalczyk (53:46 min), 18. September 2018. Abgerufen am 23. Oktober 2018