Plasmolyse
Unter Plasmolyse wird in der Biologie die Schrumpfung des Protoplasten einer pflanzlichen Zelle verstanden, wobei sich die Plasmamembran von der Zellwand ablöst. Um dies zu erreichen, muss man die Zelle einem Plasmolytikum aussetzen. Bei diesem handelt es sich um eine hypertonische Lösung, d. h. eine Lösung, die reichlich Salze oder Zuckerbestandteile enthält und somit mehr gelöste Teilchen als der Zellsaft der Vakuole besitzt. In diesem Fall strömt auf osmotischem Wege Wasser aus der Vakuole durch die Membranen (Tonoplast, Plasmalemma) in das umgebende, konzentriertere Medium, sodass der Zellsaftraum kleiner wird und den an der Vakuole klebenden Plasmaschlauch mitsamt Plasmalemma von der Zellwand abtrennt. Bei geringer Wandhaftung des Plasmas erfolgt die Ablösung rundlich (Konvexplasmolyse), bei starker Wandhaftung bilden sich bizarre Formen, in denen das Plasma zu dünnen Fäden (Hechtsche Fäden) ausgezogen ist (Konkavplasmolyse). Dieser Vorgang ist reversibel, also über die Deplasmolyse umkehrbar (vorausgesetzt, die Zelle nahm durch eine übermäßige Plasmolyse keinen Schaden).
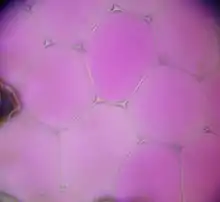
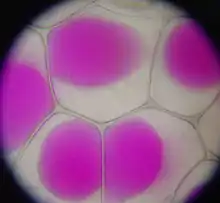
Den Zustand, bei dem sich der Protoplast gerade von der Zellwand löst – die Zelle also nicht mehr turgeszent, aber auch noch nicht richtig plasmolysiert ist –, nennt man Grenzplasmolyse. Dies ist in einem isotonischen Medium der Fall.
Ursache – die Osmose als Triebfeder der Plasmolyse
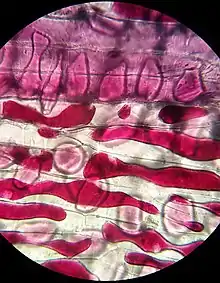
Befindet sich außerhalb von Zellen oder Geweben eine andere hoch konzentrierte Salzlösung oder eine andere hochkonzentrierte Substanz, so löst sich bereits nach kurzer Zeit der Protoplast von der Zellwand ab. Die Vakuole wird kleiner, bis sich der Protoplast im Extremfall vollständig von der Zellwand löst und schließlich als kugelförmiges Gebilde vorliegt.
Ursache
Die Konzentration der gelösten Stoffe im Wasser ist höher (hypertonisch) im Vergleich zum Innenbereich der Zelle. Derartige Ungleichgewichte gleichen sich in der Natur (wenn möglich) automatisch aus. Wasser diffundiert also aus dem Zellplasma und der Zellsaftvakuole hinaus. Die Triebfeder dieses hier stattfindenden Konzentrationsausgleiches ist die Osmose.
Der Ausgleich kommt nun vor allem durch das Diffundieren von Wasser durch die Zellmembran zustande. Dies ist alles nur möglich, weil Biomembranen vor allem für Wasser, nicht aber für gelöste Stoffe durchlässig sind. Man bezeichnet die Membran als semipermeabel (halb durchlässig) oder selektiv permeabel (nur für bestimmte Stoffe durchlässig). Die stattfindende Diffusion von Wasser durch eine selektiv permeable Membran nennt man auch Osmose.
Die hypotonische (also weniger gelöste Teilchen enthaltene) Lösung in der Zelle verliert Wasser, da die Wasserteilchen nach außen in die hypertone (höher konzentrierte) Lösung diffundieren. Mit der Abnahme der gelösten Wasserteilchen schrumpfen die Vakuole und das Cytoplasma im Inneren der Zelle.
Daraus folgt: Die Zugabe einer hypertonischen Lösung zur Zelle (bei der Plasmolyse) erhöht in Wirklichkeit die Salzkonzentration innerhalb der Zelle, welche sich somit dem Außenmedium in der Konzentration angleicht (und dieses wird ja zusätzlich durch das aus der Zelle strömende Wasser verdünnt) Der Vorgang ist umkehrbar; legt man die Zelle in destilliertes Wasser, so diffundiert dieses zurück in die Zelle und verdünnt dort die Lösung: Deplasmolyse.
Weisen beide Lösungen, Außenmedium und Zellinneres, die gleiche Konzentration eines gelösten Stoffes auf, so handelt es sich um isotonische Lösungen. Jedoch findet auch bei diesen Osmose statt, da die Osmose ein permanenter Vorgang ist. Anders als in hypertonischen und hypotonischen Lösungen ist jedoch die Wasserabgabe der Zelle gleich der Wasseraufnahme. Es handelt sich also um ein ständiges Fließgleichgewicht (auch dynamisches Gleichgewicht genannt) zwischen den isotonischen Lösungen der Zelle und des Außenmediums.
Physikalische Betrachtungsweise
Auf Teilchenebene ließe sich der Prozess wie folgt beschreiben: Die Salz-Ionen (z. B. Na+ und Cl−, also Natrium- und Chlorid-Ionen) bilden eine Hydrathülle um sich. Das heißt, dass die polaren Wassermoleküle sich entsprechend um die Ionen anordnen und so immobilisiert werden. Dadurch ist die Wahrscheinlichkeit, dass ein Wassermolekül aus der salzigen (hypertonischen) Lösung durch die Membran diffundiert, geringer als andersherum. In der weniger konzentrierten Lösung (bei der Plasmolyse: in der Vakuole) sind die Wassermoleküle also mobiler. Deshalb diffundieren sie leichter durch die Membran auf die andere Seite aus der Vakuole heraus.
Weblinks
- Plasmolyse: Animation und Erklärung
- Video: Plasmolyse und Zytorrhyse. Institut für den Wissenschaftlichen Film (IWF) 1974, zur Verfügung gestellt von der Technischen Informationsbibliothek (TIB), doi:10.3203/IWF/C-1144.