Zytostatikum
Zytostatika (oder Cytostatika, Singular Zytostatikum, von altgriechisch κύτος kýtos „Gefäß“/Zelle und στάσις stásis „Zustand“[1]) sind natürliche oder synthetische Substanzen, die das Zellwachstum beziehungsweise die Zellteilung hemmen. Da sie um so stärker wirken, je schneller das Zellwachstum vor sich geht und somit insbesondere schnell wachsende und sich vermehrende Tumorzellen schädigen, werden sie vor allem zur Behandlung von Krebs (Chemotherapie) eingesetzt, teilweise aber auch bei der Behandlung von Autoimmunerkrankungen.
Neben den klassischen Zytostatika werden heute in der Behandlung von Tumorerkrankungen auch weitere Substanzen wie zum Beispiel Hormone, therapeutische monoklonale Antikörper, Zytokine und sogenannte „small molecules“ wie zum Beispiel Signaltransduktions-Inhibitoren, Proteaseinhibitoren etc. eingesetzt. Diese Substanzen werden meist nicht als Zytostatika bezeichnet, da sie nicht direkt die Zellteilung beziehungsweise das Zellwachstum hemmen. Monoklonale Antikörper und Zytokine sind beispielsweise Krebsimmuntherapeutika.
Die Wirksamkeit von Zytostatika (Chemosensitivität) können durch Chemosensitivitätstests ex vivo vor Beginn einer Chemotherapie bewertet werden.
Geschichte
Während des Ersten Weltkriegs stellten Ärzte fest, dass der Kampfstoff Schwefel-Lost (Senfgas) antiproliferative (wachstumshemmende) Wirkung hat. Nach dem Krieg wurde der weniger giftige Stickstoff-Lost (= Mechlorethamin) entwickelt und um 1942 als erstes Zytostatikum in der Medizin eingesetzt. Bis heute ist Stickstoff-Lost in den USA zugelassen, und seine Derivate sind in zahlreichen modernen Behandlungsschemata enthalten.
Die Bezeichnung der zur Krebstherapie eingesetzten Stoffe (vor allem alkylierende Substanzen, Antimetaboliten und bestimmte Hormone) als „Cytostatika“ erfolgte nach Ludwig Heilmeyer 1947 in Analogie zu den das Wachstum von Bakterien hemmenden „Bakterostatica“.[2]
Die zytostatische Wirkung der Platinkomplexe wurde 1965 zufällig bei einem Versuch mit Zellkulturen und einer Platinelektrode entdeckt.
Andere Substanzen wie Mitotan und die Vinca-Alkaloide wurden in der Pharmaindustrie in ganz anderen Bereichen entwickelt, fielen jedoch beim Tierversuch durch ihr wachstumshemmendes Potenzial auf.
Wirkmechanismus
Zytostatika stören die Stoffwechselvorgänge, die im Zusammenhang mit Zellwachstum oder Zellteilung stehen. Daher schädigen sie vor allem schnell wachsende Zellen wie Epithelzellen (unter anderem Haarwurzelzellen, Schleimhautepithel von Mund und Magen-Darm-Trakt). Da Tumorzellen eine erhöhte Zellteilungsrate und eine eingeschränkte Reparaturkapazität haben, sind sie etwas empfindlicher gegenüber Zytostatika als gesunde Zellen. Dieser Unterschied ermöglicht erst die Therapie mit diesen häufig hochtoxischen Substanzen.
Nebenwirkungen
Da die Giftwirkung auch gesunde Zellen beeinträchtigt, kommt es zu vielerlei negativen Begleiterscheinungen. Insbesondere die Schleimhaut des Magen-Darm-Traktes und das blutbildende Knochenmark sind empfindlich. Fast alle Zytostatika verursachen in unterschiedlichem Ausmaß vorübergehenden Haarausfall, Übelkeit und Erbrechen sowie eine Verminderung der weißen und/oder roten Blutkörperchen im Blut (Myelosuppression). Darüber hinaus haben die einzelnen Wirkstoffgruppen noch weitere, unterschiedliche Nebenwirkungen, z. B. auf das zentrale Nervensystem[3] oder auf den Geschmackssinn. Einige Zytostatika sind selbst karzinogen (krebserregend) und mutagen (keimbahnschädigend).
Obwohl heutzutage komplexe Begleitbehandlungen zu den Zytostatika eingesetzt werden, muss noch immer ein Teil der Therapien dosisreduziert, unterbrochen oder gar abgebrochen werden.
Die WHO-Einteilung der Nebenwirkungen in Schweregrade richtet sich nach den Maßnahmen, die im Einzelfall getroffen wurden:
- Grad 0: keine Nebenwirkungen
- Grad 1: geringe Nebenwirkungen
- Grad 2: Allgemeinbefinden verschlechtert, Chemotherapeutika müssen vermindert werden
- Grad 3: Unterbrechung der Chemotherapie notwendig
- Grad 4: stationäre Krankenhausbehandlung erforderlich
- Grad 5: Tod durch Chemotherapie
Der als Nebenwirkung häufig auftretende Symptomkomplex der subjektiven Ermüdung einiger mit Zytostatika behandelter Patienten, ausgelöst durch oben genannte Veränderungen des Blutbildes, wird als Fatigue bezeichnet.
Umweltrelevanz von Zytostatika
Der Verbrauch an Zytostatika steigt und verbesserte und individuell angepasste Therapien mit optimierter Begleitmedikation und geringeren Nebenwirkungen verbessern die Verträglichkeit und ermöglichen längere Therapiezeiträume. Die Menschen werden immer älter, wodurch die Wahrscheinlichkeit von Krebserkrankungen und -behandlungen steigt. Damit erhöht sich die Umweltrelevanz durch nicht abgebaute zytostatisch aktive Wirkstoffe sowie Stoffwechsel- und Umwandlungsprodukte. Bereits in den achtziger Jahren wurde erstmals Methotrexat im Abwasser einer onkologischen Klinik nachgewiesen.[4] Laborexperimente zeigten, dass unterschiedliche Zytostatika nicht biologisch abbaubar sind. Cyclophosphamid, Ifosfamid, Cisplatin und Mitomycin erwiesen sich als resistent.
Bei Forschungsprojekten und Untersuchungsprogrammen der Bundesländer stellten Wissenschaftler mehr als 150 unterschiedliche Arzneimittelrückstände in Umweltproben fest. Über die aerobe und anaerobe Abbaubarkeit von Zytostatika in Kläranlagen und die Wirkung auf aquatische Organismen – u. a. in Bezug auf Stoffwechselprozesse, Erbgutschädigung und Fortpflanzungsgefährdung – ist insgesamt noch zu wenig bekannt.
Spezielle Zytostatikagruppen
Alkylantien
Alkylantien (Alkylanzien) sind die ältesten Zytostatika. Sie können Alkylgruppen auf die DNA übertragen. Da die Alkylantien mit zwei oder mehr funktionellen Gruppen versehen sind, können sie zwei DNA-Stränge vernetzen und dadurch verhindern, dass diese während der Zellteilung korrekt verdoppelt werden. Die Wirkung beruht also auf einer Hemmung der DNA-Replikation. Alkylantien sind mutagen und karzinogen. Ihre Hauptnebenwirkungen sind Übelkeit, Anämie und Immunschwächung. Sie werden bei Lymphomen, Leukämie, Brust- und Lungenkrebs sowie bei Sarkomen noch oft eingesetzt. Besondere Bedeutung haben sie gegen bösartige Hirntumore.
- Stickstoff-Lost-Derivate
- Cyclophosphamid
- Ifosfamid
- Trofosfamid
- Melphalan
- Chlorambucil
- Estramustin
- Bendamustin
- Alkylsulfonate
- Busulfan
- Treosulfan
- Nitrosoharnstoffe
Platinanaloga
Der Komplex cis-[Pt(NH3)2Cl2] = Cisplatin und seine Verwandten gehören zu den wirksamsten Chemotherapeutika überhaupt. Sie verursachen ebenfalls Quervernetzungen der DNA durch kovalente Bindung des Platinatoms an zwei Nukleinbasen. Platine verursachen Übelkeit, Anämie, Gehör-, Nerven- und Nierenschäden. Ihr Haupteinsatzgebiet sind Hoden-, Gebärmutter- und Eierstockkrebs sowie Tumoren der Halsregion. Ein neueres Platin-Analogon, Oxaliplatin, wird derzeit bei Darmkrebs eingesetzt.
Interkalantien
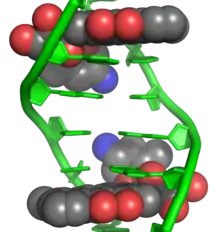
Interkalantien binden nichtkovalent an die DNA und verhindern die Anbindung der Polymerasen, welche zur Replikation und Transkription der Erbsubstanz dienen. Das heißt, Zellteilung und Zellfunktion werden gestört. Die Substanzen werden wegen der geringen Rate an resistenten Tumoren sehr oft und bei fast allen soliden Tumoren eingesetzt; sie eignen sich auch als Mono-Therapie bei Patienten, die starkwirksame Kombinationen nicht vertragen. Übelkeit und Anämie sowie verschiedene Organschäden sind ihre häufigsten Nebenwirkungen.
- Anthracycline
- Doxorubicin (Adriamycin)
- Daunorubicin
- Epirubicin
- Idarubicin
Antibiotika
Die Vertreter dieser Substanzgruppe mit antibakterieller und gleichzeitig zytostatischer Wirkung wurden aus Pilzen isoliert. Die Wirkmechanismen sind unterschiedlich, meist DNA-Vernetzung durch Interkalation oder Alkylierung. Es sind vorwiegend Peptide, daher können bei der Anwendung allergische Reaktionen auftreten. Weitere Nebenwirkungen sind Lungen- oder Leberschäden. In Protokollen gegen Hodenkrebs, Blasenkrebs und maligne Lymphome sind oft Antibiotika vertreten.
- Bleomycin
- Actinomycin D (Dactinomycin)
- Mitomycin C
Mitosehemmer
Diese Stoffe binden an das Tubulin, ein Eiweißmakromolekül, welches zur Zellteilung (siehe Mitose) notwendig ist. Der Einsatz ist bei Lymphomen und Leukämien, seltener bei soliden Tumoren üblich. Ihre unangenehmste Nebenwirkung ist eine Schädigung des Nervensystems.
- Alkaloide der Rosafarbenen Catharanthe (Catharanthus roseus, frühere Bezeichnung Vinca rosea):
- Vinorelbin
- Vincristin (Oncovin)
- Vinblastin
- Vindesin
- Vinflunin
Taxane
Eine relativ neue Substanzgruppe, obwohl sie bereits in den 1960er Jahren am National Cancer Institute in den USA durch ein systematisches Screening von 35.000 Pflanzengattungen entdeckt wurde, und zwar in der Pazifischen Eibe (Taxus brevifolia). Erst seit sie synthetisch hergestellt werden können (1994), finden Taxane zunehmende Verbreitung bei Brust-, Prostata- und Lungenkrebs und beim Hautkrebs, oft als Monotherapie. Die Wirkung beruht auf der Bildung von anormalen Molekülen im Zellskelett, was die geordnete Zellteilung verhindert.
Topoisomerasehemmer
Die Topoisomerasen I und II sind Enzyme, welche gezielte, reversible Unterbrechungen im DNA-Strang herstellen. Die Hemmung bewirkt irreguläre, nichtbehebbare DNA-Brüche und spontane Vernetzungen. Diese neue Substanzklasse ist vielversprechend bei soliden Tumoren, Lymphomen, Hirntumoren und kindlichen Tumoren. Ihre Neigung zur Knochenmarksdepression (Anämie) ist allerdings gefürchtet.
- Topoisomerase-I-Inhibitoren
Antimetaboliten
Antimetaboliten werden als falsche Bausteine in die DNA oder RNA eingebaut oder verhindern den Einbau der korrekten Bausteine, und stören so die Zellteilung und den Stoffwechsel. Ihre Nebenwirkungen sind Übelkeit und Anämie sowie Nierenschäden.
Darm- und Brustkrebs und viele andere solide Tumoren sowie Leukämie sind die Einsatzgebiete für Antimetaboliten. Man vermutet, dass die Empfindlichkeit der Zellen gegenüber Strahlung gesteigert wird. 5-Fluoruracil ist aus diesem Grund die wichtigste Substanz in der Radiochemotherapie.
- Folsäureantagonisten
- Pyrimidinanaloga
- Purinanaloga
Andere Zytostatika
- L-Asparaginase, ein im Serum von Meerschweinchen entdecktes Enzym, welches die Aminosäure L-Asparagin abbaut. Manche Leukämiezellen können diese Aminosäure nicht herstellen. Die Toxizität gegenüber normalen Zellen ist sehr gering.
- Tyrosinkinase-Inhibitoren wie Imatinib, Dasatinib, Nilotinib. Diese hemmen die Aktivität eines Proteins, das bei vielen Patienten mit Leukämie, insbesondere der überwiegenden Zahl der Patienten mit Chronischer myeloischer Leukämie vorkommt, und die abnorme Teilungsrate dieser Zellen verantwortet. Auch Tyrosinkinase-Inhibitoren wirken sehr spezifisch gegen die malignen Zellen.
- Hydroxycarbamid (Hydroxyharnstoff) hemmt das Enzym Ribonukleotid-Reduktase und dadurch die DNA-Synthese. Typische Anwendungsgebiete sind insbesondere myeloische Leukämien (vor allem bei Anzeichen einer Leukostase) und andere myeloproliferative Erkrankungen wie essentielle Thrombozythämie und Polycythaemia vera (rubra). Die Hauptnebenwirkung ist eine Knochenmarksdepression.
- Mitotan, ein Verwandter des Insektizids DDT mit spezifischer Wirksamkeit gegen den Stoffwechsel von Zellen – auch Tumorzellen – in der Nebenniere
- Amatoxine hemmen die Transkription durch Blockade der RNA-Polymerase. Damit kann keine genetische Information mehr aus dem Zellkern in das Zellplasma gelangen, und die Proteinbiosynthese ist blockiert. Durch die mannigfaltigen Funktionen der Proteine sind viele Stellen des Organismus betroffen.
- Altretamin hemmt die DNA- und RNA-Synthese im Zellkern.
- Aromatasehemmer wie Anastrozol, Exemestan oder Letrozol hemmen die Östrogenbildung und sind somit Therapieoptionen bei Tumoren wie dem Mammakarzinom.
Einzelnachweise
- κύτος und στάσις in Wilhelm Gemoll: Griechisch-deutsches Schul- und Handwörterbuch. 10., völlig neu bearbeitete Auflage. Oldenbourg, München, Düsseldorf, Stuttgart 2006, ISBN 978-3-637-00234-0.
- Paul Obrecht: Klinische Cancerologie. In: Ludwig Heilmeyer (Hrsg.): Lehrbuch der Inneren Medizin. Springer-Verlag, Berlin/Göttingen/Heidelberg 1955; 2. Auflage ebenda 1961, S. 352–375, hier: S. 371.
- Noll-Hussong M.: Wie Zytostatika das Gehirn schädigen. InfoOnkologie. 2009;12(3):55-7.
- Abfallmanager Medizin: Umweltrelevanz von CMR-Arzneimitteln – Zytostatika im Abwasser, 28. April 2017.
Literatur
Allgemeine Literatur
- Klaus Aktories, Ulrich Förstermann, Franz Hofmann, Klaus Starke: Allgemeine und spezielle Pharmakologie und Toxikologie, 10. Auflage, Elsevier, Urban & Fischer, München; Jena 2009, ISBN 978-3-437-42522-6.
- W. J. Zeller, H. zur Hausen (Hrsg.): Onkologie. Ecomed, Landsberg 1995, Loseblattausgabe
Alkylantien
- Ulrich Meyer: Die Geschichte der Alkylanzien. Pharmazie in unserer Zeit 35(2), S. 104–109 (2006), ISSN 0048-3664
Metallkomplexe
Taxane
Ethik
- Marlies Frast: Zu Staub oder Asche. (PDF) Ist eine gesetzliche Kremationspflicht von Verstorbenen nach vorausgegangener Zytostatika-Therapie aus ethischer Sicht vertretbar? Universität Zürich, 2005, archiviert vom Original am 1. Februar 2014; abgerufen am 27. Juli 2014.