Cladribin
Cladribin ist ein Arzneistoff mit antineoplastischen und immunmodulierenden Wirkungen, der unter anderem für die perorale Behandlung der Multiplen Sklerose (MS) zugelassen ist. Cladribin wurde ursprünglich für die Behandlung der Haarzellleukämie, einer Form des Blutkrebses, entwickelt und zugelassen. In dieser Indikation wird es parenteral gegeben.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
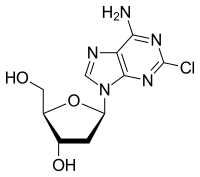 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Cladribin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C10H12ClN5O3 | |||||||||||||||||||||
| Kurzbeschreibung |
weißes bis fast weißes, kristallines, polymorphes Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 285,69 g·mol−1 | |||||||||||||||||||||
| Löslichkeit |
löslich in Dimethylsulfoxid; schwer löslich in Wasser, Methanol; praktisch unlöslich in Acetonitril[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Klinische Angaben
Multiple Sklerose
Cladribin-Tabletten (Mavenclad / Merck KGaA) werden zur Behandlung von erwachsenen Patienten mit hochaktiver schubförmiger Multipler Sklerose (MS), definiert durch klinische oder bildgebende Befunde, angewendet.[4]
Hämatologische Erkrankungen
Cladribin-Infusions- und Injektionslösung (Leustatin / Janssen-Cilag; Litak / Lipomed) für die intravenöse oder subkutane Gabe sind in der EU zur Behandlung der Haarzellleukämie zugelassen.[5]
Art und Dauer der Anwendung
Cladribin stellt die erste in Europa zugelassene orale Impulstherapie für schubförmige MS dar. Während jeder Kurzzeit-Einnahmephase („Impuls“) werden einmal täglich – abhängig vom Körpergewicht – eine oder zwei Tabletten während der ersten vier oder fünf Tage eines Monats eingenommen und zu Beginn des zweiten Monats wiederholt. Die Behandlungsphase im 2. Jahr ist wichtig für den Behandlungserfolg. Sie erfolgt analog zum ersten Jahr. Insgesamt ergeben sich daraus maximal 20 Behandlungstage in den ersten zwei Jahren.[4][6]
Nach dem kompletten Abschluss der zwei Behandlungsjahre ist keine weitere Behandlung mit Cladribin in den Jahren 3 + 4 erforderlich, da in einer klinischen Studie 75,6 % der Patienten im Jahr 3 + 4 nachhaltig schubfrei waren. Ab dem Jahr 5 kann eine weitere Behandlung mit Cladribin-Tabletten angeschlossen werden.[4]
Gegenanzeigen
Infektion mit dem Humanen Immundefizienz-Virus (HIV). Aktive chronische Infektion (Tuberkulose oder Hepatitis).[4]
Wechselwirkungen mit anderen Medikamenten
Aufgrund des Risikos additiver Wirkungen auf das Immunsystem ist der Beginn einer Behandlung mit Cladribin bei immungeschwächten Patienten kontraindiziert, einschließlich Patienten, die derzeit eine immunsuppressive oder myelosuppressive Therapie mit Wirkstoffen wie Methotrexat, Cyclophosphamid, Ciclosporin oder Azathioprin erhalten, sowie bei Patienten unter chronischer Behandlung mit Corticosteroiden.[4]
Anwendung während Schwangerschaft und Stillzeit
Männer und Frauen müssen während der Behandlung mit Cladribin und bis mindestens sechs Monate nach der letzten Dosis eine zuverlässige Verhütungsmethode anwenden. Dies ist wichtig, da Cladribin beim Fötus möglicherweise schwerwiegende Schäden verursachen könnte. Ob Cladribin in die Muttermilch übergeht, ist nicht bekannt; daher darf während der Dauer der Einnahme bis eine Woche lang danach nicht gestillt werden.[4]
Unerwünschte Wirkungen
Die häufigsten Nebenwirkungen bei Patienten mit Multipler Sklerose, die mit Cladribin-Tabletten behandelt wurden, waren eine Verminderung der Anzahl von Lymphozyten (Lymphopenie) und bestimmten weißen Blutkörperchen (neutrophile Granulozyten; Neutropenie) sowie oraler Herpes / Gürtelrose (Herpes Zoster). Hautausschlag und Haarausfall (Alopezie) traten ebenfalls gehäuft auf. Bei den meisten Patienten normalisierten sich die Lymphozytenzahlen mit der Zeit, bei weniger als 1 % der Patienten wurde eine schwere Lymphopenie (Grad 4) beobachtet.[4]
Auf dem weltweit größten jährlichen internationalen Kongress, der der Grundlagen- und klinischen Forschung bei Multipler Sklerose gewidmet ist, ECTRIMS, wurden 2019 in einem Postervortrag die Ergebnisse von nach der Zulassung gewonnenen Daten zur Sicherheit präsentiert (integrierte Analyse aus dem klinischen Studienprogramm mit oralem Cladribin;[7] Marktüberwachung nach der Zulassung (post marketing reporting)). Demzufolge sei das Nebenwirkungsspektrum mit jenem zum Zeitpunkt der Zulassung konsistent, es wurden keine neuen Signale (d. h. möglicher Kausalzusammenhang zwischen einer Medikamentenanwendung und einem Ereignis) detektiert.[8]
Nach parenteraler Gabe zur Behandlung der Haarzellleukämie kann Cladribin wegen seiner antineoplastischen und immunsuppressiven Wirkungen toxische Effekte hervorrufen wie Knochenmarksuppression und Lymphozytopenie, ferner Immunsuppression und opportunistische Infektionen. Es wurden Fälle einer progressiven multifokalen Leukenzephalopathie (PML) berichtet.[4][9] Ebenso treten die beim Einsatz von Zytostatika üblichen Nebenwirkungen, wie Fieber, Übelkeit, Appetitverlust und Schwindel, auf.[9]
Studien zur Behandlung der MS
- Cladribin wurde in zahlreichen klinischen Studien zu Multipler Sklerose untersucht. Darin zeigte die Substanz signifikante Effekte auf die relevanten Krankheitsparameter MRT, Schubaktivität und Krankheitsprogression.[6][10]
- Bei Patienten mit schubförmig remittierender MS zeigte Cladribin in der CLARITY-Studie im Vergleich zu Placebo signifikante Effekte auf klinische und MRT-Parameter: eine Reduktion der jährlichen Schubrate (schubfrei bei 77,8 % der Patienten im Jahr 1+2 und bei 75,6 % der Patienten im Jahr 3+4; Verringerung des relativen Risikos um 58 % nach zwei Jahren), eine Verlängerung der schubfreien Zeit, eine Reduktion des Risikos einer nach drei Monaten bestätigten Behinderungsprogression (Senkung des relativen Risikos um 33 %) und eine Reduktion der verschiedenen im MRT gemessenen Läsionen. Nach 96 Wochen zeigten 47 % der Patienten keine messbare Krankheitsaktivität (NEDA).[6][11][12]
- Post-hoc-Analysen der zweijährigen Phase-III-Studie CLARITY zeigten, dass Cladribin-Tabletten bei Patienten mit hoher Krankheitsaktivität* die jährliche Schubrate um 67 % und das Risiko einer über 6 Monate bestätigten Behinderungsprogression- um 82 % im Vergleich zu Placebo senkten.[6][11]
- In der ORACLE-MS-Studie wurden Wirksamkeit und Verträglichkeit von Cladribin im Vergleich zu Placebo bei Patienten mit einem ersten demyelinisierenden Ereignis (FCDE) geprüft. Cladribin senkte das relative Risiko für die Entwicklung einer klinisch manifesten MS signifikant um 67 %.[13]
- In der randomisierten Phase-IIb-Studie ONWARD wurden über zwei Jahre Wirksamkeit und Verträglichkeit von Cladribin als Zusatztherapie zu Interferon-beta bei Patienten mit mindestens einem Schub in den letzten 48 Wochen im Vergleich zu Placebo plus Interferon beta untersucht. Patienten, die zusätzlich mit Cladribin-Tabletten behandelt wurden, hatten ein um 63 % verringertes Risiko für einen erneuten Schub.[14]
Wirkungsmechanismus
Cladribin ist ein chloriertes Analogon des DNA-Bausteins Desoxyadenosin. Es handelt sich um ein sogenanntes Prodrug, das mit Hilfe spezifischer Transporterproteine (Nukleosidtransporter) von Zellen aufgenommen wird. Bevorzugt in Lymphozyten wird das inaktive Prodrug phosphoryliert und in seine aktive Form, das 2-Chlorodesoxy-Adenosin-5‘-Triphosphat (2-CdATP), umgewandelt. 2-CdATP wirkt, indem es als falscher Baustein in die DNA bzw. RNA eingebaut wird. Die Doppelhelix-Struktur wird in der Folge gestört und DNA-Reparatur und DNA-Synthese werden gehemmt. Dies führt zur gezielten Reduktion der Lymphozytenzahl. Cladribin wirkt sowohl in sich teilenden (proliferierenden) als auch in ruhenden Zellen.[15]
Bei der Behandlung der Multiplen Sklerose (MS) wirkt Cladribin als so genanntes krankheits-modifizierendes Arzneimittel (disease-modifying drug, DMD). Die Therapie mit Cladribin reduziert selektiv und vorübergehend die Zahl der T- und B-Lymphozyten, die maßgeblich am Krankheitsgeschehen der MS beteiligt sind. Anschließend erfolgt eine Repopulation der Lymphozyten, wobei die Wirkung von Cladribin auch nach Erholung der Lymphozytenzahlen nachhaltig bestehen bleibt.[16][17] Indem Cladribin vorrangig die Zahl der T- und B-Lymphozyten reduziert und nur geringe bzw. transiente Effekte auf Monozyten, Neutrophile und natürliche Killerzellen hat, bleibt die angeborene Immunabwehr erhalten.[18]
Darüber hinaus gibt es Hinweise aus Studien, dass Cladribin das Zytokinprofil von proentzündlich in Richtung antientzündlich verschiebt, indem es die Konzentration mancher antientzündlich wirkender Zytokine (Interleukin-4, Interleukin-5 und Interleukin-10) erhöht und die Spiegel von proinflammatorisch wirkendem TNF-α und Interleukin-6 normalisiert sowie die Konzentration von TGF-ß1 und basischem Fibroblasten-Wachstumsfaktor senkt.[19][20][21]
Cladribin kann die Blut-Hirn-Schranke passieren. In der Zerebrospinalflüssigkeit von Patienten, die nicht an einer Erkrankung des zentralen Nervensystems leiden, werden Konzentrationen von etwa 25 % des Plasmaspiegels erreicht.[22]
Entwicklung und Vermarktung
Cladribin wurde von einer Arbeitsgruppe um Ernest Beutler am Scripps Research Institute in den 1970er Jahren entwickelt und in den frühen 1980er Jahren erstmals bei neun Patienten mit therapieresistentem Blutkrebs untersucht.[23] Die gleiche Arbeitsgruppe berichtete 1988 über die erstmalige Behandlung von Patienten mit Haarzell-Leukämie.[24] Entsprechende Cladribin-Präparate für die intravenöse Behandlung (Leustatin) wurden 1993 in den USA und in Schweden,[25] später auch in weiteren Ländern, darunter Deutschland (1996) zugelassen.[26] In einigen Ländern umfassten die Anwendungsgebiete auch bestimmte andere maligne lymphatische Erkrankungen.
2004 erfolgte EU-weit die Zulassung einer subkutan anzuwendenden Injektionslösung (Litak) zur Behandlung der der Haarzell-Leukämie. Die Entwicklung hatte in den 1990er Jahren in der Schweiz begonnen mit dem Ziel, die Therapie für den Patienten komfortabler zu gestalten. Die subkutane Verabreichung, die an 5 aufeinanderfolgenden Tagen erforderlich ist, kann der Patient selbst vornehmen. Die Exposition ist ähnlich wie bei der intravenösen Gabe. Die subkutane Injektion von Litak wurde von der Europäischen Kommission als Arzneimittel für seltene Leiden zugelassen.[25]
Beutler und Kollegen untersuchten Cladribin in den 1990er Jahren auch bei Patienten mit Multipler Sklerose.[27] Dieser Behandlungsansatz wurde später von Merck Serono aufgegriffen.[6] Die europäische Zulassung für Cladribin-Tabletten zur Behandlung von erwachsenen Patienten mit hochaktiver schubförmiger MS, definiert durch klinische und bildgebende Befunde, erfolgte im August 2017.[28] Ein erster Zulassungsantrag von Merck im Jahr 2011 war gescheitert, da der Ausschuss für Humanarzneimittel (CHMP) die Ansicht vertrat, „dass auf Grundlage der damals vorliegenden Daten die Vorteile von Cladribin-Tabletten die Risiken bei der Behandlung der Multiplen Sklerose nicht aufwiegen.“[29] In den Vereinigten Staaten wurde Cladribin für die Behandlung der MS am 29. März 2019 zugelassen.[30]
Cladribin wird auch zur Behandlung des Mantelzelllymphom[31] und weiterer B-Zell-Lymphome[32] untersucht. Für die Indikation Mastozytose hat es in der EU den Status eines Arzneimittels für seltene Leiden.[33]
Frühe Nutzenbewertung
In Deutschland müssen seit 2011 neu zugelassene Medikamente mit neuen Wirkstoffen gemäß § 35a SGB V einer „frühen Nutzenbewertung“ durch den Gemeinsamen Bundesausschuss (G-BA) unterzogen werden, wenn der pharmazeutische Hersteller einen höheren Verkaufspreis als nur den Festbetrag erzielen möchte. Nur wenn ein Zusatznutzen besteht, kann der Arzneimittelhersteller mit dem Spitzenverband der gesetzlichen Krankenkassen einen Preis aushandeln. Die Dossierbewertungen, auf deren Basis der G-BA seine Beschlüsse fasst, erstellt das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG).
In der frühen Nutzenbewertung wurde 2018 bezüglich der zweckmäßigen Vergleichstherapie unterschieden zwischen Erwachsenen mit hochaktiver schubförmiger Multipler Sklerose, die bislang noch keine krankheitsmodifizierende Therapie erhalten hatten, und solchen mit hochaktiver Erkrankung trotz Behandlung mit einer krankheitsmodifizierenden Therapie.[34] Gemäß G-BA-Beschluss ist ein Zusatznutzen für keine dieser beiden Gruppen belegt.[35]
Chemie
Cladribin besitzt drei stereogene Zentren. Zwei Stereoisomere sind möglich, die 9-α and 9-β-Form, wobei Cladribin das 9-β-Stereoisomer darstellt.[36] 2-Chlor-9-(2-desoxy-α-D-erythro-pentofuranosyl)-9H-purin-6-amin kommt in kleinen Mengen (maximal 0,2 Prozent) als Verunreinigung vor.[1]
Handelsnamen
Weblinks
- Eintrag zu Cladribine in der Human Metabolome Database (HMDB), abgerufen am 17. Oktober 2013.
- Einträge im NIH-Studienregister
Einzelnachweise
- Europäische Arzneibuch-Kommission (Hrsg.): Europäische Pharmakopöe 8. Ausgabe. 8.0 (Grundwerk), 2014.
- Datenblatt 2-Chloro-2′-deoxyadenosine bei Sigma-Aldrich, abgerufen am 23. März 2011 (PDF).
- Eintrag zu Cladribine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Mavenclad: Zusammenfassung der Merkmale des Arzneimittels (Fachinformation). (PDF) Abgerufen am 19. April 2019.
- Haarzell-Leukämie (HZL): Onkopedia-Leitlinie. Deutsche Gesellschaft für Hämatologie und medizinische Onkologie, April 2016, abgerufen am 16. Mai 2018.
- G Giovannoni, G Comi, S Cook et al. A placebo-controlled trial of oral cladribine for relapsing multiple sclerosis. In: N Engl J Med., 2010, 362, S. 416–426, doi:10.1056/NEJMoa0902533, PMID 20089960.
- zum Studienprogramm siehe: Assessment Report Mavenclad, CHMP 22. Juni 2017, Table 2, ema.europa.eu (PDF; 2,0 MB).
- Updated safety of cladribine tablets in the treatment of patients with multiple sclerosis: Integrated safety analysis and post-approval data, ECTRIMS Kongress, Stockholm September 2019, abgerufen am 10. April 2020
- Zusammenfassung der Merkmale des Arzneimittels Litak. (PDF; 354 kB) EMA (Fachinformation); abgerufen am 20. März 2019.
- Cook S, Vermersch P, Comi G et al. Safety and tolerability of cladribine tablets in multiple sclerosis: the CLARITY (CLAdRIbine Tablets treating multiple sclerosis orallY) study. Mult Scler. 2011 May; 17(5): 578–593, PMID 21228029; doi:10.1177/1352458510391344.
- Gavin Giovannoni, Stuart Cook, Kottil Rammohan, Peter Rieckmann, Per Soelberg Sørensen: Sustained disease-activity-free status in patients with relapsing-remitting multiple sclerosis treated with cladribine tablets in the CLARITY study: a post-hoc and subgroup analysis. In: The Lancet Neurology. Band 10, Nr. 4, S. 329–337, doi:10.1016/s1474-4422(11)70023-0.
- Giancarlo Comi, Stuart D. Cook, Gavin Giovannoni, Kottil Rammohan, Peter Rieckmann: MRI outcomes with cladribine tablets for multiple sclerosis in the CLARITY study. In: Journal of Neurology. Band 260, Nr. 4, 1. April 2013, S. 1136–1146, doi:10.1007/s00415-012-6775-0.
- Thomas P Leist, Giancarlo Comi, Bruce A C Cree, Patricia K Coyle, Mark S Freedman: Effect of oral cladribine on time to conversion to clinically definite multiple sclerosis in patients with a first demyelinating event (ORACLE MS): a phase 3 randomised trial. In: The Lancet Neurology. Band 13, Nr. 3, S. 257–267, doi:10.1016/s1474-4422(14)70005-5.
- X Montalban, B Cohen, T Leist et al.: Efficacy of Cladribine Tablets as Add-On to IFN-beta Therapy in Patients with Active Relapsing MS: Final Results from the Phase II ONWARD Study (P3.029). In: Neurology. Band 86, 16 Supplement, 2016, S. P3.029 (neurology.org).
- Thomas P. Leist, Robert Weissert: Cladribine. In: Clinical Neuropharmacology. 34, 2011, S. 28, doi:10.1097/WNF.0b013e318204cd90.
- G. Giovannoni et al.: AAN 2016. P3.028.
- G. Giovannoni et al.: EAN 2017. P0542.
- Thomas P. Leist, Robert Weissert: Cladribine. In: Clinical Neuropharmacology. Band 34, Nr. 1, S. 28–35, doi:10.1097/wnf.0b013e318204cd90.
- Melanie Korsen, Sara Bragado Alonso, Lizzy Peix, Barbara M. Bröker, Alexander Dressel: Cladribine Exposure Results in a Sustained Modulation of the Cytokine Response in Human Peripheral Blood Mononuclear Cells. In: PLOS ONE. Band 10, Nr. 6, 18. Juni 2015, S. e0129182, doi:10.1371/journal.pone.0129182.
- Achille Aouba, Benjamin Terrier, Viorel Vasiliu, Sophie Candon, Nicole Brousse: Dramatic clinical efficacy of cladribine in Rosai-Dorfman disease and evolution of the cytokine profile: towards a new therapeutic approach. In: Haematologica. Band 91, 12 Suppl, Dezember 2006, S. ECR52, PMID 17194658.
- J. Gora-Tybor, J. Z. Blonski, T. Robak: Cladribine decreases the level of angiogenic factors in patients with chronic lymphocytic leukemia. In: Neoplasma. Band 49, Nr. 3, 2002, S. 145–148, PMID 12097998.
- Jan Liliemark: The Clinical Pharmacokinetics of Cladribine. In: Clinical Pharmacokinetics. Band 32, Nr. 2, 1. Februar 1997, S. 120–131, doi:10.2165/00003088-199732020-00003.
- D. A. Carson, D. B. Wasson, E. Beutler: Antileukemic and immunosuppressive activity of 2-chloro-2'-deoxyadenosine. In: Proceedings of the National Academy of Sciences. Band 81, Nr. 7, 1984, S. 2232–2236, doi:10.1073/pnas.81.7.2232, PMID 6585795.
- L. D. Piro, C. J. Carrera, E. Beutler, D. A. Carson: 2-Chlorodeoxyadenosine: an effective new agent for the treatment of chronic lymphocytic leukemia. In: Blood. Band 72, Nr. 3, 1988, S. 1069–1073, PMID 2901280.
- European Public Assessment Report Litak - Scientific Discussion. (PDF; 417 kB) Europäische Arzneimittelagentur, 21. Oktober 2005; abgerufen am 2. Oktober 2010.
- Humanarzneimittel mit neuen Wirkstoffen (1996). In: Bundesgesundheitsblatt. Band 40, Nr. 4, 1997, S. 151–153, doi:10.1007/BF03044171.
- J. C. Sipe, J. S. Romine, J. A. Koziol, et al.: Development of cladribine treatment in multiple sclerosis. In: Multiple Sclerosis Journal. Band 1, Nr. 6, 1996, S. 343–347, doi:10.1177/135245859600100612, PMID 9345414.
- Europäische Kommission erteilt Zulassung für Mavenclad (Cladribin-Tabletten). Pressemitteilung. Merck, abgerufen am 18. März 2019.
- Julia Borsch: Cladribin erhält im zweiten Anlauf Zulassung bei MS. In: deutsche-apotheker-zeitung.de. 28. August 2017, abgerufen am 30. März 2019.
- FDA approves new oral treatment for multiple sclerosis. FDA, abgerufen am 10. April 2020.
- DJ Inwards, PA Fishkin, DW Hillman et al. Long-term results of the treatment of patients with mantle cell lymphoma with cladribine (2-CDA) alone (95-80-53) or 2-CDA and rituximab (N0189) in the North Central Cancer Treatment Group. Cancer. 2008; 113:108–116. PMID 18470909; doi:10.1002/cncr.23537.
- DS Sigal, HJ Miller, ED Schram, A. Saven: Beyond hairy cell: the activity of cladribine in other hematologic malignancies. In: Blood, 2010; Jul 15, PMID 20634380.
- Eintrag EU/3/13/1182 im Community-Register für Orphan-Arzneimittel vom August 2013.
- A17-62 Cladribin (multiple Sklerose) – Nutzenbewertung gemäß § 35a SGBV. iqwig.de; abgerufen am 27. März 2020.
- Nutzenbewertungsverfahren zum Wirkstoff Cladribin (Hochaktive schubförmige Multiple Sklerose). g-ba.de; abgerufen am 27. März 2020.
- Assessment Report Mavenclad. (PDF; 2,0 MB) Ausschuss für Humanarzneimittel (CHMO), 22. Juni 2017
- Fachinformation Leustatin 10 mg/10 ml Konzentrat zur Herstellung einer Infusionslösung (PDF; 172 kB) Janssen-Cilag, Stand: Dezember 2017.