Actinomycin D
Actinomycin D oder Dactinomycin (Handelsnamen Lyovac-Cosmegen, Cosmegen (EU); Hersteller: MSD) ist ein Zytostatikum zur Behandlung von Krebserkrankungen. Es gehört zur Gruppe der zytotoxischen Antibiotika (genannt auch Tumorantibiotika). Seine antineoplastische Wirkung wird durch die Bindung an DNA vermittelt, wo Actinomycin D die RNA-Synthese hemmt.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
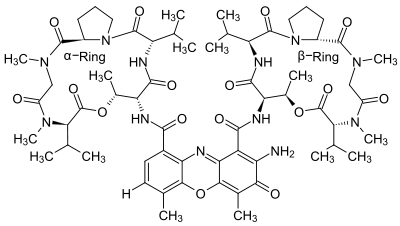 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Actinomycin D | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C62H86N12O16 | |||||||||||||||||||||
| Kurzbeschreibung |
roter, geruchloser Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
L01DA01 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 1255,42 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
schwer in Wasser (40 g·l−1 bei 10 °C)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
| Pharmakologische Informationen | |||
|---|---|---|---|
| Verabreichungsart | intravenös (i.v.) | ||
| Bioverfügbarkeit | keine orale Gabe möglich (giftig). | ||
| Metabolismus | unwesentlich. | ||
| Wechselwirkungen | Strahlentherapie | Wirkung Actinomycin D | |
| Halothan, Enfluran, Isofluran | Wirkung Actinomycin D | ||
| Andere Zytostatika | Wirkung Actinomycin D | ||
| Ausscheidung | Urin & Stuhl: 30 % der Substanz binnen 1 Woche nach Gabe. | ||
| Inkompatibilität | Benzylalkohol | Ausfällung. | |
| Filgrastim (G-CSF) | Ausfällung. | ||
| Riboflavin | Ausfällung. | ||
| Klinische Informationen | |||
| Indikation(en) | Kinder | Nephroblastom (Wilms-Tumor), Weichteilsarkome Ewing-Sarkom Rhabdomyosarkom | |
| Erwachsene | Ewing-Sarkom Weichteilsarkome Hodenkarzinom Chorionkarzinom Kaposi-Sarkom | ||
| Nebenwirkungen | Venookklusive Erkrankung Leber (VOD). Übelkeit. Erbrechen. Anorexie. Leukopenie (Neutropenie). Thrombopenie. Anämie. Mukositis (Schmerzen, Durchfall). Alopezie Hautreizung (besonders nach Bestrahlung) | ||
| Kontraindikation(en) | Schwangerschaft. Stillzeit. Impfungen (Lebendimpfstoffe). Die gleichzeitige Anwendung von Actinomycin D und Strahlentherapie ist kontraindiziert. | ||
| Zulassungsstatus | |||
| Deutschland | USA | EU | |
| Zulassungsdatum | 1. Dezember 1966[2] | 12. Oktober 1964 | --.--.---- |
| Status | Apothekenpflichtig. Rezeptpflichtig. | ||
Herkunft und Herstellung
Actinomycin D, aus der Gruppe der Actinomycine, ist ein Peptid-Antibiotikum aus Streptomyces parvulus. Es besteht aus zwei cyclischen Peptiden, die über eine oxidierte Phenoxazin-Einheit miteinander verbunden sind.
Wirkungsmechanismus
Actinomycin D wirkt als Interkalator der DNA. In ein einfaches Vergleichsbild übertragen bedeutet dies, dass Actinomycin D den Reißverschluss DNA blockiert, so dass dieser nicht geöffnet werden kann. Ohne Öffnung ist ein normaler Gebrauch der DNA nicht möglich. Alle Zellen, welche DNA enthalten, werden durch die Wirkungen des Actinomycin D betroffen. Lediglich die Gehirnzellen und Zellen des Rückenmarks sind durch die Blut-Hirn-Schranke vor den Wirkungen des Actinomycin D geschützt. Dies bedeutet auch, dass Krebserkrankungen im Gehirn und im Rückenmark durch Actinomycin D nicht behandelt werden können.
In niedrigen Dosierungen hemmt Actinomycin D die DNA-abhängige RNA-Synthese durch Interkalation (Einhängen und Vernetzung) der Guanin-Nukleotide der DNA. Für die Anlagerung von Actinomycin D an die DNA spielt das asymmetrische Phenoxazon eine wichtige Rolle, weil dieser Bestandteil sich spezifisch an die mit Guanin- und Cytosin-Nukleotid reichen (GC-rich) Stellen der DNA bindet.[3] Durch die Bindung an die DNA wird die DNA-abhängige RNA-Polymerase blockiert: Die Bildung von mRNA unterbleibt und die Proteinproduktion sinkt ab. Bei höheren Dosierung wird durch Actinomycin D auch die DNA-Replikation gehemmt. Hierbei wird die DNA-Polymerase in ihrer Aktivität blockiert. Verbindungen innerhalb eines einzelnen DNA-Strangs, zwischen zwei DNA-Strängen sowie zwischen DNA und Proteinen kommen vor.
Actinomycin D ist in seiner Wirkung nicht an eine bestimmte Phase des Zellzyklus gebunden. Allerdings gibt es experimentelle Hinweise an menschlichen Leukämiezellinien, dass Actinomycin D besonders in der S- und G2-Phase des Zellzyklus aktiv ist.[4] Hieraus wurde gefolgert, dass die Topoisomerase II eine Rolle bei der Actinomycin D Wirkung besitzen dürfte.
Pharmakokinetik
Actinomycin D wird nach intravenöser Gabe von Knochenmarkzellen und Tumorzellen aufgenommen. Auch in anderen inneren Organen und Geweben lässt sich Actinomycin D nachweisen. Die mediane Spitzenkonzentration von 25,1 ng/ml bei einer Dosierung von 0,7–1,5 mg/m2 Körperoberfläche (KOF) tritt 15 Minuten nach Gabe auf. In roten Blutkörperchen findet sich wenig Actinomycin D. Actinomycin D überwindet nicht die Blut-Hirn-Schranke. Eine Wirksamkeit im Gehirn bzw. Zentralnervensystem ist somit sehr unwahrscheinlich. Die mediane Expositionsdauer beträgt 2,67 mg/l×min (Spanne 1,12–4,90 mg/l×min). Die maximale Konzentration (Cmax) und die Area Under Curve (AUC) hängen von der Dosis ab. Bei Patienten mit einem Körpergewicht von weniger als 40 kg ist die AUC höher, was gegebenenfalls mit einem höheren Toxizitätsrisiko korreliert.[5] Die Plasmaproteinbindung von Actinomycin D beträgt ca. 5 %.
30 % einer Dosis werden innerhalb einer Woche über den Urin und Stuhl ausgeschieden, 15 % allein im Urin. Die terminale Plasmahalbwertzeit ist mit 36 Stunden ermittelt worden. Bei Funktionseinschränkungen der Leber kann die Plasmahalbwertzeit deutlich länger als 36 Stunden sein. Actinomycin D kann oral aufgrund seiner stark reizenden Eigenschaften nicht aufgenommen werden. Es steht daher auch nicht als Saft oder Tabletten zur Verfügung.
Wechselwirkungen (Interaktionen)
- Bestrahlung
- Die gleichzeitige Anwendung von Bestrahlung und Actinomycin D führt zu einer Wirkungsverstärkung von Actinomycin D in den bestrahlten Körpergeweben. Die bestrahlte Haut kann nach Gabe von Actinomycin D erröten und schmerzhaft verändert sein. Dies geschieht auch dann, wenn zwischen der Bestrahlung und Actinomycin D Gabe kein ausreichender zeitlicher Abstand eingehalten worden ist. Bei Bestrahlung der Leber (beispielsweise bei einem rechtsseitigen Nephroblastom) treten Schädigungen der Leber häufiger und schwerwiegender auf als bei alleiniger Actinomycin D Behandlung. Gleiches gilt für die Schleimhäute von Mund, Speiseröhre und Darm. Sind Teile dieser Schleimhäute vor Actinomycin D Gabe bestrahlt worden, so ist die Schleimhautschädigung (Mukositis) verursacht durch Actinomycin D zumeist ausgeprägter und schwerer im Vergleich zu alleinigen Gabe von Actinomycin D.
- Inhalationsnarkotika
- Die gleichzeitige Anwendung von halogenierten Inhalationsnarkotika wie Halothan, Isofluran und Enfluran führt zu einer Wirkungsverstärkung von Actinomycin D. Der Mechanismus hierfür ist nicht geklärt.
- Andere Zytostatika
- Andere Zytostatika können die Wirkungen und Nebenwirkungen von Actinomycin D verstärken.
Anwendungsgebiete
Actinomycin D wird zur antineoplastischen Therapie von soliden Tumoren bzw. Krebserkrankungen verwendet.
Es findet derzeit keine Anwendung zur Behandlung von Leukämien und/oder Lymphomen. Darüber hinaus wird es auch nicht als Immunsuppressivum bei der Behandlung von Autoimmunerkrankungen verwendet. Allerdings gibt es Hinweise dafür, dass Actinomycin D bei CLL von Vorteil sein könnte.[6]
Erwachsene
- Ewing-Sarkom
- Actinomycin D wird bei der Behandlung des Ewing-Sarkoms im Rahmen einer Kombinationschemotherapie mit den Zytostatika Vincristin, Adriamycin und Ifosfamid eingesetzt: Es bildet mit diesen Zytostatika den VAIA-Block, welcher sich als wirksam bei der Behandlung des Ewing-Sarkoms erwiesen hat. Der VAIA-Block kann durch Hinzunahme von Etoposid zum EVAIA-Block erweitert werden. Auch wirksam ist der VACA-Block: Hier ist das Ifosfamid gegen Cyclophosphamid getauscht.
- Weichteilsarkom
- Actinomycin D wird bei der Behandlung von Weichteilsarkomen wie Rhabdomyosarkom, Leiomyosarkom, Synovialsarkom und andere Tumorarten im Rahmen von Kombinationschemotherapien eingesetzt. Im Wesentlichen entsprechen die Kombinationschemotherapien denjenigen, welche beim Ewing-Sarkom zum Einsatz kommen, vor allem VAI, VAC, VAIA und VACA.
Kinder und Jugendliche
- Nephroblastom (Wilms-Tumor)
- Actinomycin D ist eines der wesentlichen Zytostatika in der Behandlung des Nephroblastoms (Wilms-Tumor) im Kindes- und Jugendalter. Seine Wirksamkeit beim Nephroblastom wurde wiederholt in mehreren Studien international bewiesen. Insbesondere die Kombination von Actinomycin D mit Vincristin bzw. die Kombination mit Vincristin und Adriamycin (Doxorubicin) haben sich als sehr effektiv in der Bekämpfung des Nephroblastoms erwiesen.
- Ewing-Sarkom
- Actinomycin D wurde im Protokoll EICESS 92 bei der Behandlung des Ewing-Sarkoms im Rahmen einer Kombinationschemotherapie mit den Zytostatika Vincristin, Adriamycin und Ifosfamid eingesetzt: es bildet mit diesen Zytostatika den VAIA-Block, welcher sich als wirksam bei der Behandlung des Ewing-Sarkoms erwiesen hat. Der VAIA-Block kann durch Hinzunahme von Etoposid zum EVAIA-Block erweitert werden. Auch wirksam ist der VACA-Block: Hier ist das Ifosfamid gegen Cyclophosphamid getauscht.
Die gegenwärtige (2006) Standardbehandlung in Europa entsprechend der Euro-E.W.I.N.G 99-Therapieoptimierungsstudie[7] sieht eine Behandlung mit Actinomycin D in der postoperativen Chemotherapie vor (nach Entfernung des Tumors). Actinomycin D wird dabei immer im Rahmen der VAC- (Vincristin, Actinomycin D, Cyclophosphamid) und VAI-Blöcke (Vincristin, Actinomycin D, Ifosfamid) verabreicht. Wegen der Verstärkung der Nebenwirkungen der Strahlentherapie darf Actinomycin D nicht parallel zu einer Strahlentherapie verabreicht werden.
- Weichteilsarkome
- Actinomycin D wird bei der Behandlung von Weichteilsarkomen wie Rhabdomyosarkom, Leiomyosarkom, Synovialsarkom und andere Tumorarten im Rahmen von Kombinationschemotherapien eingesetzt. Im Wesentlichen entsprechen die Kombinationschemotherapien denjenigen, welche beim Ewing-Sarkom zum Einsatz kommen, vor allem VAIA und VACA. Zusätzlich findet noch VAC (Vincristin, Actinomycin D und Cyclophosphamid) Verwendung als Standardbehandlung mit guten Ansprechraten. Bei Weichteilsarkomen mit günstigem Risikoprofil (Stadium I und günstige Histologie = Tumorart) ist die Behandlung allein mit Vincristin und Actinomycin D effektiv.
Nebenwirkungen
- Knochenmarktoxizität (Leukopenie, Thrombopenie, Anämie)
- Die dosisbegrenzende Nebenwirkung von Actinomycin D ist die Knochenmarktoxizität. Durch Einwirkung von Actinomycin D wird die Blutbildung behindert und unterdrückt. Es resultiert nach Gabe von Actinomycin D vor allem eine Thrombopenie und Leukopenie. Der Nadir (Tiefpunkt der Anzahl von Blutkörperchen) tritt 1 bis 2 Wochen nach Gabe auf. Das Knochenmark und die Blutbildung erholen sich nach Actinomycin D Gabe binnen 2 bis 3 Wochen. Zwar reichert sich Actinomycin D in roten Blutkörperchen (Erythrozyten), welche DNA-frei sind, nicht an, allerdings erfolgt die Schädigung in der Entwicklungsstufe der Erythrozyten im Knochenmark, wo diese noch DNA-haltig sind.
- Gewebereizung
- Actinomycin D ist hochgiftig. Es schädigt bei unverdünntem Kontakt mit Haut und Weichteilgewebe diese schwer. Es kann bei einer (unabsichtlichen und nicht gewollten) Verabreichung in das Bindegewebe neben die Vene zu schweren Haut- und Bindegewebsreaktionen kommen: Je nach verwendeter Menge bzw. Dosis von Actinomycin D können die betroffenen Gewebe absterben (Nekrose). Besonders schwerwiegend ist diese Nebenwirkung dann, wenn das betroffene Gebiet zuvor bestrahlt worden ist. Auch wenn die Bestrahlung bereits vor Wochen abgeschlossen wurde, können bestrahlte Gewebe nach Actinomycin D Gabe gereizt reagieren (radiation recall Phänomen).
Aufgrund seiner Giftigkeit sind die Bestimmungen zum Umgang mit Zytostatika besonders strikt einzuhalten. Der Kontakt mit Actinomycin D sollte wo immer möglich vermieden werden. Dies gilt auch für die Einatmung von Pulver bzw. für den Kontakt von Actinomycin D mit den Augen. Mit Actinomycin D kontaminierte Haut oder die Augen sind sofort für 15 Minuten mit Wasser oder Kochsalzlösung zu spülen.
- Übelkeit, Erbrechen, Appetitlosigkeit
- Das erstmalige Auftreten erfolgt 1–6 Stunden nach Actinomycin D Gabe. Bei entsprechender psychologischer Konditionierung ist auch ein schnelleres Auftreten von Erbrechen und Übelkeit möglich. Die Dauer der Übelkeit und des Erbrechens nach Actinomycin D Gabe kann 4–20 Stunden andauern. Diese Nebenwirkung ist häufig (mehr als 10 % der behandelten Patienten betroffen). Eine Behandlung (idealerweise prophylaktisch) mit Antiemetika wie Granisetron, Tropisetron, Ondansetron ist angezeigt.
- Infektionen
- Durch die Leukopenie mit einhergehender Neutropenie ist die Anfälligkeit gegenüber Infektionen unter Therapie mit Actinomycin D erhöht. Es kommt leichter zu bakterielle und mykotischen (Pilze) Infektionen. Diese können geringfügig sein, meistens handelt es sich aber um schwerwiegendere Infektionen wie Lungenentzündungen und Harnwegsinfektionen. Die Immunabwehr kann durch die Leukopenie so geschwächt sein, dass Blutvergiftungen (Sepsis) durch Bakterien, Pilze oder Viren vorkommen können. Diese sind lebensbedrohlich.
Die mit der Leukopenie auftretende Lymphopenie erhöht das Risiko von schweren Virusinfektionen.
- Schleimhautschädigung (Mukositis)
- Actinomycin D bedingt eine ausgeprägte Schädigung der Schleimhäute im Mund, der Speiseröhre und im Darm. Die Merkmale der Schleimhautschädigung (Mukositis) sind dabei Schmerzen (teilweise nur unter Verwendung von Morphin kontrollierbar) und Durchfälle. Letztere können bei ausgeprägter Schädigung auch blutig sein. Schleimhautschädigungen mit Durchfall und Schmerzen treten bei 30 % aller mit Actinomycin D behandelten Patienten auf, so dass diese Nebenwirkung sehr häufig ist. Bei gleichzeitiger Anämie und Leberfunktionseinschränkung mit nachfolgender Gerinnungsstörungen kann bei blutigen Durchfällen eine schwere (gefährliche) Blutung auftreten; dies ist selten.
- Leberschädigung (Hepatotoxizität)
- Actinomycin D kann die Leber schädigen. Neben einer geringfügigen und umkehrbaren Leberschädigung mit Anstieg der Transaminasen als Zeichen der giftigen Wirkung auf die Leberzellen kann es zu einer venösen okklusiven Leberkrankheit (Venenverschlusskrankheit der Leber, veno-occlusive disease; VOD) der Leber kommen. Hierbei thrombosieren aus nicht endgültig geklärter Ursache die Lebervenen, insbesondere die kleineren, und verursachen nachfolgend eine schwere Schädigung der Leber. Diese VOD ist zwar umkehrbar, in nicht wenigen Fällen kann eine Venenverschlusskrankheit der Leber jedoch in ein tödliches akutes Leberversagen münden.
Besonders bei vorangegangener Bestrahlung der Leber (beispielsweise im Rahmen der Therapie eines rechtsseitigen Nephroblastoms) ist die Wahrscheinlichkeit des Auftretens eines Lebenschadens deutlich erhöht. Im Falle des Nephroblastoms (rechtsseitig, Seite der Leber) gilt daher, dass bis zu zwei Monaten nach Bestrahlung keine Gabe von Actinomycin D erfolgen soll.
- Karzinogenität, Mutagenität, Embyrotoxizität
- Actinomycin D ist erwiesen mutagen und embryotoxisch. Es verändert die Erbsubstanz und schädigt ungeborenes Leben. Darüber hinaus ist es ein Kanzerogen: durch Actinomycin D können Krebserkrankungen entstehen.
- Amenorrhoe und Zeugungsunfähigkeit
- Obwohl nicht explizit untersucht ist sehr wahrscheinlich, dass Actinomycin D die Funktion der Hoden und Eierstöcke hemmt. Bei Frauen resultiert aus der Hemmung der Eierstockfunktion eine (sekundäre) Amenorrhoe (Ausfall der Monatsblutung). Bei Männern sind die Spermien entweder schwer geschädigt oder nicht vorhanden (Azoospermie).
Historisches
Die Erstbeschreibung von Actinomycin D erfolgte 1949.[8] Die Beschreibung einer kontrollierten Synthese als Grundlage einer industriellen Produktion wurde 1959 publiziert.[9] 1959 wurde die erste Untersuchung publiziert, welche sich mit dem Einsatz von Actinomycin D bei Tumorerkrankungen von Kindern befasste.[10] Giulio D'Angio beschrieb erstmals die Wirkungsverstärkung von Röntgenstrahlung durch Actinomycin D.[11] Im gleichen Jahr erfolgte auch die Beschreibung der teratogenen Effekte von Actinomycin D.[12] Der erste Einsatz von Actinomycin D bei Lymphomen (Retikulosarkom) wurde ebenfalls 1959 veröffentlicht.[13]
Actinomycin D wurde ursprünglich als Antibiotikum entwickelt. Aufgrund seiner ausgeprägten Giftigkeit kam ein Einsatz zur Behandlung bakterieller Infektionen nicht in Frage.
Siehe auch
Weblinks
- Actinomycin D Monograph der BC Cancer Agency Frei zugänglich. Stand: 1994
- US-amerikanische Packungsbeilage Actinomycin D. Stand: Juni 2005 (Memento vom 1. Dezember 2007 im Internet Archive)
Einzelnachweise
- Eintrag zu Dactinomycin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Januar 2020. (JavaScript erforderlich)
- ABDA-Datenbank (Stand 11. Juni 2008) der DIMDI
- Delepierre M. et al. Reassessment of structural characteristics of the d(CGCG)2:actinomycin D complex from complete 1H and 31P NMR. J Biomol Struct Dyn. 1989 Dec;7(3):557–589. PMID 2627299
- Wu M. H., Yung B. Y. Cell cycle phase-dependent cytotoxicity of actinomycin D in HeLa cells. Eur J Pharmacol. 1994 Apr 4;270(2-3):203–212. PMID 8039550
- Veal G. J. et al. of United Kingdom Children's Cancer Study Group, Pharmacology Working Group. Pharmacokinetics of dactinomycin in a pediatric patient population: a United Kingdom Children's Cancer Study Group Study. Clin Cancer Res. 2005 Aug 15;11(16):5893–5899. PMID 16115931
- O. Merkel, N. Wacht, E. Sifft, T. Melchardt, F. Hamacher, T. Kocher, U. Denk, J. P. Hofbauer, A. Egle, M. Scheideler, M. Schlederer, M. Steurer, L. Kenner, R. Greil: Actinomycin D induces p53-independent cell death and prolongs survival in high-risk chronic lymphocytic. In: Leukemia. 26, Nr. 12, Dezember 2012, S. 2508–2516. doi:10.1038/leu.2012.147. Abgerufen am 1. April 2014.
- EURO-E.W.I.N.G.-99 Studie kinderkrebsinfo.de
- Dalgliesch C. E., Todd A. R. Actinomycin. Nature. 1949 Nov 12;164(4176):820. PMID 15395378
- Katz E., Goss W. A. Controlled biosynthesis of actinomycin with sarcosine. Biochem J. 1959 Nov;73:458–465. PMID 14404788
- Tan C. T. et al. The effect of actinomycin D on cancer in childhood. Pediatrics. 1959 Oct;24:544–561. PMID 13836792
- D'Angio G. J. et al. Potentiation of x-ray effects by actinomycin D. Radiology. 1959 Aug;73:175–177. PMID 13813586
- Tuchmann-Duplessis H, Mercier-Parot L. Apropos of the teratogenic action of actinomycin. C R Seances Soc Biol Fil. 1959;153:1697–1700. PMID 13839737
- Shiba S. Studies on the therapy of reticulosarcoma(-tosis) with actinomycin. Acta Unio Int Contra Cancrum. 1959;15(Suppl 1):264–266. PMID 14445951