Vinorelbin
Vinorelbin ist ein zytostatischer Arzneistoff, der sich vom Vincristin, einem Alkaloid aus den Blättern von Cataranthus roseus ableitet. Vinorelbin ist zur Behandlung verschiedener Karzinome zugelassen.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
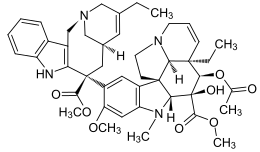 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Vinorelbin | |||||||||||||||
| Summenformel | C45H54N4O8 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code |
L01CA04 | |||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 778,93 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Hersteller
Vinorelbin wird von dem französischen Unternehmen Laboratoires Pierre Fabre aus Castres hergestellt. Es handelt sich um ein halbsynthetisches Vincaalkaloid der dritten Generation, das 1989 in Frankreich eingeführt wurde. Die Markteinführung in Deutschland erfolgte 1996. Seitdem ist in zahlreichen Phase-II- und -III-Studien die Wirkung sehr gut dokumentiert.
Wirkprinzip
Vinorelbin ist ein Spindelgift (Antitubulin) und behindert die Bildung der sog. Mikrotubuli der Kernspindel, die in der mitotischen Zellteilung (Anaphase/Telophase) die beiden neuen Chromosomensätze zu den Zellpolen ziehen, und unterbricht damit die bei Tumorerkrankungen unkontrollierte Zellteilung.
Indikation
Internationale Zulassungen bestehen insbesondere als Standardtherapie in der Behandlung des sog. "Nicht-kleinzelligen-Bronchialkarzinoms" (NSCLC) und des Brustkrebses (Mamma-Karzinom) im metastasierten Stadium; in einigen Ländern auch zugelassen für die Behandlung des metastasierten Prostatakarzinoms;[3] gute Dokumentation darüber hinaus in den Indikationen Kopf-Hals-Tumoren, Ovarial- und Zervixkarzinom. Einsatz in der Regel als Monotherapie oder in Kombination mit anderen zytostatisch wirksamen Substanzen. Sehr häufig eingesetzt zusammen mit Cisplatin oder Carboplatin, aber auch mit 5-Fluoruracil (5-FU), Anthracyclinen, Gemcitabin oder Taxanen (Docetaxel, Paclitaxel) und mit Capecitabin. Neuerdings beim Mamma-Karzinom sehr gute Ergebnisse in Kombination mit Trastuzumab (Herceptin), sofern der Tumor einen entsprechenden Rezeptorstatus (HER2/neu) aufweist. Erfolgversprechend scheint auch der kombinierte Einsatz mit dem neuen Antikörper Cetuximab (Erbitux®) zu sein. Neben der reinen Mono- oder Polychemotherapie wird Vinorelbin auch in der kombinierten Radio-Chemotherapie (Kombination mit Bestrahlung) eingesetzt; hier insbesondere beim NSCLC in den Stadien IIIa und IIIb, soweit die Tumoren nicht operabel sind. In den frühen Stadien des NSCLC (I bis III) hat sich Vinorelbin kürzlich (ASCO 2003, 2004 und 2005) in mehreren großen Phase III Studien auch in der sogenannten adjuvanten Behandlung nach erfolgreicher Operation als erheblich überlebensverlängernd herausgestellt.
Unerwünschte Wirkungen
Vinorelbin besitzt im Vergleich zu anderen Zytostatika der gleichen Generation ein subjektiv relativ günstiges Nebenwirkungsprofil bei prinzipiell gleicher Wirkungsqualität. Die in der Zytostatikatherapie bekannten Nebenwirkungen wie z. B. Haarausfall, Übelkeit und Erbrechen, Hautveränderungen, Müdigkeit etc. treten nur relativ selten und in schwacher Ausprägung auf. Insbesondere die für Vincaalkaloide typischen peripheren Neuropathien (Nervenausfälle in den Extremitäten) sind bei Vinorelbin nur gering ausgeprägt.
Die Hauptnebenwirkung ist die sog. Neutropenie / febrile Neutropenie. Man versteht darunter einen Mangel an weißen Blutkörperchen. Diese kann allerdings durch die Gabe von bestimmten Medikamenten (G-CSF) kontrolliert werden.
Orale Darreichungsform
Vinorelbin ist in Deutschland als orale Darreichungsform verfügbar. Diese ist zugelassen für die Behandlung des fortgeschrittenen nicht-kleinzelligen Bronchialkarzinoms (Stadium III oder IV) bei Patienten in gutem Allgemeinzustand (Karnofsky-Index ≥ 80 %) sowie für die Behandlung des fortgeschrittenen anthracyclin-resistenten Mammakarzinoms bei Patientinnen in gutem Allgemeinzustand.
Handelsnamen
Bendarelbin (D), Eberelbin (A), Navelbine IV und Oral (D, A, CH), Navin (A), Navirel (D), Vinocleus (A), diverse Generika (D, A, CH)
Einzelnachweise
- Datenblatt Vinorelbine ditartrate salt hydrate bei Sigma-Aldrich, abgerufen am 25. April 2011 (PDF).
- Eintrag zu Vinorelbine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- R. P. Abratt et al.Randomised phase III study of intravenous vinorelbine plus hormone therapy versus hormone therapy alone in hormone-refractory prostate cancer Annals of Oncology 2004 15(11):1613-1621 (Volltext) PMID 15520061