Gemcitabin
Gemcitabin (2′,2′-Difluordesoxycytidin) ist ein Nukleosid aus Cytosin und einer difluorierten Desoxyribose. Es ist ein chemisches Analogon des Nukleosids Cytidin. Es wird als Zytostatikum in der Chemotherapie verwendet.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
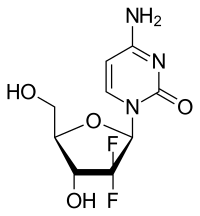 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Gemcitabin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C9H11F2N3O4 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
L01BC05 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 263,20 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt |
287–292 °C (Gemcitabin-Hydrochlorid)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Pharmakologie
Wirkungsmechanismus
Gemcitabin ist ein Zytostatikum und wird in die Gruppe der Antimetabolite eingeordnet und gehört zur Gruppe der Pyrimidinanaloga. Es handelt sich um ein Prodrug, das erst in der menschlichen Zelle zu seiner eigentlichen Wirkform umgewandelt wird.
Die zytostatische Wirkung von Gemcitabin beruht darauf, dass statt des menschlichen Nukleosids Cytidin die Wirkform des Gemcitabin, das Gemcitabintriphosphat, in die DNA eingebaut wird.[3] Dadurch wird die DNA-Synthese unterbrochen und es kommt zum Zelltod.
Aufnahme und Verteilung im Körper
Da Gemcitabin erst in der Zelle durch ein Enzym in die Wirkform umgewandelt wird, fällt diesem Enzym eine besondere Bedeutung zu. Die Wirksamkeit des Gemcitabin ist von der Dosis, aber auch von der Infusionsdauer abhängig.
In der Leber, im Blut und in der Niere wird Gemcitabindiphosphat in eine zytostatisch unwirksame Substanz abgebaut. Die Ausscheidung erfolgt über die Niere.
Die biologische Halbwertzeit ist abhängig vom Geschlecht und Alter des Patienten. Sie beträgt etwa 40 bis 90 Minuten.
Therapeutische Verwendung
Anwendungsgebiete
- Therapie des Adenokarzinom des Pankreas (häufigste Form des Bauchspeicheldrüsenkrebs)
- Monotherapie oder in Kombination mit Paclitaxel[4] oder mit Erlotinib
- Nicht-kleinzelliges Bronchialkarzinom
- Kombination mit Cisplatin
- Mammakarzinom (Brustkrebs)
- Kombination mit Paclitaxel
- Kombination mit Cisplatin
- Ovarialkarzinom (Eierstockkrebs)
- Kombination mit Carboplatin
- Rezidivtherapie bei Lymphomen (Non-Hodgkin- und Hodgkin-Lymphome)
- Kombination mit Dexamethason
- Monotherapie oder in Kombination mit Cisplatin
Unerwünschte Wirkungen
Die häufigsten Nebenwirkungen, die bei über 10 Prozent der Behandelten beobachtet wurden, sind eine Knochenmarksschädigung, die sich in einer verminderten Anzahl von Granulozyten, Thrombozyten und Leukozyten sowie einer Anämie äußert, Atemnot, Übelkeit und Erbrechen, Erhöhung von Leberenzymen, allergische Hautausschläge und Haarausfall, Hämaturie und Proteinurie, sowie grippeähnliche Beschwerden und Ödeme.
Die toxischen Nebenwirkungen an Nieren, Leber und Blut erfordern ein sorgfältiges Monitoring der Patienten, um ggf. Dosisanpassungen vornehmen zu können.
Nebenwirkungen, die schwerwiegend sind oder einen schweren Verlauf nehmen können, wie das Stevens-Johnson-Syndrom, die toxische epidermale Nekrolyse, das posteriore reversible Enzephalopathie-Syndrom (PRES), Kapillarlecksyndrom, interstitielle Lungenentzündung, Lungenödem, akutes Atemnotsyndrom beim Erwachsenen (ARDS), und anaphylaktische Reaktionen treten selten (0,01 – 0,1 Prozent) bis sehr selten (bei unter 0,01 Prozent der Behandelten) auf.
Wechselwirkungen
- Strahlentherapie bei bestimmten Krankheitsbildern
Gegenanzeigen
Gemcitabin darf in folgenden Fällen nicht angewendet werden:
- Bei einer Überempfindlichkeit gegenüber Gemcitabin,
- Bei mäßig bis stark eingeschränkter Leberfunktion oder stark eingeschränkter Nierenfunktion sollte Gemcitabin nicht gegeben werden, da keine entsprechenden Studien durchgeführt wurden.
Dosierung
Je nach Krankheitsbild 1.000–2.000 mg/m² Körperoberfläche.
Literatur
- Arzneimittel-Therapie-Kritik, München, 2005 Jahrg. 37, S. 121–128.
- Fachinfo: Gemzar.
- Textbook of Primary Care Medicine, 3rd ed, Mosby 2001.
Handelsnamen
Cytogembin (A), Ebegemcit (A), Gemcapyr (A), Gemcitara (A), Gemzar (D, A, CH, EU), Tabinell (A), diverse Generika (D, A, CH)
Weblinks
- Ricarda Wessinghage: Bösartige Lebererkrankungen: Aussicht auf neue Therapieoption mit Gemcitabin. Klinikum der Johann Wolfgang Goethe-Universität, Frankfurt a. M., Pressemitteilung vom 15. September 2006 beim Informationsdienst Wissenschaft (idw-online.de), abgerufen am 24. August 2015.
Einzelnachweise
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, ISBN 978-0-911910-00-1, S. 755.
- Datenblatt Gemcitabine hydrochloride bei Sigma-Aldrich, abgerufen am 3. April 2011 (PDF).
- P. Huang, S. Chubb, L. W. Hertel, G. B. Grindey, W. Plunkett: Action of 2’,2’-difluorodeoxycytidine on DNA synthesis. In: Cancer Research. Band 51, Nr. 22, 15. November 1991, ISSN 0008-5472, S. 6110–6117, PMID 1718594.
- David Goldstein, Robert Hassan El-Maraghi, Pascal Hammel, Volker Heinemann, Volker Kunzmann: nab-Paclitaxel Plus Gemcitabine for Metastatic Pancreatic Cancer: Long-Term Survival From a Phase III Trial. In: Journal of the National Cancer Institute. Band 107, Nr. 2, 1. Februar 2015, S. dju413, doi:10.1093/jnci/dju413, PMID 25638248.