Asparaginase
Asparaginasen (L-Asparaginamidohydrolasen) sind im Allgemeinen Enzyme, die die Hydrolyse von Asparagin zu Asparaginsäure katalysieren. Diese Reaktion ist eine Möglichkeit des Abbaus von Asparagin. Asparaginasen kommen in allen Lebewesen vor, in großen Mengen wurden sie im Serum des Meerschweinchens und des Agutis, sowie in der Leber mehrerer Wirbeltier-Arten, außerdem in Pilzen und mehreren Bakterienstämmen gefunden. Im Menschen wird sie im Gehirn, den Nieren, Hoden und im Darm exprimiert.[1][2]
| Asparaginase (Homo sapiens) | ||
|---|---|---|
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 309 Aminosäuren | |
| Isoformen | 2 | |
| Bezeichner | ||
| Gen-Name | ASRGL1 | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 3.5.1.1, Hydrolase | |
| Reaktionsart | Hydrolyse | |
| Substrat | L-Asparagin + H2O | |
| Produkte | L-Aspartat + NH3 | |
| Vorkommen | ||
| Homologie-Familie | Asparaginase | |
| Übergeordnetes Taxon | Lebewesen | |
| Asparaginase 2 (Escherichia coli K12) | ||
|---|---|---|
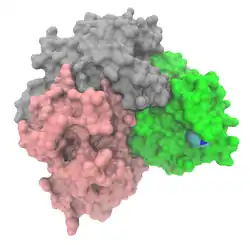
| ||
| Oberflächenmodell des Tetramers, mit Asparagin als Kalotten, nach PDB 3ECA | ||
| Masse/Länge Primärstruktur | 326 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homotetramer | |
| Bezeichner | ||
| Gen-Name(n) | ansB (EcoGene) | |
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code | L01XX02 | |
| DrugBank | BTD00011 | |
| Wirkstoffklasse | Zytostatika | |
| Enzymklassifikation | ||
| EC, Kategorie | 3.5.1.1, Hydrolase | |
| Reaktionsart | Hydrolyse | |
| Substrat | L-Asparagin + H2O | |
| Produkte | L-Aspartat + NH3 | |
Asparaginase aus Aspergillus wird zur Reduktion des Acrylamidgehalts in Lebensmitteln, z. B. Backwaren, verwendet.[3]
Asparaginase im engeren Sinn ist ein Arzneistoff aus der Gruppe der Zytostatika zur Behandlung von akuter lymphatischer Leukämie (ALL) und Subtypen des Non-Hodgkin-Lymphoms eingesetzt wird. Gewonnen wird sie aus verschiedenen Bakterien, vor allem aus Escherichia coli.
Klinische Angaben
Anwendungsgebiete
Als Zytostatikum wird Asparaginase zur Behandlung der akuten lymphatischen Leukämie (ALL) und des Non-Hodgkin-Lymphoms eingesetzt. Es kann sowohl als Monotherapie als auch im Rahmen einer Polytherapie eingesetzt werden und wird seit den 1960er Jahren für Induktions- und Konsolidationsbehandlung der malignen lymphatischen Erkrankungen genutzt.
Art und Dauer der Anwendung
Asparaginase wird als Pulver in Wasser gelöst und intramuskulär oder intravenös verabreicht.
Es ist bei Asparaginase von besonderer Bedeutung, die Serum-Asparaginase gut zu kontrollieren. Nur bei richtiger Dosierung treten Verbesserung des krankheitsfreien und Gesamt-Überlebens auf. Bei zu niedriger Dosierung kann Asparaginase sogar negative Effekte auf beide haben. Für dieses „Drug-Monitoring“ sind häufige Blutabnahmen noch nicht zu vermeiden, was besonders bei jungen Patienten Schwierigkeiten hervorrufen kann (ALL ist sehr häufig bei Kindern von vier Jahren und kommt auch schon im Alter von weniger als ein Jahr vor).
Gegenanzeigen
Patienten mit Pankreatitis darf keine Asparaginase verabreicht werden. In der Geschichte sind dadurch Fälle akuter hämorrhagischer Pankreatitis mit Todesfolge bekannt geworden.
Ebenso sollte bei Patienten, die bereits anaphylaktische Reaktionen gezeigt haben, auf Asparaginase verzichtet werden.
Wechselwirkungen mit anderen Medikamenten
Studien haben gezeigt, dass Asparaginase bzw. die niedrige Asparaginkonzentration im Blut die Wirkung von Methotrexat auf maligne Zellen vermindert. Diese sollten also nicht in Kombination verabreicht werden.
Anwendung während Schwangerschaft und Stillzeit
Es liegen keine Studien mit schwangeren Frauen vor, jedoch hat sich in Studien mit Mäusen und Ratten gezeigt, dass Asparaginase das Wachstum und die Gewichtszunahme des Kindes negativ beeinflussen könnte. Ebenso scheint es das Risiko auf Fehlgeburt oder Missbildung zu erhöhen. In Kaninchen sind Missbildungen beobachtet worden.
Es ist nicht bekannt, ob und wie Asparaginase in die Muttermilch gerät.
Grundsätzlich wird von Schwangerschaft und Stillen während einer Behandlung mit Asparaginase abgeraten.
Unerwünschte Wirkungen
Die häufigsten Nebenwirkungen sind Appetitlosigkeit, Übelkeit und Erbrechen. Diese sind heute meistens gut zu behandeln. Ebenso wirkt sich Asparaginase negativ auf das Immunsystem aus, was zu Infektionen führen kann.
Weil es sich bei Asparaginase um ein Fremdprotein handelt, besitzt es eine hohe Immunogenität, was für immunologische Reaktionen sorgt. Dies können klinische Reaktionen sein, bis hin zum anaphylaktischen Schock, aber auch Reaktionen, die sich nicht klinisch manifestieren, aber die Aktivität von Asparaginase beeinflussen.
Außerdem sind Fälle von Pankreatitis und Leberfunktionsstörungen bekannt sowie Koagulopathie. Da Asparaginase die Proteinsynthese beeinflusst, beeinflusst es auch die Synthese von Gerinnungsfaktoren. Dies kann Blutungen oder Thrombose verursachen.
Asparaginasetherapie kann zu einem erhöhten Blutzuckerspiegel führen.
Wirkungsmechanismus
Gesunde Zellen können eigenes Asparagin herstellen. Leukämische Zellen (Lymphoblasten) bei der ALL können dies nicht. Sie sind daher abhängig von zirkulierendem Asparagin. Das macht man sich in der Behandlung mit Asparaginase zunutze. Asparaginase katalysiert die Spaltung von Asparagin in Asparaginsäure und Ammonium und sorgt so für eine niedrige Asparaginkonzentration im Blut. So bekommen die leukämischen Zellen nicht mehr genug Asparagin, um zu überleben.
Sonstiges
Die Aufnahme in den Therapiealltag fand in den 1960er Jahren statt. In den USA erfolgte die Zulassung 1978 unter dem Namen Elspar.[4]
Studien
Varianten
Pegaspargase
Pegaspargase ist eine PEGylierte rekombinante L-Asparaginase aus Escherichia coli.
Crisantaspase
Crisantaspase (Asparaginase Erwinia chrysanthemi) wurde in Deutschland 1990 unter dem Namen Erwinase zugelassen als Bestandteil einer krebshemmenden Kombinationstherapie bei ALL im Kindes- und Erwachsenenalter hauptsächlich bei Patienten, die überempfindlich auf L-Asparaginase aus Escherichia coli, entweder nativ oder pegyliert (Pegaspargase), reagieren.[9] Erwinia chrysanthemi (Name seit 2005 Dickeya dadantii[10]) ist ein gramnegatives Bakterium aus der Familie der Pectobacteriaceae. Im Jahr 2019 wurde über anhaltende Lieferprobleme für Crisantaspase berichtet.[11]
Im Juni 2021 wurde eine rekombinant hergestellte Crisantaspase als Rylaze (Jazz Pharmaceuticals) in den USA zugelassen zur Behandlung der ALL und des lymphoblastischen Lymphoms bei erwachsenen und pädiatrischen Patienten, die allergisch gegen die von E. coli abgeleiteten Asparaginase-Produkte sind. Das Mittel wird im Rahmen einer Kombinationstherapie mit anderen Arzneimitteln verabreicht und intramuskulär injiziert. Der Wirkstoff ist identisch mit der nativen L-Asparaginase Erwinia chrysanthemi und wird durch Fermentation mittels eines gentechnisch veränderten Pseudomonas-fluorescens-Bakteriums hergestellt, das die für Crisantaspase kodierende DNA enthält.[12] Das Analogpräparat war zuvor weltweit knapp geworden.[13]
Die Wirksamkeit von Rylaze wurde in der offenen, multizentrischen Studie JZP458-201 mit mehreren Kohorten mit insgesamt 102 Patienten untersucht, die entweder eine Überempfindlichkeit gegen von E. coli abgeleitete Asparaginasen hatten oder eine stille Inaktivierung erlebten. Die Bestimmung der Wirksamkeit basierte auf dem Nachweis des Erreichens und der Aufrechterhaltung der Nadir-Serum-Asparaginase-Aktivität (NSAA) oberhalb eines bestimmten Levels an Asparaginase-Aktivität. Die Studie ergab, dass die empfohlene Dosierung bei 94 % der Patienten das Ziel für die Asparaginase-Aktivität erreichte.[12]
Zu den häufigsten Nebenwirkungen von Crisantaspase gehören Überempfindlichkeitsreaktionen, Pankreastoxizität, Blutgerinnsel, Blutungen und Lebertoxizität.[12]
Calaspargasepegol
Calaspargasepegol ist eine rekombinante, variante und PEGylierte Form der L-Asparaginase 2 des Stamms K12 von Escherichia coli.
Weblinks
- Eintrag zu Asparaginase in der DrugBank der University of Alberta
- Drugs.com: Asparaginase Injection consumer information
- Datenblatt Asparaginase from Escherichia coli bei Sigma-Aldrich, abgerufen am 16. Juni 2011 (PDF).
Einzelnachweise
- John C. Wriston, Jr.: L-Asparaginase. In: Paul D. Boyer, Edwin G. Krebs, David S. Sigman (Hrsg.): The Enzymes. Edition: 3, Academic Press, 1971. ISBN 0-12-122704-9, S. 101ff.
- UniProt Q7L266
- Zofia Olempska-Beer: Asparaginase from Aspergillus Niger expressed in A. Niger. (PDF; 98 kB) Chemical and Technical Assessment. In: fao.org. Food and Agriculture Organization of the United Nations, abgerufen am 24. Februar 2016 (englisch).
- Database FDA-Approved Drugs. Abgerufen am 20. Juli 2021.
- RH Adamson, S Fabro: Antitumor activity and other biologic properties of L-asparaginase (NSC-109229)-a review. In: Cancer Chemother Rep. 52, Nr. 6, Oktober 1968, S. 617–626. PMID 4895425.
- RL Capizzi, JR Bertino, RE Handschumacher: L-asparaginase. In: Annu. Rev. Med.. 21, 1970, S. 433–44. doi:10.1146/annurev.me.21.020170.002245. PMID 4913953.
- SE Sallan, BM Cammita, JR Cassady, DG Nathan, E Frei: Intermittent combination chemotherapy with adriamycin for childhood acute lymphoblastic leukemia: clinical results. In: Blood. 51, Nr. 3, März 1978, S. 425–33. PMID 272207.
- MD Amylon, J Shuster, J Pullen et al.: Intensive high-dose asparaginase consolidation improves survival for pediatric patients with T cell acute lymphoblastic leukemia and advanced stage lymphoblastic lymphoma: a Pediatric Oncology Group study. In: Leukemia. 13, Nr. 3, März 1999, S. 335–42. PMID 10086723.
- Jazz Pharmaceuticals: Zusammenfassung der Merkmale des Arzneimittels (Fachinformation) - Erwinase Pulver zur Herstellung einer Injektionslösung. Hrsg.: Bundesinstitut für Arzneimittel und Medizinprodukte. Oktober 2019.
- Régine Samson et al.: Transfer of Pectobacterium chrysanthemi (Burkholder et al. 1953) Brenner et al. 1973 and Brenneria paradisiaca to the genus Dickeya gen. nov. as Dickeya chrysanthemi comb. nov. and Dickeya paradisiaca comb. nov. and delineation of four novel species, Dickeya dadantii sp. nov., Dickeya dianthicola sp. nov., Dickeya dieffenbachiae sp. nov. and Dickeya zeae sp. nov. In: International Journal of Systematic and Evolutionary Microbiology. Band 55, S. 1415–1427, doi:10.1099/ijs.0.02791-0.
- Erwinase: Nur noch als Einzelimport. In: Apotheke adhoc. Abgerufen am 20. Juli 2021.
- Jazz Pharmaceuticals: Rylaze - Prescribing Information. Hrsg.: FDA. Juni 2021.
- FDA Approves Component of Treatment Regimen for Most Common Childhood Cancer. 30. Juni 2021, abgerufen am 20. Juli 2021.